工业催化_催化剂的组成与功能
- 格式:ppt
- 大小:238.00 KB
- 文档页数:30

工业催化知识点总结1. 催化剂的定义和分类催化剂是指能加速化学反应速率而本身不参与反应的物质。
根据催化反应的类型和应用范围,催化剂可以分为三类:均相催化剂、非均相催化剂和酶催化剂。
均相催化剂指在反应体系中与反应物相同的物质,非均相催化剂指在反应体系中与反应物相异的物质,酶催化剂是一种生物催化剂。
2. 催化剂的作用原理催化作用的基本原理是通过改变活化能,使得反应能够以更低的能量障碍进行。
催化剂在化学反应过程中会形成过渡态,通过吸附和解离反应物分子来降低活化能,从而提高反应速率。
而酶催化作用则是通过特定的活性位点使得反应物分子以更高效的方式进行化学反应。
3. 催化剂表面结构和活性位点催化剂表面结构和活性位点是催化剂催化作用的关键。
催化剂的活性位点是指能够吸附和反应反应物的部位,而催化剂的表面结构决定了活性位点的分布和特性。
在催化剂的设计和研究过程中,对催化剂表面结构和活性位点的理解和控制是至关重要的。
4. 催化反应的热力学和动力学催化反应的热力学和动力学性质对于理解和优化催化反应过程至关重要。
热力学研究了反应物与产物之间的化学平衡,而动力学研究了反应速率随时间的变化。
通过研究催化反应的热力学和动力学性质,可以优化催化剂的设计和反应条件。
5. 工业催化反应的应用工业催化反应在化工、能源、环保等领域具有重要的应用价值。
以氢气和氧气为反应物的合成氨催化反应、以氢气和一氧化碳为反应物的甲醇合成催化反应、汽油和柴油的加氢精制催化反应等都是工业上重要的应用。
6. 催化剂的设计和研究方法催化剂的设计和研究方法包括实验室合成和表征、计算模拟和理论研究等。
通过实验室合成和表征可以获得催化剂的物理和化学性质,通过计算模拟和理论研究可以对催化剂的结构和活性进行深入的理解。
在工业催化领域,通过对催化剂的设计和研究方法的不断深入和发展,可以为工业催化反应的高效和环保提供重要的技术支持。
7. 环保催化技术环保催化技术是指在保证催化反应效率的前提下,减少对环境的污染。
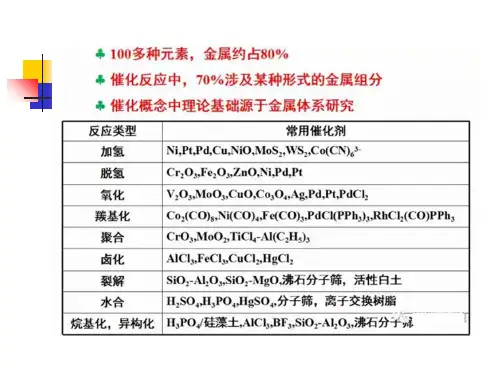

工业催化剂的原理及应用催化剂在化学工业中扮演着至关重要的角色。
它们能够加速反应速度、提高反应选择性和产品质量,从而使得反应更加高效。
其中,工业催化剂就是指应用于化学工业中的催化剂。
本文主要讲述工业催化剂的原理及应用。
一、工业催化剂的原理工业催化剂的原理主要基于催化反应的两个关键概念:催化活性和催化剂选择性。
催化活性是指催化剂参与反应的能力。
在一个催化剂表面,它的活性中心使得化学反应发生时需要的化学键发生断裂和形成。
这个反应的速率将会受到活性中心的数量和类型的限制,以及表面结构和反应条件的影响。
由于催化活性中心的数量和类型在每个不同的催化剂中都不同,因此,催化剂的催化活性通常会因催化剂的化学性质和物理性质而变化。
催化剂选择性是指催化剂选择生成的产物的能力。
催化剂精确地选择反应产物的生成是很复杂的,它取决于催化剂对反应机理的了解、催化作用的决定性步骤,以及催化剂和反应物的触发点。
因为具有不同的表面性质和晶体结构的不同催化剂,会与反应物的不同物理和化学性质和它们的作用有所不同,因此,催化剂选择性和活性之间存在一定的关系和相互影响。
二、工业催化剂的应用工业催化剂的应用非常广泛,包括合成氨、裂解石油、制造聚合物、制备精细化学品等。
其中,以下是工业中常用的催化剂。
1. 合成氨催化剂合成氨催化剂通常是氧化铁、铁、铝或铜的混合物。
该催化剂广泛应用于合成氨反应中。
氢气和氮气在催化剂上的反应可产生氨。
在这个过程中,而且,铁、氧化铁或锌和其他几种金属通常通过混合和煅烧处理来制备这种催化剂。
2. 裂解催化剂石油裂解是重要的工业反应之一,可以利用催化剂分解长链烃成小分子烃。
此过程通常在高温和高压下进行,并且需要长时间处理。
裂解反应的触发因素是催化剂表面的酸性位点,这些位点的作用使得反应中出现的物种与催化剂反应形成类似碳烯烃的层状结构。
3. 聚合催化剂聚合催化剂是制备聚合物的重要催化剂。
这种催化剂分为阴离子聚合催化剂和阳离子聚合催化剂两种。



工业催化剂的研究和应用工业催化剂是指在工业生产中用于催化反应的材料。
它通过提高反应速率、降低反应温度和增加选择性等作用,促进化学反应的进行。
工业催化剂可以应用于化学、能源、环保、食品等多个领域,是现代社会发展不可或缺的一项技术。
一、工业催化剂的分类根据化学反应类型和催化剂的组成成分,工业催化剂可以分为以下几类:1. 原位催化剂:催化剂在反应中起催化作用,反应后从催化剂中脱离,形成新的物质。
2. 催化剂负载剂:负载剂是指将一种催化剂物质扩散到其他材料表面,形成固体催化剂。
负载剂通常包括氧化铝、硅胶和活性炭等材料。
催化剂负载剂广泛应用于车用尾气净化、燃料电池、氢气生产和精细化学品生产等领域。
3. 催化剂膜:催化剂膜是指在两个反应物之间形成的膜结构。
它可以分为表面催化和气体相催化两类。
表面催化是指在液体反应中催化剂的活性部分面朝反应物,将反应物吸附在催化剂表面,使反应物分子处于高能态。
气体相催化是指催化剂直接接触反应气体,通过反应体系中的惰性成分,促进反应的进行。
4. 金属催化剂和非金属催化剂:金属催化剂通常是指活性金属离子,例如铂、钴、铁、铬、铜等。
非金属催化剂则包括氧化物、硫化物、氮化物、磷化物等。
二、工业催化剂的应用1. 化学领域:工业催化剂在化学领域应用广泛,其主要应用包括基础化学品、精细化学品、石化、聚合及无机化学等领域。
例如,石化生产中的炼油、裂化和合成气等过程中,都需要使用催化剂来促进化学反应的进行,提高产品的纯度和产量。
2. 能源领域:催化技术在能源领域的应用也非常广泛,它涉及到能源转化、储存和利用等方面。
例如,催化剂在燃料电池中需要发挥极其重要的作用,它可以提高燃料电池的效率、降低反应温度和延长使用寿命。
3. 环保领域:由于催化技术需要较低反应温度和较短反应时间,所以在环保领域中应用广泛。
例如,在车用尾气净化、废水处理、废气处理和垃圾焚烧等方面,均需要使用催化剂来加快污染物的分解和去除。

催化剂的组成取功能之阳早格格创做催化剂的组成:活性组分载体帮催化剂催化剂组分取功能闭系:一、活性组分它是催化剂的主要组分,偶尔由一种物量组成,偶尔由多种物量组成如:乙烯氧化制环氧乙烷的银催化剂;丙烯氨氧化制丙烯腈用的钼战铋催化剂活性组分的分类:二、载体载体是催化剂活性组分的分别剂、粘合剂战收撑物,是背载活性组分的骨架.比圆,乙烯氧化制环氧乙烷催化剂中的Ag便是背载正在“α—Al2O3上的,那里的α—Al2O 3称为载体.载体还常分为惰性载体取活性载体.庄重去道,催化剂中的组分皆没有是惰性的,皆对于主剂取帮剂有所效率,只没有过活性载体的效率更为明隐而已.载体的效率取帮催化剂的效率正在很多圆里有类似之处,分歧的是载体量大,帮催化剂量小;前者效率较慢战,后者较明隐.其余,由于载体量大,可给予催化剂以基础的物理结构取本能,如孔结构、比表面、宏瞅形状、板滞强度等.别的,对于主催化剂战帮催化剂起分别效率,更加对于贵金属既可缩小其用量,又可普及其活性,落矮催化剂成本.动做下效催化剂,活性组分取裁体的采用皆非常要害.底下是载体的分类战部分罕睹载体的种类:催化剂的活性随载体比表面的减少而减少,为赢得较下的活性,往往将活性组分背载于大比表面载体上.载体取催化剂的活性、采用性、热宁静性、板滞强度以及催化历程的传播个性有闭,果此,正在筛选战制制劣良的催化剂时,需要弄浑载体的物理本量战它的功能.催化剂组分取含量的表示要领:比圆:合成氨催化剂Fe—K2O—Al2O3用“—’将催化剂中的各组分开启:加氢脱硫催化剂Co—Mo/α—Al2O3,斜线上为主剂战帮剂,斜线下为载体.各组分的含量可用沉量%、沉量比表示,也可用本子%、本子比表示.载体的功能:提供灵验的表面战相宜的孔结构⏹巩固催化剂的板滞强度⏹革新催化剂的传导性⏹缩小活性组分的含量⏹载体提供附加的活性核心⏹活性组分取载体之间的溢流局里战强相互效率理念的催化剂载体应具备的个性能符合某一特定反应的形状;有脚够的抗破碎强度;有脚够的反应表面战符合的孔结构;有脚够的宁静性,包罗活性宁静性取热宁静性;导热、热容量及堆稀度适中;没有含使催化剂中毒的物量;本料易得,载机制备历程烦琐.三、帮催化剂定义:加进少量的某种物量,不妨隐著革新催化剂效能,包罗活性,采用性取宁静性战寿命等.它是通过改变催化剂的化教组成、化教结构、离子价态、酸碱性、晶格结构、表面结构、孔结构、分别状态、板滞强度等去普及催化剂的本能.帮催化剂的分类:(1)结构型帮催化剂(2)电子型帮催化剂:(3)晶格缺陷型帮催化剂:使活性物量晶里的本子排列无序化,删大晶格缺陷浓度去普及催化剂的催化活性.第(2)、(3)类也合称为调变性帮催化剂结构型帮催化剂:效率:普及活性组分的分别性战热宁静性.本理:能使催化活性物量粒度变小、表面积删大,预防大概延慢果烧结而落矮活性等,工业催化历程常常正在几百度的条件下举止,本本没有宁静的微晶简单烧结,果而引导催化剂的活性下落.而帮催化剂的加进不妨遏止大概减慢微晶的删少速度,进而延少催化剂的使用克日.比圆:合成氨的铁催化剂,加进少量的Al2O3电子型帮催化剂:效率:改变催化剂活性物量的结媾战化教组成,促进催化活性采用性.本理:催化剂活性组分的空d轨讲能交受帮催化剂提供的电子,改变了活性组分的电子结构,普及了催化剂的活性战采用性;大概死成新的晶相,大概者也大概爆收大概删加催化剂中晶相大概微晶间活性界里的数目.进而普及活性大概采用性.比圆:Fe-Al2O3中加进K2O罕睹帮催化剂举例:。

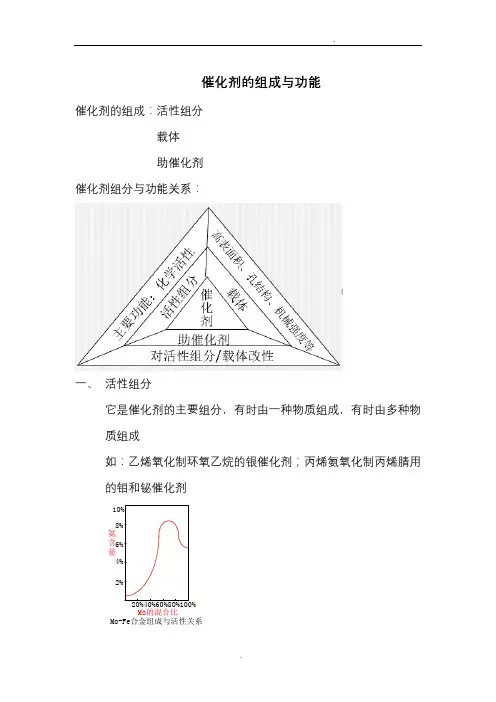
催化剂的组成与功能催化剂的组成:活性组分载体助催化剂催化剂组分与功能关系:一、 活性组分它是催化剂的主要组分,有时由一种物质组成,有时由多种物质组成如:乙烯氧化制环氧乙烷的银催化剂;丙烯氨氧化制丙烯腈用的钼和铋催化剂2%4%6%8%10%氨含量Mo的混合比Mo-Fe合金组成与活性关系活性组分的分类:二、载体载体是催化剂活性组分的分散剂、粘合剂和支撑物,是负载活性组分的骨架。
例如,乙烯氧化制环氧乙烷催化剂中的Ag就是负载在“α—Al2O3上的,这里的α—Al2O 3称为载体。
载体还常分为惰性载体与活性载体。
严格来说,催化剂中的组分都不是惰性的,都对主剂与助剂有所影响,只不过活性载体的作用更为明显而已。
载体的作用与助催化剂的作用在很多方面有类似之处,不同的是载体量大,助催化剂量小;前者作用较缓和,后者较明显。
另外,由于载体量大,可赋予催化剂以基本的物理结构与性能,如孔结构、比表面、宏观外形、机械强度等。
此外,对主催化剂和助催化剂起分散作用,尤其对贵金属既可减少其用量,又可提高其活性,降低催化剂成本。
作为高效催化剂,活性组分与裁体的选择都非常重要。
下面是载体的分类和部分常见载体的种类:催化剂的活性随载体比表面的增加而增加,为获得较高的活性,往往将活性组分负载于大比表面载体上。
载体与催化剂的活性、选择性、热稳定性、机械强度以及催化过程的传递特性有关,因此,在筛选和制造优良的催化剂时,需要弄清载体的物理性质和它的功能。
催化剂组分与含量的表示方法:例如:合成氨催化剂Fe—K2O—Al2O3用“—’将催化剂中的各组分隔开:加氢脱硫催化剂Co—Mo/α—Al2O3,斜线上为主剂和助剂,斜线下为载体。
各组分的含量可用重量%、重量比表示,也可用原子%、原子比表示。
载体的功能:⏹提供有效的表面和适宜的孔结构⏹增强催化剂的机械强度⏹改善催化剂的传导性⏹减少活性组分的含量⏹载体提供附加的活性中心⏹活性组分与载体之间的溢流现象和强相互作用理想的催化剂载体应具备的特性能适应某一特定反应的外形;有足够的抗破碎强度;有足够的反应表面和合适的孔结构;有足够的稳定性,包括活性稳定性与热稳定性;导热、热容量及堆密度适中;不含使催化剂中毒的物质;原料易得,载体制备过程简便。

工业催化剂概述详解工业催化剂是指在化学反应中起催化作用的物质。
催化剂可以增加反应速率,降低反应温度,提高产率和选择性,并且在反应结束后可以被回收和再利用。
工业催化剂广泛应用于石油化工、化学合成、环境保护和新能源等领域。
工业催化剂主要可分为贵金属、非贵金属、酸性催化剂和碱性催化剂四大类。
贵金属催化剂包括铂、钯、铑等贵金属,常用于催化氢气的加氢反应和有机物的氧化反应。
非贵金属催化剂主要包括氧化物、硅胶和金属催化剂。
氧化物催化剂广泛应用于氧化反应和脱氢反应,硅胶催化剂主要用于裂化反应和有机合成反应。
酸性催化剂具有高酸性,常用于酸催化反应如酯化、酸解和醇醚化等反应。
碱性催化剂具有高碱性,常用于碱催化反应如醇碱酯化和羰基化反应。
工业催化剂的活性主要取决于催化剂的结构和表面特性。
催化剂的结构可以是单一组分的金属或氧化物,也可以是复合物或复合催化剂。
表面特性包括表面活性位点和氧化还原特性。
表面活性位点是催化剂上能与反应物相互作用的活性位点,通常是金属或氧化物表面的缺陷或边缘位点。
氧化还原特性是催化剂在反应中通过催化剂表面上的氧化还原反应参与反应,并影响催化剂的活性。
工业催化剂的制备方法多种多样,常见的方法包括沉淀法、共沉淀法、共沉积法、浸渍法、共掺法和溶胶凝胶法等。
沉淀法是将催化剂前驱体溶液中的金属或氧化物通过加入一定的沉淀剂,使之沉淀成固体的方法。
浸渍法是将催化剂前驱体溶液通过浸渍方式使其渗透到载体中,并通过干燥和煅烧使前驱体转化为催化剂。
溶胶凝胶法是将催化剂前驱体逐渐溶解在溶胶中,然后通过凝胶化和热处理使之形成催化剂。
总之,工业催化剂在化学工业中发挥了重要的作用。
通过催化作用,催化剂能够加速化学反应,提高产率和选择性,降低能量消耗和环境污染。
随着科学技术的不断进步,工业催化剂的研究和发展将会为化学工业的可持续发展做出更大的贡献。

工业催化_催化剂的组成与功能工业催化是工业化生产过程中广泛应用的一种技术手段,它通过添加催化剂来加速化学反应的速率和选择性。
催化剂是催化反应中起到催化作用的物质,它能在反应中降低活化能,提高反应速率,并且在反应结束后能够重新生成。
催化剂的组成和功能是工业催化的核心内容,下面将详细介绍。
催化剂的组成主要有两个元素组成:载体和活性物质。
载体是催化剂中的固体物质,通常是一种高表面积的材料,如氧化铝、硅胶等。
载体具有高比表面积,能够提供更多的活性位点,增大反应物分子与催化剂的接触面积,从而提高反应速率。
活性物质是催化反应中发挥催化作用的物质,可以是金属、金属氧化物、金属盐等。
活性物质的选择通常是根据反应性质和催化剂制备条件来确定的。
催化剂的功能主要有两个方面:活化物质和提供反应路径。
活化物质是指催化剂能够降低反应物质的活化能,使反应物质易于发生化学反应。
在催化剂的作用下,反应物质的活化能降低,使得反应能够在较低的温度和压力下进行,从而节省能源、降低生产成本。
提供反应路径是指催化剂能够提供一个新的反应路径,使得反应路径更加有利于生成产物。
通过选择合适的催化剂,可以使得反应选择性增加,产物纯度提高,减少产生副产物的可能性。
催化剂的选择与催化反应有密切关系。
不同的催化反应需要选择不同的催化剂,以满足不同的反应条件和要求。
一般来说,催化剂的选择应考虑以下几个方面:反应活性、选择性、稳定性和成本。
反应活性是催化剂的重要指标,它反映了催化剂对反应物质的活化能降低效果。
选择性是指催化剂在反应中所产生的产物与副产物的选择性,选择性高的催化剂能够提高产品的纯度。
稳定性是指催化剂在反应过程中的稳定性,稳定性好的催化剂能够长时间使用,降低成本。
成本是指催化剂的制备成本和使用成本,成本低的催化剂更具有竞争力。
工业催化在许多领域有广泛的应用,例如石油化工、化学制品生产、气体处理、环境保护等。
在石油化工领域,工业催化用于石油加工、裂化、氢化、脱硫、脱氮等反应,能够提高石油产品的质量和产量。
第二章催化剂:一种能够与反应物相互作用,加速反应的速率而不改变反应的标准吉布斯自由焓变,且反应终结时本身保持不变的化学物质。
催化剂的特征: 特征1:催化剂只能加速热力学上可以进行的反应,而不能加速热力学无法进行的反应。
特征2:催化剂只能加速反应趋于平衡,不能改变平衡位置。
特征3:催化剂对反应具有选择性。
4:催化剂的寿命。
催化剂的组成:主催化剂、共催化剂、助催化剂(结构型助催化剂、电子型助催化剂)、载体结构型助催化剂:1、主要作用是提高活性组分的分散性和热稳定性。
使活性组分的细小晶粒间隔开来,不易烧结;与活性组分形成固熔体而达到热稳定,提高活性。
2、能起结构稳定作用的助催化剂,多为熔点较高、难还原的金属氧化物。
电子型助催化剂:1、作用是调整催化剂主要活性组分的电子结构、表面性质或晶形结构,从而提高催化剂的活性和选择性。
2、电子型助催化剂能使催化反应活化能降低。
电子和晶格缺陷两类助催化剂又合称调变性助催化剂。
载体的作用: 分散作用、稳定化作用、支撑作用、传热作用、助催化作用初级粒子,其尺寸多为埃级(10-10m),其内部为紧密结合的原始粒子;次级粒子,大小为微米级(10-6m),是由初级粒子以较弱的附着力聚集而成的。
催化剂颗粒是由次级粒子构成的(毫米级,10-3 m)对工业催化剂的要求:1、工业催化剂应具有适宜的活性、高选择性和长寿命。
2、工业催化剂的活性、选择性和寿命除决定于催化剂的组成结构外,与操作条件也有很大关系(包括原料的纯度、生产负荷、操作温度和压力等)。
3、催化剂的价格也需要考虑。
活性:衡量催化剂效能大小,表示催化剂加快化学反应速率程度的一种度量。
时空产率:指在一定条件(温度、压力、进料组成、空速)下,单位时间内,使用单位体积或单位质量的催化剂所能得到目的产物的量(摩尔数NB、或质量)来表示。
比活性:对于固体催化剂,与催化剂单位表面积相对应的活性称为比活性(α)。
α=k/S;k--催化反应速度常数;S---活性比表面积。
工业上常用的催化剂类型催化剂是在化学反应中被添加到反应物中,以加速反应速度或降低反应所需的温度和能量成本的一种物质。
在工业上,催化剂的应用已经成为必不可少的环节。
本文将讨论工业上常用的催化剂类型,并介绍其在工业上的应用。
一、氧化剂类催化剂氧化剂类催化剂主要是将一种物质氧化成另一种物质,常用于化学反应中,例如制造化学品。
氧化剂类催化剂的常见类型如下:1.铬酸催化剂铬酸催化剂是一种常见的氧化剂类催化剂。
它的主要成分是铬酸盐,它被广泛应用于石油化学、有机合成和涂料工业中。
铬酸催化剂具有高活性、较好的选择性和灵活的反应条件等特点。
2.过氧化氢催化剂过氧化氢催化剂是另一种常见的氧化剂类催化剂。
它的主要成分是过氧化氢,通常被用于加氢过程的催化剂中。
过氧化氢催化剂在制造化学品、食品和饮料制造过程中起着重要的作用。
二、还原剂类催化剂还原剂类催化剂是将一种物质还原成另一种物质的催化剂类别。
这种类型的催化剂通常用于制造化学品和制造非化学生产过程中。
还原剂类催化剂的常见类型如下:1.氢化镍催化剂氢化镍催化剂是一种常见的还原剂类催化剂。
其主要成分是氢化镍,通常与氢气反应以降低化合物的不饱和度。
氢化镍催化剂在化学品、塑料和医药工业中广泛应用。
2.钼酸催化剂钼酸催化剂是另一种常见的还原剂类催化剂。
其主要成分是钼酸盐,通常用于减少氧化物和酸化物。
它在石油、汽车和航空工业中有广泛应用。
三、酸性催化剂酸性催化剂是化学反应中使用的常见催化剂之一。
酸性催化剂通常用于促进纳米级反应(与原始分子密度相似的化学反应)。
酸性催化剂的常见类型如下:1. 硫酸催化剂硫酸催化剂是一种常见的酸性催化剂。
硫酸催化剂通常由硫酸和水混合而成。
它在制造投资和金属生产中起着重要作用。
2. 磷酸催化剂磷酸催化剂是另一种常见的酸催化剂。
其主要成分是磷酸盐。
磷酸催化剂通常在化学品制造和农业生产中使用。
四、基础型催化剂基础型催化剂是另一种催化剂类型。
基础型催化剂可用于不同类型的反应,与酸性催化剂截然不同。
1.催化剂的定义是:催化剂是一种能够改变一个化学反应的反应速度,却不改变化学反应热力学平衡位置,本身在化学反应中不被明显地消耗的化学物质.2.催化作用是指催化剂对化学反应所产生的效应。
3.催化剂的基本特征:1)催化剂只能加速热力学上可以进行的反应,而不能加速热力学上无法进行的反应。
2)催化剂只能加速反应趋于平衡,不能改变平衡的位置(平衡常数)。
3)催化剂对反应具有选择性;4)催化剂的寿命。
4.工业催化剂一般有哪些组分组成?各组分具有什么功能?①活性组分:提供改变反应历程的组分,多为金属、氧化物、酸碱②载体组分:提供高的比表面积、孔结构、活性组分的分散剂、粘合剂、或支撑体.多数为硅和铝的氧化物③助催化剂组分:催化剂的辅助组分,本身没有活性或者活性很低,用于活性组分或载体改性。
5.载体的功能主要体现在哪几个方面?(分散作用、稳定作用、支撑作用,传热和稀释作用、助催化作用)①提供适宜的比表面和孔结构②维持催化的形状和机械强度③改善催化剂热传导性④提高催化剂中活性组分分散度⑤提供附加活性中心⑥活性组分和载体的溢流现象和强相互作用6.催化剂的反应性能是评价催化剂好坏的主要指标,它包括催化剂的活性、选择性和稳定。
7。
多相催化反应过程中,从反应物到产物一般经历哪些步骤包括五个连续的步骤。
(1)反应物分子从气流中向催化剂表面和孔内扩散;(2)反应物分子在催化剂表面上吸附;(3)被吸附的反应物分子在催化剂表面上相互作用或与气相分子作用进行化学反应;(4)反应产物自催化剂表面脱附;(5)反应产物离开催化剂表面向催化剂周围的介质扩散。
8.当气体与固体表面接触时,固体表面上气体的浓度高于气相主体浓度的现象称为吸附现象。
9.几种等温吸附等温吸附平衡过程用数学模型方法来描述可得到等温方程,其中包括:Langmuir(朗格缪尔)等温方程,Freundlich(弗郎得力希)等温方程,T}MKI}IH(焦姆金)等温方程及BET(Brunauer,Emmett及Teller)等温方程等。
一、绪论1、环境催化:它是指运用催化剂控制或消除环境有害化学物质的排放,运用催化技术生产少污染或无污染、废弃物最少的有价值的新产品工艺。
2、生物催化:是利用生物催化剂(主要是酶或微生物)来改变(通常是加速)化学反应的速率。
确切地说是利用微生物代谢过程中某个酶或一组酶对底物进行催化反应。
3、择形催化:沸石它具有规则的孔道和孔笼结构,宽敞的通道和孔道,可限制及区分进出的分子,使其具有形状和大小选择性的催化。
4、手性催化:包括均相手性催化和多相手性催化两大体系。
二、催化作用与催化剂1、催化剂:是一种物质,它能够加速反应的速率而不改变该反应的标准Gibbs自由焓变化。
这种作用称为催化作用。
涉及催化剂的反应称为催化反应。
2、催化作用具有4个基本特征:(1)催化剂只能加速热力学上可以进行的反应,而不能加速热力学上无法进行的反应。
(2)催化剂只能加速反应趋于平衡,而不能改变平衡的位置(平衡常数)。
催化作用不能改变化学平衡。
(3)催化剂对反应具有选择性(4)催化剂具有寿命。
3、催化剂三个重要指标:活性、选择性和稳定性。
4、催化剂的组成和功能:(1)活性组分:催化剂的主要成分,发挥化学活性(2)助催化剂:对活性组分或载体改性(3)载体:提供表面和孔结构、提高机械强度等。
5、催化剂的分类:1)按催化过程分:均相、多相、酶催化剂。
2)按所具有的催化功能分:氧化还原、酸碱、双功能催化剂。
3)按所催化的具体反应类型分:氧化、加氢、脱氢、异构、环化等催化剂。
4)按催化剂在使用条件下的物态分:过渡金属催化剂;金属氧化物催化剂;金属硫化物催化剂;固体酸催化剂;过渡金属络合物催化剂等。
6、助催化剂:简称助剂,也称促进剂。
它是催化剂中占量较少的物质,虽然它本身常无催化活性,但是加入后可以大大提高主催化剂的活性、选择性和寿命,改善催化剂性能。
分类:(1)结构型助剂(惰性助剂)(2)调变型助剂:包括电子助剂和晶格缺陷助剂。
7、载体:是指担载活性组分和助催化剂的催化剂组分。
《工业催化》考点汇总(历年真题汇总)一、名词解释题1.催化剂答:催化剂是一种物质,它能够加速反应的速率而不改变该反应的Gibbs自由焓变化。
2.催化作用答:催化剂是一种物质,它能够加速反应的速率而不改变该反应的Gibbs自由焓变化.将这种催化剂引起的作用称之为催化作用.3.催化反应答:催化剂是一种物质,它能够加速反应的速率而不改变该反应的Gibbs自由焓变化。
把涉及催化剂的反应称之为催化反应.4.活化能答:分子从常态转变为容易发生化学反应的活跃状态所需要的能量称为活化能。
(活化能是指化学反应中,由反应物分子到达活化分子所需的最小能量)5.表观活化能答:对于复杂反应,如果得到有明确级数的总反应速率方程,则总反应的活化能是各基元反应活化能的代数和,即:a=E1+1/2E2+E—1这时Ea称为总包反应的表观活化能。
6.催化剂的失活答:催化剂在长期的受热和化学作用下,经受了一系列不可逆的物理、化学的变化,如:晶相变化、晶粒分散度的变化、易挥发组分的流失、易熔物的熔融等.这些过程导致催化剂的活性逐渐降低直至消失。
其失活过程可划分为三种类型:中毒失活,积碳堵塞失活,烧结、挥发与剥落失活。
7.催化剂载体答:载体是催化活性组分的分散剂、粘合物或支撑体,是负载活性组分的骨架。
载体有以下功能:1.提供有效的表面和适宜的孔结构(维持活性组分高分散度)。
2.增强催化剂的机械强度,使其具有一定的形状。
3.改善催化剂的传导性。
4。
提供附加的活性中心.5。
减少活性组分的含量.6。
活性组分与载体之间的溢流现象和强相互作用.8.原子经济反应答:原子经济性是绿色化学以及化学反应的一个专有名词。
绿色化学的“原子经济性"是指,在化学品合成过程中,合成方法和工艺应被设计成能把反应过程中所用的所有原材料尽可能多的转化到最终产物中。
原子经济性/%=(被利用原子的质量/反应中所用全部反应物原子的质量)X 100原子利用率达到100%的反应有两个最大的特点:1。
《工业催化》教学大纲一、课程基本信息课程中文名称:工业催化课程英文名称:Industrial Catalysis课程编号:06141191课程类型:专业(方向)课总学时:36学分:2.0适用专业:化学工程与工艺(无机化工)专业先修课程:基础化学、有机化学、物理化学、化工原理开课院系:化工与制药学院二、课程的性质与任务本课程论述催化作用的基本原理,工业催化剂的基本要求,热力学平衡原理对催化作用的制约,介绍各类催化剂及其催化作用,并介绍催化剂的组成、制备原理和方法,催化实验用的反应器和检测仪器、手段等。
让学生掌握催化作用的基本规律,了解催化过程的化学本质和熟悉工业催化技术的基本要求和特性,为培养化工工艺类专业工程师提供坚实的理论基础服务。
三、课程教学基本要求通过本课程的学习,让学生掌握催化作用的基本规律和基本原理,工业催化剂的基本要求,理解热力学平衡原理对催化作用的制约。
掌握各类催化剂及其催化作用,包括固体酸碱催体、分子筛催化、金属催化、络合催化、金属氧化物和金属硫化物催化等,并了解催化剂的组成、制备原理和方法,催化实验用的反应器和检测仪器、手段等。
熟悉工业催化技术的基本要求和特性,为培养化工工艺类专业工程师提供坚实的理论基础服务。
四、理论教学内容和基本要求第一章催化作用与催化剂第一节催化作用的定义与特征;第二节催化剂的组成与功能;第三节对工业催化剂的要求;第四节均相催化与均相催化简介第二章吸附作用与多相催化:第一节多相催化的反应步骤;第二节吸附等温线;第三节金属表面上的化学吸附;第四节氧化物表面上的化学吸附第三章各类催化剂及其催化作用:第一节酸碱催化剂及其催化作用;第二节分子筛催化剂及其催化作用;第三节金属催化剂及其催化作用;第四节金属氧化物和硫化物催化剂及其催化作用;第五节络合催化剂及其催化作用第四章工业催化剂的制备与使用:第一节工业催化剂的制备;第二节工业催化剂的使用第五章工业催化剂的活性评价与宏观物性的表征:第一节催化剂活性测试的基本概念;第二节催化剂活性的测定;第三节催化剂的宏观物性及其测定五、有关教学环节的要求教学以课堂教学、老师讲授为主,开展启发式教学,鼓励学生提出问题,展开讨论,最后进行归纳总结。