盐类水解的应用
- 格式:doc
- 大小:35.50 KB
- 文档页数:2

盐类水解的应用及原理1. 应用•盐类水解在食品加工中的应用–调味剂:盐类水解可以增加食品的鲜味,提升口感。
–食品防腐:盐类水解可以抑制食品中细菌的繁殖,延长食品的保质期。
•盐类水解在化妆品中的应用–护肤品:盐类水解可以改善皮肤质地,增加皮肤的保湿性。
–洗发水:盐类水解可以去除头皮屑,并增强发质。
•盐类水解在农业中的应用–作物生长促进:盐类水解可以为作物提供氮、磷、钾等营养元素,促进作物的生长。
–土壤改良:盐类水解可以调节土壤的酸碱度和结构,改良土壤的肥力。
2. 原理盐类水解是指盐类在水中离子化的过程,其中溶解的盐分解成阳离子和阴离子。
盐类在水中水解的原理主要包括以下几个方面:•水的极性:水是一种极性分子,具有正负两极,使得离子能够在水中溶解而发生水解。
•离子间作用力:水中的离子与其他离子或极性分子发生静电作用,增加了离子在水中溶解的可能性。
•晶格能:溶解盐时需要克服盐晶格的结合力,这需要提供一定的能量,使得水解过程变得不可逆。
•水解反应:盐的水解反应使得盐解离成其阳离子和阴离子。
水解反应的速率与盐的溶解度、水的温度和压力等因素有关。
3. 盐类水解的应用案例3.1 食品加工中的应用案例•味精的制备:味精是一种常用的调味品,制备味精需要通过盐类水解,使得谷氨酸钠被水解并形成味精。
•肉类加工中的腌制:盐类水解在肉类加工中的腌制过程中起到调味和防腐的作用,增加肉质的鲜嫩。
•熟食加工中的使用:盐类水解可以加速熟食中的食材的水解和溶解,提高熟食的风味和质量。
3.2 化妆品中的应用案例•护肤品中的使用:盐类水解通过提供皮肤所需的营养物质,有助于保护皮肤和改善皮肤质地。
•洗发水的配方:盐类水解可以通过调节头皮的酸碱度,清洁头皮并去除头皮屑,改善发质。
3.3 农业中的应用案例•土壤改良:通过添加盐类水解制剂到土壤中,可以改善土壤的结构和肥力,促进作物的生长。
•肥料制备:盐类水解可以将肥料中的营养元素分解为可供作物吸收的形式,提高肥料的效率。



盐类水解的应用
1 什么是盐类水解
盐类水解是一种化学分解过程,其特点是原料分子不改变,只是改变了它们之间的键类型。
在盐类水解反应中,原料分子中的碳-碳键(甚至C-三价和其他碳-元素键)被水分解,产生氢键和非碳原子的位置焕发的反应,从而分离其中的分子。
2 盐类水解的原理
盐类水解的主要反应就是原料分子中的碳-碳键由于水的存在而发生分解,从而使原料分子的结构逐步发生变化,分离出不同的物质分子。
在反应过程中,水分子攻击到碳碳键中的其中一个碳原子上,然后,由于另一个碳原子失去单电子,形成一种新的价态和结构,从而使原分子分解成新的产物。
3 盐类水解的应用
盐类水解最常见的应用是化学工业中的有机合成。
因为盐类水解反应的扩散速率比偶联反应快,特别适用于合成有机物中含羟基的大分子,可以比较快地进行有机合成反应。
此外,盐类水解还可以用于食品、药物、纤维素或橡胶等生物活性物质的分子重组或分解,也可以将其分解成更小的分子,从而改变物理或化学性质。

盐类水解应用的例子
盐类水解应用的例子
1. 食用食品:食用盐水解可以提取水溶性营养成分,如维生素、蛋白质、淀粉等,从而制作出更美味的食品。
2. 工业化学:盐类水解可把植物油或动物油中的脂肪和油脂分解成小分子的物质,从而制作润滑剂、漆、清洁剂等产品。
3. 生物工程:盐类水解可分解细胞壁和蛋白质,获取植物细胞和蛋白质的隐藏组分,从而制造植物细胞培养基、基因技术产物等生物制品。
4. 生物酶:盐类水解可分解生物体内的蛋白质,提取活性酶,并掩盖酶的活力,从而制备各种酶制剂、细胞分析剂、实验试剂等产品。
5. 农业:盐类水解可分解植物细胞壁,从而得到植物细胞壁的组分,如有机酸、碳水化物等,从而研制出植物生长调节剂和农药。
- 1 -。

盐类的水解应用1. 哎呀,今天咱们来聊聊盐类水解这个有趣的话题!化学老师总说:"盐类水解就像是化学界的变色龙,能让溶液显现不同的酸碱性,在生活中可有大用处啦!"2. 小明家种花时,妈妈总爱用硫酸铝调节土壤。
老师解释说:"这就是盐类水解的应用啊,硫酸铝遇水后,就像个魔法师,能让土壤变酸,某些花儿就特别喜欢这种环境。
"3. 做豆腐时放的石膏,也是利用盐类水解原理。
张奶奶笑着说:"以前不懂为啥石膏能让豆浆变成豆腐,原来是水解在起作用,就像变魔术一样!"4. 李叔叔家的鱼塘用生石灰调节水质。
"这也是盐类水解的妙用,"化学老师说,"生石灰遇水后就像个清道夫,能调节水质酸碱度,让鱼儿住得舒服。
"5. 化肥里的磷酸铵施到地里,也会发生水解。
农业专家王大叔说:"这就像给庄稼准备了一桌营养大餐,水解后的物质正好被庄稼吸收。
"6. 小红家用明矾洗菜,老师说:"明矾遇水后的水解反应,就像个小警察,能抓住蔬菜里的脏东西。
"7. 制药厂利用碳酸钠水解制取某些药物。
厂里的张工程师说:"这个过程就像是化学界的厨师,把复杂的原料'烹饪'成药物。
"8. 纺织厂用醋酸铝处理布料。
"这是利用醋酸铝水解产生的胶体,"老师解释说,"就像给布料穿上了一件防水衣。
"9. 造纸厂用明矾做纸张增白剂。
小华参观造纸厂时问:"为啥要用明矾啊?"工人师傅说:"明矾水解后就像个画家,能让纸张变得又白又亮。
"10. 食品工业中,碳酸氢钠的水解让面团发松。
面包师傅说:"这就像给面团装了个小气球,让面包松松软软的。
"11. 化妆品中也有盐类水解的应用。
化妆品研发师说:"某些金属盐的水解产物就像天然的护肤品,能调节皮肤的酸碱度。

盐类水解的应用应用一:判断溶液的酸碱性——强者显性Na2CO3溶液呈碱性的原因是:CO2-3+H2O HCO-3+OH-应用二:判断盐溶液离子的种类及浓度的大小如Na2CO3溶液中存在的粒子有:Na+、CO2-3、H2CO3、HCO-3、OH-、H+、H2O,且c(Na+)>2c(CO2-3),c(OH-)>c(H +)。
应用三:判断离子能否共存若阴、阳离子发生水解相互促进的反应,水解程度较大而不能大量共存,有的甚至水解完全。
常见的水解相互促进的反应进行完全的有:Fe3+、Al3+与AlO-2、CO2-3(HCO-3)。
应用四:判断盐溶液蒸干时所得的产物(1)盐溶液水解生成难挥发性酸和酸根阴离子易水解的强碱盐,蒸干后一般得原物质,如CuSO4(aq)蒸干得CuSO4(s);Na2CO3(aq)蒸干得Na2CO3(s)。
(2)盐溶液水解生成易挥发性酸时,蒸干灼烧后一般得对应的氧化物,如AlCl3(aq)蒸干得Al(OH)3灼烧得Al2O3。
(3)考虑盐受热时是否分解。
Ca(HCO3)2、NaHCO3、KMnO4、NH4Cl固体受热易分解,因此蒸干灼烧后分别为Ca(HCO3)2―→CaCO3(CaO);NaHCO3―→Na2CO3;KMnO4―→K2MnO4和MnO2;NH4Cl―→NH3↑+HCl↑。
(4)还原性盐在蒸干时会被O2氧化如Na2SO3(aq)蒸干得Na2SO4(s)。
(5)弱酸的铵盐蒸干后无固体。
如NH4HCO3、(NH4)2CO3。
应用五:保存、配制某些盐溶液如配制FeCl3溶液时,为防止出现Fe(OH)3沉淀,常加几滴盐酸来抑制FeCl3的水解;在实验室盛放Na2CO3、CH3COONa、Na2S等溶液的试剂瓶不能用玻璃塞,应用橡胶塞。
应用六:水解除杂如MgCl2溶液中混有少量FeCl3杂质,因Fe3+的水解程度比Mg2+水解程度大,可加入MgO或Mg(OH)2或MgCO3等,使Fe3+的水解平衡右移,生成Fe(OH)3沉淀而除去。


例析盐类水解的十大应用
盐类水解是一种重要的化学反应,它可以将盐类分解成其他化合物,并产生一些有用的物质。
盐类水解的十大应用如下:
1、制造食品添加剂:盐类水解可以用来制造食品添加剂,如酸味剂、香料、色素等,以改善食品的口感和外观。
2、制造医药:盐类水解可以用来制造一些药物,如抗生素、抗病毒药物、抗炎药物等,以治疗疾病。
3、制造清洁剂:盐类水解可以用来制造清洁剂,如洗衣粉、洗洁精等,以清洁衣物和家具。
4、制造润滑剂:盐类水解可以用来制造润滑剂,如机油、润滑油等,以润滑机械设备。
5、制造燃料:盐类水解可以用来制造燃料,如汽油、柴油等,以满足人们的能源需求。
6、制造化妆品:盐类水解可以用来制造化妆品,如护肤霜、粉底液等,以改善人们的外观。
7、制造染料:盐类水解可以用来制造染料,如染料、染料等,以染色纺织品。
8、制造纸张:盐类水解可以用来制造纸张,如纸张、纸板等,以满足人们的文具需求。
9、制造精细化工产品:盐类水解可以用来制造精细化工产品,如涂料、油漆等,以改善人们的生活质量。
10、制造环保产品:盐类水解可以用来制造环保产品,如污水处理剂、污水处理设备等,以保护环境。
以上就是盐类水解的十大应用,它们在食品、医药、清洁剂、润滑剂、燃料、化妆品、染料、纸张、精细化工产品和环保产品等方面都有着重要的作用。

盐类水解的应用概念盐类水解是指盐类在水中发生水解反应,产生酸性或碱性溶液的过程。
在化学中,盐类是由阳离子和阴离子组成的化合物,当盐类溶解在水中时,阳离子和阴离子会与水分子发生反应,形成酸性或碱性的溶液。
盐类水解在生活和工业中有着广泛的应用,下面将详细介绍盐类水解的应用概念。
1. 盐类水解在生活中的应用:a. 调节酸碱平衡:盐类水解可以用于调节酸碱平衡,例如在烹饪中,我们常常使用食盐(氯化钠)来调味,食盐溶解在水中会产生氯离子和钠离子,氯离子可以与水分子发生水解反应,产生酸性溶液,而钠离子则可以与水分子发生水解反应,产生碱性溶液,从而调节食物的酸碱度。
b. 调节水质:盐类水解可以用于调节水质,例如在游泳池中,我们常常使用氯化钠来消毒水质,氯化钠溶解在水中会产生氯离子和钠离子,氯离子可以与水中的有机物发生反应,起到消毒的作用,从而保证游泳池水的卫生安全。
c. 调节土壤酸碱度:盐类水解可以用于调节土壤的酸碱度,例如在农业中,我们常常使用石灰来调节土壤的酸碱度,石灰溶解在水中会产生氢氧根离子和钙离子,氢氧根离子可以与土壤中的酸性物质发生反应,中和土壤的酸性,从而改善土壤的肥力。
2. 盐类水解在工业中的应用:a. 制备酸碱溶液:盐类水解可以用于制备酸碱溶液,例如在化学实验室中,我们常常使用氯化氢溶液来调节实验的酸碱度,氯化氢溶液是由氯化氢盐类水解产生的酸性溶液。
b. 制备金属:盐类水解可以用于制备金属,例如在冶金工业中,我们常常使用氯化铝来制备铝金属,氯化铝溶解在水中会产生氯离子和铝离子,铝离子可以与水分子发生反应,生成氢气和氢氧根离子,氢氧根离子与铝离子反应生成氢氧化铝,进一步还原生成铝金属。
c. 制备化学品:盐类水解可以用于制备化学品,例如在化工工业中,我们常常使用氯化钠来制备氯气和氢氧化钠,氯化钠溶解在水中会产生氯离子和钠离子,氯离子可以与水分子发生反应,生成氯气,而钠离子则与水分子发生反应,生成氢氧化钠。
盐类水解原理的应用
盐类水解是指盐在水中溶解后,离子会与水分子发生反应,水分子同时接受和释放H+离子,从而形成酸性或碱性溶液的化学反应。
盐类水解的应用包括:
1. 食品加工:盐类水解可调节食品溶液的pH值,增强食品的味道和保存时间。
2. 化学分析:盐类水解可用于分析化学实验中,测量酸性或碱性。
3. 工业生产:盐类水解可用于纺织、皮革、造纸、金属加工等工业生产中,调节反应环境,改变反应结果。
4. 医学应用:盐类水解可用于医学诊断与治疗上。
如碳酸氢钠的水解可使人体血液酸性度下降,有助于治疗酸中毒。
总之,盐类水解是化学领域中的一个重要现象,在许多领域都有广泛的应用。
盐类水解的应用
盐类水解是指将盐类物质(如氯化钠)分解成其中的离子,这是一种重要的化学反应,在医药、食品、纺织和其他行业中都有着重要的应用。
盐类水解可以用来提取有用成分,例如,在医药行业,可以将有机物质分解成碳水化合物、氨基酸和其他有效成分,从而提取活性物质,用于制药、研究和生产药物。
此外,盐类水解还可以用于食品加工,以提取食品中的有效成分,例如蛋白质,以及制造食品添加剂,以增加食品的口感和营养价值。
此外,盐类水解还可以用于纺织行业。
纤维制成的衣物可以通过水解成碱性物质,通过这种方式来改善纤维的性能,使其更有弹性、耐磨性和耐腐蚀性。
另外,盐类水解还可以用于石油行业,将石油分解成烃类物质,从而制造汽油、柴油等燃料。
总之,盐类水解有着广泛的应用,可以用于医药、食品、纺织、石油等行业,为各行各业的发展提供了重要的帮助。
盐类水解的应用一、在生活中的应用1、去污:纯碱具有去污作用,加热后,去污能力增强,原因是碳酸钠溶液水解显碱性,且温度升高水解程度增大,碱性增强,油脂在碱性条件下水解为溶于水的高级脂肪酸盐和甘油。
2、泡沫灭火器原理:成分为NaHCO 3与Al 2(SO 4)3,发生反应的方程式为:3、明矾净水原理:明矾溶于水电离出的Al 3+水解 (写水解方程式),生成的Al(OH)3具有吸附性,可吸附水中杂质,达到净水的效果。
4、化肥的使用:铵态氮肥与草木灰(主要成分为K 2CO 3)不得混用,原因:CO 32-与NH 4+发生双水解 (写方程式),NH3挥发到空气中,氮元素损失,铵态氮肥肥效降低。
5、除锈剂:NH 4Cl 与ZnCl 2溶液可作焊接时的除锈剂,原因:NH 4Cl 与ZnCl 2溶液因NH 4+和Zn 2+水解而显酸性,铁锈(Fe 2O 3)会溶于该酸性溶液。
二、在实验中的应用1、配制或贮存易水解的盐溶液:加入相应的酸或碱抑制其水解eg :(1)配制CuSO 4溶液时,加入少量 ,防止Cu 2+水解;(2)贮存Na 2CO 3溶液、Na 2SiO 3溶液的试剂瓶要用 塞而不用磨口玻璃塞原因:(3)如何配制FeCl 3溶液?(4)保存FeCl 2溶液时,需要加入铁粉,目的是2、Fe(OH)3胶体的制备方法为: 方程式为:3、盐溶液蒸干所得产物的判断(1)蒸干后得原物质:强碱盐、弱碱的难挥发性酸盐eg :Na 2CO 3 (aq)――→蒸干( ) KAl(SO 4)2 (aq)――→蒸干( )(2)蒸干后得水解产物:弱碱的易挥发性酸盐,再灼烧得氧化物eg :AlCl 3(aq)――→蒸干 ( )――→灼烧( )。
FeCl 3(aq)――→蒸干 ( )――→灼烧( )。
(3)蒸干或灼烧后得分解产物:受热易分解的物质eg : Ca(HCO 3)2―→CaCO 3(CaO); NaHCO 3―→Na 2CO 3;KMnO 4―→K 2MnO 4+MnO 2; NH 4Cl ―→NH 3↑+HCl ↑。
盐类水解的应用
1、判断盐溶液的酸碱性和比较盐溶液酸碱性的强弱时,通常需考虑盐的水解。
例1:相同条件,相同物质的量浓度的下列八种溶液:Na2CO3、NaClO、NaAc、Na2SO4、NaHCO3、NaOH 、(NH4)2SO4、NaHSO4等溶液,PH值由大到小的顺序为:
(NaOH—NaClO—Na2CO3—NaHCO3—NaAc—Na2SO4—(NH4)2SO4—NaHSO4)
例2、相同条件下测得①NaHCO3②CH3COONa③NaClO三种稀溶液的PH值相同,则它们的摩尔浓度由大到小的关系是() C
A.①②③
B.③①②
C.②①③
D.③②①
2、比较盐溶液中各离子浓度的相对大小时,当盐中含有易水解的离子,需考虑盐的水解。
例3:25℃时,在浓度均为1mo/L的(NH4)2SO4、(NH4)2CO
3、(NH4)2Fe(SO4)2三种溶液中,若测得其中[NH4+]分别为a、b、c(单位为mo/L),则下列判断正确的是()B
A.a=b=c
B.c>a>b
C.b>a>c
D.a>c>b
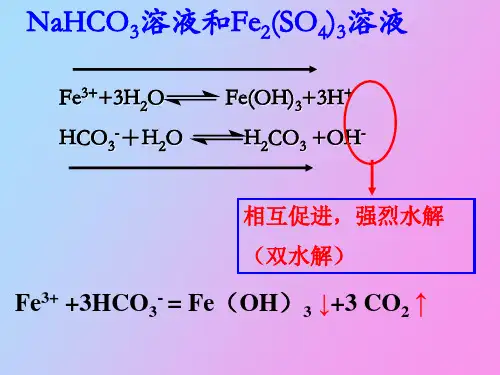
3、双水解的应用—泡沫灭火器的原理思考1:泡沫灭火器内玻璃桶内盛硫酸铝溶液、铁桶内盛碳酸氢钠溶液,说明反应原理。
双水解反应:两种盐单独水解时,一个显较强的酸性,一个显较强的碱性,但毕竟水解程度都很小,不能进行到底;若混合时,则因彼此互相促进而进行到底。
常见能发生双水解的有:Al3+,Fe3+,AlO2-HCO3-,S2-,ClO-等。
4、判断溶液中离子能否大量共存。
当有弱碱阳离子和弱酸阴离子之间能发出双水解,则不能在溶液中大量共存。
思考2:用盐类水解的知识解释Al3+和AlO2-在溶液中为什么不能共存。
、用盐溶液来代替酸碱例如:“焊药”—金属焊接时常用于除去金属表面的氧化膜,常用ZnCl2、NH4Cl。
思考3:金属镁与水反应比较困难,若加一些NH4Cl马上产生大量气体?为什么?写出相应的方程式。
6、在实际生产和生活中的运用。
(1)配制溶液:容易水解的盐溶液配制时要抑制水解以防止浑浊。
思考4:①为什么配制AlCl3溶液时要加入适量的盐酸?
②配制Al2(SO4)3怎么做,配制Na2SiO3溶液时呢?
(2)蒸发结晶:若希望通过蒸发结晶来得到溶质晶体,则要考虑水解因素。
思考5:将AlCl3溶液加热蒸发,最终析出的固体是什么?为什么?那么如何使AlCl3析出?如果是蒸发Al2(SO4)3和Na2CO3溶液有什么不同?
(3)选择制备盐的途径时,需考虑盐的水解。
如制备Al2S3时,因无法在溶液中制取,会完全水解,只能由干法直接反应制取。
(4)试剂瓶的选用:
说明盛放Na2S Na2CO3的试剂瓶不能用玻璃塞的原因,NaF溶液能否用玻璃瓶?例4:实验室有下列试剂:①NaOH溶液②水玻璃③Na2S溶液④Na2CO3溶液⑤NH4Cl溶液⑥澄清石灰水⑦浓硫酸,其中必须用带橡胶塞的试剂瓶保存的是 B
A.①⑥ B。
①②③④⑥ C。
①②③⑥ D。
①②③④
(5)除杂:例5:为了除去氯化镁酸性溶液中的Fe3+离子,可在加热搅拌下加入一种试剂,过滤后再加入适量盐酸。
这种试剂是()AD
A.氧化镁 B.氢氧化钠 C.碳酸钠 D. 碳酸镁(6)化肥的使用——
草木灰不能和铵态氮肥混合使用,为什么?
例6、为了同时对某农作物施用分别含有N、P、K三种元素的化肥,对于给定的化肥:①K2CO3②KCl ③Ca(H2PO4)2④(NH4)2SO4⑤氨水,最适合的组合是 B
A.①③④ B。
②③④ C。
①③⑤ D。
②③⑤
思考6:Mg(OH)2不溶于水但溶于NH4Cl溶液中
思考7:酸式盐的水溶液一定显酸性吗?。