《元素周期表》(元素周期表的结构)
- 格式:ppt
- 大小:4.46 MB
- 文档页数:39

一、一、元素周期表及其结构1.编排原则(1)周期:把电子层数相同的元素按原子序数递增顺序从左到右排列成一横行。
(2)族:把不同横行中最外层电子数相同的元素,按电子层数递增的顺序从上到下排成一纵行。
2.结构(1)周期(7个横行,7个周期):短周期长周期序号1234567元素种数288181832320族元素原子序数21018365486118(2)族(18个纵行,16个族)主族列121314151617族ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 副族列345671112族ⅢBⅣBⅤBⅥBⅦBⅠBⅡBⅧ族第8、9、10,共3个纵行0族第18纵行3.元素周期表中元素的分区4.元素周期表中必记的4个关系(1)常见的四组等量关系①核电荷数=质子数=原子序数;②核外电子层数=周期序数;③主族序数=最外层电子数=最高正价;④非金属元素:最低负价=最高正价−8。
(2)同主族元素的原子序数差的关系①位于过渡元素左侧的主族元素,即第ⅠA、第ⅡA族,同主族、邻周期元素原子序数之差为上一周期元素所在周期所含元素种数;②位于过渡元素右侧的主族元素,即第ⅢA~第ⅦA族,同主族、邻周期元素原子序数之差为下一周期元素所在周期所含元素种数。
例如,氯和溴的原子序数之差为35−17=18(溴所在第四周期所含元素的种数)。
(3)同周期第ⅡA族和第ⅢA族元素原子序数差的关系周期序数1234567原子序数差无1111112525增加了过渡元素和原因——增加了过渡元素镧系或锕系元素(4)奇偶关系①原子序数是奇数的主族元素,其所在主族序数必为奇数;②原子序数是偶数的主族元素,其所在主族序数必为偶数。
二、元素周期表的应用考向一元素周期表的结构典例1如图为元素周期表中前四周期的一部分,若B元素的核电荷数为x,则这五种元素的核电荷数之和为A.5x+10B.5x C.5x+14D.5x+16【解析】【答案】A【规律总结】同主族、邻周期元素的原子序数差的关系①ⅠA族元素,随电子层数的增加,原子序数依次相差2、8、8、18、18、32。

元素周期表的结构1 .原子序数:按照元素在周期表中的顺序给元素编号,称之为原子序数,原子序数=核电荷数=质子数=核外电子数。
2 .编排原则⑴周期:把电子层数相同的元素,按原子序数递增的顺序,从左至右排成的横行。
(2)族:把最外层电子数相同的元素,按电子层数递增的顺序,从上至下排成的纵行。
3 .元素周期表的结构L 口[第一、二、三周期短周期 <[元素种数分别为2、8、8种周期"个)口]第四、五、六、七周期长周期1元素种数分别为18、18、32、32(排满时)种〃主族:由短周期和长周期共同构成,共7个副族:完全由长周期元素构成,共7个第VI 族:第8、9、10共3个纵行 2族:第18纵行⑴元素周期表中位于金属与非金属分界线附近的元素属于过渡元素(X) ⑵第IA 族全部是金属元素(X)⑶元素周期表中镧系元素和锕系元素都占据同一格,它们是同位素(X)(4)两短周期元素原子序数相差8,则周期数一定相差1(J)请在下表中画出元素周期表的轮廓,并在表中按要求完成下列问题: ⑴标出族序数。
⑵画出金属与非金属的分界线,写出分界线处金属的元素符号,并用阴影表示出过渡元素的位置。
⑶标出锢系、钢系的位置。
<族(16个)(4)写出各周期元素的种类。
⑸写出稀有气体元素的原子序数。
(6)标出113号〜118号元素的位置。
答案题组一元素周期表的结构应用1.在元素周期表中,伯元素如图所示,下列有关说法正确的是()A.铂是非金属元素,在常温下呈固态B.208Pt和%8Pt的核外电子数相同,互为同位素C."195.1”是铂的质量数D.由78可以推出Pt为第五周期元素答案B解析铂为金属元素,A项错误;208Pt和1788Pt的质子数相同,中子数不同,是两种不同的核素,二者互为同位素,B项正确;“195.1”是铂元素的相对原子质量,C项错误;由78推出Pt为第六周期元素,D 项错误。
题组二周期表的片段在元素推断题中的应用2.A、B、C均为短周期元素,它们在周期表中的位置如图所示。


第一章物质结构元素周期律第一节元素周期表重难点一元素周期表1.构成原子(离子)的微粒间关系(1)原子序数=核电荷数=核内质子数=核外电子数(原子中)。
(2)离子电荷数=质子数-核外电子数。
(3)质量数(A)=质子数(Z)+中子数(N)。
(4)质子数(Z)=阳离子的核外电子数+阳离子的电荷数。
(5)质子数(Z)=阴离子的核外电子数-阴离子的电荷数。
2.元素周期表的结构(3)过渡元素元素周期表中从ⅢB到ⅡB共10个纵行,包括了第Ⅷ族和全部副族元素,共60多种元素,全部为金属元素,统称为过渡元素。
特别提醒族序数为Ⅱ、Ⅲ的地方是主族和副族的分界线,第一次分界时主族在副族的前面,第二次分界时副族在主族的前面。
“第一次”指ⅠA ⅡA ⅢB ⅣB ⅤB ⅥB ⅦB Ⅷ依次排列。
“第二次”指ⅠB ⅡB ⅢA ⅣA ⅤA ⅥA ⅦA 0依次排列。
重难点二 零族定位法确定元素的位置 1.2.比大小定周期比较该元素的原子序数与0族元素的原子序数大小,找出与其相邻近的两种0族元素,那么该元素就和序数大的0族元素处于同一周期。
3.求差值定族数(1)若某元素原子序数比相应的0族元素多1或2,则该元素应处在该0族元素所在周期的下一个周期的ⅠA 族或ⅡA 族。
(2)若比相应的0族元素少1~5时,则应处在同周期的ⅢA ~ⅦA 族。
(3)若差其他数,则由相应差值找出相应的族。
重难点三 元素的性质与原子结构 1.碱金属单质的相似性和递变性 (1)相似性①与O 2反应生成相应的氧化物,如Li 2O 、Na 2O 等。
②与Cl 2反应生成RCl ,如NaCl 、KCl 等。
③与H 2O 反应,能置换出H 2O 中的氢,反应通式为2R +2H 2O===2ROH +H 2↑。
④与非氧化性酸反应,生成H 2,反应通式为2R +2H +===2R ++H 2↑。
(R 表示碱金属元素)(2)递变性从Li 到Cs ,随着核电荷数的增加,碱金属元素原子的电子层数逐渐增多,原子核对核外电子的吸引能力逐渐减弱,失电子能力逐渐增强,金属性逐渐增强。
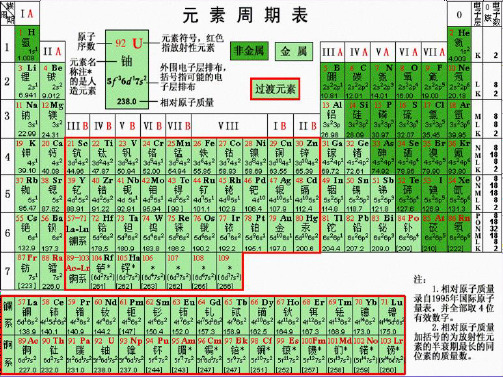



化学元素周期表的结构与特点化学元素周期表是化学领域中一张重要的工具,用于分类和组织元素。
它的结构和特点反映了元素的性质和规律。
本文将介绍化学元素周期表的结构与特点。
一、周期表的结构化学元素周期表基本上由一系列的水平行(周期)和垂直列(族)组成。
每个元素都根据其原子序数(即核中质子的数量)进行排序和编号。
以下是元素周期表的一些重要结构特点:1. 期(或主能级):元素周期表的水平行被称为期。
它们按照原子的能级顺序排列,从1到7。
随着周期数的增加,原子的能级也逐渐增大。
每个新的周期都代表着新的电子壳的填充。
2. 组(或族):元素周期表的垂直列被称为组。
它们是根据原子的电子配置和化学性质进行分类。
第1组到第2组被称为“s”区,第3组到第8组被称为“p”区,第9组到第10组被称为“d”区,第11组到第18组被称为“f”区。
3. 过渡元素区和稀土元素区:在元素周期表中,第4周期到第7周期被称为过渡元素区。
这个区域包含具有类似化学性质的元素。
稀土元素区则包括在f区内,这些元素在化学性质上也有一定的相似性。
4. 分区:元素周期表通常被分为两个部分,即主族元素和过渡元素。
主族元素一般是周期表最左边的一列,包括所有的s和p区元素。
过渡元素则在主族元素的右边,包括所有的d和f区元素。
二、周期表的特点元素周期表不仅反映了元素的结构,还展示了一些重要的周期性规律和特点。
以下是几个周期表的特点:1. 周期性:元素周期表的排列遵循一定的周期性规律,即元素的性质会随着原子序数的增加而呈现出周期性的变化。
例如,原子半径、离子半径、电负性等属性在周期表中都有可见的趋势规律。
2. 原子半径:原子半径是指元素中心核和最外层电子之间的距离。
周期表中,原子半径呈现出一个明显的趋势:从左到右呈递减,而从上到下呈递增。
这是由于核电荷的增加和电子层的填充。
3. 电离能:元素的电离能是指从一个原子中去除一个电子所需的能量。
周期表中,电离能也呈现出一定的规律:从左到右呈递增,在同一周期内,电离能随着原子序数的增加而递增。

元素周期表各原子结构示意图第1周期[1] K 氢1[2] He 氦2第2周期[3] Li 锂2 1[4] Be 铍2 2[5] B 硼2 3[6] C 碳2 4[8] O 氧2 6[9] F 氟2 7[10]Ne 氖2 8第3周期[11]Na 钠2 8 1[12]Mg 镁2 8 2[13]Al 铝2 8 3[14]Si 硅2 8 4[15] P 磷2 8 5[16] S 硫2 8 6[17]Cl 氯2 8 7[18]Ar 氩2 8 8第4周期[19]K 钾2 8 8 1[20]Ca 钙2 8 8 2[21]Sc 钪2 8 9 2[22]Ti 钛2 8 10 2[23]V 钒2 8 11 2[24]Cr 铬2 8 13 1[25]Mn 锰2 8 13 2[26]Fe 铁2 8 14 2[27]Co 钴2 8 15 2[28]Ni 镍2 8 16 2[29]Cu 铜2 8 18 1[30]Zn 锌2 8 18 2[31]Ga 镓2 8 18 3[32]Ge 锗2 8 18 4[33]As 砷2 8 18 5[34]Se 硒2 8 18 6[35]Br 溴2 8 18 7[36]Kr 氪2 8 18 8第5周期[37]Rb 铷2 8 18 8 1[38]Sr 锶2 8 18 8 2[40]Zr 锆2 8 18 10 2[41]Nb 铌2 8 18 12 1[42]Mo 钼2 8 18 13 1[43]Tc 锝2 8 18 13 2[44]Ru 钌2 8 18 15 1[45]Rh 铑2 8 18 16 1[46]Pd 钯2 8 18 18[47]Ag 银2 8 18 18 1[48]Cd 镉2 8 18 18 2[49]In 铟2 8 18 18 3[50]Sn 锡2 8 18 18 4[51]Sb 锑2 8 18 18 5[52]Te 碲2 8 18 18 6[53]I 碘2 8 18 18 7[54]Xe 氙2 8 18 18 8第6周期[55]Cs 铯2 8 18 18 8 1[56]Ba 钡2 8 18 18 8 2[57]La 镧2 8 18 18 9 2[58]Ce 铈2 8 18 19 9 2[59]Pr 镨2 8 18 21 8 2[60]Nd 钕2 8 18 22 8 2[61]Pm 钷2 8 18 23 8 2[62]Sm 钐2 8 18 24 8 2[63]Eu 铕2 8 18 25 8 2[64]Gd 钆2 8 18 25 9 2[65]Tb 铽2 8 18 27 8 2[66]Dy 镝2 8 18 28 8 2[67]Ho 钬2 8 18 29 8 2[68]Er 铒2 8 18 30 8 2[69]Tm 铥2 8 18 31 8 2[70]Yb 镱2 8 18 32 8 2[71]Lu 镥2 8 18 32 9 2[72]Hf 铪2 8 18 32 10 2[73]Ta 钽2 8 18 32 11 2[74]W 钨2 8 18 32 12 2[75]Re 铼2 8 18 32 13 2[76]Os 锇2 8 18 32 14 2[77]Ir 铱2 8 18 32 15 2[78]Pt 铂2 8 18 32 17 1[79]Au 金2 8 18 32 18 1[81]Tl 铊2 8 18 32 18 3[82]Pb 铅2 8 18 32 18 4[83]Bi 铋2 8 18 32 18 5[84]Po 钋2 8 18 32 18 6[85]A 砹2 8 18 32 18 7[86]Rn 氡2 8 18 32 18 8第7周期[87]Pr 钫2 8 18 32 18 8 1[88]Ra 镭2 8 18 32 18 8 2[89]Ac 锕2 8 18 32 18 9 2[90]Th 钍2 8 18 32 18 102[91]Pa 镤2 8 18 32 20 9 2[92]U 铀2 8 18 32 21 92[93]Np 镎2 8 18 32 22 92[94]Pu 钚2 8 18 32 24 82[95]Am 镅*2 8 18 32 25 82[96]Cm 锔*2 8 18 32 25 92[97]Bk 锫*2 8 18 32 27 82[98]Cf 锎*2 8 18 32 28 82[99]Es 锿*2 8 18 32 29 82[100]Fm 镄* 2 8 18 32 308 2[101]Md 钔* 2 8 18 32 318 2[102]No 锘* 2 8 18 32 328 2[103]Lr 铹* 2 8 18 32 329 2[104]Rf*[105]Db*[106]Sg*[107]Bh*[108]Hs*[109]Mt*[110]Ds*[111]Rg*[112]Uub*104-112号暂未列出57-71号为镧系元素89-103号为锕系元素红色(深红色)为放射性元素带*号为人造元素。

元素周期表的结构
1,周期含义:元素周期表共有7个横行,每一横行是一个周期,第1横行是第一周期,第2横行是第二周期,以此类推共7个周期。
2,族的含义:元素周期表共有18个纵行,每一纵行叫一族(其中8、9、10三个纵行共同组成一个族),共16个族。
3,周期的特点:同一周期元素的原子核外电子层数相同,从左到右:核外电子数依次增多,最外层电子数由1——8
4,族的特点:同一族元素的原子最外层电子数相同,均为8个电子(氦特殊情况最外层是2个电子),从上到下:电子层数逐渐增多(由1层——7层)。
5,元素周期表中每一格中元素的相关信息
原子序数=核电荷数=核内质子数=核外电子数。
相对原子质量的近似值=质子数+中子数。

元素周期表知识点一.元素周期表的结构1.世界上第一张元素周期表是在1869年由俄国化学家门捷列夫绘制完成的,随着科学的不断发展,已逐渐演变为现在的常用形式。
2.原子序数:按照元素在周期表中的顺序给元素编号,称之为原子序数,原子序数=核电荷数=质子数=核外电子数。
3.编排原则(1)周期:把电子层数相同的元素,按原子序数递增的顺序,从左至右排成的横行。
(2)族:把最外层电子数相同的元素,按电子层数递增的顺序,从上至下排成的纵行。
4.元素周期表的结构5.元素周期表中的特殊位置(1).分区①分界线:沿着元素周期表中铝、锗、锑、钋与硼、硅、砷、碲、砹的交界处画一条斜线,即为金属元素区和非金属元素区分界线(氢元素除外)。
②各区位置:分界线左面为金属元素区,分界线右面为非金属元素区。
③分界线附近元素的性质:既表现金属元素的性质,又表现非金属元素的性质。
(2).过渡元素:元素周期表中部从ⅢB族到ⅡB族10个纵列共六十多种元素,这些元素都是金属元素。
(3).镧系:元素周期表第六周期中,57号元素镧到71号元素镥共15种元素。
(4).锕系:元素周期表第七周期中,89号元素锕到103号元素铹共15种元素。
(5).超铀元素:在锕系元素中92号元素铀(U)以后的各种元素。
结构巧记口诀:横行叫周期,现有一至七,四长三个短,第七尚不满。
纵列称为族,共有十六族,一八依次现①,一零再一遍②。
一纵一个族,Ⅷ族搞特殊,三纵算一族,占去8、9、10。
镧系与锕系,蜗居不如意,十五挤着住,都属ⅢB族。
说明:①指ⅠA、ⅡA、ⅢB、ⅣB、ⅤB、ⅥB、ⅦB、Ⅷ;②指ⅠB、ⅡB、ⅢA、ⅣA、ⅤA、ⅥA、ⅦA、0。
知识点二.元素的性质与原子结构1 .碱金属元素:周期表中第IA族的元素(除H元素外)。
(1).碱金属的原子结构①.相同点:碱金属元素原子结构的最外层电子数相同,都为1。
②.递变性:从Li到Cs,碱金属元素的原子结构中,电子层数依次增多,原子半径依次增大。


元素周期表的结构与性质元素周期表是现代化学中最基本的工具之一,它反映着元素之间的关系,可以帮助我们更好地理解化学反应和物质性质。
本文将介绍元素周期表的结构和性质。
一、周期表的结构元素周期表是由俄国化学家季莫费耶夫 (D.I.Mendeleev) 和德国化学家洛塔尔·迈耶 (J.Lothe) 独立开发的,它们都是基于元素物理和化学性质的相似性来组织的。
周期表的主体是由元素原子序数排列而成,它从左到右,由上到下按照原子序数的递增顺序排列,即“周期表周期上元素原子序数递增,周期表周期内元素原子序数递减”的基本规律。
常规的元素周期表按原子序数分为7个周期,每个周期由两个元素逐渐加入,形成18个元素族(有时称为“栏”或“列”)。
从第1周期中的氢(H)到第7周期中的钅(原子序数118),这些元素的数量不断增加,有时会存在括号中。
在周期表中,水平行称为“周期”,由左到右逐渐加上元素;垂直栏称为“族”,元素具有类似的性质。
周期表的左侧通常由金属和金属化合物组成,右侧则主要由非金属元素组成。
中间从碳到锗的元素则有时被称为“半金属”,拥有一些金属和非金属元素的性质。
元素的周期相应地反映了元素的原子结构,其中第1周期中只含有一个电子壳层——K壳,而最后一个周期则具有七个电子壳层——K、L、M、N、O、P、Q层,这就意味着周期表的右下角元素具有较多的电子层和较强的金属和非金属元素性质。
二、元素周期表的核心元素周期表中最重要的发现之一是化学元素之间的周期性性质。
尤其是元素周期表上的族性质,使我们可以根据元素的周期位置,预测它们在反应和化学性质方面的规律。
根据元素周期表,我们可以得出以下推论:1.元素具有周期性的物理性质周期表上的元素根据它们的原子结构,拥有周期性的电离势、电子亲和能、原子半径、电负性等性质。
例如,周期表上的右侧元素通常比左侧元素拥有更高的电离势和电子亲和能,这表明它们对电子的吸引力更强,并且更加稳定,因此不容易与其他元素发生化学反应。

