高中化学复习知识点:几种铁的氧化物的化学性质
- 格式:docx
- 大小:107.16 KB
- 文档页数:10

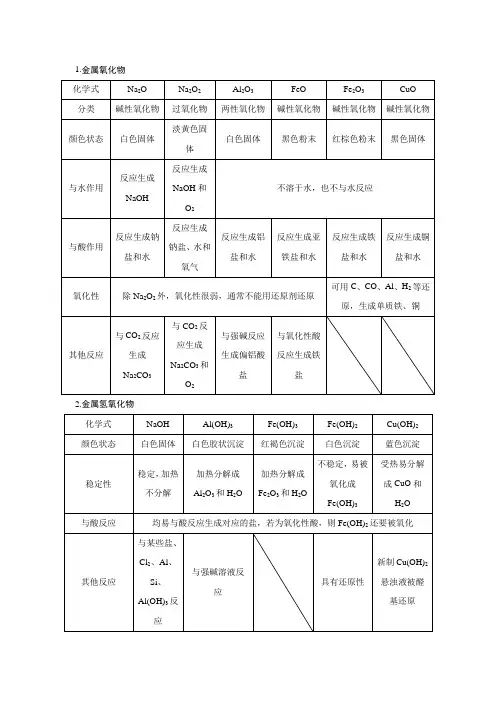
1.金属氧化物2.金属氢氧化物二、金属元素分点突破物质一 “活泼”金属代表——钠 1.思维线索2.三维考查3.认知拓展(1)钾及其重要化合物钾的活泼性超过钠,钾与O 2反应除生成K 2O 2外,还生成KO 2(超氧化钾)。
KO 2的阴离子为O -2,有极强的氧化性,与H 2O 、CO 2的反应分别为4KO 2+2H 2O===4KOH +3O 2↑、4KO 2+2CO 2===2K 2CO 3+3O 2。
(2)钙及其重要化合物Ca与水反应生成H 2:Ca +2H 2O===Ca(OH)2+H 2↑。
在空气中燃烧:Ca +O 2=====点燃CaO 2、3Ca +N 2=====点燃Ca 3N 2。
CaO 2溶于酸生成H 2O 2:CaO 2+2H +===Ca 2++H 2O 2。
与水反应:2CaO 2+2H 2O===2Ca(OH)2+O 2↑。
在碱性条件下,CaCl 2与H 2O 2反应可制得CaO 2。
草酸钙(CaC 2O 4)CaC 2O 4难溶于水。
溶于盐酸:CaC2O4+2H+===Ca2++H2C2O4物质二“两性”金属的代表——铝1.经典转化“价—类”二维图转化反应①2Al+6HCl===2AlCl3+3H2↑②2Al+2NaOH+2H2O===2NaAlO2+3H2↑③AlCl3+4NaOH===NaAlO2+3NaCl+2H2O④NaAlO2+4HCl===NaCl+AlCl3+2H2O⑤NaAlO2+2H2O+CO2===Al(OH)3↓+NaHCO3⑥AlCl3+3NH3·H2O===Al(OH)3↓+3NH4Cl2.认知拓展(1)锌及其化合物物质性质与盐酸反应:Zn+2H+===Zn2++H2↑;Zn与NaOH溶液反应:Zn+2OH-===ZnO2-2+H2↑。
ZnO ZnO+2H+===Zn2++H2O;ZnO+2OH-===ZnO2-2+H2O。
Zn(OH)2Zn(OH)2+2H+===Zn2++2H2O;Zn(OH)2+2OH-===ZnO2-2+2H2O。

高中金属的氧化物知识点总结高中金属的氧化物知识点总结氧化物是由元素和氧原子组成的化合物。
在高中化学中,我们学习了许多金属的氧化物,这些金属的氧化物在生产和日常生活中扮演着重要的角色。
下面是高中金属的氧化物知识点的总结。
一、金属元素和非金属元素在首先了解金属的氧化物之前,我们需要了解金属元素和非金属元素的区别。
金属是一种具有良好的导电性和导热性的元素。
它们主要在左侧的周期表中找到,而非金属元素主要在右侧的周期表中找到。
这两种元素的主要区别是它们的电子结构。
金属元素的电子结构具有低电离能和低电子亲和力。
这使得它们能够被解离成离子,并形成具有金属性的阳离子。
非金属元素的电子结构具有高电离能和高电子亲和力,难以形成阳离子。
由于金属元素的电子结构,金属能够极易氧化,形成氧化物。
二、金属氧化物的命名金属氧化物的命名方法遵循一定的规则,其中包含两个信息:金属元素的名称和氧元素的名称。
对于只有两个元素的化合物,我们把该化合物中金属元素的名称写在前面,把氧元素的名称写在后面,并在两个元素之间加上“氧化”这个词。
例如,氧化钙的化学式为CaO,氧化铜的化学式为CuO,氧化铁的化学式为Fe2O3。
对于一些具有多价的金属(如铁、锰、铬等),为区分不同的氧化物,需使用罗马数字来表示其氧化态,置于元素名称的右上角。
例如,三氧化二铁的化学式为Fe2O3,其中的“三”表示氧化铁物质中铁的氧化态为+3。
三、金属氧化物的性质1. 氧化性:金属氧化物中的金属可以被氧化。
例如,在氧气中,氧化亚铁(FeO)会被氧气氧化成氧化铁(Fe2O3)。
这反应过程是吸热的。
2. 酸性:一些金属氧化物是酸性物质,它们具有将碱中和的能力。
例如,氧化铝(Al2O3)是一种酸性物质,它可以中和碱,如钠氢氧化物(NaOH),生成盐和水。
这种反应称为酸碱反应。
3. 碱性:金属氧化物中的一些金属具有碱性,它们可以将酸中和。
例如,氢氧化钙(Ca(OH)2)是一种碱性物质,它可以将盐酸中和,生成盐和水。

铁及其化合物(答案在最后)1.掌握铁及其化合物的主要性质及其应用。
2.了解铁及铁氢氧化物的制备方法。
3.能鉴别溶液中的Fe2+、Fe3+。
考点一铁的单质、氧化物1.变价金属——铁(1)物理性质银白色固体,熔点较高,具有良好的导热、导电、延展性,能被磁体吸引。
(2)化学性质①与非金属的反应Fe与Cl2:2Fe+3Cl22FeCl3;Fe与S:________________________;Fe与I2:________________________。
②Fe与水蒸气的反应:______________________。
③与酸反应Fe与H+:Fe+2H+===Fe2++H2↑;常温下,Fe遇浓HNO3、浓H2SO4发生钝化反应,加热时可将铁氧化为+3价铁盐。
④与某些盐溶液的反应与CuSO4溶液反应的离子方程式:Fe+Cu2+===Fe2++Cu。
与FeCl3溶液反应的离子方程式:________________________。
(3)生铁的冶炼(苏教版教材)①原料:铁矿石、焦炭、空气、石灰石。
②设备:高炉。
③主要反应a.还原剂的生成:C+O2CO2,CO2+C2CO;b.铁的还原:____________________________;c.造渣反应:CaCO3CaO+CO2↑,CaO+SiO2CaSiO3。
【师说·助学】铁在空气中形成铁锈的主要成分是Fe2O3·x H2O,在纯氧中燃烧的产物是Fe3O4。
2.铁的氧化物(1)(2)①与盐酸反应的离子方程式分别为:FeO:FeO+2H+===Fe2++H2O;Fe2O3:Fe2O3+6H+===2Fe3++3H2O;Fe3O4:____________________________。
②Fe x O y与CO反应:Fe x O y+y CO x Fe+y CO2。
【易错诊断】判断正误,错误的说明理由。
1.铁与过量的硫粉共热产物是Fe2S3:________________________________________________________________________ ________________________________________________________________________。

第13讲铁及其重要化合物复习目标 1.掌握铁及其重要化合物的主要性质及应用。
2.了解铁及其重要化合物的制备方法。
考点一铁的单质、氧化物1.铁(1)位置与物理性质(2)化学性质:比较活泼,常表现变价,重要化学反应为2.铁的氧化物的比较化学式FeO Fe2O3Fe3O4俗名铁红磁性氧化铁颜色状态黑色粉末红棕色粉末黑色晶体(有磁性)溶解性难溶于水难溶于水难溶于水铁的化合价+2 +3 +2、+3稳定性 不稳定 稳定稳定与H +反应的 离子方程式 FeO +2H +===Fe 2++H 2OFe 2O 3+6H +===2Fe 3++3H 2OFe 3O 4+8H +===Fe 2++2Fe 3++4H 2O与CO 的反应 (炼铁原理) Fe x O y +y CO=====高温x Fe +y CO 21.铁的化学性质比较活泼,所以铁在自然界中全部以化合态形式存在( ) 2.Fe 分别与Cl 2和盐酸反应所得氯化物相同( ) 3.常温下可用铁制容器储存、运输浓硝酸、浓硫酸( )4.铁是较活泼的金属,它与卤素单质(X 2)反应生成物为FeX 2( ) 5.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe 3O 4( ) 答案 1.× 2.× 3.√ 4.× 5.√一、铁与酸、水蒸气的反应1.请列举铁与硝酸反应的各种情况,写出相关的离子方程式。
提示 (1)常温下,铁在冷的浓硝酸中钝化。
(2)加热时,铁可溶于浓硝酸中:Fe +6H ++3NO -3=====△Fe 3++3NO 2↑+3H 2O (3)铁与稀硝酸反应:①少量铁:Fe +NO -3+4H +===Fe 3++NO ↑+2H 2O ②过量铁:3Fe +2NO -3+8H +===3Fe 2++2NO ↑+4H 2O 2.铁与水蒸气反应,通常有以下两种装置,请回答下列问题:装置一装置二(1)。
(2)实验完毕后,取出装置一的少量固体,溶于足量稀盐酸,再滴加KSCN 溶液,溶液颜色无明显变化,试解释原因:________________________________________(用离子方程式表示)。

第二课时铁的重要化合物学习目标:1.了解铁的氧化物的性质及应用。
2.了解Fe(OH)2、Fe(OH)3的制备原理及化学性质。
3.掌握Fe2+、Fe‘+间的相互转化以及Fe3+、Fe2+的检验方法。
菖课前自主预习■一―_____________________________________ E]知识梳理1.铁的氧化物(1)物理性质氧化物FeO Fe2O3Fe3O4颜色状态黑色粉末红棕色粉末黑色晶体(具有磁性)铁的价态+2+3+2、+3溶解性不溶于水(2)化学性质①氧化亚铁不稳定,在空气中受热易被氧化为珏血。
②氧化亚铁和氧化铁属于碱性氧化物,与非强氧化性酸反应生成Fe2+^1Fe3+O③写出氧化亚铁和氧化铁分别与盐酸反应的离子方程式:a.氧化亚铁:FeO+2H=Fe2++H2O ob.氧化铁:Fe2O3+6H=2Fe3++3H2O o(3)主要用途氧化铁俗称铁红,常用作红色油漆和涂料。
2.铁的氢氧化物(1)铁的氢氧化物的制备(2)化学性质Fe(()H)2Fe(OH)3操作J NaOHqt 溶液|FeSO,溶液卡NaOH 溶液T FeCl,溶液71553现象产生亘鱼絮状沉淀,迅速变为灰绿色,最终变为红褐色产生红褐色沉淀有关反Fe 2+ +2(旧一一Fe(OH)2 I ,Fe3++3OH- =_Fe(OH)3应(离子方程式)4Fe(OH)2+O2+2H2。
——4Fe(OH)3±Fe(OH)2Fe(OH)3稳定性不稳定,易被氧 化,受热易分解,但 产物复杂不稳定、受热易分解:△ 2Fe(OH)3 — Fe 2O 3+ 3田。
3.铁盐和亚铁盐与盐酸反 应(离子方程式)Fe ( OH )2 + 2H+Fe(OH)3 + 3H + ——^=Fe 2++2H 2O Fe 3++3H 2O 常见的铁盐有Fe2(SOQ3、FeCF 等,常见的亚铁盐有FeSO 4>FeCl 2(l)Fe 3+的检验①向FeCG溶液中滴入KSCN溶液现象:溶液显血红色;化学反应方程式:FeCl3+3KSCN===Fe(SCN)3+3KCL ②向FeCL溶液中滴入KSCN溶液现象:无现象。

高中金属的氧化物知识点氧化物属于化合物(当然也一定是纯净物)。
其组成中只含两种元素,其中一种一定为氧元素,另一种若为金属元素,则称为金属氧化物;若另一种不为金属元素,则称之为非金属氧化物。
下面小编给大家分享一些高中金属的氧化物知识,希望能够帮助大家,欢迎阅读!高中金属的氧化物知识1钠及其化合物(一)、钠1. Na与水反应的离子方程式:命题角度为是否违反电荷守恒定律。
2. Na的保存:放于煤油中而不能放于水中,也不能放于汽油中;实验完毕后,要放回原瓶,不要放到指定的容器内。
3. Na、K失火的处理:不能用水灭火,必须用干燥的沙土灭火。
4. Na、K的焰色反应:颜色分别黄色、紫色,易作为推断题的推破口。
注意做钾的焰色反应实验时,要透过蓝色的钴玻璃,避免钠黄光的干扰。
5. Na与熔融氯化钾反应的原理:因钾的沸点比钠低,钾蒸气从体系中脱离出来,导致平衡能向正反应移动。
(Na+KCl(熔融)=NaCl+K(二)、氢氧化钠1. 俗名:火碱、烧碱、苛性钠2. 溶解时放热:涉及到实验室制取氨气时,将浓氨水滴加到氢氧化钠固体上,其反应原理为:一是NaOH溶解放出大量的热,促进了氨水的分解,二是提供的大量的OH-,使平衡朝着生成NH3的方向移动。
与之相似的还有:将浓氨水或铵盐滴加到生石灰上。
涉及到的方程式为NH4++OH-NH3·H2O NH3↑+ H2O3. 与CO2的反应:主要是离子方程式的书写(CO2少量和过量时,产物不同)4. 潮解:与之相同的还有CaCl2、MgCl2(三)、过氧化钠1. 非碱性氧化物:金属氧化物不一定是碱性氧化物,因其与酸反应除了生成盐和水外,还有氧气生成,化学方程式为:2Na2O2+4HCl=4NaCl+2H2O+O2↑2. 过氧化钠中微粒的组成:1mol过氧化钠中所含有离子的数目为3NA,或说它们的微粒个数之比为2:1,命题角度为阿伏加德罗常数。
3. 过氧化钠与水、CO2的反应:一是过氧化钠既是氧化剂也是还原剂,水既不是氧化剂也不是还原剂;二是考查电子转移的数目(以氧气的量为依据)。


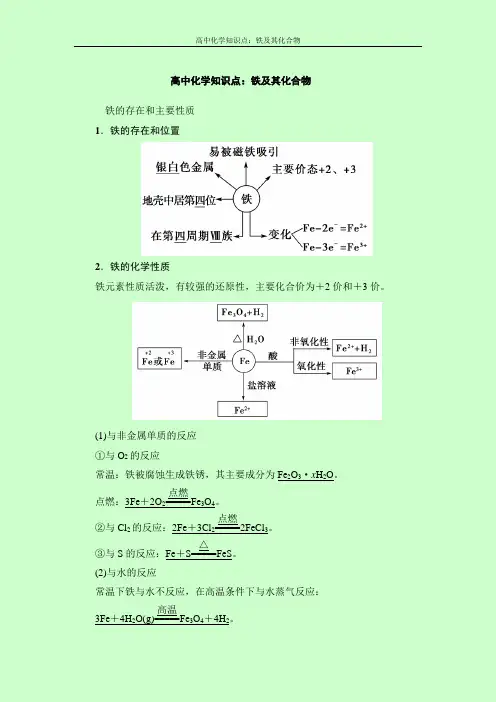
高中化学知识点:铁及其化合物铁的存在和主要性质 1.铁的存在和位置2.铁的化学性质铁元素性质活泼,有较强的还原性,主要化合价为+2价和+3价。
(1)与非金属单质的反应 ①与O 2的反应常温:铁被腐蚀生成铁锈,其主要成分为Fe 2O 3·x H 2O 。
点燃:3Fe +2O 2=====点燃Fe 3O 4。
②与Cl 2的反应:2Fe +3Cl 2=====点燃2FeCl 3。
③与S 的反应:Fe +S=====△FeS 。
(2)与水的反应常温下铁与水不反应,在高温条件下与水蒸气反应: 3Fe +4H 2O(g)=====高温Fe 3O 4+4H 2。
(3)与酸的反应①与非氧化性酸反应的离子方程式:Fe+2H+===Fe2++H2↑。
②与氧化性酸遇冷的浓硫酸或浓硝酸钝化,与稀硝酸或在加热条件下与浓硫酸、浓硝酸反应无H2产生。
Fe与足量稀HNO3反应的离子方程式为Fe+4H++NO-3===Fe3++NO↑+2H2O。
(4)与某些盐溶液的反应①与CuSO4溶液反应的离子方程式:Fe+Cu2+===Cu+Fe2+。
②与FeCl3溶液反应的离子方程式:Fe+2Fe3+===3Fe2+。
铁的重要化合物1.铁的氧化物氧化亚铁(FeO) 氧化铁(Fe2O3) 四氧化三铁(Fe3O4) 俗名铁红磁性氧化铁色态黑色粉末红棕色粉末黑色晶体铁元素价态+2 +3 +2、+3 说明:①FeO、Fe2O3、Fe3O4分别与盐酸反应的离子方程式:FeO+2H+===Fe2++H2O、Fe2O3+6H+===2Fe3++3H2O、Fe3O4+8H+===2Fe3++Fe2++4H2O。
②FeO与硝酸反应的化学方程式:3FeO+10HNO3===3Fe(NO3)3+NO↑+5H2O。
2.铁的氢氧化物Fe(OH)2Fe(OH)3色态白色固体红褐色固体与H+反应Fe(OH)2+2H+=== Fe2++2H2O Fe(OH)3+3H+=== Fe3++3H2O二者的关在空气中,Fe(OH)2能够非常迅速地被氧气氧化成Fe(OH)3,现象是白色絮状沉淀迅速变成灰绿色,最后变成红褐色,反应方程式为4Fe(OH)2+系O2+2H2O===4Fe(OH)3说明:Fe(OH)2、Fe(OH)3的制备可利用相应亚铁盐、铁盐与碱液反应。

高中化学必修一铁及其化合物要点一:单质铁的物理及化学性质1、铁单质的物理性质铁具有金属的通性,具有被吸引的特性,一般铁粉为黑色,铁块为银白色。
2、化学性质3、注意事项(1)铁与弱氧化剂(如S、I2、H+、Fe3+、Cu2+)等反应所得产物为Fe2+,铁元素的价态为+2价。
(2)铁与强氧化剂(如Cl2、Br2、浓H2SO4、硝酸等)反应所得产物为Fe3+,铁元素的价态为+3价。
①在氯气中燃烧,只生成氯化铁;与稀硝酸反应时则先产生+3价铁,若铁过量时则+3价铁再变为+2价铁;②铁在常温下遇到冷的浓硫酸、浓硝酸时发生钝化,属于化学反应。
(3)铁在纯氧中燃烧以及在高温下与H2O(g)反应得到的产物为Fe3O4,铁元素的价态为+2、+3价。
(4)铁不能与冷、热水反应,但能与水蒸气反应,与水蒸汽反应的产物也是Fe3O4。
典型例题1、某稀溶液中含有4mol KNO3和2.5mol H2SO4,向其中加入1.5mol Fe,充分反应(已知NO3﹣被还原为NO).下列说法正确的是()A.反应后生成NO的体积为28 LB.所得溶液中c(Fe2+):c(Fe3+)=1:1C.所得溶液中c(NO3﹣)=2.75 mol/LD.所得溶液中的溶质只有FeSO4解:溶液中氢离子总物质的量为:n(H+)=2.5mol×2=5mol,n(NO3﹣)=4mol,铁粉的物质的量为1.5mol,由3Fe+2NO3﹣+8H+=3Fe2++2NO↑+4H2O,3 2 81.5mol 1mol 4mol,则1.5molFe完全反应时,硝酸根离子与氢离子均过量,则发生Fe+NO3﹣+4H+=Fe3++NO↑+2H2O,若1.5molFe完全反应时,氢离子不足,则两个反应均发生,Fe+NO3﹣+4H+=Fe3++NO↑+2H2Ox 4x x x3Fe+2NO3﹣+8H+=3Fe2++2NO↑+4H2Oy y y y则:x+y=1.5、4x+y=5,解得:x=0.75mol,y=0.75mol生成NO的体积为(0.75mol+0.75mol×)×22.4L/mol=28L,A.根据分析可知,反应后生成标况下28LNO,不是标况下,NO气体不一定为28L,故A错误;B.反应后生成铁离子为0.75mol,亚铁离子为0.75mol,c(Fe2+):c(Fe3+)=n(Fe2+):n(Fe3+)=1:1,故B正确;C.反应消耗硝酸根离子等于生成NO的量=0.75mol+0.75mol×=1.25mol,缺少溶液体积,无法计算溶液中硝酸根离子浓度,故C错误;D.反应后中含有硫酸铁和硫酸亚铁,故D错误;故选B.变式训练1、向500mL 2mol/L 的CuSO4溶液中插入一块铁片,反应片刻后取出铁片,经洗涤、烘干,称其质量比原来增重2.0g.下列说法错误的是(设反应后溶液的体积不变)()A.则此过程中参加反应的铁的质量是14gB.析出铜物质的量是0.25molC.反应后溶液中溶质物质的量浓度:c(CuSO4)=1.5mol/LD.反应后溶液中溶质物质的量浓度:c(FeSO4)=1.5mol/L2、将15g两种金属的混合物投入足量的盐酸中,反应完全后得到11.2L H2(标准状况),该混合物的组成可能是()A.钠和铁B.镁和铜C.铝和镁D.锌和铁要点二:铁的氧化物要点三:铁的氢氧化物1、常见的物理及化学性质4Fe(OH)2 + O2 + 2H2O =4Fe(OH)32Fe(OH)3Fe2O3+3H2O(受热分解)(2)Fe(OH)2的制备Fe(OH)2易被空气中的氧气氧化,生成Fe(OH)3,所以在制备Fe(OH)2时:①要确保Fe2+溶液中无Fe3+,故需加Fe粉,把Fe3+转化为Fe2+。
铁高中化学的知识点总结铁高中化学的知识1一、铁1.铁与水蒸气的反应:3Fe+4H2O(g)=(△)Fe3O4+4H22.铁与氯气、盐酸反应:产物分别为FeCl2、FeCl3。
二、氧化物1.铁的氧化物成分:废铁屑的主要成分Fe2O3;铁锈的主要成分为Fe2O3.nH2O;黑色晶体、磁性氧化铁为Fe3O4;红棕色粉未,俗称铁红,作红色油漆和涂料的为Fe2O3,赤铁矿的主要成分为Fe2O3,它是炼铁的原料。
铁在氧气燃烧与铁与水蒸气反应的产物都是Fe3O4。
以上知识,往往容易出现在推断题和实验题中。
三、氢氧化物1.实验室制备Fe(OH)2:现象:白色沉淀→灰绿色→红褐色沉淀。
为较长时间的看到Fe(OH)2白色沉淀,采取的防护:一是煮沸,二是将胶头滴管插入液面以下,三是加一层油膜,如苯、汽油等。
2.Fe(OH)3的受热分解:2Fe(OH)3=Fe2O3+3H2O与此相以的还有Cu(OH)2、Al(OH)3。
3.氢氧化铁胶体的制备,实验操作要点:①先煮沸,②加入饱和的FeCl3溶液,③再煮沸至红褐色,④停止加热。
对应的离子方程式:Fe3++3H2O=Fe(OH)3(胶体)+3H+注意:一,要用等号,二,标明胶体而不是沉淀,三,加热。
铁高中化学的知识2铁盐与亚铁盐1.Fe2+、Fe3+的检验:(1)Fe2+:一是碱液法:先生成白色沉淀,又迅速转变成灰绿色,最后变成红褐色沉淀;二是先加入KSCN溶液,不变色,再加入氯水后,出现血红色。
(注意:此处不用高锰酸钾溶液氧化,因其具有紫色)(2)Fe3+:一碱液法:加入碱液,出现红褐色沉淀。
二是加入KSCN溶液,出现血红色,离子方程式为:Fe3++3SCN-=Fe(SCN)3(络合物)2.铁盐与亚铁盐的配制:因Fe2+、Fe3+易水解,且Fe2+易被空气中的氧气氧化,故配制过程为:先将它们溶解在对应的酸中,然后加水冲稀到指定的浓度。
(注意:配制亚铁盐溶液时,要加入少量的铁粉,以防止Fe2+的氧化)3.制印刷电路板常用FeCl3作腐蚀液:一是离子方程式的书写正误(违反电荷守恒定律),二是利用此反应式设计成原电池,考查原电池原理的应用。