化学:人教版九年级上册燃烧和灭火
- 格式:doc
- 大小:238.55 KB
- 文档页数:3





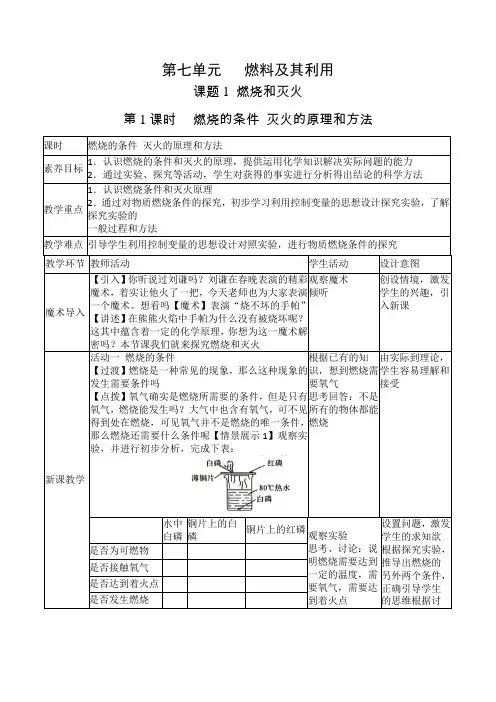
第七单元燃料及其利用课题1 燃烧和灭火第1课时燃烧的条件灭火的原理和方法课时燃烧的条件灭火的原理和方法素养目标1.认识燃烧的条件和灭火的原理,提供运用化学知识解决实际问题的能力2.通过实验、探究等活动,学生对获得的事实进行分析得出结论的科学方法教学重点1.认识燃烧条件和灭火原理2.通过对物质燃烧条件的探究,初步学习利用控制变量的思想设计探究实验,了解探究实验的一般过程和方法教学难点引导学生利用控制变量的思想设计对照实验,进行物质燃烧条件的探究教学环节教师活动学生活动设计意图魔术导入【引入】你听说过刘谦吗?刘谦在春晚表演的精彩魔术,着实让他火了一把,今天老师也为大家表演一个魔术。
想看吗【魔术】表演“烧不坏的手帕”【讲述】在熊熊火焰中手帕为什么没有被烧坏呢?这其中蕴含着一定的化学原理,你想为这一魔术解密吗?本节课我们就来探究燃烧和灭火观察魔术倾听创设情境,激发学生的兴趣,引入新课新课教学活动一燃烧的条件【过渡】燃烧是一种常见的现象,那么这种现象的发生需要条件吗【点拨】氧气确实是燃烧所需要的条件,但是只有氧气,燃烧能发生吗?大气中也含有氧气,可不见得到处在燃烧,可见氧气并不是燃烧的唯一条件,那么燃烧还需要什么条件呢【情景展示1】观察实验,并进行初步分析,完成下表:根据已有的知识,想到燃烧需要氧气思考回答:不是所有的物体都能燃烧由实际到理论,学生容易理解和接受水中白磷铜片上的白磷铜片上的红磷观察实验思考、讨论:说明燃烧需要达到一定的温度,需要氧气,需要达到着火点设置问题,激发学生的求知欲根据探究实验,推导出燃烧的另外两个条件,正确引导学生的思维根据讨是否为可燃物是否接触氧气是否达到着火点是否发生燃烧【问题探究】根据薄铜片上的白磷燃烧而红磷不燃烧的事实说明燃烧需要什么条件?由薄铜片上的白磷燃烧而热水下的白磷不燃烧的事实,又说明燃烧需要什么条件 【归纳总结】薄铜片上的白磷燃烧而红磷不燃烧的事实说明燃烧需要温度达到可燃物的着火点,薄铜片上的白磷燃烧而热水下的白磷不燃烧的事实,说明燃烧需要氧气 【老师介绍】着火点:可燃物达到燃烧所需要的最低温度,这个温度是可燃物的着火点。




一、自制简易灭火器其及其原理反应原理Na2CO3+2HCl === 2NaCl+H2O+CO2↑注意事项切勿让管口对着别人或自己二、常见灭火器灭火器干粉灭火器二氧化碳灭火器水基型灭火器灭火原理利用压缩的二氧化碳吹出干粉(主要含有碳酸氢钠或磷酸铵盐)加压时将液态二氧化碳压缩在小钢瓶中,灭火时再将其喷出,有降温和隔绝空气的作用产生的泡沫喷射到燃料表面,泡沫层析出的水在燃烧表面形成一层水膜,使可燃物与空气隔绝,达到灭火的目的课题12 燃烧和灭火知识导航知识精讲三、火灾自救措施1.如果火势不大,可根据起火原因选择合适的方法或灭火器灭火。
2. 如果火势较大或有蔓延趋势,应立即拨打119火警 ,并用湿毛巾捂住口鼻,蹲下靠近地面或墙壁逃离火灾现场。
3. 若是燃气炉灶失火,应迅速关闭燃气阀门,再灭火。
4. 电器或线路失火,要先切断电源,再灭火。
5. 救火时,不要贸然开门窗,以免空气对流加速火势蔓延。
四、爆炸 1. 爆炸可燃物在有限的空间内急剧地燃烧,就会在短时时间内聚集大量的热,使气体的体积迅速膨胀而引起起爆炸。
2. 爆炸极限可燃性气体等在空气中达到一定的含量时,遇到火源就会发生爆炸。
这个能发生爆炸的含量范围,叫做爆3. 粉尘爆炸实验点燃蜡烛,易错提醒爆炸不一定是化学变化,如气球爆炸、轮胎爆炸属于物理变化。
4.与燃烧和爆炸有关的图标5. 常见的易燃物固体:硫、磷、面粉、棉絮、木炭等;液体:酒精、石油产品(汽油、柴油、煤油);气体:液化石油气、氢气、乙炔、沼气、一氧化碳、甲烷等。
6. 使用和贮存易燃物和易爆物时的注意事项(1)易燃、易爆物不能和其他物质混合存放、应隔离储存;不能放在露天或高温的地方。
(2)存放易燃、易爆物品的地方应贴好图标及注意事项,以便及时提醒人们。
(3)在搬运易燃、易爆物品时,要轻拿、轻放,切勿撞击,以免发生意外。
7. 燃烧、爆炸和缓慢氧化的区别和联系(1)联系:燃烧、缓慢氧化、爆炸的本质都是氧化反应,都是放出热量(2)区别反应条件反应程度反应现象燃烧跟氧气接触,温度达到着火点剧烈发光、发热爆炸在有限空间内急速燃烧,热量来不及散失非常剧烈发光、发热,爆炸缓慢氧化跟氧气接触,温度没有达到着火点缓慢放热不明显,不易察觉对点训练题型一:燃烧与灭火【例1】学校图书馆在考虑消防时,应选择下列哪种灭火器比较合适A.消防水龙头B.水基型灭火器C.干粉灭火器D.二氧化碳灭火器【变11】火灾发生时我们要正确使用灭火器。
课题一燃烧和灭火【知识要点】1. 燃烧的条件可燃物与发生的一种、、的氧化反应叫做燃烧,燃烧需要三个条件:(1);(2);(3)。
2. 灭火的原理和方法灭火的根本是;灭火的原理是;;。
如果遭遇火灾时,可以采取的自救措施有。
3. 易燃物和易爆物的安全知识可燃物在内急剧地燃烧,就会在短时间内聚积使气体的体积迅速膨胀而引起。
越大,燃烧就越剧烈。
【要点分析】燃烧、爆炸、缓慢氧化和自燃的区别和联系:一般说燃烧、爆炸、自燃与缓慢氧化的本质都是氧化反应,只是由于条件不同而产生了不同的现象。
①本质特征:都是氧化反应,都放热。
②反应进行的剧烈程度不同。
燃烧——是剧烈的氧化反应。
爆炸——急速的燃烧发生在有限的空间内而引起的,是剧烈的氧化反应。
缓慢氧化——反应过程中几乎不升温、不发光、现象很不显著,反应缓慢,是氧化反应的一种形式。
自燃——指可燃物由于缓慢氧化而引起的自发燃烧。
例1 燃烧是生活中的一种常见现象。
下列有关燃烧或灭火的说法错误的是()A.钠可以在氯气中燃烧,说明燃烧不一定要有氧气参与B.碳、硫在氧气中燃烧比在空气中燃烧剧烈C.锅里的油着火时可用锅盖盖灭,是因为隔绝了氧气D.用水可以灭火,是因为降低了可燃物的着火点解析钠在氯气中燃烧,说明氯气可以支持燃烧,所以A是正确的;着火点是物质固有的一种属性,一般不会随外界条件的变化而变化,用水灭火,降低的是可燃物的温度,使温度低于着火点,而不是降低其着火点,所以D错误。
答案 D例2古语道:“人要实,火要虚”。
此话的意思是说:做人必须脚踏实地,事业才能有成;燃烧固体燃料需要架空,燃烧才能更旺。
从燃烧的条件看,“火要虚”的实质是()A.增大可燃物的热值 B.增大可燃物与空气的接触面积C.提高可燃物的着火点 D.提高空气中氧气的含量解析使可燃物充分燃烧的条件一是增大可燃物与氧气的接触面积,二是增加氧气的浓度。
一般情况下,增大氧气的浓度较难操作,在空气中氧气浓度是一定的,要想燃烧更旺,可增大与氧气的接触面积。
化学:人教版九年级上册燃烧和灭火
课下作业
1.(2008年安徽肇庆)1854年5月30日,英国战舰“欧罗巴”的船舱里装滿了供战马吃的草料,航行途中突然草料着火,整个战舰瞬间变为火海。
则下列有关说法错误
..的是()A·草料舱没有氧气B·草料舱通风不好
C·草料发生缓慢氧化积累了大量的热D·草料温度达到了草料的着火点
2.(2008年山东烟台)如图,将两支燃着的蜡烛罩上茶杯,过了一会儿高的蜡烛先
熄灭,低的蜡烛后熄灭,同时还观察到茶杯内壁变黑。
由此我们可以得到启发:从着
火燃烧的房间逃离时,下列做法中不正确的是()
(A)用湿毛巾捂住鼻子(B)成站立姿势跑出
(C)伏低身子逃出(D)淋湿衣服爬出
3.(2008年江苏南通)古语道:“人要实,火要虚”。
此话的意思是说:做人必须脚踏实地,事业才能有成;燃烧固体燃料需要架空,燃烧才能更旺。
从燃烧的条件看,“火要虚”的实质是()A·增大可燃物的热值B·提高空气中氧气的含量
C·提高可燃物的着火点D·增大可燃物与空气的接触面积
4.(2008年山东泰安)从防止空气污染的角度考虑,下列实验过程应在通风橱中进行的是()
5.(2008年黑龙江哈尔滨)干粉灭火器是利用压缩的二氧化碳吹出白色干粉来灭火。
这种灭火器可用来扑灭油、气等燃烧引起的失火。
其中干粉的主要成分是碳酸氢
钠·它受热后生成苏
打、水和一种参与植物光合作用的气体。
请根据以上信息回答:
(1)碳酸氢钠的性质有
(2)灭火时碳酸氢钠发生反应的化学方程式为
(3)该反应的基本反应类型是反应。
6.(2008年福建福州)某兴趣小组话动中,同学们按图11装置对“可燃物
燃烧的条件”进行探究。
探究过程中,大家对磷燃烧生成的大量白烟是否危害人体健康提出疑问。
【查阅资料】白磷的着火点是40℃,红磷的着火点是240℃,……燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3)。
【变流与讨论】白烟对人体健康有害,该实验装置必须改进。
【改进与实验】同学们按改进后的图12装置进行实验。
现象解释
a试管中白磷燃烧,热水中白磷没有燃烧. b试管中红磷没有燃烧. b试管中红磷、热水中白磷都没有燃烧的原因是① ;②。
【反思与评价】(1)改进后的图12装置与图11装置比较,优点是。
(2)小林同学指出图12装置仍有不足之处,并设计了图13装置,其中气球
的作用是。
【拓展与迁移】
实验小结时,小朱同学说:“待a试管冷却后,如果将试管口紧贴水面(室温下)。
并取下橡皮塞,将看到液体进入试管。
”这一说法得到大家的一致认同。
小晶问:“如果不考虑橡皮塞占试管的容积,进入a试管内液体的体积会是多少呢?大家争论后,出现两种预测。
甲:接近试管容积的1/5;乙:不一定接近试管容积的1/5。
你赞同的预测是(填“甲”或“乙”),理由是。
课下作业答案:
1.A
2·B 解析:该题是从探究灭火的原理,上面的蜡烛由于缺氧先熄灭启发我们从火灾中逃生的正确方法。
3.D 解析:使可燃物充分燃烧的条件一是增大可燃物欲扬起的接触面积,二是增加扬起的浓度。
一般情况下,增大氧气的浓度较难操作,在空气中燃烧的物质,氧气浓度时一定的,要想燃烧更旺,可增大与氧气的接触面积。
“火要虚”就是在燃料中间留一些空气,以增大与扬起的接触面积。
故D对。
点评:本题是考察燃烧的条件和使可燃物充分燃烧的措施。
生活中,燃料充分燃烧不仅可以节约能源,而且可以减少因不充分燃烧而产生的污染。
4.B 解析:本题考查的是实验与污染。
这四个实验中,铁与氧气反应产物只有四氧化三铁,电解水产生氢气和氧气,石灰石与稀盐酸反应产生二氧化碳,均无污染;唯有白磷燃烧产生的五氧化二磷会造成污染。
5·(1)白色固体(或白色粉末或白色粉末状固体)、受热能分解(或受热易分解)
(2)2NaHCO3△
2CO3+ H2O + CO2↑
(3)分解
解析:从题目提供的信息可以看出碳酸氢钠的一条物理性质——白色固体和一条化学性质——受热易分解,分解的产物苏打是碳酸钠(Na2CO3)、参与植物光合作用的气体是CO2,该反
应属于分解反应。
点评:本题主要以信息给予的形式考察碳酸氢钠的性质和用途。
6.①温度未达到红磷的着火点②热水中的白磷没有与氧气(或空气)接触
[反思与评价](1)能防止白磷燃烧产生的五氧化二磷逸散,危害人体健康。
(2)避免橡皮塞因试管内气体热膨胀而松动。
(合理答案均可)
[拓展与迁移]甲氧气约占空气体积的1/5。
且上述实验白磷足量、气密性良好,所以进入a试管内液体的体积能接近试管容积的1/5 (或乙装置漏气等) (其它合理答案均可) 解析:根据资料提供的信息,白磷和红磷燃烧后的产物五氧化二磷会刺激呼吸道,故实验的改进就是为了避免生成物扩散到空气中,图2避免了这一问题。
但是白磷燃烧放热,试管内温度升高、压强增大容易将塞子弹开,图13绑上气球解决了这一问题。
由于白磷燃烧消耗了试管内的氧气,故压强减小,水进入试管内的体积就是原来氧气占空气的体积,即1/5体积。
点评:本题以实验探究的形式考察了燃烧的条件、空气中氧气含量的测定等知识,同时考察了实验装置的评价与改进问题。