实验十二-菠菜色素的提取和分析
- 格式:docx
- 大小:64.95 KB
- 文档页数:6

菠菜色素的提取和分离实验报告菠菜色素提取实验报告菠菜中色素的提取和色素分离绿色植物如菠菜叶中含有叶绿素(绿)、胡萝卜素(橙)和叶黄素(黄)等多种天然色素。
叶绿素存在两种结构相似的形式即叶绿素a(C55H72O5N4Mg)和叶绿素b(C55H70O6N4Mg)),差别仅是a中一个甲基被b中的甲酰基所取代。
它们都是吡咯衍生物与金属镁的络合物,是植物进行光合作用所必需的催化剂,也是食用的绿色色素,可用于糕点、饮料水等中,添加于胶姆糖中还可消除口臭。
植物中a的含量通常是b的3倍。
尽管叶绿素分子中含有一些极性基团,但大的烃基结构使它易溶于石油醚等一些非极性溶剂。
胡萝卜素(C40H56)是具有长链结构的共轭多烯。
它有三种异构体α—,β—,和γ—胡萝卜素,其中β—异构体含量最多,也最重要。
生长期较长的绿色植物中,异构体中β—的含量多达90,。
β—具有维生素A的生理活性,其结构是两分子维生素A在链端失去两分子水结合而成。
生物体内,β—体受酶催化氧化即形成维生素A。
目前,β—体可作为维生素A使用,也可作为食品工业的色素,β一胡萝卜素还有防癌功能。
叶黄素(C40H56O2)是胡萝卜素的羟基衍生物,在光合作用中能起收集光能的作用。
在绿叶中通常是胡萝卜素的两倍。
较易溶于醇而在石油醚中溶解度较小。
由此可见,叶绿素等天然色素有广泛的用途,对于色素的提取与分离就显得很重要了(本实验就提取和分离做了相关的研究。
1 实验部分1.1 仪器与试剂仪器:研钵、分液漏斗、显微载玻片、毛细管、层析柱(20×10 cm)、UV-240 紫外分光光度计试剂:石油醚、乙醇(95%)、菠菜叶、丙酮(化学纯)、乙酸乙酯(化学纯)、无水硫酸钠、硅胶G、中性氧化铝(150目,160目)1.2 提取与分离1.2.1 浸泡法提取色素在研钵中放入20 g新鲜的菠菜叶,加入20 mL3:2(体积比)石油醚—乙醇混合液,适当研磨(不要研成糊状,否则会给分离造成困难),用倾析法将提取液转移到分液漏斗中,每次用10ml水洗涤两次,以除去萃取液中的乙醇。

菠菜色素的提取和分离实验报告
一、实验目的:
本次实验的主要目的是学习和掌握菠菜色素的提取和分离技术,了解菠菜中色素的提取和分离原理以及实验操作过程。
二、实验方法:
1、制备样品:将新鲜的菠菜叶片洗净晾干,切碎成小块备用;
2、提取菠菜色素:将切碎的菠菜叶片加入适量无水乙醇,研
磨成泥状物,过滤后取得浸提液;
3、进一步提取:将浸提液过滤并再次提取,过滤得到过滤液;
4、分离:将过滤液使用氯仿进行分离,水相和氯仿相层的色
素分离;
5、测定:将得到的色素溶于适量乙醇,测定菠菜色素的吸光度。
三、实验结果:
经过提取和分离,得到了深绿色的液体,与纯菠菜色素溶液比
较后发现两者颜色相似。
测定得到吸光度为0.54。
四、实验分析:
本次实验成功提取和分离了菠菜色素,并得到了较为准确的测定值。
在实验中,氯仿和无水乙醇是常用的有机溶剂,主要是因为在这些溶剂中菠菜色素的溶解度较高。
但是,在实验操作过程中需要注意保持实验环境的卫生和安全,氯仿是一种易挥发的有机物,需要注意防火和防烟。
五、实验结论:
通过本次实验,我们成功地提取和分离了菠菜色素,并且得到了较为准确的测定值。
同时,我们也了解了菠菜中色素的提取和分离原理以及实验操作过程。
本次实验的成功对于今后相关实验研究以及实际应用具有一定的指导意义。

菠菜色素的提取和分离实验报告菠菜色素的提取和分离实验报告引言:菠菜是一种常见的绿叶蔬菜,富含多种营养物质,其中包括一种被称为菠菜色素的成分。
菠菜色素是一类天然的色素,具有良好的生物活性和抗氧化性质。
本实验旨在通过提取和分离的方法,研究菠菜色素的性质和应用。
实验材料和方法:材料:新鲜菠菜叶片、无水乙醇、丙酮、石油醚、二氯甲烷、硅胶G柱、色谱柱、色谱试纸等。
方法:1. 取适量新鲜菠菜叶片,洗净并切碎成细末状。
2. 将菠菜末置于研钵中,加入适量无水乙醇,浸泡30分钟,搅拌均匀。
3. 将菠菜浸提液过滤,收集滤液。
4. 取少量滤液,加入石油醚,振荡混合,使菠菜色素溶于石油醚中。
5. 将石油醚层收集,加入少量无水乙醇,使溶液变为淡绿色。
6. 将淡绿色溶液倒入色谱柱中,以无水乙醇为洗脱剂,收集洗脱液。
7. 将洗脱液浓缩,得到菠菜色素。
实验结果和讨论:通过以上实验步骤,我们成功地从菠菜中提取和分离出了菠菜色素。
在实验过程中,我们使用了无水乙醇作为提取剂,因为乙醇能够有效溶解菠菜中的色素成分。
同时,我们使用石油醚作为分离剂,因为石油醚能够与菠菜色素发生亲和作用,使其溶于石油醚中。
在分离过程中,我们使用了色谱柱和色谱试纸进行分离和检测。
色谱柱是一种常见的分离工具,通过其内部填充的固定相材料,能够将混合物中的成分按照其亲和性和分子大小进行分离。
我们选择了硅胶G柱作为固定相材料,因为硅胶G柱对菠菜色素具有较好的亲和性。
通过使用无水乙醇作为洗脱剂,我们成功地将菠菜色素从硅胶G柱中洗脱出来。
在实验中,我们观察到菠菜色素呈现淡绿色。
这是因为菠菜色素主要由叶绿素和类胡萝卜素等成分组成,这些成分赋予了菠菜独特的颜色。
叶绿素是一种绿色的色素,具有光合作用的功能。
类胡萝卜素则是一类黄、橙、红等颜色的色素,具有抗氧化和免疫调节等作用。
菠菜色素不仅在食品工业中有广泛应用,还在医药和化妆品等领域发挥着重要作用。
菠菜色素富含抗氧化物质,能够有效清除自由基,延缓衰老和预防疾病。

菠菜色素的提取和分离一、实验目的1、通过绿色植物色素的提取,学习天然物质的提取方法;2、通过薄层色谱分析,掌握有机物色谱分析的原理和方法。
二、实验原理1 菠菜色素的提取绿色植物如菠菜叶中含有叶绿素(绿)、胡萝卜素(橙)和叶黄素(黄)等多种天然色素。
叶绿素存在两种结构相似的形式即叶绿素a(C 55H 72O 5N 4Mg)和叶绿素b(C 55H 70O 6N 4Mg),其差别仅是叶绿素a 中一个甲基被甲酰基所取代从而形成了叶绿素b 。
它们都是吡咯衍生物与金属镁的络合物,是植物进行光合作用所必需的催化剂。
植物中叶绿素a 的含量通常是b 的3倍。
尽管叶绿素分子中含有一些极性基团,但大的烃基结构使它易溶于醚、石油醚等一些非极性的溶剂。
胡萝卜素(C 40H 56)是具有长链结构的共轭多烯。
它有三种异构体,即 -胡萝卜素、β-胡萝卜素和γ-胡萝卜素,其中β-胡萝卜素含量最多,也最重要。
在生物体,β-胡萝卜素受酶催化氧化形成维生素A 。
目前β-胡萝卜素已可进行工业生产,可作为维生素A 使用,也可作为食品工业中的色素。
叶黄素(C 40H 56O 2)是胡萝卜素的羟基衍生物,它在绿叶中的含量通常是胡萝卜素的两倍。
与胡萝卜素相比,叶黄素较易溶于醇而在石油醚中溶解度较小。
N N NNH 3CCHCH 2RCH 2CH 3CH 3H 3COCO 2CH 3CH 2CH 2OO3CH 3CH 3CH 3CH 3Mg叶绿素a (R = CH 3) 叶绿素b (R = CHO )H 3C CH 3RCH 3H 3CRH 3CCH 3CH 3CH 3CH 3CH 3β-胡萝卜素(R = H ) 叶黄素(R = OH )H 3CCH 3CH 3CH 2OHCH 3CH 3维生素A2 薄层色谱原理常用TLC 表示,又称薄层层析,属于固液吸附色谱。
样品在薄层板上的吸附剂(固定相)和溶剂(移动相)之间进行分离。
由于各种化合物的吸附能力各不相同,在展开剂上移时,它们进行不同程度的解吸,从而达到分离的目的。
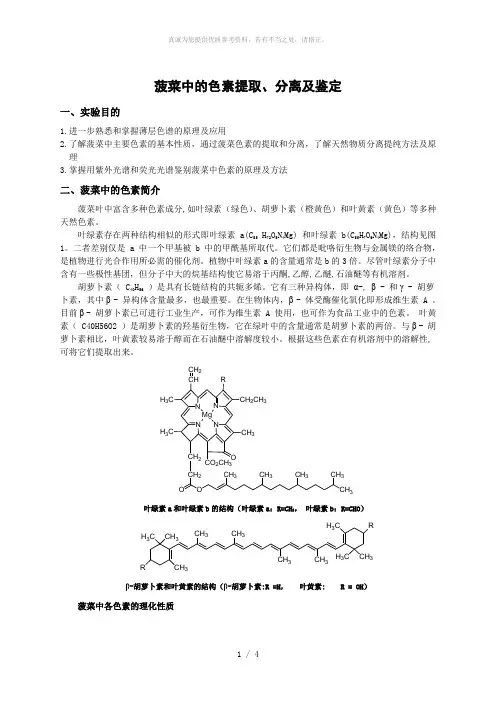
菠菜中的色素提取、分离及鉴定一、实验目的1.进一步熟悉和掌握薄层色谱的原理及应用2.了解菠菜中主要色素的基本性质,通过菠菜色素的提取和分离,了解天然物质分离提纯方法及原理3.掌握用紫外光谱和荧光光谱鉴别菠菜中色素的原理及方法二、菠菜中的色素简介菠菜叶中富含多种色素成分,如叶绿素(绿色)、胡萝卜素(橙黄色)和叶黄素(黄色)等多种天然色素。
叶绿素存在两种结构相似的形式即叶绿素 a(C 55 H 72O 5N 4Mg) 和叶绿素 b(C 55H 7O 6N 4Mg),结构见图1。
二者差别仅是 a 中一个甲基被 b 中的甲酰基所取代。
它们都是吡咯衍生物与金属镁的络合物,是植物进行光合作用所必需的催化剂。
植物中叶绿素a 的含量通常是b 的3倍。
尽管叶绿素分子中含有一些极性基团,但分子中大的烷基结构使它易溶于丙酮,乙醇,乙醚,石油醚等有机溶剂。
胡萝卜素( C 40H 56 )是具有长链结构的共轭多烯。
它有三种异构体,即 α-, β - 和γ - 胡萝卜素,其中β - 异构体含量最多,也最重要。
在生物体内,β - 体受酶催化氧化即形成维生素 A 。
目前β - 胡萝卜素已可进行工业生产,可作为维生素 A 使用,也可作为食品工业中的色素。
叶黄素( C40H56O2 )是胡萝卜素的羟基衍生物,它在绿叶中的含量通常是胡萝卜素的两倍。
与β - 胡萝卜素相比,叶黄素较易溶于醇而在石油醚中溶解度较小。
根据这些色素在有机溶剂中的溶解性,可将它们提取出来。
N N NNH 3CCHCH 2RCH 2CH 3CH 3H 3C OCO 2CH 3CH 2CH 2OOCH 3CH 3CH 3CH 3CH 3Mg叶绿素a 和叶绿素b 的结构(叶绿素a :R=CH 3, 叶绿素b :R=CHO )H 3C CH 3RCH 3H 3CH 3CCH 3CH 3CH 3CH 3CH 3β-胡萝卜素和叶黄素的结构(β-胡萝卜素:R =H , 叶黄素: R = OH ) 菠菜中各色素的理化性质绿色植物中的叶绿体色素在把光能转变为化学能的光和作用中起着重要作用。

2014年山东英语作文With the rapid development of technology, the educational landscape in Shandong Province has undergone significant changes in 2014. This essay aims to explore the impact of technological advancements on the education system, focusing on how it has transformed teaching methods, student engagement, and the overall learning experience.Firstly, the integration of technology in classrooms has led to a more interactive and dynamic learning environment. Teachers are now able to utilize multimedia tools such as interactive whiteboards and digital projectors to enhance their lessons. These tools not only make the learning process more engaging for students but also allow for a more diverse range of teaching materials to be introduced, including videos, animations, and online resources.Secondly, the advent of online learning platforms has provided students with access to a wealth of knowledge beyond the traditional classroom setting. In 2014, Shandong Province saw a surge in the number of educational websites and online courses available to students. This has facilitated a more self-directed approach to learning, where students can explore subjects of interest at their own pace and according to their individual learning needs.Moreover, the use of technology has also improved administrative efficiency within schools. Digital managementsystems for enrollment, grading, and scheduling have streamlined these processes, allowing educators to focus more on teaching and less on paperwork. This has also led to more accurate record-keeping and better communication between schools, teachers, and parents.However, the integration of technology in education is not without its challenges. One of the major concerns is the digital divide, where students from less affluent backgrounds may not have access to the same level of technology as their peers. This can lead to disparities in educational outcomes and exacerbate existing inequalities.In conclusion, the year 2014 marked a significant milestonein the integration of technology into the educational system of Shandong Province. While there are challenges to overcome, the benefits of technology in enhancing the learning process and improving administrative efficiency are clear. It is crucial for educational policymakers to address the digital divide and ensure that all students, regardless of their socioeconomic background, can reap the benefits of technological advancements in education.。

从菠菜中提取叶绿素实验报告三篇实验报告一:菠菜中提取叶绿素的方法比较1.引言叶绿素是一种重要的植物色素,它在光合作用中承担着捕获光能和转化化学能的重要角色。
菠菜是叶绿素含量较高的植物之一,因此本实验旨在比较不同方法提取菠菜中的叶绿素,探索最有效的提取方式。
2.材料与方法2.1 材料:- 新鲜菠菜叶片- 无水乙醚- 丙酮- 高速离心机- 比色皿2.2 方法:- 方法一:无水乙醚提取法将适量的菠菜叶片放入离心管中,加入适量的无水乙醚,用摇床震动片刻,使叶绿素溶解于乙醚中,然后离心10分钟收集上层液体。
- 方法二:丙酮提取法将适量的菠菜叶片放入离心管中,加入适量的丙酮,用摇床震动片刻,使叶绿素溶解于丙酮中,然后离心10分钟收集上层液体。
- 方法三:乙醇提取法将适量的菠菜叶片放入离心管中,加入适量的乙醇,用摇床震动片刻,使叶绿素溶解于乙醇中,然后离心10分钟收集上层液体。
3.结果在三种提取方法中,通过观察可以发现,方法一和方法二提取的叶绿素溶液呈现绿色,而方法三提取的叶绿素溶液呈现黄绿色。
利用分光光度计测定三个试管中叶绿素溶液的吸光度,发现方法一和方法二提取的叶绿素吸光度较高,而方法三的吸光度较低。
4.讨论方法一使用无水乙醚作为提取溶剂,乙醚能有效溶解叶绿素,并且在离心过程中上层液体的分离效果较好。
方法二使用丙酮作为提取溶剂,丙酮也能有效溶解叶绿素,并且丙酮相对于乙醚来说更易于购买。
方法三使用乙醇作为提取溶剂,乙醇对叶绿素的溶解能力较差,导致提取的叶绿素溶液吸光度较低。
5.结论通过对菠菜中提取叶绿素的实验比较,我们发现使用无水乙醚和丙酮作为提取溶剂的方法能够较好地提取菠菜中的叶绿素,并且吸光度较高。
因此,在菠菜中提取叶绿素的实验中,建议使用无水乙醚或丙酮作为提取溶剂。
实验报告二:叶绿素在光合作用中的作用研究1.引言叶绿素是植物体内最重要的色素之一,它在光合作用中起着关键作用。
本实验旨在研究叶绿素在光合作用中的功能和重要性。

菠菜叶中色素的提取实验报告一、实验目的1、了解菠菜叶中所含色素的种类和化学性质。
2、掌握从菠菜叶中提取和分离色素的实验方法。
3、学习使用分光光度计测定色素溶液的吸光度。
二、实验原理菠菜叶中含有多种色素,如叶绿素 a、叶绿素 b、叶黄素和胡萝卜素等。
这些色素在有机溶剂中的溶解度不同,因此可以通过萃取的方法将它们分离出来。
叶绿素 a 和叶绿素 b 为吡咯衍生物,可溶于有机溶剂,如乙醇、丙酮等。
叶绿素 a 为蓝绿色,叶绿素 b 为黄绿色。
叶黄素和胡萝卜素属于类胡萝卜素,叶黄素为黄色,胡萝卜素为橙黄色,它们也能溶于有机溶剂。
根据不同色素在层析液中的溶解度不同,在层析过程中,溶解度大的色素随层析液在滤纸上扩散得快;溶解度小的色素扩散得慢,从而将不同的色素分离开来。
三、实验材料与仪器1、材料:新鲜菠菜叶2、仪器:研钵、漏斗、玻璃棒、分液漏斗、容量瓶、分光光度计、滤纸、脱脂棉等。
3、试剂:无水乙醇、石油醚、丙酮、层析液(石油醚:丙酮=9:1)四、实验步骤1、提取色素称取 5g 新鲜菠菜叶,剪碎后放入研钵中,加入 5mL 无水乙醇、少许碳酸钙和石英砂,充分研磨成匀浆。
将研磨好的匀浆用漏斗过滤到分液漏斗中,用 5mL 无水乙醇冲洗研钵和漏斗,将滤液合并到分液漏斗中。
轻轻振摇分液漏斗,静置分层,放出下层的水相,保留有机相。
2、制备色素溶液将有机相转移到容量瓶中,用无水乙醇定容至 25mL,得到色素提取液。
3、色素的分离取一块干燥的滤纸,剪成 15cm×3cm 的长条,在一端剪去两角,在距离剪角一端 1cm 处用铅笔轻轻画一条横线。
用毛细吸管吸取少量色素提取液,在铅笔线处点样,每次点样后吹干,重复多次,使点样处形成一条细而直的色素线。
将点样好的滤纸放入装有层析液的层析缸中,层析液液面不能超过滤纸的铅笔线。
盖上盖子,进行层析。
当层析液前沿接近滤纸的上端边缘时,取出滤纸,用铅笔标记出色素带的位置。
4、色素的鉴定用分光光度计分别测定叶绿素 a、叶绿素 b、叶黄素和胡萝卜素溶液在不同波长下的吸光度,绘制吸光度波长曲线,确定最大吸收波长。

菠菜色素实验报告1. 引言菠菜是一种富含营养的绿色蔬菜,其中含有一种特殊的绿色色素,称为菠菜色素。
菠菜色素具有抗氧化和抗癌的作用,在食品和药物工业中有广泛的应用。
本实验旨在通过提取菠菜中的色素,并利用分光光度计测定其吸光度,最终确定菠菜色素的浓度。
2. 实验步骤2.1 材料准备•新鲜菠菜叶片•无水乙醇•无水二氯甲烷•磨杵和研钵•过滤纸•取代皿•离心管•分光光度计2.2 色素提取1.取适量新鲜菠菜叶片,用清水洗净。
2.将菠菜叶片切碎放入研钵中,并加入少量的无水乙醇。
3.用磨杵搅拌菠菜叶片,使其完全破碎,以帮助色素的溶解。
4.将研磨好的菠菜叶片及溶解的色素转移至离心管中。
5.将离心管放入离心机中,离心10分钟,使菠菜色素与乙醇分离出来。
2.3 菠菜色素的分光光度测定1.取一定量的色素溶液加入取代皿中,用过滤纸将溶液上的杂质滤去。
2.使用分光光度计调整选取的波长,一般选择吸光度最大的波长进行测定。
3.调零分光光度计,以去除背景吸光度。
4.将取代皿放入分光光度计中,记录吸光度值。
5.根据标准曲线,计算菠菜色素的浓度。
3. 结果与讨论3.1 实验数据吸光度菠菜色素浓度 (mg/L)0.27 0.50.52 1.00.88 1.51.152.01.422.51.74 3.03.2 标准曲线绘制与浓度计算根据实验数据,绘制菠菜色素的吸光度与浓度的曲线图。
通过线性回归分析,得到表达式:吸光度 = 0.676 × 浓度 + 0.065,R² = 0.987。
根据标准曲线的方程,可以根据测得的吸光度值计算菠菜色素的浓度。
3.3 实验结果根据标准曲线计算吸光度为0.95的菠菜色素浓度为1.27 mg/L。
4. 结论通过本实验,成功提取了菠菜中的色素,并利用分光光度计测得吸光度值。
根据标准曲线,计算得到菠菜色素浓度为1.27 mg/L。
本实验结果可为菠菜色素的定量测定提供参考。
5. 参考文献(文献引用格式根据需求进行调整)。

菠菜色素的提取与分离(实验方案)
菠菜色素是一种天然的色素,在食品、药品和化妆品等领域得到广泛应用。
本实验旨在通过提取和分离菠菜中的色素,探索其化学结构和性质。
实验步骤:
1.新鲜的菠菜叶子切碎后加入乙醇中,浸泡过夜。
2.过滤得到菠菜浸液,加5%的NaCl,搅拌均匀,沉淀后过滤,收集菠菜蛋白,保留上清液。
3.将上清液进行浓缩,得到浓缩液。
4.将浓缩液加入正己烷中,振荡后离心,得到两层液体,上层为绿色菠菜色素,下层为无色的正己烷。
5.倒出上层菠菜色素液,用NaOH溶液调整其PH值,得到纯净的菠菜色素。
实验原理:
菠菜色素是一种叶绿素和类胡萝卜素的混合物,其中叶绿素是绿色的,未成熟的植物中含量较高,而类胡萝卜素是黄色的,成熟的植物中含量较高。
为了提取出纯净的菠菜色素,需要将其与其他杂质分离开来。
在实验中,我们选择了乙醇作为提取菠菜中色素的溶剂,乙醇对叶绿素和类胡萝卜素有较好的溶解作用。
随着浸泡时间的延长,色素的溶解度不断增加。
在分离紫胡萝卜素和叶绿素时,利用了两种色素溶解度不同的特性。
正己烷是一种非极性溶剂,对叶绿素有良好的溶解度,而对紫胡萝卜素的溶解度较差。
因此,在将浓缩菠菜色素液加入正己烷中时,不同色素会分层,方便分离纯净的菠菜色素。
实验注意事项:
1.实验中使用的器材和试剂要洁净干燥,避免杂质污染。
2.提取菠菜中的色素时,要控制乙醇的浓度和浸泡时间,避免色素的损失。
3.在调整菠菜色素液的PH值时,要逐渐加入NaOH溶液,避免PH值过高导致色素分解。
4.实验过程中如有任何异常情况,应及时停止实验并处理。

菠菜中的色素提取、分离及鉴定一、实验目的1.进一步熟悉和掌握薄层色谱的原理及应用2.了解菠菜中主要色素的基本性质,通过菠菜色素的提取和分离,了解天然物质分离提纯方法及原理3.掌握用紫外光谱和荧光光谱鉴别菠菜中色素的原理及方法二、菠菜中的色素简介菠菜叶中富含多种色素成分,如叶绿素(绿色)、胡萝卜素(橙黄色)和叶黄素(黄色)等多种天然色素。
叶绿素存在两种结构相似的形式即叶绿素 a(C 55 H 72O 5N 4Mg) 和叶绿素 b(C 55H 7O 6N 4Mg),结构见图1。
二者差别仅是 a 中一个甲基被 b 中的甲酰基所取代。
它们都是吡咯衍生物与金属镁的络合物,是植物进行光合作用所必需的催化剂。
植物中叶绿素a 的含量通常是b 的3倍。
尽管叶绿素分子中含有一些极性基团,但分子中大的烷基结构使它易溶于丙酮,乙醇,乙醚,石油醚等有机溶剂。
胡萝卜素( C 40H 56 )是具有长链结构的共轭多烯。
它有三种异构体,即 α-, β - 和γ - 胡萝卜素,其中β - 异构体含量最多,也最重要。
在生物体内,β - 体受酶催化氧化即形成维生素 A 。
目前β - 胡萝卜素已可进行工业生产,可作为维生素 A 使用,也可作为食品工业中的色素。
叶黄素( C40H56O2 )是胡萝卜素的羟基衍生物,它在绿叶中的含量通常是胡萝卜素的两倍。
与β - 胡萝卜素相比,叶黄素较易溶于醇而在石油醚中溶解度较小。
根据这些色素在有机溶剂中的溶解性,可将它们提取出来。
N N NNH 3CCHCH 2RCH 2CH 3CH 3H 3C OCO 2CH 3CH 2CH 2OOCH 3CH 3CH 3CH 3CH 3Mg叶绿素a 和叶绿素b 的结构(叶绿素a :R=CH 3, 叶绿素b :R=CHO )H 3C CH 3RCH 3H 3CRH 3CCH 3CH 3CH 3CH 3CH 3β-胡萝卜素和叶黄素的结构(β-胡萝卜素:R =H , 叶黄素: R = OH ) 菠菜中各色素的理化性质绿色植物中的叶绿体色素在把光能转变为化学能的光和作用中起着重要作用。
菠菜色素的提取和分离实验报告菠菜色素的提取和分离实验报告引言:菠菜是一种常见的食材,它不仅味道鲜美,而且富含多种营养物质。
其中,菠菜叶中的色素成分具有重要的生物学和营养学意义。
本实验旨在通过提取和分离菠菜叶中的色素,探究其组成和结构。
一、实验材料与方法:1. 实验材料:菠菜叶、无水乙醇、正己烷、醋酸乙酯、石油醚、氯仿、硅胶薄层色谱板。
2. 实验步骤:(1)菠菜叶的提取:将菠菜叶洗净并切碎,加入适量的无水乙醇中,浸泡30分钟,使色素充分溶解。
然后用滤纸过滤,收集菠菜叶提取液。
(2)色素的分离:将菠菜叶提取液与正己烷进行液液分配,重复3次,使色素分配到正己烷层中。
然后将正己烷层收集,蒸发溶剂,得到色素提取物。
(3)色素的纯化:将色素提取物溶解于醋酸乙酯中,进行液液分配,重复3次,使色素分配到醋酸乙酯层中。
然后将醋酸乙酯层收集,蒸发溶剂,得到纯化后的色素。
(4)色素的分离:将纯化后的色素溶解于石油醚中,进行液液分配,重复3次,使色素分配到石油醚层中。
然后将石油醚层收集,蒸发溶剂,得到分离后的色素。
(5)色素的鉴定:将分离后的色素溶解于氯仿中,进行薄层色谱分析。
将硅胶薄层色谱板浸泡于氯仿中,然后将色素溶液滴于色谱板上,放入色谱槽中,进行上升式开发。
开发完毕后,用紫外灯照射,观察色谱板上的色素带。
二、实验结果与分析:经过提取、分离和纯化,成功地从菠菜叶中提取到了色素。
通过薄层色谱分析,我们观察到了色谱板上的色素带,根据色素带的位置和颜色,可以初步判断菠菜叶中含有叶绿素、类胡萝卜素等多种色素成分。
三、实验总结与思考:通过本次实验,我们成功地提取和分离了菠菜叶中的色素。
然而,我们只能初步判断色素成分的种类,对于具体的结构和含量还需要进一步的分析和研究。
此外,本实验采用的是传统的提取和分离方法,还可以尝试其他更先进的技术,如高效液相色谱等,以提高分离效果和准确性。
结语:菠菜色素的提取和分离实验为我们了解菠菜叶中的色素成分提供了基础。
菠菜色素提取实验报告菠菜色素提取实验报告引言:菠菜是一种常见的蔬菜,富含多种营养物质,其中包括一种被称为菠菜色素的物质。
菠菜色素具有丰富的抗氧化性质,对人体健康具有重要作用。
本实验旨在提取菠菜中的色素,并通过实验验证提取方法的有效性和色素的特性。
实验方法:1. 菠菜样品准备:选取新鲜的菠菜叶子,洗净并切碎,以便于提取色素。
2. 提取色素:将切碎的菠菜叶子放入搅拌器中,加入适量的乙醇,搅拌均匀后,过滤得到浸提液。
3. 分离色素:将浸提液倒入离心管中,进行离心分离,得到上层的菠菜色素液。
4. 色素纯化:将菠菜色素液转移到干净的容器中,加入适量的醋酸乙酯,轻轻搅拌后,过滤得到纯净的菠菜色素。
实验结果:通过实验,我们成功地提取到了菠菜中的色素。
菠菜色素呈现出深绿色的液体,具有一定的黏稠度。
经过纯化后,色素更加纯净,颜色更加鲜艳。
实验讨论:1. 提取方法的选择:本实验采用了乙醇作为提取剂,乙醇具有良好的溶解性,可以有效地提取菠菜中的色素。
此外,乙醇还能够保持色素的稳定性,不易发生降解。
2. 色素的稳定性:菠菜色素具有一定的稳定性,不易受到光照和氧化的影响。
这使得菠菜色素在食品工业中具有广泛的应用前景。
3. 色素的应用:菠菜色素可以用作食品添加剂,为食品增添颜色的同时,还具有抗氧化和抗炎作用,有助于保护人体健康。
4. 色素的安全性:菠菜色素是一种天然的色素,相比合成色素更加安全可靠。
然而,在应用过程中仍需注意用量控制,以免过量摄入对人体健康造成不良影响。
结论:通过本次实验,我们成功地提取到了菠菜中的色素,并验证了提取方法的有效性。
菠菜色素具有丰富的抗氧化性质,可以作为食品添加剂使用。
然而,色素的应用仍需谨慎,合理控制用量,以确保人体健康。
参考文献:1. 陈晓明,赵丽华,李建中. 菠菜色素的提取与分离[J]. 化学教育, 2016, 37(12): 95-98.2. 张玉华,李红梅,张建华. 菠菜色素的提取工艺研究[J]. 食品科学, 2019, 40(4): 116-119.。
竭诚为您提供优质文档/双击可除菠菜色素实验报告篇一:菠菜中色素的提取预习实验报告实验名称:菠菜中的色素提取一:实验目的:了解薄层色谱在有机物分离中的应用,掌握薄层色的基本原理;加强有机物分离提纯技术的训练。
二:实验基本原理:菠菜的叶片中含有叶绿素(包括叶绿素a和叶绿素b)、叶黄素及胡萝卜素等天然色素。
叶绿素是绿色植物的主要色素,分子由脱镁叶绿素母环、叶绿酸、叶绿醇、甲醇、二价镁离子等部分构成。
高等植物中有两种叶绿素即叶绿素a和叶绿素b共存,叶绿素a为一蓝黑色固体粉末,在乙醇溶液中为蓝绿色,并有深红色荧光。
而叶绿素b为暗绿色固体粉末,其乙醇溶液为黄绿色,并有红色荧光。
叶绿素不溶于水,易溶于有机溶剂,常可用极性有机溶剂,例如丙酮、乙醇、乙酸乙酯等。
从植物匀浆中提取它。
叶绿素存在于植物细胞的叶绿体中,与类胡萝卜素、类脂物质及脂蛋白复合在一起,分布在叶绿体内的蝶形体的片层膜上。
胡萝卜素是一种橙色的天然色素,属于四萜类,为一长链共轭多烯。
有α、β、γ三种异构体,其中β异构体最多。
叶黄素是一种黄色色素,与叶绿素同存在与植物体内,是胡萝卜素的羟基衍生物,较易溶于乙醇,在石油醚中溶解度较小。
根据它们的化学特性,可将它们从植物叶片中提取出来,并通过萃取、沉淀和色谱方法将它们分离出来。
色谱法的基本原理是利用混合物中各组分在某一物质中的吸附或溶解性能的不同,或和其它亲和作用性能的差异,使混合物的溶液流经该种物质,进行反复的吸附或分配等作用,从而将各组份分开。
薄层层析是一种微量、快速和简便的色谱方法。
由于各种化合物的极性不同,吸附能力不相同,在展开剂上移动,进行不同程度的解析,根据原点至斑点中心及展开剂前沿的距离,计算比移值。
化合物的吸附能力与它们的极性成正比,具有较大极性的化合物吸附较强。
在给定的条件下(吸附剂、展开剂、板层厚度等),化合物移动的距离和展开剂移动的距离之比是一定的,即Rf值是化合物的物理常数,其大小只与化合物本身的结构有关,因此可以根据Rf值鉴别化合物。
实验十二菠菜叶中叶绿素的提取和分离实验十二菠菜叶中叶绿素的提取和分离(07-05-26) 一实验目的1(掌握从菠菜叶中提取叶绿素的方法;2(了解薄层层析的原理,掌握薄层层析的一般操作和定性鉴定方法二实验原理1(叶绿素提取高等植物体内的叶绿体色素有叶绿素和类胡萝卜素两类,主要包括叶绿素a (CHONMg)、叶绿素b(CHONMg)、β—胡萝卜素(CH)和叶黄素(CHO)等4种。
562叶绿素a和叶绿素b为吡咯衍生物与金属镁的配合物,胡萝卜素是一种橙色天然色素,属于四萜类,为一长链共轭多烯,有α、β、γ三种异构体,其中,β异构体含量最多。
叶黄素为一种黄色色素,与叶绿素同存在于植物体中,是胡萝卜素的羟基衍生物,较易溶于乙醇,在乙醚中溶解度较小。
根据它们的化学特性,可将它们从植物叶片中提取出来,并通过萃取、沉淀和色谱方法将它们分离开来。
RR=H; 叶黄素 R= OH 2(薄层色谱薄层层析是快速分离和定性分析微量物质的一种极为重要的实验技术,具有设备简单、操作方便而快速的特点。
它是将固定相支持物均匀地铺在玻片上制成薄层板,将样品溶液点加在起点处,置于层析容器中用合适的溶剂展开而达到分离的目的。
用此法分离时几乎不受温度的影响,可采用腐蚀性显色剂,而且可在高温下显色,特别适用于挥发性小或在较高温度下易发生反应的物质,同时也常用来跟踪有机反应或监测有机反应完成的程度。
薄层层析按分离机制不同可分为吸附层析、分配层析、离子交换层析等,最常用的为吸附薄层层析,在此主要讨论。
吸附层析中样品在薄层板上经过连续、反复的被吸附刑吸附及展开剂解吸附过程,由于不同的物质被吸附剂吸附的能力及被展开剂解吸附的能力不同,放在薄层上以不同速度移动而得以分离。
通常用比移值(Rf)表示物质移动的相对距离:色斑最高浓度中心至原点中心的距离,R f展开剂前沿至原点中心的距离1CH2RCH3CH3NNMg R=CH; 叶绿素a;3NNCHCH33R=CHO; 叶绿素b;HHOCOOCHO3OCH3CH3CH3 CH3 Rf值计算示意图叶绿素:吡咯衍生物和镁的配合物,是植物进行光1(起点线; 2. 展开剂前沿合作用必需的催化剂,易溶于石油醚等非a. 色斑最高浓度中心至原点中心的距离极性溶剂中。
实验4菠菜中色素的提取与分离【实验目的】1.学会用有机溶剂提取菠菜中的色素并进行分离,了解从植物中提取有机化合物的一般方法;2.学会根据物质的性质选择合适的溶剂,知道选用混合溶剂是提取物质的有效途径;3.了解利用纸色谱法分离物质的原理和操作。
【实验原理】菠菜中含有多种色素,如叶绿素(绿色)、胡萝卜素(橙黄色)、叶黄素(黄色)等。
1.菠菜中色素的提取叶绿素a、叶绿素b和胡萝卜素易溶于石油醚,叶黄素易溶于乙醇,石油醚和乙醇可以混溶。
因此,可以选择石油醚—乙醇混合溶剂来提取菠菜中的色素,然后用水洗去乙醇和少量易溶于水的杂质,这样就可得到色素的石油醚溶液。
2.色素的分离提取菠菜色素得到的石油醚溶液可用纸色谱法分离:将少量含有几种物质的溶液涂在滤纸条的一端,并在这一端用适当的溶剂(称为展开剂)润湿,在滤纸的毛细作用下,展开剂携带待分离的物质沿滤纸纤维向上移动。
由于不同的组分的移动速度不同,一段时间后,不同的组分移动的距离不同,从而达到将这些组分分离开来的目的,如下图所示。
这种分离方法称为纸色谱法,又叫纸上层析。
【实验器具】试剂:石油醚、乙醇,丙酮、无水硫酸钠、脱脂棉。
仪器:研钵、锥形瓶、漏斗、铁架台(带铁圈)、分液漏斗、大试管。
【实验过程】一、菠菜中色素的提取1.研磨:取10g菠菜切成小块,用研钵捣烂,装入锥形瓶中。
2.浸取:向锥形瓶中加入10mL石油醚—乙醇混合溶剂(体积比为1:1),塞上橡胶塞,振荡。
3.过滤:将小团棉花放在漏斗颈部,过滤浸取液(如图1)。
4.洗涤:将滤液移人分液漏斗,用10mL水洗涤两次,以除去乙醇及浸取液中的少量水溶性物质。
注意不要剧烈振荡,以防止乳化;静置分层(如图2),弃去下层(水—乙醇层),将上层(石油醚层)溶液移至干燥的小锥形瓶中。
注意:洗涤后,下层水层从下口放出,上层有机层从上口倒出。
5.干燥:加入少量无水硫酸钠,干燥,备用。
图1图2二、色素的分离1.裁纸:取一张滤纸裁成1.5cm×20cm的长方形,注意使滤纸纤维呈竖直走向。
有机实验-菠菜中色素的提取和分析
菠菜中色素的提取和分析是有机化学实验中的一个经典实验。
本实验主要是通过对菠
菜中的色素进行提取和分析,来了解天然色素的结构和性质。
实验步骤:
1.菠菜的准备
将新鲜的菠菜洗净后,去除根和水分,然后用手将菠菜叶子捏碎成小片状备用。
2.色素的提取
将捏碎的菠菜叶子放入料理机中,加入适量的酒精和石油醚,再开启料理机进行打浆,在打浆过程中注意随时观察,避免料理机出现卡顿的情况。
将打好的菠菜混合物过滤,将过滤得到的过滤液收集到干净的试管中,然后用滤纸进
行一次二次过滤,得到浅绿色的菠菜色素提取物。
3.色素的分离
4.色素的鉴定
将得到的菠菜色素溶液分别加入稀盐酸和稀碱液中,观察颜色变化,记录下来。
然后
将菠菜色素溶液加入小麦酰胺溶液中,搅拌均匀,观察颜色变化,记录下来。
实验原理:
本实验主要是利用了酒精、石油醚等有机溶剂的沸点差异,对菠菜中的色素进行了提取。
然后利用硅胶G的极性和吸附作用对菠菜色素进行了分离。
最后,通过加入稀盐酸、
稀碱液和小麦酰胺溶液来鉴定提取出来的色素种类和结构。
实验中所用到的酸和碱,可以将菠菜色素分解成不同的成分。
这些成分所表现出来的
颜色不同,可以通过色谱分析来确定其化学结构。
总结:
通过本实验,我们可以了解到菠菜中含有的天然色素,同时也可以学习到色素的分离
和分析技术。
此外,本实验还可以作为有机化学实验中的基础实验,为我们今后的学习和
研究提供了良好的基础。
实验十二- 菠菜色素的提取和分析
菠菜色素的提取和分离
实验目的
1、通过绿色植物色素的提取,学习天然物质的提取方法;
2、通过薄层色谱分析,掌握有机物色谱分析的原理和方法。
二、 实验原理
1 菠菜色素的提取
绿色植物如菠菜叶中含有叶绿素(绿) 、胡萝卜素(橙)和叶黄素(黄)等 多种天然色素。
叶绿素 存在两种结构相似的形式即叶绿素 a (C 55H 72O 5N 4Mg )和叶绿素 b
(C 55H 70O 6N 4Mg ),其差别仅是叶绿素 a 中一个甲基被甲酰基所取代从而形成了叶 绿素 b 。
它们都是吡咯衍生物与金属镁的络合物, 是植物进行光合作用所必需的 催化剂。
植物中叶绿素 a 的含量通常是 b 的 3 倍。
尽管叶绿素分子中含有一些 极性基团,但大的烃基结构使它易溶于醚、石油醚等一些非极性的溶剂。
胡萝卜素( C 40H 56)是具有长链结构的共轭多烯。
它有三种异构体,即 - 胡 萝卜素、β -胡萝卜素和γ - 胡萝卜素,其中β -胡萝卜素含量最多,也最重要。
在生物体内, β- 胡萝卜素受酶催化氧化形成维生素 A 。
目前β -胡萝卜素已可进 行工业生产,可作为维生素 A 使用,也可作为食品工业中的色素。
叶黄素( C 40H 56O 2)是胡萝卜素的羟基衍生物,它在绿叶中的含量通常是胡萝 卜素的两倍。
与胡萝卜素相比,叶黄素较易溶于醇而在石油醚中溶解度较小。
叶绿素 a (R
=
CH )
CH 3 CH 3 CH 3
OO
CH 3 CH 2
CH R
N N
Mg
N
N H 3C
CH 2CH 3 CH 3 CO 2CH 3 2 CH 3
H 3C R
维生素 A
2 薄层色谱原理
常用 TLC 表示,又称薄层层析,属于固液吸附色谱。
样品在薄层板上的吸 附剂(固定相)和溶剂(移动相)之间进行分离。
由于各种化合物的吸附能力 各不相同,在展开剂上移时,它们进行不同程度的解吸,从而达到分离的目的。
3 薄层色谱的用途:
1)化合物的定性检验。
(通过与已知标准物对比的方法进行未知物的鉴定) 在条件完全一致的情况,纯碎的化合物在薄层色谱中呈现一定的移动距 离,称比移值( Rf 值),所以利用薄层色谱法可以鉴定化合物的纯度或确定两种 性质相似的化合物是否为同一物质。
但影响比移值的因素很多,如薄层的厚度, 吸附剂颗粒的大小,酸碱性,活性等级,外界温度和展开剂纯度、组成、挥发 性等。
所以,要获得重现的比移值就比较困难。
为此,在测定某一试样时,最 好用已知样品进行对照。
溶质最高浓度中心至原 点中心的距离 溶剂前沿至原点中心的 距离
2、快速分离少量物质。
(几到几十微克,甚至 0.01 μg )
3、跟踪反应进程。
在进行化学反应时,常利用薄层色谱观察原料斑点的逐步消 失,来判断反应是否完成。
4、化合物纯度的检验(只出现一个斑点,且无拖尾现象,为纯物质。
)
此法特别适用于挥发性较小或在较高温度易发生变化而不能用气相色谱分 析的物质
β-胡萝卜素( R = H )
叶黄素( R = OH ) CH 3 CH 3 H3C CH3 CH 2OH
CH 3
4 薄层色谱的操作步骤
1、吸附剂的选择
薄层色谱的吸附剂最常用的是氧化铝和硅胶。
1)、硅胶:
“硅胶 H ”—不含粘合剂;
“硅胶 G ”—含煅石膏粘合剂;
其颗粒大小一般为 260 目以上。
颗粒太大,展开剂移动速度快,分离效果不好;反之,颗粒太小,溶剂移动太慢,斑点不集中,效果也不理想。
化合物的吸附能力与它们的极性成正比,具有较大极性的化合物吸附较强,因而R f 值较小。
酸和碱 > 醇、胺、硫醇 > 酯、醛、酮 > 芳香族化合物 > 卤代物、醚 > 烯 > 饱和烃
本实验选择的吸附剂为薄层色谱用硅胶 G。
2、薄层板的制备(湿板的制备)
薄层板制备的好坏直接影响色谱的结果。
薄层应尽量均匀且厚度要固定。
否则,在展开时前沿不齐,色谱结果也不易重复。
在烧杯中放入2g 硅胶 G,加
入 5—6ml 0.5% 的羧甲基纤维素钠水溶液,调成糊状。
将配制好的浆料倾注到清洁干燥的载玻片上,拿在手中轻轻的左右摇晃,使其表面均匀平滑,在室温下晾干后进行活化。
本实验用此法制备薄层板 4 片。
3、薄层板的活化将涂布好的薄层板置于室温凉干后,放在烘箱内加热活化,活化条件根据需要而定。
硅胶板一般在烘箱中渐渐升温,维持105—110℃活化 30min 。
氧化
铝板在200℃烘 4h 可得到活性为Ⅱ级的薄板,在 150—160℃烘 4h 可得活性为Ⅲ—Ⅳ级的薄板。
活化后的薄层板放在干燥器内保存待用。
4、点样
先用铅笔在距薄层板一端 1cm 处轻轻划一横线作为起始线,然后用毛细管吸取样品,在起始线上小心点样,斑点直径一般不超过 2mm 。
若因样品溶液太稀,可重复点样,但应待前次点样的溶剂挥发后方可重新点样,以防样点过大,造成拖尾、扩散等现象,而影响分离效果。
若在同一板上点几个样,样点间距
离应为 1。
点样要轻,不可刺破薄层。
5、展开薄层色谱的展开,需要在密闭容器中进行。
为使溶剂蒸气迅速达到平衡,
可在展开槽内衬一滤纸。
在层析缸中加入配好的展开溶剂,使其高度不超过 1cm 将点好的薄层板小心放入层析缸中,点样一端朝下,浸入展开剂中。
盖好瓶盖,观察展开剂前沿上升到一定高度时取出,尽快在板上标上展开剂前沿位置。
晾干,观察斑点位置,计算 Rf 值。
6、显色被分离物质如果是有色组分,展开后薄层色谱板上即呈现出有色斑点。
如果化合物本身无色,则可用碘蒸气熏的方法显色。
还可使用腐蚀性的显色剂如浓硫酸、浓盐酸和浓磷酸等。
对于含有荧光剂的薄层板在紫外光下观察,展开后的有机化合物在亮的荧光背景上呈暗色斑点。
本实验样品本身具有颜色,不必在荧光灯下观察。
三、主要试剂和仪器
1 试剂:硅胶 G, 95% 乙醇 , 石油醚(60—90℃), 丙酮 , 无水 MgSO4, 菠菜
2 仪器:层析板(25mm×75mm), 125ml 广口瓶 , 研钵 , 分液漏斗
四、实验步骤
1 菠菜色素的提取
称取 5g无水的新鲜菠菜叶,用研钵研碎,加入 15 ml 石油醚-乙醇溶剂(3:2)研磨至桨,抽滤,滤液放至分液漏斗中,加入 5ml饱和 NaCl 水溶液,分层,上层再用饱和 NaCl 水溶液洗涤,有机层用无水 MgSO4干燥,滤去 MgSO4后,滤液放入小烧杯中,水浴蒸去溶剂(控制温度(60°-70 ℃),浓缩至 2.5ml 左右为止。
2 薄层层析
取活化后的层析板,点样,小心放入盛有展开剂( 7:3 石油醚- 丙酮)的广口瓶内,样点不能浸到展开剂中,盖好瓶盖,待展开剂上升至规定高度时,取出层析板,在空气中晾干,计算三种色素(叶绿素、叶黄素和胡萝卜素)的 Rf 值。
注:叶绿素会出现两点(叶绿素 a,叶绿素 b)。
叶黄素易溶于醇而在石油醚中溶解度小,从嫩绿叶中得到提取液,叶黄素会显很少。
五、注意事项
注意薄层色谱、柱层析实验操作要点的掌握和应用
六、思考题
1、如何利用 Rf 值来鉴定化合物?
2、薄层色谱法点样应注意些什么?
3、常用的薄层色谱的显色剂是什么?。