丙型肝炎病毒的生物危害评估报告
- 格式:docx
- 大小:48.30 KB
- 文档页数:11

一、生物学特性(一)种类和病毒分型丙型肝炎病毒(Hepatitis Cvirus,HCV)引起的丙型肝炎曾被称为肠道外传播的非甲非乙型肝炎(PT-NANB)。
病毒颗粒呈球形,有包膜,直径约55~65nm。
基因组为单正链线状RNA,长度约为。
基因组由5'端非编码区(5'UTR)、编码区和3'端非编码区(3'UTR)组成。
5'端非编码区是HCV基因组中最保守的序列,是设计诊断用PCR引用的首选部位。
编码区仅含一个长的开放阅读框(ORF),编码一个大分子的多聚蛋白前体。
该前体蛋白在病毒蛋白酶和宿主信号肽酶的作用下切割产生病毒的结构蛋白和非结构蛋白。
病毒的结构蛋白包括核心蛋白C和包膜蛋白E1、E2。
非结构蛋白包括NS2、NS3、NS4a、NS4b、NS5a和NS5b。
对于3'端非编码区的功能尚不清楚,可能与病毒复制有一定关系。
根据HCV NS5区基因序列的同源性,可将HCV分为6个基因型,11个亚型,即1a、1b、1c、2a、2b、2c、3a、3b、4a、5a、6a。
其中,欧美流行株多为1a、1b、2a、2b和3a;中东地区以4a为主;亚洲包括我国以1b、2a和2b亚型较为多见。
(二)来源1989年,美国学者Choo等应用了分子克隆技术在实验室感染PT-NANB的黑猩猩血浆中首次获得了病毒的cDNA克隆,测定了约70%的HCV基因序列,并利用这些基因表达的蛋白质为抗原,检测到PT-NANB病人血清中的特异性抗体。
此后,又获得了来自PT-NANB患者血清的病毒全基因组序列,从而确定了PT-NANB的病原体,并将命名为丙型肝炎病毒。
1991年,国际命名委员会将其归类为黄病毒科丙型肝炎病毒属。
(三)传染源主要传染源为急、慢性患者和无症状HCV携带者。
慢性患者和病毒携带者有更重要的传染源意义。
(四)传播途径传播途径主要为输血及血制品传播。
此外,亦可通过非输血隐性途径的微小创伤、性接触、家庭密切接触及母婴接触进行传播。

免疫生物实验室风险评估报告一、医学检验科概况医学检验科为临床医学检验实验室,免疫生物实验室主要是 HBV、HCV、HIV、HAV、HEV和梅毒螺旋体标本进行检验分析,实验室房屋1间。
设备有:生物安全柜、高压灭菌锅、紫外线消毒灯等设备。
二、组织管理医院成立生物安全委员会,负责医院生物安全管理总体工作。
负责制定包括教育,定位及培训、审核及评估促进实验室安全行为的程序的实验室安全计划。
督导生物安全制度的执行和措施的落实;重大实验室生物安全事故的认定、危害评估和处置方案的制定。
三、人员管理实验室配备2名专业技术人员,均参加过省临检中心实验室生物安全管理培训,并获得培训证书。
四、实验室设备实验室有独立的实验室专用房间,并严格划分污染区、半污染区和清洁区。
设备配备有酶标仪、洗板机、生物安全柜、恒温箱和压力蒸汽灭菌器。
并建立SOP文件,严格按照规范操作。
五、评估目的确定实验室防护等级,建立生物安全防护机制,配备适当的防护用品,采取相应的防护措施。
有效预防和控制实验室工作人员发生职业暴露感染。
六、评估依据评估依据:中华人民共和国国家标准《实验室生物安全通用要求》(GB19489-2008)、国务院《病原微生物实验室生物安全管理条例》卫生部令《人间传染的病原微生物名录》。
七、病原体风险评估及控制措施1、乙型肝炎病毒危害1.1 危害程度分类1.1.1 分类等级:乙型肝炎病毒(hepatitis B virus,HBV)是引起乙型肝炎的病原体,卫生部公布的《人间传染的病原微生物名录》中将其列为第三类病原微生物(危害程度为II级),属致病性病原微生物。
1.1.2 不同实验操作生物安全实验室级别需求:根据《人间传染的病原微生物名录》的规定,在实验操作涉及HBV的培养、未经培养的感染材料的操作及HBV的动物实验,应在BSL-2实验室进行,灭活材料的操作和无感染材料的操作可在BSL-1实验室进行。
1.2一般生物学特性1.2.1 病毒稳定性:HBV对外界抵抗力较强。

肝炎病毒的生物危害评估报告肝炎病毒是引起病毒性肝炎的病原体。
人类肝炎病毒有甲型、乙型、非甲非乙型和丁型病毒之分。
甲型肝炎病毒呈球形,无包膜,核酸为单链RNA。
乙型肝炎病毒呈球形,具有双层外壳结构,外层相当一般病毒的包膜,核酸为双链DNA。
对非甲非乙型肝炎病毒和丁型肝炎病毒目前正在研究之中。
甲型肝炎病毒引起甲型肝炎,这种肝炎的传染源主要是病人。
其病毒通常由病人粪便排出体外,通过被污染的手、水、食物、食具等传染,严重时会引起甲型肝炎流行。
如1988年1月,上海市出现了较大规模的流行性甲型肝炎,主要原因是人们食用了被甲肝病毒污染的毛蚶。
乙型肝炎主要通过注射、输血等方式进行传播。
为防止甲型肝炎的发生和流行,应重视保护水源,管理好粪便,加强饮食卫生管理,讲究个人卫生,病人排泄物、食具、床单衣物等应认真消毒。
为防止乙型肝炎的传播,在输血时应严格筛除乙型肝炎抗原阳性献血者,血液和血液制品应防止乙型肝炎抗原的污染,注射品及针头在使用之前应严格消毒。
一、肝炎病毒的分类:(一)甲型肝炎病毒(HAV)是一种RNA病毒,属微小核糖核酸病毒科,是直径约27nm的球形颗粒,由32个壳微粒组成对称20面体核衣壳,内含线型单股RNA。
HAV具有4个主要多肽,即VP1、VP2、VP3、VP4、其中VP1与V P3为构成病毒壳蛋白的主要抗原多肽,诱生中和抗体。
HA V在体外抵抗力较强,在-20℃条件下保存数年,其传染性不变,能耐受56℃30分钟的温度及PH3的酸度。
(二)乙型肝炎病毒(HBV)是一种DNA病毒,属嗜肝DNA病毒科(hepadnavividae),是直径42nm的球形颗粒。
又名Dane颗粒,有外壳和核心两部分。
外壳厚7-8nm,有表面抗原(HBsAg),核心直径27nm,含有部分双链,部分单链的环状DNA,DNA聚合酶,核心抗原及e抗原。
HBV DNA的基因组约含3200个硷基对。
长链的长度固定,有一缺口(nick)此处为DAN聚合酶;短链的长度不定。

实验活动生物危害评估报告为保证实验室工作人员在工作中不被危害性生物及物品所侵害,保证危害性物品不外泄,对实验室工作环境进行评估,以鉴定生物安全防护等级,保证生物安全。
一、危害程度分类及生物安全防护水平评估本实验室是为医院科研工作提供公共科研平台。
生物源危害主要是由临床取材标本(如血液、组织等)中的微生物,尤其是病原微生物引起的,包括细菌、病毒、寄生虫等,具有潜在危险性,可能引起实验室感染;此外,实验室还存在触电、火灾、化学腐蚀、偷盗等危险。
根据《实验室生物安全通用要求》,本实验室不涉及《人间传染的病原微生物名录》中高致病性微生物的分离培养及高致病性微生物的菌、毒种的保藏,实验室采用一定防护措施就能控制感染或防范灾害,或者对相应病原体存在有效的免疫方法。
评估我实验室生物安全防护水平按二级实验室(BSL-2)生物安全要求。
二、实验室工作人员和实验室安全防护的一般要求1. 吸烟危害评估及防护(1)实验室工作区内绝对禁止吸烟;(2)点燃的香烟是易燃液体的潜在火种2. 实验区内食用食物、饮料及其他危害评估及防护(1)实验室工作区内不得有食物、饮料及存在“手-口”接触可能的其他物质;(2)实验室工作区内的冰箱禁止存放食物,专用存放食物的冰箱应放置在允许进食、喝水的休息区内。
3. 使用化妆品危害评估及防护实验工作区内禁止使用化妆品进行化妆,但允许并建议经常洗手的实验人员使用护手霜。
4. 实验中眼睛和面部的风险评估及防护(1)处理腐蚀性或毒性物质时,需使用护目镜、面罩或其他保护眼睛和面部的防护用品;(2)工作人员在实验室的危险区内不要佩戴隐形眼镜,除非同时使用护目镜或面罩;(3)使用、处理能通过粘膜或皮肤感染的试剂,或有可能发生试剂溅溢的情况时,必须佩带护目镜、面罩。
5. 实验中服装和个人防护装备的一般要求(1)应穿着符合实验室工作需要的服装,工作服应干净、整洁;当工作中有危险喷溅到身上的可能时,应使用一次性塑料围裙或防渗外罩;有时还需要佩戴其他防护装备,如:手套、护目镜、面罩等;(2)个人防护服应定期更换以保持清洁,遇被危险物品严重污染,则应立即更换;(3)不得在实验室内设置值班床,严禁在实验室内住宿。

丙型肝炎病毒实验活动风险评估报告HCV的潜伏期一般为2-26周,平均为6-7周。
但有些患者可长达6个月或更长时间才出现症状。
二、实验活动风险评估一)实验室操作风险1.病毒分离、培养和纯化:在实验室中进行HCV的分离、培养和纯化,是进行HCV研究的必要步骤。
但这些操作存在一定的危险性,可能导致实验人员的HCV感染。
2.实验室检测:实验室检测HCV的方法主要有免疫学和分子生物学两种。
在实验室进行检测时,需要使用HCV抗原或HCV基因,这些物质可能会对实验室人员造成污染和感染风险。
3.实验室废弃物处理:实验室中产生的废弃物包括病毒培养物、污染的培养物、实验器皿等,这些废弃物需要进行严格的处理,以避免对环境和人员造成污染和感染风险。
二)实验室安全管理1.实验室人员培训:实验室人员需要接受相关的培训,了解HCV的生物学特性、传播途径、感染机制等,掌握正确的实验操作技能和安全防护知识,以降低感染风险。
2.实验室安全设施:实验室需要配备符合安全标准的生物安全柜、洗眼器、紫外线消毒器等设施,以保障实验室人员的安全。
3.实验室操作规程:实验室需要制定完善的操作规程,包括实验室人员的行为规范、实验操作流程、废弃物处理方法等,以规范实验室操作,降低感染风险。
三)实验室应急措施1.实验室人员应急预案:实验室需要制定完善的应急预案,包括事故处理流程、应急处置措施、紧急联系方式等,以应对突发情况。
2.实验室安全检查:实验室需要定期进行安全检查,发现问题及时整改,确保实验室的安全运行。
三、结论HCV是一种存在较高感染率的病毒,实验室操作中存在一定的感染风险。
因此,实验室需要制定完善的安全管理制度和应急预案,加强实验室安全培训和安全设施建设,确保实验室人员的安全和实验室的安全运行。
一般来说,病毒在离开宿主后会很快死亡,丙型肝炎病毒也不例外,通常在10分钟左右就会死亡。
国内外的研究已经证实,丙型肝炎和乙型肝炎是肝癌的重要病因。
国外的Meta分析结果显示,HCV感染对肝癌的危险比值比(OR)达到了11.5,并且与HCV的混合感染表现出协同作用。
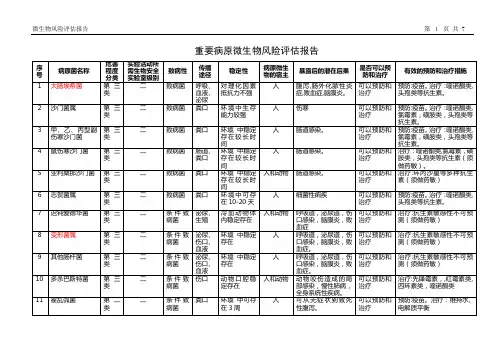
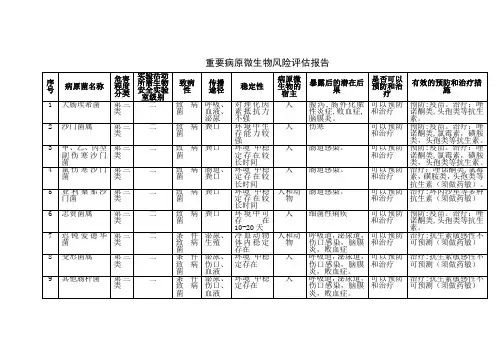

生物安全风险评估及控制一、检验职业感染的现状经血、呼吸道、粘膜传播疾病直接危害着检验工作者身体健康。
我国是HBV感染的高发区,约有1.3亿人携带HBV,HBV表面抗原(HBsAg)的携带率为8%-20%;自90年代以来HCV感染也呈上升趋势,其感染率为3%。
目前艾滋病感染在我国的流行已进入增长期。
在无偿献血人群中检出乙型肝炎、丙型肝炎、梅毒、艾滋病等病毒感染占有一定的比例。
经调查显示,针头和玻璃碎片是主要锐器致伤因子,经常接触针头者发生锐器伤的危险是不经常接触者的23倍。
多种传染病是通过血液传染的,而血液检验中的职业暴露大多数来自实验室工作人员在实验操作和标本采集过程中,意外被带病原体的血液污染破损的皮肤或被病原体感染的针头、血常规采血针、采血玻璃管、吸头等锐器刺破皮肤,呼吸道吸入气溶胶也是传播方式之一。
因此,检验人员面临着严峻的职业暴露危险。
1.传播途径检验人员感染疾病的一般传染途径有:(1)皮肤破损:带有HIV、HBV、HCV、梅毒等病原体的血液,长时间接触小伤口、溃疡、擦伤等破损皮肤,将会造成机体的感染。
(2)穿刺:由于针头、刀片等对皮肤的意外损伤,使带有病毒的全血、血清或血浆进入皮下或循环系统,造成感染。
这种针头意外损伤是职业性HBV和HIV感染最重要的原因。
带有HIV 的针头意外穿刺皮肤后,HIV感染的可能性在0--0.9%之间,平均为0.4%。
而对于HBV,这个可能性在6%-30%之间,平均为18%。
有学者进行了相应的统计推算,每1000个艾滋病病人,每年会产生1例由于针头意外造成的职业性HIV感染;而每1000个乙肝患者,每年会产生45例类似职业性HBV感染。
由于HBV在人群中的感染率比HIV高得多,在一定人群中,每年产生的因针头意外造成的职业性HBV感染比HIV多得多。
(3)粘膜:由于试管未封闭、离心意外等造成的血液飞溅,带有病原体的血液与口腔、鼻腔黏膜或眼结膜等接触,可以造成感染。

丙型肝炎危害评估丙型肝炎病毒危害评估报告1.危害程度分类1.1分类等级根据《中华人民共和国传染病防治法》,丙型肝炎病毒(HCV)属于乙类传染病。
在卫生部2006年公布的《人间传染的病原微生物名录》中将丙型肝炎病毒列为危害程度第三类病原微生物。
运输包装仅病毒培养物为B类,UN编号为UN3373。
1.2不同实验室操作生物安全实验室级别要求根据《人间传染的病原微生物名录》要求:丙型肝炎血清学检测属于未经培养的感染材料的操作,应在符合Ⅱ级生物安全实验室(BSL-2)要求的实验室中进行。
2.背景资料2.1一般生物学特性HCV病毒体呈球形,直径小于80nm(在肝细胞中为36~40nm,在血液中为36-62nm),为单股正链RNA病毒,在核衣壳外包绕含脂质的囊膜,囊膜上有刺突。
2.2对外界环境的稳定性对情况敏理性:对温度较敏感,加热100℃5分钟或60℃1小时可将其灭活。
20%次氯酸钠可消除其沾染性,对氯仿、甲醛、乙醚等有机溶剂敏感。
2.3致病性丙型肝炎病人约50%可发展为慢性肝炎,甚至部分病人会招致肝硬及肝细胞癌。
别的约半数病人为自限性,可自动康复。
丙型肝炎发病机理仍未十分分明,当HCV在肝细胞内复制引起肝细胞布局和功能改变或干扰肝细胞蛋白合成,可造成肝细胞变性坏死,表明HCV直接损害肝脏,招致发病起一定作用。
但多数学者以为细胞免疫病理反应大概起重要作用,发现丙型肝炎与乙型肝炎一样,其组织浸润细胞以CD3+为主,细胞毒T细胞(TC)特异攻击HCV感染的靶细胞,可引起肝细胞损伤。
临床观察材料表明,人感染HCV后所产生的保护性免疫力很差,能再感染不同,甚至部分病人会招致肝软化及肝细胞癌。
别的约半数病人为自限性,可自动康复。
2.4传播途径:2.5丙型肝炎的预防、诊断和治疗2.5.1预防丙型肝炎的预防方法基本与乙型肝炎的相同。
目前,我国预防丙型肝炎的重点应放在对献血员的管理,加强消毒隔离制度,防止医源性传播。
2.5.2尝试室检查及其诊断临床施展阐发形式多样,诊断的根据除病人症状,体征外,须根据流行病学,尝试室检查和或肝活检等手腕进行综合分析,动态观察诊断。

XXX生物安全风险评估报告报告:XXX生物安全风险评估依据《病原微生物实验室生物安全管理条例》、《实验室生物安全通用要求》、《微生物和生物医学实验室生物安全通用准则》、《医疗废物管理条例》,我们按照检验科制定的《实验室生物安全管理制度》,由医院生物安全委员会主持,生物安全委员会成员参与,对检验科生物安全进行了风险评估,形成报告如下:一、科室基本情况1.专业组:根据检验科的实际情况,按照生物安全二级防护实验室的要求划分实验室区域:临床血液学实验室、临床体液学实验室、临床化学实验室、临床免疫学实验室、临床PCR实验室、微生物实验室、采血室、标本接收室。
2.实验室的环境布局及平面图(见环境分布图)清洁区:包括会议室、办公室、休息室、浴室2个、男女更衣室、管理室、库房。
半污染区:洗刷室、试剂库、中间通道。
污染区:临床血液学实验室、临床体液学实验室、临床化学实验室、临床免疫学实验室、临床PCR实验室、微生物实验室、采血室、标本接收室、洗涤室。
3.任务:承担临床检验、教学及科研。
二、实验室生物安全风险评估一)对生物源危害风险评估临床实验室生物源危害主要是由微生物,尤其是病原微生物引起的。
包括细菌、病毒、寄生虫等。
在实验室内做试验、研究等操作时,实验人员需要处理大量的病源微生物,很容易引起污染。
根据生物污染的对象,为空气污染、水污染、人体污染、物体表面污染等种类。
1.对空气的污染:根据污染空间,可分为实验室内环境空气污染、实验室外环境空气污染。
许多操作可产生气溶胶,是悬浮于气体介质中粒子一般为0.001-100um的固体,液体微子粒子形成胶溶状态分散体系。
当气溶胶不能安全有效地限定在一定范围内,便导致实验室内空气污染。
下述操作可能产生气溶胶:使用涡旋震荡器、用力拍干反应板超声波处理、试液开封、开启冰箱和离心机及舍弃离心后的上清液时、另外动物接种从动物体内采血、清洗注射器、调整液量也可产生。
2.对水的污染:实验中会产生大量污水,医院污水尤其是传染病医院,综合医院传染病房的污水,有大量的有机悬浮物和固体残渣,还不同程度的含有多种细菌、病毒和寄生虫虫卵。

丙型肝炎病毒实验活动风险评估报告一、生物学特性(一)种类和病毒分型丙型肝炎病毒(Hepatitis Cvirus,HCV)引起的丙型肝炎曾被称为肠道外传播的非甲非乙型肝炎(PT-NANB)。
病毒颗粒呈球形,有包膜,直径约55~65nm。
基因组为单正链线状RNA,长度约为9.5kb。
基因组由5'端非编码区(5'UTR)、编码区和3'端非编码区(3'UTR)组成。
5'端非编码区是HCV基因组中最保守的序列,是设计诊断用PCR引用的首选部位。
编码区仅含一个长的开放阅读框(ORF),编码一个大分子的多聚蛋白前体。
该前体蛋白在病毒蛋白酶和宿主信号肽酶的作用下切割产生病毒的结构蛋白和非结构蛋白。
病毒的结构蛋白包括核心蛋白C和包膜蛋白E1、E2。
非结构蛋白包括NS2、NS3、NS4a、NS4b、NS5a和NS5b。
对于3'端非编码区的功能尚不清楚,可能与病毒复制有一定关系。
根据HCV NS5区基因序列的同源性,可将HCV分为6个基因型,11个亚型,即1a、1b、1c、2a、2b、2c、3a、3b、4a、5a、6a。
其中,欧美流行株多为1a、1b、2a、2b和3a;中东地区以4a为主;亚洲包括我国以1b、2a和2b亚型较为多见。
(二)来源1989年,美国学者Choo等应用了分子克隆技术在实验室感染PT-NANB的黑猩猩血浆中首次获得了病毒的cDNA克隆,测定了约70%的HCV基因序列,并利用这些基因表达的蛋白质为抗原,检测到PT-NANB病人血清中的特异性抗体。
此后,又获得了来自PT-NANB患者血清的病毒全基因组序列,从而确定了PT-NANB的病原体,并将命名为丙型肝炎病毒。
1991年,国际命名委员会将其归类为黄病毒科丙型肝炎病毒属。
(三)传染源主要传染源为急、慢性患者和无症状HCV携带者。
慢性患者和病毒携带者有更重要的传染源意义。
(四)传播途径传播途径主要为输血及血制品传播。
丙型肝炎危害评估丙型肝炎是一种由丙型肝炎病毒(HCV)引起的肝炎,它是一种全球性的公共卫生问题。
丙型肝炎病毒主要通过血液传播,但也可通过其他途径如性接触和母婴传播。
丙型肝炎病毒感染后,可能导致急性或者慢性肝炎,严重情况下可能导致肝硬化和肝癌。
丙型肝炎的危害主要体现在以下几个方面:1. 健康影响:丙型肝炎病毒感染后,大部份人会浮现急性肝炎症状,如乏力、食欲不振、恶心、呕吐、黄疸等。
在急性期过后,约75-85%的感染者会发展成慢性肝炎。
长期的慢性肝炎可能导致肝纤维化、肝硬化和肝癌等严重并发症。
2. 经济负担:丙型肝炎病毒感染对患者和社会经济造成为了巨大负担。
患者需要进行长期的药物治疗,并时常进行肝功能监测和病毒载量检测。
治疗费用和医疗费用对患者和家庭来说是一笔巨大的开支。
此外,丙型肝炎病毒感染还会导致患者长期失去工作能力,给个人和家庭带来经济难点。
3. 传播风险:丙型肝炎病毒主要通过血液传播,但也可通过其他途径如性接触和母婴传播。
因此,丙型肝炎病毒感染的传播风险较高。
在医疗机构和注射毒品者中,由于血液暴露和共用注射器等因素,感染风险更高。
此外,丙型肝炎病毒感染者在无症状的情况下也可能传播病毒给其他人。
为了减少丙型肝炎的危害,我们可以采取以下措施:1. 提高公众意识:通过开展健康教育活动,提高公众对丙型肝炎的认识和了解,宣传丙型肝炎的传播途径和预防方法,促进个人和社会的防控意识。
2. 加强病毒检测:建立健全的丙型肝炎病毒检测体系,提高感染者的检出率。
对高风险人群如医务人员、注射毒品者等进行定期检测,及时发现感染者并采取相应的干预措施。
3. 推广疫苗接种:丙型肝炎疫苗是预防丙型肝炎最有效的方法之一。
加强疫苗接种宣传,推广疫苗接种,特殊是对高风险人群和儿童进行疫苗接种,有效预防丙型肝炎的发生。
4. 加强医疗服务:提高丙型肝炎患者的就诊率和诊断率,加强对患者的医疗管理和治疗。
提供规范的药物治疗和监测服务,减轻患者的经济负担,降低丙型肝炎病毒的传播风险。
丙肝风险评估报告一、引言丙型肝炎(HCV)是一种由丙型肝炎病毒引起的传染病,通过血液传播。
该疾病在全球范围内广泛流行,是一种慢性肝炎,也是引起肝硬化和肝癌的主要原因之一。
针对丙肝的高风险人群,进行风险评估是非常重要的。
本报告旨在通过详细调查和评估丙肝风险因素,帮助个人了解自己的风险程度,从而采取相应的预防和治疗措施。
二、调查方法本次风险评估报告通过以下方法进行数据收集和分析:1.风险因素调查表:参与者填写风险因素调查表,包括相关的个人信息和生活习惯等。
2.个人家族史调查:参与者提供相关的个人家族史信息,以评估遗传因素的风险。
3.医学记录:参与者提供医学记录和检测结果,如肝功能检测报告等。
以上信息被匿名收集和分析,确保个人隐私和数据安全。
三、风险因素评估根据参与者提供的信息,我们对风险因素进行了评估,并将其分为以下几个方面:1. 血液接触•有无注射毒品史•是否有输血史•是否有器官移植史•是否有使用过未经消毒的注射器具2. 医疗操作•是否有进行过肝脏手术或其他有血液接触的操作•是否有进行过血透或血浆制品注射3. 个人生活习惯•是否有过性行为传播丙肝病毒的风险•是否有共用个人卫生用品的习惯•是否有从事危险职业的经历,如医疗工作者、卫生部门从业人员等4. 个人家族史•家族是否有丙肝患者•家族成员是否有肝癌等相关疾病四、风险等级划分根据参与者的风险因素信息和评估结果,我们将其风险等级划分为以下几个类别:•高风险:具有明显的风险因素,如注射毒品史、器官移植史、肝脏手术等•中风险:存在一定的风险因素,如血透、共用个人卫生用品等•低风险:风险因素较少或没有明显的风险因素,如无相关家族史、从事非危险职业等五、预防和控制建议根据参与者的风险等级,我们提出以下预防和控制建议:1.高风险群体:–定期进行丙肝病毒抗体检测,了解感染情况;–避免使用未经消毒的注射器具;–避免共用个人卫生用品;–咨询医生,了解相关预防和治疗措施。
丙型肝炎病毒实验活动风险评估报告一、生物学特性(一)种类和病毒分型丙型肝炎病毒(HepatitisCvirus,HCV)引起的丙型肝炎曾被称为肠道外传播的非甲非乙型肝炎(PT-NANB)。
病毒颗粒呈球形,有包膜,直径约55~65nm。
基因组为单正链线状RNA,长度约为9.5kb。
基因组由5'端非编码区(5'UTR)、编码区和3'端非编码区(3'UTR)组成。
5'端非编码区是HCV基因组中最保守的序列,是设计诊断用PCR引用的首选部位。
编码区仅含一个长的开放阅读框(ORF),编码一个大分子的多聚蛋白前体。
该前体蛋白在病毒蛋白酶和宿主信号肽酶的作用下切割产生病毒的结构蛋白和非结构蛋白。
病毒的结构蛋白包括核心蛋白C和包膜蛋白E1、E2。
非结构蛋白包括NS2、NS3、NS4a、NS4b、NS5a和NS5b。
对于3'端非编码区的功能尚不清楚,可能与病毒复制有一定关系。
根据HCVNS5区基因序列的同源性,可将HCV分为6个基因型,11个亚型,即1a、1b、1c、2a、2b、2c、3a、3b、4a、5a、6a。
其中,欧美流行株多为1a、1b、2a、2b和3a;中东地区以4a为主;亚洲包括我国以1b、2a和2b亚型较为多见。
(二)来源1989年,美国学者Choo等应用了分子克隆技术在实验室感染PT-NANB的黑猩猩血浆中首次获得了病毒的cDNA克隆,测定了约70%的HCV基因序列,并利用这些基因表达的蛋白质为抗原,检测到PT-NANB病人血清中的特异性抗体。
此后,又获得了来自PT-NANB患者血清的病毒全基因组序列,从而确定了PT-NANB的病原体,并将命名为丙型肝炎病毒。
1991年,国际命名委员会将其归类为黄病毒科丙型肝炎病毒属。
(三)传染源主要传染源为急、慢性患者和无症状HCV携带者。
慢性患者和病毒携带者有更重要的传染源意义。
(四)传播途径传播途径主要为输血及血制品传播。
乙肝生物安全评估
乙肝是由丙型肝炎病毒(HBV)引起的一种传染病。
针对乙
肝的生物安全评估主要从以下几个方面进行:
1. 病毒的生物学特性:乙肝病毒是一种DNA病毒,具有很高
的传染性和稳定性。
其在人体内的复制能力强,且可以通过各种途径传播。
2. 疫情调查:通过对乙肝疫情的调查研究,评估乙肝传播的范围和程度,了解其对人群和社会的危害性。
3. 传播途径:评估乙肝的传播途径,包括垂直传播(婴幼儿从感染母亲传播)、血液传播(输血、注射药物和医疗器械传播)和性传播等。
4. 乙肝病毒检测方法:评估目前用于乙肝病毒检测的方法,包括血清学检测、核酸检测和免疫学检测等。
评估这些方法的准确性和敏感性,以便及时发现感染者并进行干预措施。
5. 传播防控措施:评估乙肝的传播防控措施,包括疫苗接种、卫生教育、血液安全管理和医疗器械的安全使用等。
评估这些措施的有效性和可行性,以减少乙肝的传播风险。
6. 社会经济影响:评估乙肝对社会经济的影响,包括医疗资源的消耗、劳动力的损失和患者家庭的负担等。
评估这些影响的大小和可持续性,以制定相关的政策和措施。
综上所述,乙肝生物安全评估是为了全面了解乙肝的病原学特性、传播途径和预防措施,并评估其对人群和社会的危害性。
通过评估,可以提出有效的防控策略和政策,减少乙肝的传播风险和社会经济影响。
丙型肝炎病毒的生物危害评估报告丙型肝炎病毒的传播与致病丙型肝炎的传染源主要为急性临床型和无症状的亚临床病人,慢性病人和病毒携带者。
一般病人发病前12天,其血液即有感染性,并可带毒12年以上。
HCV主要血源传播,国外30-90%输血后肝炎为丙型肝炎,我国输血后肝炎中丙型肝炎占1/3。
此外还可通过其他方式如母婴垂直传播,家庭日常接触和性传播等。
输入含HCV或HCV-RNA的血浆或血液制品,一般经6-7周潜伏期例急性发病,临床表现全身无力,胃纳差,肝区不适,1/3病人有黄疸,ALT升高,抗HCV抗体阳性。
临床丙型肝炎病人50%可发展为慢性肝炎,甚至部分病人会导致肝硬及肝细胞癌。
其余约半数病人为自限性,可自动康复。
丙型肝炎发病机理仍未十分清楚,当HCV在肝细胞内复制引起肝细胞结构和功能改变或干扰肝细胞蛋白合成,可造成肝细胞变性坏死,表明HCV直接损害肝脏,导致发病起一定作用。
但多数学者认为细胞免疫病理反应可能起重要作用,发现丙型肝炎与乙型肝炎一样,其组织浸润细胞以CD3+为主,细胞毒T细胞(TC)特异攻击HCV感染的靶细胞,可引起肝细胞损伤。
临床观察资料表明,人感染HCV后所产生的保护性免疫力很差,能再感染不同,甚至部分病人会导致肝硬化及肝细胞癌。
其余约半数病人为自限性,可自动康复。
结核杆菌通常指结核分枝杆菌和牛分枝杆菌,其中结核分枝杆菌(Mycobacterium tuberculosis)是引起人类结核病的主要病原体。
结核分枝杆菌的主要传染途径是经呼吸道传播,由排菌的肺结核病人在咳嗽、喷嚏或大声说话时随呼吸道分泌物排出到空气中,或排菌的肺结核病人随地吐痰通过再生气溶胶(尘埃),携带结核杆菌,飞扬在空气中,被健康的人吸入后发生感染和发病,因此排菌的肺结核患者(尤其是痰涂片阳性未经治疗者)是结核病的主要传染源。
一般结核病患者痰中结核杆菌越多,传播的危险性越大。
患者排出的飞沫在1-10微米者,在空气中漂浮时间长,传染性越大。
患者病变和症状越严重,传染性也越大。
周围人群与患者接触越密切者,受感染的机会越多。
与患者同处于空气不流通的室内的密切接触者,受感染的可能性增大。
未受结核感染的人是结核病易感人群,由于结核病是人畜共患病,哺乳类动物如牛、鹿、猴、猪、猫、狗等也都可以患结核病。
感染结核杆菌后,终身都有可能发病,发病时间因人而异,一般2个月~20年才发病。
典型肺结核起病缓慢,病程较长,有低热、倦怠、食欲不振、咳嗽及少量咯血。
但多数患者病灶轻微,无显著症状。
(1)症状①全身症状表现为午后低热、乏力、食欲不振、消瘦、盗汗等。
②呼吸系统症状通常为干咳或带少量黏液痰;继发感染时,痰呈粘液脓性。
约1/3患者有不同程度咯血,咯血后常有低热。
大咯血时可发生失血性休克,偶因血块阻塞大气道引起窒息。
病灶炎症累及壁层胸膜时,相应胸壁有刺痛,一般多不剧烈,随呼吸及咳嗽而加重。
若并发气胸或大量胸腔积液,呼吸困难症状尤为严重。
(2)体征早期病灶小或位于肺组织深部,多无异常体征。
若病变范围较大,患侧肺部呼吸运动减弱,叩诊呈浊音,听诊时呼吸音减低,或为支气管肺泡呼吸音。
因肺结核好发于肺上叶尖后段及下叶背段,故锁骨上下、肩胛区叩诊略浊,咳嗽后偶可闻及湿啰音,对诊断有参考意义。
肺部病变发生广泛纤维化或胸膜粘连增厚时,患侧胸廓常呈下陷、肋间隙变窄、气管移位与叩浊,对侧可有代偿性肺气肿征。
二、结核杆菌的生物学特性从分类学上看结核杆菌属于裂殖菌纲、放线菌目、分枝杆菌科、分枝杆菌属。
结核分枝杆菌正常典型的形态是直或稍弯曲、两端钝圆的杆菌,菌体长1-4纳米,宽0.3-0.6纳米,无芽胞、无荚膜、无鞭毛,生长发育期间有分枝生长倾向。
镜下常呈单个散在或呈“人、V、T、Y”形排列,菌体多时细菌扭集一起呈绳索状、束状或丛状。
此外结核杆菌菌体还具有多形态特征,受不良生长条件的影响可分别表现为杆菌型(基本形态)、滤过型、颗粒型和球菌型(L型)4种不同的类型。
分枝杆菌生长缓慢,在人工培养基内繁殖一代约需15-20小时,一般需2-4周或更长时间始见菌落生长,甚至有极少数生长极为缓慢者需8周以上才开始有菌落生长。
它为专性需氧菌,生长的温度范围是35-40℃,pH 5.5-7.2。
培养营养要求较高且特殊,培养基需含鸡蛋、血清、氨基酸、甘油等营养丰富的复杂有机物及少量无机盐类。
而且结核杆菌随着环境的改变易发生菌落形态、毒力、L型及药物耐药性变异,如在人工培养基上反复连续传代,可产生变异而致毒力降低。
三、丙型肝炎病毒的检测与诊断一、实验室检查(一)血常规急性肝炎初期白细胞总数正常或略高,一般不超过10×109/L,黄疸期白细胞总数正常或稍低,淋巴细胞相对增多,偶可见异型淋巴细胞。
重型肝炎时白细胞可升高,红细胞下降,血红蛋白下降。
肝炎肝硬化伴脾功能亢进可有血小板、红细胞、白细胞减少的“三少”现象。
(二)尿常规尿胆红素和尿胆原的检测是早期发现肝炎的简易有效方法,同时有助于黄疸的鉴别诊断。
肝细胞性黄疸时两者均阳性,溶血性黄疸时以原为主,梗阻性黄疸以尿胆红素为主。
深度黄疸或发热患者,尿中除胆红素阳性外,还可出现蛋白质、红、白细胞或管型。
(三)肝功能检查1、血清酶测定(1)丙氨酸氨酶(ALT,曾称为谷丙氨酶GPT):是目前林装上反映肝细胞功能的最常用指标。
ALT在肝细胞损伤时释放入血流。
血清ALT升高,对肝病诊断的特异性比天冬氨酸氨酶(AST)高,因为其他脏器中ALT含量比AST低得多。
急性肝炎时ALT明显升高,AST/ALT常小于1,黄疸出现后ALT开始下降。
慢性肝炎和肝硬化时ALT轻度或中度升高或反复异常,AST/ALT常大于1。
比值越高,则预后愈差,病程中AST/ALT比值降低,提示未损及肝细胞线粒体,预后较佳。
重型肝炎患者可出现ALT快速下降,胆红素不断酶升高、胆分离现象,提示肝细胞大量坏死。
(2)天冬氨酸转氨酶(AST,曾称为谷草转氨酶GOT):此酶在心肌含量最高,依次为肝、骨骼肌、肾、胰。
在肝脏,AST80%存在于肝细细胞线粒体中,仅20%在胞浆。
在肝病时血清AST升高,与肝病严重程度呈正相关。
当病变持久且较严重时,线粒体中AST释放入血流,其值可明显升高。
急性肝炎时如果AST持续在高水平,有转为慢性肝炎的可能。
心肌其其他脏器细胞受损时,AST亦升高,应予以鉴别,以免此类疾病被肝炎症状所掩盖。
(3)乳酸脱氢酶(LDH):肝病时可显著升高,但肌病时亦可升高,须配合临床加以鉴别。
(4)Y谷氨酰胎酶(Y—GT):肝炎和肝癌患者可显著升高,在胆管阻塞的情况下更明显,YGT活性变化与肝病病理改变有良好的一致性。
(5)胆碱酯酶:由肝细胞合成,其活性降低提示肝细胞已有较明显损伤,其值愈低,提示病情愈重。
(6)碱性磷酸酶(ALP或AKP):正常人血清中ALT主要来源于肝和骨组织,ALP测定主要用于肝病和骨病的临床诊断。
当肝内或肝外胆汁排泄受阻时,组织表达的ALP不能排出体而回流入血,导致血清ALP活性升高。
2、血清蛋白主要由比蛋白(A),α1、α2、β及Y球蛋白组成。
前4种主要由肝细胞合成,Y球蛋白主要由浆细胞合成。
在急性肝炎时,由于白蛋白半衰期较长,约21天,以及肝脏的代偿功能,血清蛋白质和量可在正常范围内。
慢性肝炎中度以上、肝硬化、重型肝炎时出现白蛋白下降,Y球蛋白升高,白/球(A/G)比例下降甚至倒置。
血清蛋白电泳分析则从另一角度来检测白、球蛋白各成份的相对比值,起到相同的诊断作用。
3、胆红素急性或慢性黄疸型肝炎时血清胆红素升高,活动性肝硬化亦可升高且消退缓慢,重型肝炎常超过171vmol/L。
一般情况下,肝损程度与胆红素含量呈正相关。
直接胆红素在总胆红素中的比例尚可反映淤胆程度。
4、凝血酶原活动度(PTA)PTA高低与肝损程度成反比。
<40%是诊断重型肝炎的重要依据,亦是判断重型肝炎预后的敏感指标。
5、血氨肝衰竭时氨的能力减退或丧失导致血氨升高,常见于重型肝炎。
肝性脑病患者。
(四)其他生化指标检测1、电解质重型肝炎常见低K+、低Na+、低CI-,亦可有低Ca2+、低Mg2+、低P2-等。
肝肾综合征时可出现高K+。
2、血糖超过40%的重型肝炎患者有血糖降低。
临床上应注意低血糖昏迷与肝性脑病的鉴别。
3、血浆胆固醇60%—80%的血浆胆固醇来自肝脏。
肝细胞严重损伤时,胆固醇在肝内合成减少,故血浆胆固醇明显下降,胆固醇愈低,预后愈险恶。
梗阻性黄疸时胆固醇升高。
4、补体当肝细胞严重损害时,补体合成减少。
临床简则CH50和C3补体对预后有评估作用。
5、甲胎蛋白(AFP)HBV和HCV感染与HCC的发生有明显相关性,AFP含量的检测是率选和早期诊断HCC的常规方法。
肝炎活动、肝细胞癌变和肝细胞修复时,AFP均有不同程度的升高,应进行动态观察。
急性重型肝炎AFP升高时,提示有肝细胞再生,为预后良好的标志。
6、胆汁酸血清中胆汁含量很低,当肝炎活动时胆汁酸升高。
由于肝脏对胆红素和胆汁酸的运转活动不同,检测胆汁酸有助于鉴别胆汁淤积和高胆红素血症。
(五)肝纤维化指标一些检测项目已在临床上应用,如3型较胶原体,4型胶原、层连蛋白、透明质酸、脯氨酰羟化酶等,对肝纤维化的诊断有一定参考价值,但缺乏特异性。
(六)病原学检查(1)抗HCV IgM和抗HCV IgG:HCV抗体不是保护性抗体,HCV感染的标志。
HCV Igm阳性提示现症HCV感染,抗HCV IgG阳性提示现正感染或既往感染。
抗HCV IgM的检测受较多因素的影响,如球蛋白、RF等,稳定性不如抗HCV IgG。
目前国内多用酶免疫试验(EIA)检测抗HCV IgG,试剂质量与国外第三代诊断试剂持平。
抗HCV IgG低滴度提示病毒处于静止,高滴度提示病毒复制活跃(2)HCV RNA:HCV在血液中含量很少,分子杂交甚至一次性PCR均难以检出HCV RNA,常采用套式PCR以提高检出率。
由于影响因素较多及技术要求较高易产生假阳性和假阴性,分析结果时应结合临床做出正确判断。
HC RNA阳性是病毒感染和复制的直接标志。
HCV RNA亦可定量,方法包括b五DNA探针技术、竞争PCR法、荧光定量法等,定量测定有助于了解病毒复制程度、抗病毒治疗的选择及疗效评估等。
对HCV RNA尚可进行基因分型,方法包括序列测定、PCR、酶切、探针杂交等,基因分型在流行病学和抗病毒治疗等方法有一定意义,但不作为常规。
组织中HCV标志物的检测基本同HBV,可检测HCV抗原及HCV RNA,一般单位难开展此项目。
(七)影像学检查B型超声有助于鉴别阻塞性黄疸、脂肪肝及肝内占位性病变。
对肝硬化有较高的诊断价值,能够反映肝脏表面变化,门静脉、脾静脉直径,脾脏大小,胆囊异常变化,腹水等。
彩色超声尚未可观察到血流变化。
在重型肝炎中可动态观察肝脏大小变化等。