初中化学常见化学物质的性质及转化关系
- 格式:docx
- 大小:298.28 KB
- 文档页数:4

初中化学知识总结(常见物质的性质和⽤途)初中化学知识总结(常见物质的性质和⽤途)物质物理性质化学性质⽤途氧⽓O2通常情况下,氧⽓是⼀种⽆⾊、⽆味的⽓体。
不易溶于⽔,⽐空⽓略重,可液化和固化。
氧⽓是⼀种化学性质⽐较活泼的⽓体,能与许多物质发⽣化学反应,在反应中提供氧,具有氧化性,是常⽤的氧化剂2Mg+O2点燃2MgO 3Fe+2O2点燃Fe3O42Cu+O2△2CuO 4Al + 3O2点燃 2Al2O32H2+ O2点燃 2H2O 4P + 5O2点燃 2P2O5S + O2点燃 SO2C + O2点燃 CO22C + O2点燃 2CO(1)供呼吸。
病⼈的急救。
(2)利⽤氧⽓⽀持燃烧并放热的性质,⾦属的⽓焊和⽓割、作⽕箭发动机的助燃剂、制液氧炸药等。
空⽓1、空⽓的成分按体积分数计算:氮⽓78%,氧⽓21%,稀有⽓体0.94%,CO20.03%2、环境污染知识:排放到空⽓中的⽓体污染物较多的是⼆氧化硫、⼆氧化氮、⼀氧化碳3、测定空⽓成份或除去⽓体⾥的氧⽓,要⽤易燃的磷,磷燃烧后⽣成固体,占体积⼩易分离。
不能⽤碳、硫代替磷。
碳、硫跟氧⽓反应⽣成⽓体,难跟其他⽓体分离。
分离液态空⽓制取氧⽓,此变化是物理变化,不是分解反应氢⽓H2通常状况下,纯净的氢⽓是⽆⾊、⽆⽓味的⽓体,是密度最⼩的⼀种⽓体(1)氢⽓的可燃性注意:点燃氢⽓前⼀定要先检验氢⽓的纯度。
(2)氢⽓的还原性(1)充灌探空⽓球。
(2)做燃料有三个优点:资源丰富,燃烧后发热量⾼,产物⽆污染。
(3)冶炼⾦属,⽤氢⽓做还原剂。
⽔H2O净化⽔的⽅法:吸附、沉淀、过滤、蒸馏。
单⼀操作相对净化程度由⾼到低的顺序是:蒸馏,吸附沉淀,过滤,静置沉淀。
a.与某些氧化物反应:H2O + CaO == Ca(OH)2b. 分解反应:2H2O 通电== 2H2↑+O2↑;(正极O2 负极H2 ,体积⽐1:2)⽔污染途径:⼯业“三废”排放;⽣活污⽔的排放;农业上的农药、化肥等。

点燃 高温 点燃 点燃 点燃 点燃 点燃 点燃 点燃 通电 MnO 2 初中常见物质的化学性质及化学方程式一、物质与氧气的反应⑴单质与氧气的反应: 1. 镁在空气中燃烧:2Mg+O 2 2MgO(实验现象:发出耀眼的白光,放出热量,生成一种白色粉末状固体。
) 2. 铁在氧气中燃烧:3Fe+2O 2 Fe 3O 4(实验现象:剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体。
)3. 铜在空气中受热:2Cu+O 24. 铝在空气中燃烧:4Al+3O 2 2Al2O 3 5. 氢气中空气中燃烧:2H 2+O 2 2H 2O6. 红磷在空气中燃烧:4P+5O 2 2P 2O 5(实验现象:产生黄色火焰,放出热量,冒出大量白烟。
)7. 硫粉在空气中燃烧: S+O 2 SO 2(实验现象:发出微弱的淡蓝色火焰,放出热量,生成一种有刺激性气味的无色气体。
硫粉在氧气中燃烧:发出明亮的蓝紫色火焰。
)⑵化合物与氧气的反应:8. 甲烷在空气中燃烧:CH 4+2O 2 CO 2+2H 2O9. 酒精在空气中燃烧:C 2H 5OH+3O 2 2CO 2+3H 2O二.几种气体的制法:(1)实验室制氧气的反应原理:10. 加热氯酸钾(有少量的二氧化锰):2KClO 3 2KCl+3O 2↑11. 加热高锰酸钾:2KMnO 4 K 2MnO 4+MnO 2+O 2↑12.分解过氧化氢:2H 2O 2 2H 2O+O 2↑(2)实验室制二氧化碳的反应原理:13. CaCO 3+2HCl CaCl 2+H 2O+CO 2↑二氧化碳的工业制法原理:14. 高温煅烧石灰石:CaCO 3 CaO+CO 2↑(3)实验室制氢气的反应原理:15. Zn+H 2SO 4 ZnSO 4+H 2↑三、水的电解: 16. 水在直流电的作用下分解:2H 2O 2H 2↑+O 2↑四、碳的化学性质(1)常温下,碳的化学性质不活泼高温点燃点燃点燃高温高温(2)可燃性17.碳在氧气中充分燃烧:C+O2CO218. 碳在氧气中不充分燃烧:2C+O22CO(3)还原性19.木炭还原氧化铜:C+2CuO 2Cu+CO2↑20. 木炭还原二氧化碳:C+CO22CO五、二氧化碳的化学性质(1)二氧化碳既不能燃烧,也不能支持燃烧,而且也不能供给呼吸(2)二氧化碳与水反应,生成碳酸: CO2+H2O H2CO3 (H2CO3 CO2↑+H2O)(3)二氧化碳与澄清石灰水发生反应(检验二氧化碳):Ca(OH)2+CO2 CaCO3↓+H2O(4)氧化性:CO2 +C 2CO六、一氧化碳的化学性质(1)可燃性:2CO+O22CO2(2)还原性:Cu+CO2(3)毒性七、金属的化学性质(1)金属+氧气金属氧化物(化学方程式见氧气的化学性质)(2)活泼金属+盐酸、稀硫酸盐+氢气镁、锌、铁、铝和盐酸、稀硫酸反应:Mg+2HCl MgCl2+H2↑Mg+H2SO4MgSO4+H2↑Zn+2HCl ZnCl2+H2↑Zn+H2SO4ZnSO4+H2↑Fe+2HCl FeCl2+H2↑Fe+H2SO4FeSO4+H2↑2Al+6HCl 2AlCl3+3H2↑2Al+3H2SO4Al2(SO4)3+3H2↑(3)金属+盐溶液另一种金属+另一种盐铁和硫酸铜溶液反应:Fe+CuSO4FeSO4+Cu锌和硫酸铜溶液反应:Zn+CuSO4ZnSO4+Cu铜和硝酸银溶液反应:Cu+2AgNO3Cu(NO3)2+2Ag八、酸的化学性质(1)酸+酸碱指示剂酸能使紫色石蕊溶液变红,使无色酚酞溶液不变色。

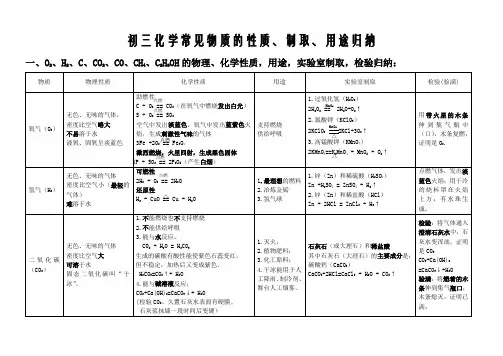


一、初中化学物质的转化关系1、氧气、氧化物、酸、氢气、水H2OKMnO4↘↓↑↗CO、CO2↗SO2H2SO4H2O2→→P2O5+ Mg Al Zn Fe→ H2→H2O ↘MgO HClKClO3↗↓↘Al2O3 Fe3O42、碳与碳的化合物3、氢氧化钠、碳酸钠、氯化钠+ CO2↗ Na2SO4 → BaSO4↓(白)NaOH → Na2CO3 → CaCO3↓(白)(变质)↘ NaCl → AgCl↓(白)4、含钙化合物的关系:↙↗―――――――↘↖CaCO3→CaO→Ca(OH)2→CaCl2↖CO2↙5、氧化钡、氢氧化钡与硫酸钡1 / 32 /3 ↗BaCl 2 → BaSO 4↓(白)BaO → Ba(OH)2 ↗↘ + CuS O 4↘Cu(OH)2↓(蓝)6、硫酸铜、碳酸氢钙、碳酸氢钠、碳酸氢铵CuO ↗ CO 2↙ ↘ Ca(HCO 3)2 → CaCO 3→CaOCuSO 4.5H 2O →CuSO 4→ Cu ↘ H 2O↗Na 2CO 3 ↗ NH 3 → NH 3.H 2O NaHCO 3 →CO 2 NH 4HCO 3 → H 2O↘H 2O → H 2CO 3 ↘ CO 2 → H 2CO 37、铝、镁、锌、铁、铜及其化合物↗ZnSO 4↖ ↗ AlCl 3↖Zn → ZnO Al → Al 2O 3 ↘ZnCl 2↙ ↘Al 2(SO 4)3↙Fe Al↗MgCl 2↖ ↙﹉﹉﹉﹉↗ CuCl 2↘↖Mg → MgO Cu ←→CuO Cu(OH)2 ↘MgSO 4↙ ↖____↘ CuSO 4↗↙ Fe Al↙ FeCl 3 ↖ C CO H 2 Mg Al ↗FeSO 4Fe(OH)3 Fe 2O 3 ←――――→ Fe↖Fe 2(SO 4)3↙ O 2 H 2O ↘ FeCl 2 8、常见物质的相互转化关系(即注明必要的反应物、反应条件)CO 2 CO C 或O 2 O 2 H 2O H 2O 2Al 2O 3 AlCl 3 Al CuO CuSO 4 Cu ⑴ ⑵ ⑶ ⑷ MgO MgSO 4 Mg Cu H 2 Fe CaO Ca(OH)2 CaCO 3 CaCl 2 Ca(OH)2CaCO 3 ⑸ ⑹ ⑺ ⑻CaCO3Na2CO3CO2CO2NaOHNa2CO3CO2O2H2ONaOH NH4ClNH3⑼⑽⑾⑿3 / 3。

初中化学常见物质的性质和用途常见物质的性质和用途:1.水(H2O):性质:水是一种无色、无味、无臭的液体。
它的分子由两个氢原子和一个氧原子组成,呈现出特殊的极性质,并且具有高的比热容和高的表面张力。
用途:水是生命的基础,广泛应用于日常生活中的饮用、洗涤、煮食等方面。
此外,水还应用于农业灌溉、工业制造、能源生产等众多领域。
2.氧气(O2):性质:氧气是一种无色、无味、无臭的气体。
它是空气中最常见的组分之一,具有高的氧化性,能够支持燃烧和维持动植物的呼吸过程。
用途:氧气广泛应用于医疗领域,用于治疗呼吸系统疾病或急救情况下的氧疗。
此外,氧气还用于工业中的氧化、切割、焊接等领域。
3.二氧化碳(CO2):性质:二氧化碳是一种无色、无味的气体,具有较高的密度。
它在自然界中广泛存在,是植物进行光合作用的重要物质之一用途:工业上,二氧化碳被用作冷却剂、溶剂、气体保护剂等。
此外,它还用于特殊场合下的灭火、人造饮料的气泡制造等。
4.氨(NH3):性质:氨是一种无色、有刺激性气味的气体。
它具有较强的碱性,能够与酸反应,产生相应的盐类。
用途:氨用于制造化肥、合成尼龙等化学物质。
此外,氨的溶液被用作清洁剂、玻璃表面涂层等。
5.盐酸(HCl):性质:盐酸是一种无色、刺激性气味的挥发液体,呈酸性。
它具有很强的腐蚀性,能够溶解许多金属。
用途:盐酸广泛用于实验室中的化学分析、金属表面的清洗等领域。
此外,盐酸也用于工业上的冶炼、染料制备等过程。
6.硝酸(HNO3):性质:硝酸是一种无色、刺激性气味的液体,呈酸性。
它可以与多种物质发生剧烈的反应,具有很强的腐蚀性。
用途:硝酸被广泛应用于农业中的肥料制备、爆炸物品生产、矿石的提取等领域。
此外,硝酸还可用于电子工业、药物制造等。
7.硫酸(H2SO4):性质:硫酸是一种无色、黏稠的液体,呈酸性。
它具有很强的腐蚀性和漂白性。
用途:硫酸被广泛用于工业中的废水处理、金属表面涂层等。
此外,它还可以用于制造肥料、玻璃、洗涤剂等。


物质俗称性质用途S 硫磺淡黄色粉末、易燃、于空气中燃烧火焰为淡蓝色、纯氧为蓝紫色,并伴有刺鼻气体产生(SO2)P 赤磷白磷燃烧时产生大量的烟(P2O5固体) 用物制烟雾弹C 金刚石、石墨、活性炭金刚石是最硬物质;石墨具有导电性、润滑性、质软;活性炭用于吸附剂金刚石用于制钻头,切割物质。
石墨用于电极、润滑、制铅笔Fe 化学性质活泼、在潮湿空气中易生锈,于纯氧中燃烧生成Fe3O4)P2O5 白色固体、易吸水用作干燥剂CO2 干冰碳酸气易溶于水、水呈酸性、比空气重人工降雨、工业原料SO2 ρSO2>ρ空气、有刺激气味、其水溶液为H2SO3SO3 ρSO3>ρ空气其水溶液为H2SO4CH4 沼气坑气ρCH4<ρ空气难容于水,无味、易燃、是最简单有机物C2H5OH 酒精易燃烧用于燃料、消毒(70%~75%)CH3OH (甲醇) 与乙醇相似;有毒(使人眼睛失眠、甚至死亡)易燃烧CH3COOH(乙酸)醋酸水醋酸有刺激气味、具有酸性、能使指示变色CaO 生石灰白色固体、易吸水、溶于水后反应生成熟石灰[Ca(OH)2]用于干燥剂Fe3O4 磁铁矿的主要成分黑色物质、难溶于水、可用酸来溶解用于治炼金属铁Fe2O3 磁铁矿的主要成分、铁锈主要成分红褐色难溶物质、可用酸来溶用于治炼生铁CuO 黑色难溶于水2Cu+O2=CuO、可被还原剂还原成单质铜、可用酸来溶解用于治炼单质Cu、即Cu+H2=Cu+H2OCuSO4 白色固体、溶于水变成蓝色能与活性比其强的金属反应置换出单质铜来用于检验物质中是否含有水CuSO4"5H2O 胆矾蓝矾蓝色晶体、溶于水后其性质与CuSO4 溶液一致,易风化即: CuSO4"5H2O=CuSO4+5H2OCO 难溶于水,ρCO>ρ空易燃烧、无味有毒气体用作还原剂、治炼金属CaCO3 石灰石大理石白色难溶于水、易溶于酸的固体用于制CO2及制生石灰CaO一. 物质与氧气的反应: (1) 单质与氧气的反应:1. 镁在空气中燃烧:2Mg + O2 点燃 2MgO2. 铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O43. 铜在空气中受热:2Cu + O2 加热 2CuO4. 铝在空气中燃烧:4Al + 3O2 点燃 2Al2O35. 氢气中空气中燃烧:2H2 + O2 点燃 2H2O6. 红磷在空气中燃烧:4P + 5O2 点燃 2P2O57. 硫粉在空气中燃烧: S + O2 点燃 SO28. 碳在氧气中充分燃烧:C + O2 点燃 CO29. 碳在氧气中不充分燃烧:2C + O2 点燃 2CO (2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2 点燃 2CO2 11. 甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O 12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O 二.几个分解反应:13. 水在直流电的作用下分解:2H2O 通电 2H2↑+ O2 ↑14. 加热碱式碳酸铜:Cu2(OH)2CO3 加热 2CuO + H2O + CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl + 3O2 ↑ 16. 加热高锰酸钾:2KMnO4 加热 K2MnO4 + MnO2 + O2↑ 17. 碳酸不稳定而分解:H2CO3 === H2O + CO2↑ 18. 高温煅烧石灰石:CaCO3 高温 CaO + CO2↑ 三.几个氧化还原反应:19. 氢气还原氧化铜:H2 + CuO 加热 Cu + H2O 20. 木炭还原氧化铜:C+ 2CuO 高温 2Cu + CO2↑ 21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温 4Fe + 3CO2↑ 22. 焦炭还原四氧化三铁:2C+ Fe3O4 高温 3Fe + 2CO2↑ 23. 一氧化碳还原氧化铜:CO+ CuO 加热 Cu + CO224. 一氧化碳还原氧化铁:3CO+ Fe2O3 高温 2Fe + 3CO2 25. 一氧化碳还原四氧化三铁:4CO+ Fe3O4 高温 3Fe + 4CO2 四.单质、氧化物、酸、碱、盐的相互关系(1) 金属单质 + 酸 -------- 盐 + 氢气 (置换反应) 26. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑ 27. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑HCI 盐酸无色、有刺激气味液体,具有挥发性、腐蚀性。

初中化学知识点归纳常见物质的分类与性质初中化学知识点归纳:常见物质的分类与性质化学是研究物质的性质、组成、变化和应用的科学。
在初中化学学习中,我们需要了解常见物质的分类与性质。
本文将对常见物质的分类和性质进行归纳,并介绍一些典型的例子。
一、常见物质的分类1. 纯净物与混合物:纯净物是由同一种物质组成的,具有一定的化学性质和固定的组成比例。
常见的纯净物包括金属、非金属元素、化合物等。
混合物是由两种或多种物质混合而成的,其组成比例可以发生变化。
常见的混合物包括空气、海水、沙子和水等。
2. 单质与化合物:单质是由同一种元素构成的纯净物质。
例如氧气、氢气、金属元素等都是单质。
化合物是由不同元素按照一定的化学组成比例结合而成的。
例如水、二氧化碳等都属于化合物。
3. 无机物与有机物:无机物主要是指无机化合物,包括无机酸、无机碱、无机盐等。
它们大多数是由金属和非金属元素组成的。
有机物是指含有碳元素的化合物,包括烃、醇、酮、酸等。
有机物广泛存在于自然界和人造物品中。
4. 金属与非金属:金属具有良好的导电性、导热性和延展性等特点。
常见的金属有铁、铜、铝、锌等。
非金属的导电性和导热性相对较差,大多数处于非固态。
例如氧气、氮气、碳等都属于非金属。
二、常见物质的性质1. 物理性质:物理性质是物质自身所具有的性质,如颜色、形状、密度、熔点、沸点等。
例如水的沸点是100摄氏度,密度是1克/立方厘米。
2. 化学性质:化学性质是物质在化学变化过程中所表现出的性质,如燃烧性、可溶性、酸碱性等。
例如氧气可以与其他物质燃烧生成氧化物。
3. 燃烧性质:燃烧是氧化物与可燃物质在适当的条件下发生的化学反应。
常见的可燃物质包括木材、煤炭、油类等。
燃烧过程中会产生光、热和气体等。
4. 酸碱性质:物质根据溶液中的氢离子(H+)或氢氧根离子(OH-)的浓度可分为酸性、碱性和中性。
酸性物质如硫酸,碱性物质如氢氧化钠,中性物质如水。
5. 氧化性与还原性:氧化性是指物质在与氧气接触时能够发生氧化反应的性质。
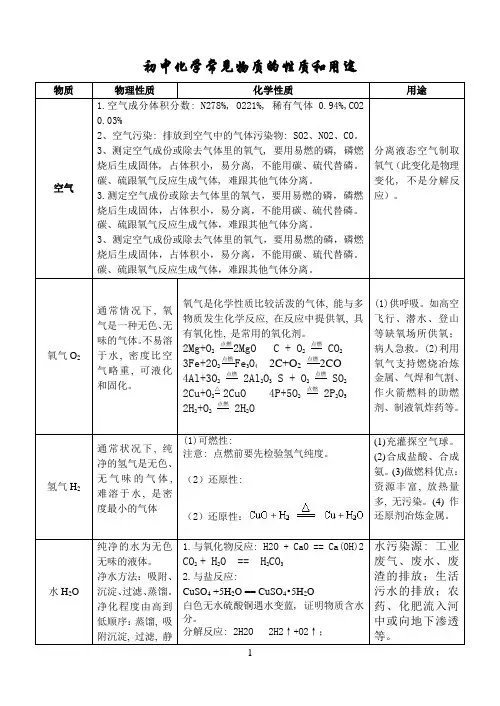
初中化学常见物质的性质和用途物质物理性质化学性质用途空气1.空气成分体积分数: N278%, O221%, 稀有气体0.94%,CO20.03%2、空气污染: 排放到空气中的气体污染物: SO2、NO2、CO。
3、测定空气成份或除去气体里的氧气, 要用易燃的磷, 磷燃烧后生成固体, 占体积小, 易分离, 不能用碳、硫代替磷。
碳、硫跟氧气反应生成气体, 难跟其他气体分离。
3.测定空气成份或除去气体里的氧气,要用易燃的磷,磷燃烧后生成固体,占体积小,易分离,不能用碳、硫代替磷。
碳、硫跟氧气反应生成气体,难跟其他气体分离。
3、测定空气成份或除去气体里的氧气,要用易燃的磷,磷燃烧后生成固体,占体积小,易分离,不能用碳、硫代替磷。
碳、硫跟氧气反应生成气体,难跟其他气体分离。
分离液态空气制取氧气(此变化是物理变化, 不是分解反应)。
氧气O2 通常情况下, 氧气是一种无色、无味的气体。
不易溶于水, 密度比空气略重, 可液化和固化。
氧气是化学性质比较活泼的气体, 能与多物质发生化学反应, 在反应中提供氧, 具有氧化性, 是常用的氧化剂。
2Mg+O2点燃2MgO C + O2点燃 CO23Fe+2O2点燃Fe3O42C+O2点燃2CO4Al+3O2点燃 2Al2O3S + O2点燃 SO22Cu+O2△2CuO 4P+5O2点燃 2P2O52H2+O2点燃 2H2O(1)供呼吸。
如高空飞行、潜水、登山等缺氧场所供氧;病人急救。
(2)利用氧气支持燃烧冶炼金属、气焊和气割、作火箭燃料的助燃剂、制液氧炸药等。
氢气H2 通常状况下, 纯净的氢气是无色、无气味的气体,难溶于水, 是密度最小的气体(1)可燃性:注意: 点燃前要先检验氢气纯度。
(2)还原性:(2)还原性:(1)充灌探空气球。
(2)合成盐酸、合成氨。
(3)做燃料优点:资源丰富, 放热量多, 无污染。
(4) 作还原剂冶炼金属。
水H2O 纯净的水为无色无味的液体。
净水方法:吸附、沉淀、过滤、蒸馏。
初中化学各类物质间的转化关系:
一、转化关系图
列举: (1)金属+
金属氧化物(碱性氧化物)
(2)碱性氧化物(可溶)+水
碱(可溶)
(3)碱(难溶)
碱氧(难溶)+水
(4)酸+碱
盐+水
;
(5)非金属+
非金属氧化物(酸性氧化物)
(6)酸性氧化物(易溶)+水
酸(易溶)
①
金属 非金属
碱性 氧化物 酸性 氧化物 盐 碱
盐和水 酸
盐
盐
两种新盐
碱和盐 酸和盐 盐+氢 气
盐
+ 金
属
②
③
④
④
④
⑤ ⑥
⑦ ⑧ ⑨
⑩
⑪
⑩
⑫
⑬
⑭
⑮
⑯
⑰
(7)酸(易挥发/难溶)酸氧+水(易挥发/难溶)
从纵向来看,金属碱性氧化物碱盐,其中金属元素相同。
非金属酸性氧化物酸(含氧酸)盐,其中非金属元素相同。
横向:
(8)金属+非金属(无氧酸)盐
(9)碱氧+酸氧(含氧酸)盐
(10)含氧酸盐碱氧+酸氧
(11)盐+盐两种新盐
交叉:
(12)酸+碱氧盐+水
(13)碱+酸氧盐+水
(14)酸+盐新酸+新盐
;
(15)碱+盐新碱+新盐
(16)金属+酸盐+
(17)金属+盐新盐+新金属
(18)金属+盐新盐+新金属
(置换反应)。
初中化学常见物质的性质、用途分类记忆你是不是觉得初三化学的物质学问繁多难以记忆,只要你学会使用分类记忆方法就会混乱了,我在此整理了相关资料,希望能关怀到您。
气体类物质物理性质化学性质用途氧气O比较活泼的气体,能与许多物质发生化学反应,在反应中提供氧,具有氧化性,是常用的氧化剂(1)供呼吸。
如高空飞行、潜水、登山等缺氧的场所,其工作人员都需要供氧;病人的急救。
(2)利用氧气支持燃烧并放热的性质,用于冶炼金属(吹氧炼钢)、金属的气焊和气割、作火箭发动机的助燃剂、制液氧炸药等。
空气1、空气的成分按体积分数计算:氮气78%,氧气21%,稀有气体0.94%,CO 气体污染物较多的是二氧化硫、二氧化氮、一氧化碳3、测定空气成份或除去气体里的氧气,要用易燃的磷,磷燃烧后生成固体,占体积小易分别。
不能用碳、硫代替磷。
碳、硫跟氧气反应生成气体,难跟其他气体分别。
分别液态空气制取氧气,此转变是物理转变,不是分解反应氢气H可燃性留意:点燃氢气前确定要先检验氢气的纯度。
〔2〕氢气的还原性(1)充灌探空气球。
(2)做合成盐酸、合成氨的原料。
(3)做燃料有三个优点:资源丰富,燃烧后发热量高,产物无污染。
(4)冶炼金属,用氢气做还原剂。
二氧化碳CO固态二氧化碳叫“干冰”〕1、既不能燃烧,也不支持燃烧。
2、不供给呼吸3、与水反应4、与石灰水反应可用于灭火,植物的气肥,制饮料,干冰用于人工降雨,保鲜剂等。
但大气中二氧化碳的增多,会使地球产生“温室效应”。
一氧化碳CO无色、无味、比空气的密度略小、难溶于水。
⑴可燃性⑴还原性⑴毒性:一氧化碳易与血液中的血红蛋白结合,且不易分别,使人体因缺氧而死亡CO是煤气的主要成分,还可用于冶金工业。
甲烷CH可燃性动植物的残体可分解出甲烷,可用作燃料。
检验CO、CH物质物理性质化学性质用途金刚石无色透亮,正八面体样子的固体,是自然最硬的物质。
1/ 31、常温下,碳的化学性质不活泼,但在高温或点燃条件下,碳的活性大大增添。
物质的分类和转化规律一.物质的转化规律:1.金属+氧==金属氧化物2.金属氧化物+还原剂=金属+非金属氧化物①CuO+H2== 现象:,H2还原优点是反应生成物之一是,且产物较纯净。
②CuO+CO== (CO有剧毒,实验时一定)③2CuO+C;现象:(虽然C的还原能力强于H2,但固体还原剂与氧化物的充分接触程度没有固体与气体还原剂充分,自然反应温度就比H2要高,最好使用酒精喷灯或加罩的酒精灯。
C要稍微过量。
)④2Fe2O3+3C;⑤Fe2O3+3CO;(加热时一定要持续高温)⑥Fe2O3+3H2 ;现象:3.金属氧化物+水==碱4.碱==金属氧化物+水5.非金属+氧==非金属氧化物①氢气在空气中燃烧:2H2+O2现象:相关知识点: (1)氢气是一种常见的还原剂; (2)点燃前,一定要检验它的纯度否则会爆炸。
②红磷在空气中燃烧:4P+5O2现象:相关知识点: (1)烟是固体小颗粒;雾是液体小颗粒. (2)测量氧气在空气中的体积分数。
(3)可做烟雾弹。
③硫粉在空气中燃烧: S+O2现象:在空气中是发出微弱的火焰,在氧气中是发出明亮的火焰. 有强烈气味。
相关知识点:(1)反应后的产物可用紫色的石蕊试液来检验(紫色变成红色);(2)SO2污染空气,要用溶液进行尾气处理。
(3)SO2是气体,所以测量氧气在空气中的体积分数,若将水改为溶液,也可以测量氧气在空气中的体积分数。
④碳在氧气中充分燃烧:C+O2现象:在空气中是发出 ,在氧气中是发出。
相关知识点:反应后的产物可用来进行检验.⑤碳在氧气中不充分燃烧:2C+O26.非金属氧化物 + 活泼金属 == 非金属+金属氧化物①金属钠与水反应:2Na+2H2O== ,现象:浮(钠块浮在水面上)、游(钠块在水面上无规则游动)、熔(钠块熔化为小球)、响(发出嘶嘶的响声)、红(使滴入酚酞试液的溶液变红)②金属镁与CO2反应:2Mg+CO22MgO+C 现象:发出白光,有白色粉末(MgO)生成,有黑色固体(C)生成,同时放出大量的热。
专题3 八圈图及物质的转化1一、单质、氧化物、酸、碱、盐的相互反应1、金属+氧气→碱性氧化物如:2、碱性氧化物+水→可溶性碱(不溶性碱除外)如:3、不容性碱→碱性氧化物(可溶性碱除外)+水如:4、酸+盐→盐+水5、非金属+ O2→酸性氧化物(H2燃烧、C不完全燃烧等除外)如:6、酸性氧化物+水→含氧酸(二氧化硅除外)如:7、含氧酸→酸性氧化物+水如:8、金属+非金属(除O2、H2外)→无氧酸盐如:9、碱性氧化物+酸性氧化物→含氧酸盐如:10、不容性盐→碱性氧化物+酸性氧化物如:11、盐1+盐2→盐3+盐412、碱性氧化物+酸→盐+水13、酸性氧化物+碱→盐+水14、酸+盐→新酸+新盐15、碱+盐→新碱+新盐16、金属+酸→盐+ H217、金属+盐溶液→新金属+新盐溶液1、一定条件下,下列物质的转化均可一步实现的是()A.CaCl2→CaCO3→Ca(OH)2 B. AgNO3→Fe(NO3)2→Zn(NO3)2C. NaNO3→NaOH→Na2CO3D. Fe2O3→FeSO4→Fe(OH)32、下列物质间的转化,在一定条件下均能一步实现的是①C→CO→CO2 ②Cu→CuO→CuSO4 ③Na2CO3→NaCl→NaNO3 ④CaCO3→CaO→Ca(OH)2 A.①②③B.①③④C.①②④ D.①②③④3、下列物之间的转化,能通过一步反应实现的是( )①C2H5OH→CO2②CaO→Ca(OH)2③H2O2→H2O④HNO3→HCl⑤Fe3O4→Fe A.①②③④ B.①②③⑤ C.①③④⑤ D.②③④⑤4、下列物质间的每一转化不能..都通过一步反应实现的是()A.CuO→Cu→CuO B.NaOH→H2O→NaOH C.O2→Fe3O4→O2D.Fe→FeCl2→Fe5、下列物质间的每一转化不能都通过一步反应实现的是()A.Ca→CaO→CaCl2B.NaOH→Na2CO3→NaClC.O2→CuO→Cu(OH)2D.C→CO2→Na2CO36、下列转化能一步完成的()① CH4→CO2 ②HNO3→HCl ③CaO→Ca(OH)2 ④Ba(OH)2→NaOH ⑤C→CuA.①③④⑤ B.②③④⑤ C.①②④⑤ D.①②③④7、下列转化能一步完成的是()①CaCO3→CO2②HCl→NaCl③CaO→Ca(OH)2④Ca(OH)2→NaOH⑤CuO→Cu.A.①②③④⑤B.②③④⑤C.①②④⑤D.①②③④8、下列转化能一步完成的是()①Ba(OH)2→NaOH②CuO→Cu(OH)2 ③HNO3→HCl④SO2→Na2SO3.A.①④ B.②③ C.③④ D.只有④9、下列物质之间的转化能够实现的是()10、下列物质间的转化关系正确的是()A.①②B.②③ C.①③ D.①②③【类型2】1、现有Fe、CuO、MgCl2、Ca(OH)2、稀H2SO4等五种物质,在常温下它们两两相互发生的化学反应有()A.7个B.6个C.5个D.4个2、现有氧化铁、稀硫酸、氢氧化钠溶液、氯化钡溶液和碳酸钾溶液五种物质,在常温下它们两两相互发生的化学反应有()A.4个B.5个C.6个D.7个3、现有Zn、Fe2O3、MgCl2、Cu(OH)2、稀H2SO4等五种物质,在常温下它们两两相互发生的化学反应有()A.3个B.4个C.5个D.6个4、对于化学反应X + Na2CO3 == 2Y+ CaCO3↓的分析错误的是()A.该反应属于复分解反应B.Y中一定含有钠元素C.X一定是熟石灰D.X中阴离子化合价是—1价5、对于复分解反应:X+2NaOH2Y+Cu(OH)2↓,下列分析中正确的是()A.X一定是CuCl2B.相对分子质量大小:X>Y C.Y可能是H2O D.Y可能是Na2SO4【类型3】1、下列各组变化中,每一转化在一定条件下均能一步实现的是()A.①和② B.②和③ C.①和③ D.①②③2、下列各组物质间通过一步反应就能实现如图所示的转化,则甲、乙、丙可能分别是()A.NaOH、NaCl、NaNO3B.CO、CO2、H2 CO3C.CaO、Ca(OH)2、CaCO3D.H2O2、H2O、O23、(2013•徐州一模)下列各组中物质间的转化不都是通过一步反应实现的是()4、下列各组物质间通过一步反应就能实现如右图转化,则甲、乙、丙可能是()A.KOH KCl KNO3B.CuO CuCl2Cu(OH)2C.C CO2COD.H2O2H2O O25、(2014·宿迁)下列物质的三角转化关系中都能按箭头方向一步实现的是( )A.① B.①② C.①②③ D.②③6、下列各组转化中,一定条件下均能一步实现的组合是()A.①②B.②③C.①③D.①②③专题3 八圈图及物质的转化2【类型3】7、下列有关说法正确的是( ) A .实现CO CO 2的相互转化,都只有一种途径B .Al 可以实现单质氧化物碱C .实现C CO 的转化,都利用了碳的可燃性D .实现H 2OO 2相互转化,化学反应的基本类型不同8、比较归纳是化学学习中常用的一种方法.以下是C 、CH 4、CO 三种物质转化为CO 2的转化关系,即:①C→CO 2②CH 4→CO 2③CO→CO 2,对它们的比较归纳正确的是( )A .三种转化发生的都是化合反应B .三种物质都只能跟氧气反应转化为二氧化碳C .三种物质都可以在点燃条件下转化为二氧化碳D .三种转化所有的生成物在常温下都是气体 9、(2014黄冈市)已知甲、乙、丙、丁是初中化学中的四种常见物质,丁是甲与乙、乙与丙反应的生成物之一(反应条件均已略去),转化关系如图:(1)常温下,若乙为红色粉末,甲为黑色粉末,则丙的化学式是______,甲与乙反应的化学方程式为______。