(完整版)图吸收光谱曲线
- 格式:ppt
- 大小:1.77 MB
- 文档页数:81


原子吸收光谱法原理1、光的简短历史人们可以追溯到17世纪,当时艾萨克-牛顿爵士发现,当白光通过玻璃棱镜时,会分解成其组成的光谱颜色[1]。
从这项工作中,他提出了光的体质理论(光由粒子组成的事实),而不是只具有波的性质,这为近两个世纪后的一些发现打开了大门。
英国化学家沃拉斯顿是第一个观察到太阳光谱中的暗线的人,这些暗线后来被称为弗劳恩霍夫线。
1832年,布鲁斯特得出结论,大气层中的原子蒸气吸收了来自太阳的一些辐射,从而探测到了这些线。
本生和基尔霍夫很快证明,每种化学元素在加热到炽热时都有一种特有的颜色或光谱(例如,钠(Na)的黄色;钾(K)的紫色)。
他们能够在实验室中重现在太阳光谱中观察到的黑线,从而能够通过发射光谱识别日冕中的吸收原子。
艾伦-沃尔什[2],一位出生于兰开夏郡的物理学家,在20世纪50年代初的某个周日早晨,在他的花园里工作时,一个能解决巨大分析化学难题的想法突然出现在他的脑海中:如何通过光谱学精确测量金属元素的小浓度。
光谱学的正常程序是汽化一个元素并测量其发射光谱,但这种技术有缺陷,产生的结果不准确。
沃尔什决定测量吸收,而不是发射。
到了星期一早上的茶点,他表明这是可以做到的。
他又花了几年时间说服制造商使用原子吸收光谱法(AAS)来检测金属,但他最终成功了。
今天,大多数分析实验室都会拥有至少一台原子吸收分光光度计。
2、什么是原子吸收光谱?AAS是一种分析技术,用于确定样品中金属原子/离子的浓度。
金属占地球化学元素的75%左右。
在某些情况下,材料中的金属含量是可取的,但金属也可能是污染物(毒物)。
因此,测量金属含量在许多不同的应用中是至关重要的,我们将在本文的后面探讨。
现在只需要说,它在质量控制、毒理学和环境测试中找到了用途,仅举几例。
3、原子吸收光谱法的原理是什么?AAS的基本原理可以表述如下。
首先,所有的原子或离子都能吸收特定的、独特波长的光。
例如,当一个含有铜(Cu)和镍(Ni)的样品暴露在铜的特征波长的光下时,那么只有铜原子或离子会吸收这种光。

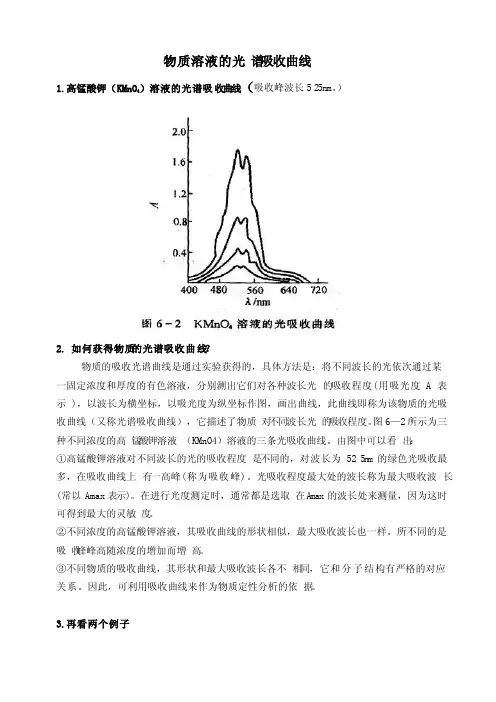
物质溶液的光谱吸收曲线1.高锰酸钾(KMnO4)溶液的光谱吸收曲线(吸收峰波长525nm。
)2. 如何获得物质的光谱吸收曲线?物质的吸收光谱曲线是通过实验获得的,具体方法是:将不同波长的光依次通过某一固定浓度和厚度的有色溶液,分别测出它们对各种波长光的吸收程度(用吸光度A表示),以波长为横坐标,以吸光度为纵坐标作图,画出曲线,此曲线即称为该物质的光吸收曲线(又称光谱吸收曲线),它描述了物质对不同波长光的吸收程度。
图6—2所示为三种不同浓度的高锰酸钾溶液(KMnO4)溶液的三条光吸收曲线。
由图中可以看出:①高锰酸钾溶液对不同波长的光的吸收程度是不同的,对波长为525n m的绿色光吸收最多,在吸收曲线上有一高峰(称为吸收峰)。
光吸收程度最大处的波长称为最大吸收波长(常以Amax表示)。
在进行光度测定时,通常都是选取在A max的波长处来测量,因为这时可得到最大的灵敏度。
②不同浓度的高锰酸钾溶液,其吸收曲线的形状相似,最大吸收波长也一样。
所不同的是吸收峰峰高随浓度的增加而增高。
③不同物质的吸收曲线,其形状和最大吸收波长各不相同,它和分子结构有严格的对应关系。
因此,可利用吸收曲线来作为物质定性分析的依据。
3.再看两个例子1)还原型辅酶(NADH )的光谱吸收曲线(吸收峰分别在260nm 和340nm )生化谷丙转氨酶检验试剂的反应原理如下:α-酮戊二酸 + L-丙氨酸 −−→−ALT L-谷氨酸 + 丙酮酸(初反应)丙酮酸 + NADH + H+ −−→−LDH L- 乳酸 + NAD + (主反应)NADH 的氧化速率与样本中A LT 酶活力成正比,NADH 在340nm 处有特征吸收峰,在340nm 处测其吸光度的下降速率即可计算出AL T 的活性。
2)维生素B12水溶液的光谱吸收曲线 (峰值365n m )吸收光谱曲线2.光吸收定律比尔定律:当一束平行的单色光垂直照射到一定浓度的均匀透明溶液时,入射光被溶液吸收的程度与溶液浓度成正比,这就是比尔定律。


原子吸收光谱分析4。
2.1 概述4。
2。
1。
1 基本概念1)原子光谱根据原子外层电子跃迁所产生的光谱进行分析的方法,称为原子光谱法,包括原子发射光谱法、原子吸收光谱法和原子荧光光谱法。
本章重点介绍应用广泛的原子吸收光谱法。
2)原子吸收光谱原子吸收光谱法,又称原子吸收分光光度法或简称原子吸收法,它是基于测量试样所产生的原子蒸气中基态原子对其特征谱线的吸收,从而定量测定化学元素的方法.4。
2.1。
2 仪器结构和过程图4-21 原子吸收示意图如上图,含Pb溶液将经过预处理-喷射成雾状进人燃烧火焰中,Pb化合物雾滴在火焰温度下,挥发并离解成Pb原子蒸气。
用Pb空心阴极灯作光源,产生Pb的特征谱线,通过Pb原子蒸气时,由于蒸气中基态Pb原子的吸收,Pb的特征谱线强度减弱,通过单色器和检测器测得其减弱程度,即可计算出溶液中Pb的含量。
4。
2。
1。
3 方法特点灵敏度高,10—9g/ml-10—12g/ml。
选择性好,准确度高。
单一元素特征谱线测定,多数情况无干扰。
测量范围广.测定70多种元素。
操作简便,分析速度快。
4。
2.2 原子吸收法基本原理 4。
2。
2.1 共振线和吸收线 1) 基本概念➢ 共振线电子从基态跃迁到能量最低的激发态(称为第一激发态),为共振跃迁,所产生的谱线称为共振吸收线(简称共振线).当电子从第一激发态跃回基态时,则发射出同样频率的谱线,称为共振发射线(也简称共振线)。
对大多数元素来说,共振线是指元素所有谱线中最灵敏的线。
➢ 特征谱线各种元素的原子结构和外层电子排布不同.不同元素的原子从基态激发至第一激发态(或由第一激发态跃回基态)时,吸收(或发射)的能量不同,因此各种元素的共振线不同而有其特征性,这种共振线称为元素的特征谱线。
2) 朗伯原理图4-22 原子吸收法的朗伯定律示意图原理公式:b K e I I νν-=0νK :吸收系数;ν:频率。
吸收线图4-23 吸收线轮廓图 图4—24 吸收线半宽度比较上述两个图,注意图的纵坐标参量的不同。


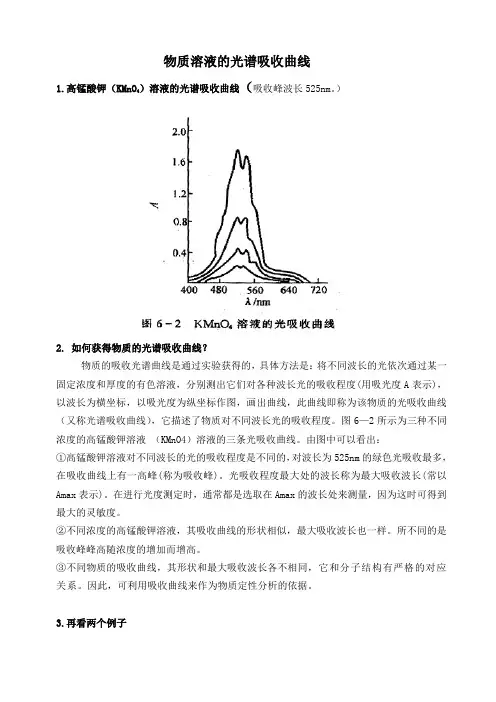
物质溶液的光谱吸收曲线)溶液的光谱吸收曲线(吸收峰波长525nm。
)1.高锰酸钾(KMnO42. 如何获得物质的光谱吸收曲线?物质的吸收光谱曲线是通过实验获得的,具体方法是:将不同波长的光依次通过某一固定浓度和厚度的有色溶液,分别测出它们对各种波长光的吸收程度(用吸光度A表示),以波长为横坐标,以吸光度为纵坐标作图,画出曲线,此曲线即称为该物质的光吸收曲线(又称光谱吸收曲线),它描述了物质对不同波长光的吸收程度。
图6—2所示为三种不同浓度的高锰酸钾溶液(KMnO4)溶液的三条光吸收曲线。
由图中可以看出:①高锰酸钾溶液对不同波长的光的吸收程度是不同的,对波长为525nm的绿色光吸收最多,在吸收曲线上有一高峰(称为吸收峰)。
光吸收程度最大处的波长称为最大吸收波长(常以Amax表示)。
在进行光度测定时,通常都是选取在Amax的波长处来测量,因为这时可得到最大的灵敏度。
②不同浓度的高锰酸钾溶液,其吸收曲线的形状相似,最大吸收波长也一样。
所不同的是吸收峰峰高随浓度的增加而增高。
③不同物质的吸收曲线,其形状和最大吸收波长各不相同,它和分子结构有严格的对应关系。
因此,可利用吸收曲线来作为物质定性分析的依据。
3.再看两个例子1)还原型辅酶(NADH )的光谱吸收曲线(吸收峰分别在260nm 和340nm )生化谷丙转氨酶检验试剂的反应原理如下:α-酮戊二酸 + L-丙氨酸 −−→−ALT L-谷氨酸 + 丙酮酸(初反应) 丙酮酸 + NADH + H + −−→−LDH L- 乳酸 + NAD + (主反应)NADH 的氧化速率与样本中ALT 酶活力成正比,NADH 在340nm 处有特征吸收峰,在340nm 处测其吸光度的下降速率即可计算出ALT 的活性。
2)维生素B12水溶液的光谱吸收曲线 (峰值365nm )吸收光谱曲线2.光吸收定律比尔定律:当一束平行的单色光垂直照射到一定浓度的均匀透明溶液时,入射光被溶液吸收的程度与溶液浓度成正比,这就是比尔定律。
