常用有机溶剂苯的纯化
- 格式:doc
- 大小:25.00 KB
- 文档页数:1

纯苯的生产工艺
纯苯是一种有机化合物,常用于工业领域,用作溶剂和原料。
下面是一种常见的纯苯生产工艺。
首先,通过石化工艺从石油中提取石脑油。
石脑油是一种混合的碳氢化合物,主要由苯、甲苯和二甲苯组成。
石脑油通常在蒸馏塔中进行精馏,将其中的苯分离出来。
然后,将蒸馏得到的苯进一步纯化。
首先,苯经过加热以去除其中的杂质,如酚和硫化物。
然后,将苯传送到蒸馏塔中进行分馏,以去除其中的甲苯和二甲苯等杂质。
在这个过程中,通过控制温度和压力,使得只有纯苯得以从蒸馏塔中收集。
最后,对收集到的纯苯进行进一步的纯化。
一种常用的方法是将苯通过储罐中的氮气冷凝,以去除其中的水分和其他杂质。
此外,还可以通过添加一些特定的試剂,如硅胶和活性炭,对苯进行吸附和脱除其中的杂质。
纯苯的生产工艺需要严格控制温度和压力,以及选择合适的催化剂和吸附剂,以确保纯苯的质量。
此外,还需要进行定期的检验和监控,以确保生产过程的安全和稳定。
总之,纯苯的生产工艺包括石脑油的提取、苯的分离和纯化等步骤。
通过合理的操作和控制,可以获得高质量的纯苯产品。

苯酚纯化方法
苯酚是一种重要的有机化合物,它具有多种用途,如制药、染料、香料等。
因此,苯酚的纯化是一个重要的步骤,以确保其质量。
苯酚的纯化主要通过溶剂萃取、沉淀法、蒸馏法和分子筛等方法来实现。
其中,溶剂萃取是最常用的方法,它可以有效地将苯酚从混合物中分离出来。
首先,将混合物加入溶剂,然后将溶剂和混合物混合均匀,使苯酚溶解在溶剂中,最后将溶剂和混合物分离,即可得到纯净的苯酚。
沉淀法也是一种常用的苯酚纯化方法,它可以有效地将苯酚从混合物中分离出来。
首先,将混合物加入溶剂,然后加入沉淀剂,使苯酚沉淀,最后将沉淀物和混合物分离,即可得到纯净的苯酚。
蒸馏法也是一种常用的苯酚纯化方法,它可以有效地将苯酚从混合物中分离出来。
首先,将混合物加入蒸馏器,然后加热蒸馏,使苯酚蒸发,最后将蒸馏液和混合物分离,即可得到纯净的苯酚。
最后,分子筛也是一种常用的苯酚纯化方法,它可以有效地将苯酚从混合物中
分离出来。
首先,将混合物加入分子筛,然后将分子筛放入真空容器中,使苯酚被吸附在分子筛上,最后将分子筛和混合物分离,即可得到纯净的苯酚。
总之,苯酚的纯化主要通过溶剂萃取、沉淀法、蒸馏法和分子筛等方法来实现,这些方法都可以有效地将苯酚从混合物中分离出来,从而获得纯净的苯酚。

&常用有机溶剂的纯化方法1. 甲醇(CH 3OH)工业甲醇含水量在0.5%~1%,含醛酮(以丙酮计)约0.1%。
由于甲醇和水不形成共沸混合物,因此可用高效精馏柱将少量水除去。
精制甲醇中含水0.1%和丙酮0.02%,一般已可应用。
若需含水量低于0.1%,可用3A 分子筛干燥,也可用镁处理(见绝对乙醇的制备)。
若要除去含有的羰基化合物,可在500mL 甲醇中加入25mL 糠醛和60mL10%NaOH 溶液,回流6~12小时,即可分馏出无丙酮的甲醇,丙酮与糠醛生成树脂状物留在瓶内。
纯甲醇b.p. 64.95℃,n D 20 1.3288,d 4200.7914。
甲醇为一级易燃液体,应贮存于阴凉通风处,注意防火。
甲醇可经皮肤进入人体,饮用或吸入蒸气会刺激视神经及视网膜,导致眼睛失明,直到死亡。
人的半致死量LD 50为13.5g/kg ,经口服甲醇的致死量LD 为1g/kg ,15mL 可致失明。
2. 乙醇(CH 3CH 2OH)工业乙醇含量为95.5%,含水4.4%,乙醇与水形成共沸物,不能用一般分馏法去水。
实验室常用生石灰为脱水剂,乙醇中的水与生石灰作用生成氢氧化钙可去除水分,蒸馏后可得含量约99.5%的无水乙醇。
如需绝对无水乙醇,可用金属钠或金属镁将无水乙醇进一步处理,得到纯度可超过99.95%的绝对乙醇。
(1)无水乙醇(含量99.5%)的制备在500ml 圆底烧瓶中,加入95%乙醇200mL 和生石灰50g, 放置过夜。
然后在水浴上回流3小时,再将乙醇蒸出,得含量约99.5%的无水乙醇。
另外可利用苯、水和乙醇形成低共沸混合物的性质,将苯加入乙醇中,进行分馏,在64.9℃时蒸出苯、水、乙醇的三元恒沸混合物,多余的苯在68.3℃与乙醇形成二元恒沸混合物被蒸出,最后蒸出乙醇。
工业多采用此法。
(2)绝对乙醇(含量99.95%)的制备①用金属镁制备在250mL 的圆底烧瓶中,放置0.6g 干燥洁净的镁条和几小粒碘,加入10mL99.5%的乙醇,装上回流冷凝管。

实验室中常⽤的有机溶剂的纯化⽅法1.⼄酸⼄酯市售的⼄酸⼄酯常含有微量⽔、⼄醇和⼄酸。
可先⽤等体积的5%碳酸钠溶液洗涤,再⽤饱和氯化钙溶液洗涤,酯层倒⼊⼲燥的锥形瓶中,加⼊适量⽆⽔碳酸钾⼲燥1h后,蒸馏,收集77.0。
77.5℃馏分。
2.⽯油醚⽯油醚是低级烷烃的混合物。
根据沸程范围不同可分为30~60℃、60~90℃和90~120℃等不同规格。
⽯油醚中常含有少量沸点与烷烃相近的不饱和烃,难以⽤蒸馏法进⾏分离,此时可⽤浓硫酸和⾼锰酸钾将其除去。
⽅法如下。
在150mL分液漏⽃中,加⼊100mL⽯油醚,⽤10mL浓硫酸分两次洗涤,再⽤10%硫酸与⾼锰酸钾配制的饱和溶液洗涤,直⾄⽔层中紫⾊不再消失为⽌。
⽤蒸馏⽔洗涤两次后,将⽯油醚倒⼊⼲燥的锥形瓶中,加⼊⽆⽔氯化钙⼲燥lh。
蒸馏,收集需要规格的馏分。
3.氯仿普通氯仿中含有1%⼄醇(这是为防⽌氯仿分解为有毒的光⽓,作为稳定剂加进去的)。
除去⼄醇的⽅法是⽤⽔洗涤氯仿5~6次后,将分出的氯仿⽤⽆⽔氯化钙⼲燥24h,再进⾏蒸馏,收集60.5~61.5℃馏分。
纯品应装在棕⾊瓶内,置于暗处避光保存。
4.苯普通苯中可能含有少量噻吩,除去的⽅法是⽤少量(约为苯体积的15%)浓硫酸洗涤数次,再分别⽤⽔、10%碳酸钠溶液和⽔洗涤。
分离出苯,置于锥形瓶中,⽤⽆⽔氯化钙⼲燥24h后,⽔浴加热蒸馏,收集79.5~80.5℃馏分。
在有机化学实验中,经常使⽤各类溶剂作为反应介质或⽤来分离提纯粗产物。
由于反应的特点和物质的性质不同,对溶剂规格的要求也不相同。
有些反应(如格⽒试剂的制备反应)对溶剂的要求较⾼,即使微量杂质或⽔分的存在,也会影响实验的正常进⾏。
这种情况下,就需对溶剂进⾏纯化处理,以满⾜实验的正常要求。
这⾥介绍⼏种实验室中常⽤的有机溶剂的纯化⽅法。
5.⽆⽔⼄醚市售⼄醚中常含有微量⽔、⼄醇和其他杂质,不能满⾜⽆⽔实验的要求。
可⽤下述⽅法进⾏处理,制得⽆⽔⼄醚。
在250mL⼲燥的圆底烧瓶中,加⼊100mL⼄醚和⼏粒沸⽯,装上回流冷凝管。

实验室中常用的有机溶剂的纯化方法
1.蒸馏纯化法:蒸馏是将混合溶剂加热,利用其沸点差异使溶剂分离的过程。
对于常见的有机溶剂如乙醚、甲苯、丙酮等,通过简单蒸馏或分馏装置的使用,可以获得高纯度的有机溶剂。
2.结晶纯化法:这种方法适用于具有较高熔点的有机溶剂,如苯、甲苯、二甲苯等。
可以通过溶剂的逐渐蒸发,使溶剂慢慢冷却,从而得到高纯度的结晶物。
3.活性炭吸附纯化法:将有机溶剂与活性炭接触,利用活性炭表面的吸附作用去除其中的杂质。
这种方法适用于易挥发的溶剂,例如醇类、醚类等。
经过活性炭吸附后,可以得到高质量的有机溶剂。
4.沉淀纯化法:通过加入适量的沉淀剂,如醋酸铅或硫酸铅,使有机溶剂中的杂质发生反应生成固体沉淀,在离心或过滤后分离得到纯净的有机溶剂。
5.撇液法:对于含有多种有机溶剂的混合物,可以通过不同溶剂的密度差异,使其中一个有机溶剂相对较轻的浮于另一个有机溶剂之上,然后通过撇除上层溶剂来实现纯化。
6.含水溶剂的干燥纯化法:对于一些有机溶剂中存在的水分和其他杂质,可以通过将溶剂与干燥剂如无水氯化钙、无水硫酸铜等接触,使其吸附或抽除水分,从而实现溶剂的干燥纯化。
此外,还有一些其他的纯化方法,如提取纯化法、油墨、树脂吸附纯化法等。
总的来说,对于不同的有机溶剂,选择合适的纯化方法可以提高溶剂的纯度和质量,有助于实验的顺利进行。
需要注意的是,实验室中进
行有机溶剂的纯化时,要注意安全操作,避免有机溶剂的挥发和火灾的发生。
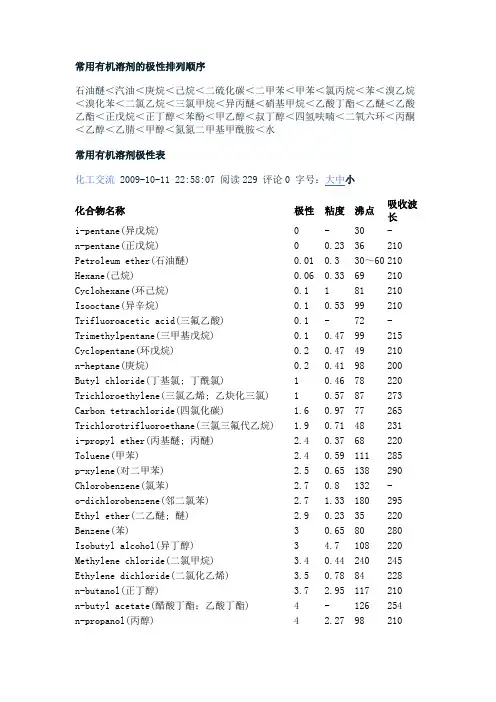
常用有机溶剂的极性排列顺序石油醚<汽油<庚烷<己烷<二硫化碳<二甲苯<甲苯<氯丙烷<苯<溴乙烷<溴化苯<二氯乙烷<三氯甲烷<异丙醚<硝基甲烷<乙酸丁酯<乙醚<乙酸乙酯<正戊烷<正丁醇<苯酚<甲乙醇<叔丁醇<四氢呋喃<二氧六环<丙酮<乙醇<乙腈<甲醇<氮氮二甲基甲酰胺<水常用有机溶剂极性表化工交流 2009-10-11 22:58:07 阅读229 评论0 字号:大中小化合物名称极性粘度沸点吸收波长i-pentane(异戊烷) 0 - 30 -n-pentane(正戊烷) 0 0.23 36 210 Petroleum ether(石油醚) 0.01 0.3 30~60 210 Hexane(己烷) 0.06 0.33 69 210 Cyclohexane(环己烷) 0.1 1 81 210 Isooctane(异辛烷) 0.1 0.53 99 210 Trifluoroacetic acid(三氟乙酸) 0.1 - 72 - Trimethylpentane(三甲基戊烷) 0.1 0.47 99 215 Cyclopentane(环戊烷) 0.2 0.47 49 210n-heptane(庚烷) 0.2 0.41 98 200 Butyl chloride(丁基氯; 丁酰氯) 1 0.46 78 220 Trichloroethylene(三氯乙烯; 乙炔化三氯) 1 0.57 87 273 Carbon tetrachloride(四氯化碳) 1.6 0.97 77 265 Trichlorotrifluoroethane(三氯三氟代乙烷) 1.9 0.71 48 231i-propyl ether(丙基醚; 丙醚) 2.4 0.37 68 220 Toluene(甲苯) 2.4 0.59 111 285p-xylene(对二甲苯) 2.5 0.65 138 290 Chlorobenzene(氯苯) 2.7 0.8 132 -o-dichlorobenzene(邻二氯苯) 2.7 1.33 180 295 Ethyl ether(二乙醚; 醚) 2.9 0.23 35 220 Benzene(苯) 3 0.65 80 280 Isobutyl alcohol(异丁醇) 3 4.7 108 220 Methylene chloride(二氯甲烷) 3.4 0.44 240 245 Ethylene dichloride(二氯化乙烯) 3.5 0.78 84 228n-butanol(正丁醇) 3.7 2.95 117 210n-butyl acetate(醋酸丁酯;乙酸丁酯) 4 - 126 254n-propanol(丙醇) 4 2.27 98 210 Methyl isobutyl ketone(甲基异丁酮) 4.2 - 119 330Tetrahydrofuran(四氢呋喃) 4.2 0.55 66 220 Ethyl acetate(乙酸乙酯) 4.30 0.45 77 260 i-propanol(异丙醇) 4.3 2.37 82 210 Chloroform(氯仿) 4.4 0.57 61 245 Methyl ethyl ketone(甲基乙基酮) 4.5 0.43 80 330 Dioxane(二恶烷; 二氧六环; 二氧杂环己烷) 4.8 1.54 102 220 Pyridine(吡啶) 5.3 0.97 115 305 Acetone(丙酮) 5.4 0.32 57 330 Nitromethane(硝基甲烷) 6 0.67 101 330 Acetic acid(乙酸) 6.2 1.28 118 230 Acetonitrile(乙腈) 6.2 0.37 82 210 Aniline(苯胺) 6.3 4.4 184 - Dimethyl formamide(二甲基甲酰胺) 6.4 0.92 153 270 Methanol(甲醇) 6.6 0.6 65 210 Ethylene glycol(乙二醇 ) 6.9 19.9 197 210 Dimethyl sulfoxide(二甲亚砜 DMSO) 7.2 2.24 189 268 Water(水)10.2 1 100 268。

常用有机溶剂分类第一类溶剂是指已知可以致癌并被强烈怀疑对人和环境有害的溶剂。
在可能的情况下,应避免使用这类溶剂。
如果在生产治疗价值较大的药品时不可避免地使用了这类溶剂,除非能证明其合理性,残留量必须控制在规定的范围内,如:苯(2ppm)、四氯化碳(4ppm)、1,2-二氯乙烷(5ppm)、1,1-二氯乙烷(8ppm)、1,1,1-三氯乙烷(1500ppm)。
第二类溶剂是指无基因毒性但有动物致癌性的溶剂。
按每日用药10克计算的每日允许接触量如下:2-甲氧基乙醇(50ppm)、氯仿(60ppm)、1,1,2-三氯乙烯(80ppm)、1,2-二甲氧基乙烷(100ppm)、1,2,3,4-四氢化萘(100ppm)、2-乙氧基乙醇(160ppm)、环丁砜(160ppm)、嘧啶(200ppm)、甲酰胺(220ppm)、正己烷(290ppm)、氯苯(360ppm)、二氧杂环己烷(380ppm)、乙腈(410ppm)、二氯甲烷(600ppm)、乙烯基乙二醇(620ppm)、N,N-二甲基甲酰胺(880ppm)、甲苯(890ppm)、N,N-二甲基乙酰胺(1090ppm)、甲基环己烷(1180ppm)、1,2-二氯乙烯(1870ppm)、二甲苯(2170ppm)、甲醇(3000ppm)、环己烷(3880ppm)、N-甲基吡咯烷酮(4840ppm)。
第三类溶剂是指对人体低毒的溶剂。
急性或短期研究显示,这些溶剂毒性较低,基因毒性研究结果呈阴性,但尚无这些溶剂的长期毒性或致癌性的数据。
在无需论证的情况下,残留溶剂的量不高于0.5%是可接受的,但高于此值则须证明其合理性。
这类溶剂包括:戊烷、甲酸、乙酸、乙醚、丙酮、苯甲醚、1-丙醇、2-丙醇、1-丁醇、2-丁醇、戊醇、乙酸丁酯、三丁甲基乙醚、乙酸异丙酯、甲乙酮、二甲亚砜、异丙基苯、乙酸乙酯、甲酸乙酯、乙酸异丁酯、乙酸甲酯、3-甲基-1-丁醇、甲基异丁酮、2-甲基-1-丙醇、乙酸丙酯。

溶剂分类、纯化、选择原则的介绍。
1、溶剂分类原则:①按化学组成分类:分为有机溶剂和无机溶剂。
②按极性分类:分为极性溶剂和非极性溶剂,对于常用溶剂的极性有:水>甲酸>甲醇>乙酸>乙醇>异丙醇>乙腈>DMSO>DMF>丙酮>HMPA>CH2Cl2>吡啶>氯仿>氯苯>THF>二氧六环>乙醚>苯>甲苯>CCl4>正辛烷>环己烷>石油醚。
③按结构分类,有机溶剂按化学结构可大致分为十类:(1) 芳香烃类:苯、甲苯等;(2) 脂肪烃类:戊烷、己烷等;(3) 脂环烃类:环己烷、环己酮等;(4) 卤化烃类:氯苯、二氯甲烷等;(5) 醇类:甲醇、乙醇等;(6) 醚类:乙醚、环氧丙烷等;(7) 酯类:乙酸乙酯、苯甲酸乙酯等;(8) 酮类:丙酮、甲基丁酮等;(3) 多羟基化合物及衍生物:乙二醇单甲醚、丙三醇等;(10) 其他:乙腈、吡啶等。
④按毒性分类:(1)第一类:是指已知可以致癌并被强烈怀疑对人和环境有害的溶剂,如:苯、四氯化碳、氯乙烷类等;(2)第二类:是指无基因毒性但有动物致癌性的溶剂,如:氯仿、二甲苯、甲醇、环己烷、N-甲基吡咯烷酮等、正己烷、氯苯;(3)第三类:是指对人体低毒的溶剂。
急性或短期研究显示,这些溶剂毒性较低,基因毒性研究结果呈阴性,但尚无这些溶剂的长期毒性或致癌性的数据,如:乙醚、丙酮、苯甲醚、乙酸乙酯、甲酸乙酯、甲基异丁酮等。
⑤按沸点高低的分类:(1)低沸点溶剂(沸点在100℃以下)这类溶剂的特点是蒸发速度快,易干燥、粘度低,大多数具有芳香气味。
属于这类溶剂的一般是活性溶剂或稀释剂。
例如:甲醚、甲酸甲酯、丙酮、苯等等;(2)中沸点溶剂(沸点在100~150℃)这类溶剂用于硝基喷漆,流平性好。
例如:丁醇、甲苯、环己酮等等;(3)高沸点溶剂(沸点在150~200℃)这类溶剂的特点是蒸发速度慢,溶解能力强,作涂料用时涂膜流动性好,可以防止沉淀合涂膜发白。


苯分离和提纯苯是一种常见的有机化合物,广泛应用于化工、医药、农药等领域。
苯的纯度对于其应用性能至关重要,因此分离和提纯苯是一个重要的工艺过程。
一、苯的分离方法苯的分离可以采用许多不同的方法,下面将介绍两种常见的分离方法。
1. 蒸馏法蒸馏是最常用的苯分离方法之一。
苯和其他有机物在沸点上有较大的差异,通过控制温度和压力,在适当的蒸馏装置中进行蒸馏,可以使苯和其他杂质分离。
在蒸馏过程中,苯会先于其他有机物蒸发,进而通过冷凝收集得到纯苯。
2. 结晶法结晶法也是一种常用的苯分离方法。
苯和其他杂质在溶解度上有所差异,通过适当的溶剂和温度条件,使苯在溶液中结晶出来,进而分离出纯苯。
结晶法分离苯的优点是操作简单,但对溶剂和温度的选择要求较高。
二、苯的提纯方法苯的提纯方法可以采用以下两种常见的方法。
1. 重结晶法重结晶法是一种常用的苯提纯方法。
首先将苯通过适当的溶剂溶解,然后通过加热溶解,再通过冷却结晶出纯苯。
重结晶法可以去除苯中的杂质,提高苯的纯度。
2. 萃取法萃取法是一种常用的苯提纯方法之一。
通过选择合适的溶剂,将含有苯和杂质的混合物进行萃取。
在适当的条件下,苯可以被溶剂提取出来,从而实现苯的提纯。
三、苯的分离与提纯工艺流程苯的分离与提纯工艺流程可以根据具体情况进行设计,下面是一个常见的工艺流程示例。
1. 分离过程:(1) 将含有苯和其他有机物的混合物经过预处理,去除固体杂质。
(2) 将混合物经过加热,进入蒸馏塔进行蒸馏,控制温度和压力,使苯和其他有机物分离。
(3) 将蒸馏得到的苯进行冷凝收集,得到大部分的苯。
2. 提纯过程:(1) 将蒸馏得到的苯通过重结晶法进行提纯,加热苯溶液使其溶解,然后通过冷却结晶出纯苯。
(2) 通过重复结晶的方式,可以进一步提高苯的纯度。
(3) 若需要更高纯度的苯,可以采用萃取法进行提纯,选择合适的溶剂进行苯的萃取。
四、苯的分离与提纯设备苯的分离与提纯需要使用适当的设备,以保证操作效果和产品质量。
一、实验目的1. 了解苯分子的结构、性质及反应特点;2. 掌握苯分子的提取、纯化方法;3. 熟悉苯分子的性质实验操作,加深对苯分子性质的理解。
二、实验原理苯(C6H6)是一种无色、易挥发的有机溶剂,具有特殊的芳香性。
苯分子由6个碳原子和6个氢原子组成,呈平面正六边形结构。
苯分子在空气中燃烧时产生明亮的火焰,并伴有浓烟。
本实验通过苯的提取、纯化,观察苯的物理性质和化学性质,验证苯分子的结构、性质及反应特点。
三、实验仪器与试剂1. 仪器:烧杯、漏斗、玻璃棒、铁架台、酒精灯、试管、冷凝管、蒸发皿、滤纸、石棉网、量筒、电子天平、蒸馏装置等。
2. 试剂:苯(工业级)、浓硫酸、无水硫酸钠、蒸馏水、氢氧化钠溶液、碘化钾溶液、溴水、高锰酸钾溶液等。
四、实验步骤1. 苯的提取(1)将工业苯加入烧杯中,加入适量的水;(2)用玻璃棒搅拌,使苯与水分层;(3)静置,待分层后,用漏斗分离苯层,收集苯。
2. 苯的纯化(1)将收集到的苯加入烧杯中,加入适量的浓硫酸,搅拌;(2)加入适量的无水硫酸钠,搅拌;(3)静置,待分层后,用漏斗分离苯层,收集苯。
3. 苯的物理性质实验(1)观察苯的颜色、气味;(2)测定苯的沸点;(3)测定苯的密度。
4. 苯的化学性质实验(1)苯的燃烧实验:将苯加入试管中,用酒精灯点燃,观察火焰颜色;(2)苯与溴水的反应实验:将苯加入试管中,加入溴水,观察溶液颜色变化;(3)苯与碘化钾溶液的反应实验:将苯加入试管中,加入碘化钾溶液,观察溶液颜色变化;(4)苯与高锰酸钾溶液的反应实验:将苯加入试管中,加入高锰酸钾溶液,观察溶液颜色变化。
五、实验结果与分析1. 苯为无色、易挥发的有机溶剂,具有特殊的芳香性;2. 苯的沸点为80.1℃,密度为0.879g/mL;3. 苯在空气中燃烧时产生明亮的火焰,并伴有浓烟;4. 苯与溴水反应,溶液颜色由黄色变为无色;5. 苯与碘化钾溶液反应,溶液颜色由紫色变为棕色;6. 苯与高锰酸钾溶液反应,溶液颜色由紫色变为棕色。
医药中常用有机溶剂分类及残留限度医药中常用有机溶剂分类及残留限度医药中常用有机溶剂分类及残留限度药品的残留溶剂无治疗作用并可能对人体的健康和环境造成危害,本文对国际协调大会(ICH)制订的指导原则及各国执行情况作了较为详尽的介绍。
药品的残留溶剂,又称有机挥发性杂质,是指在活性药物成分、辅料和药品生产过程中使用和产生的有机挥发性化学物质。
药品还可被来自包装、运输、仓储中的有机溶剂污染。
药品生产商有责任确保终产品中的任何一种残留溶剂对人体无害。
各国药监部门曾使用不同的药品残留溶剂指导原则,为此国际组织展开了协调工作。
经相关程序讨论和审查后,国际协调大会的指导原则于1997年7月17日获得通过,被推荐至国际协调大会(ICH)的指导委员会采用。
该指导原则要求,如果某个药品的生产或纯化过程可导致溶剂残留,就应对这个药品进行检测,并且只检测生产过程或纯化中使用或产生的那种溶剂。
根据使用量的多少,可采用累加的方法计算药品中残留溶剂的量。
如果累加量低于或等于指导原则中的推荐量,则该药品无需进行残留溶剂检测;如果累加量高于推荐量,则必须对该药品进行残留溶剂检测。
该指导原则适用于颁布以后上市的所有剂型和给药途径,但不适用于在临床研究阶段使用的潜在新药和新辅料,也不适用于已上市的现有药物。
在某些情况如短期(小于30天)或局部应用下,视具体情况,溶剂的高残留量也可接受。
按照毒性大小和对环境的危害程度,该指导原则将溶剂分成三类(所列举的溶剂并不完全,应对合成和生产过程所有可能的残留溶剂进行评估):第一类溶剂是指已知可以致癌并被强烈怀疑对人和环境有害的溶剂。
在可能的情况下,应避免使用这类溶剂。
如果在生产治疗价值较大的药品时不可避免地使用了这类溶剂,除非能证明其合理性,残留量必须控制在规定的范围内,如:苯(2ppm)、四氯化碳(4ppm)、1,2-二氯乙烷(5ppm)、1,1-二氯乙烷(8ppm)、1,1,1-三氯乙烷(1500ppm)。
常用有机试剂的纯化1.丙酮沸点56.2℃,折光率1.3588,相对密度0.7899。
普通丙酮常含有少量的水及甲醇、乙醛等还原性杂质。
其纯化方法有:⑴.于250mL丙酮中加入2.5g高锰酸钾回流,若高锰酸钾紫色很快消失,再加入少量高锰酸钾继续回流,至紫色不褪为止。
然后将丙酮蒸出,用无水碳酸钾或无水硫酸钙干燥,过滤后蒸馏,收集55~56.5℃的馏分。
用此法纯化丙酮时,须注意丙酮中含还原性物质不能太多,否则会过多消耗高锰酸钾和丙酮,使处理时间增长。
⑵.将100mL丙酮装入分液漏斗中,先加入4mL10%硝酸银溶液,再加入3.6mL1mol/L 氢氧化钠溶液,振摇10min,分出丙酮层,再加入无水硫酸钾或无水硫酸钙进行干燥。
最后蒸馏收集55~56.5℃馏分。
此法比方法⑴要快,但硝酸银较贵,只宜做小量纯化用。
2.二氧六环沸点101.5℃,熔点12℃,折光率1.4424,相对密度1.0336。
二氧六环能与水任意混合,常含有少量二乙醇缩醛与水,久贮的二氧六环可能含有过氧化物(鉴定和除去参阅乙醚)二氧六环的纯化方法,在500mL二氧六环中加入8mL浓盐酸和50mL水的溶液,回流6~10h,在回流过程中,慢慢通入氮气以除去生成的乙醛。
冷却后,加入固体氢氧化钾,直到不能再溶解为止,分去水层,再用固体氢氧化钾干燥24h。
然后过滤,在金属钠存在下加热回流8~12h,最后在金属钠存在下蒸馏,压入饥丝密封保存。
精制过的1,4‐二氧环己烷应当避免与空气接触。
3.吡啶沸点115.5℃,折光率1.5095,相对密度0.9819。
分析纯的吡啶含有少量水分,可供一般实验用。
如要制得无水吡啶,可将吡啶与粒氢氧化钾(钠)一同回流,然后隔绝潮气蒸出备用。
干燥的吡啶吸水性很强,保存时应将容器口用石蜡封好。
4.石油醚石油醚为轻质石油产品,是低相对分子质量烷烃类的混合物。
其沸程为30~150℃,收集的温度区间一般为30℃左右。
有30~60℃,60~90℃,90~120℃等沸程规格的石油醚。
在有机化学实验中,经常使用各类溶剂作为反应介质或用来分离提纯粗产物。
由于反应的特点和物质的性质不同,对溶剂规格的要求也不相同。
有些反应(如格氏试剂的制备反应)对溶剂的要求较高,即使微量杂质或水分的存在,也会影响实验的正常进行。
这种情况下,就需对溶剂进行纯化处理,以满足实验的正常要求。
这里介绍几种实验室中常用的有机溶剂的纯化方法。
1.无水乙醚市售乙醚中常含有微量水、乙醇和其他杂质,不能满足无水实验的要求。
可用下述方法进行处理,制得无水乙醚。
在250mL干燥的圆底烧瓶中,加入100mL乙醚和几粒沸石,装上回流冷凝管。
将盛有10mL浓硫酸的滴液漏斗通过带有侧口的橡胶塞安装在冷凝管上端接通冷凝水后,将浓硫酸缓慢滴入乙醚中,由于吸水作用产生热,乙醚会自行沸腾。
当乙醚停止沸腾后,拆除回流冷凝管,补加沸石后,改成蒸馏装置,用干燥的锥形瓶作接收器。
在接液管的支管上安装一支盛有无水氯化钙的干燥管,干燥管的另一端连接橡胶管,将逸出的乙醚蒸气导入水槽中。
用事先准备好的热水浴加热蒸馏,收集34.5℃馏分70~80mL,停止蒸馏。
烧瓶内所剩残液倒入指定的回收瓶中(切不可向残液中加水!)。
向盛有乙醚的锥形瓶中加入1g钠丝,然后用带有氯化钙干燥管的塞子塞上,以防止潮气侵入并可使产生的气体逸出。
放置24h,使乙醚中残存的痕量水和乙醇转化为氢氧化钠和乙醇钠。
如发现金属钠表面已全部发生作用,则需补加少量钠丝,放置至无气泡产生,金属钠表面完好,即可满足使用要求。
2.绝对乙醇市售的无水乙醇一般只能达到99.5%的纯度,而许多反应中需要使用纯度更高的绝对乙醇,可按下法制取。
在250mL干燥的圆底烧瓶中,加入0.6g干燥纯净的镁丝和10mL99.5%的乙醇,安装回流冷凝管,冷凝管上口附加一支无水氯化钙干燥管。
在沸水浴上加热至微沸,移去热源,立刻加入几粒碘(注意此时不要振荡),可见随即在碘粒附近发生反应,若反应较慢,可稍加热,若不见反应发生,可补加几粒碘。
常用有机溶剂纯化处理常用有机溶剂纯化处理常用有机试剂的纯化-丙酮沸点56.2℃,折光率1.358 8,相对密度0.789 9。
普通丙酮常含有少量的水及甲醇、乙醛等还原性杂质。
其纯化方法有:⑴于250mL丙酮中加入2.5g高锰酸钾回流,若高锰酸钾紫色很快消失,再加入少量高锰酸钾继续回流,至紫色不褪为止。
然后将丙酮蒸出,用无水碳酸钾或无水硫酸钙干燥,过滤后蒸馏,收集55~56.5℃的馏分。
用此法纯化丙酮时,须注意丙酮中含还原性物质不能太多,否则会过多消耗高锰酸钾和丙酮,使处理时间增长。
⑵将100mL丙酮装入分液漏斗中,先加入4mL10%硝酸银溶液,再加入3.6mL1mol/L氢氧化钠溶液,振摇10min,分出丙酮层,再加入无水硫酸钾或无水硫酸钙进行干燥。
最后蒸馏收集55~56.5℃馏分。
此法比方法⑴要快,但硝酸银较贵,只宜做小量纯化用。
常用有机溶剂的纯化-二氧六环沸点101.5℃,熔点12℃,折光率1.442 4,相对密度1.033 6。
二氧六环能与水任意混合,常含有少量二乙醇缩醛与水,久贮的二氧六环可能含有过氧化物(鉴定和除去参阅乙醚)。
二氧六环的纯化方法,在500mL二氧六环中加入8mL浓盐酸和50mL水的溶液,回流6~10h,在回流过程中,慢慢通入氮气以除去生成的乙醛。
冷却后,加入固体氢氧化钾,直到不能再溶解为止,分去水层,再用固体氢氧化钾干燥24h。
然后过滤,在金属钠存在下加热回流8~12h,最后在金属钠存在下蒸馏,压入饥丝密封保存。
精制过的1,4-二氧环己烷应当避免与空气接触。
常用有机溶剂的纯化-吡啶沸点115.5℃,折光率1.509 5,相对密度0.981 9。
分析纯的吡啶含有少量水分,可供一般实验用。
如要制得无水吡啶,可将吡啶与粒氢氧化钾(钠)一同回流,然后隔绝潮气蒸出备用。
干燥的吡啶吸水性很强,保存时应将容器口用石蜡封好。
常用有机溶剂的纯化-石油醚石油醚为轻质石油产品,是低相对分子质量烷烃类的混合物。
有机溶剂的干燥-几种常用溶剂的无水化处理概述1)不含氯溶剂的干燥:一般指己烷,甲苯,苯,乙醚,THF,戊烷。
可以用Na和二苯甲酮回流,等到变色时蒸出,蒸出的溶剂要在N2下保存,加上活化过的分子筛。
要是含水量很大,可以先用P2O5等预干燥,蒸出,重复前面的过程2)含氯溶剂的干燥:一般指CH2Cl2,CHCl3,CCl4等一般会用CaH浸泡12h以后,再加热回流蒸出,蒸出的溶剂要在N2下保存,加上活化过的分子筛。
不能用Na干燥,含氯溶剂与Na会发生连锁反应发生爆炸。
要是含水量很大,可以先用P2O5等预干燥,蒸出,重复前面的过程。
3)活泼氢的溶剂:一般指甲醇,乙醇。
可以用新打磨得镁条,剪成镁屑,加I2用来引发反应,加热,不搅拌,等到引发已经开始的时候再搅拌,回流到出现白色的混浊时就可以蒸出,这是制备绝对甲醇,乙醇的方法。
4)乙酸除水。
在乙酸中加入乙酸酐加热回流,蒸出乙酸就可以。
无水乙醇对于要求不太高的乙醇,可以加人氧化钙(生石灰)煮沸回流,使乙醇中的水与生石灰作用生成氢氧化钙,然后再将无水乙醇蒸出。
这样得到无水乙醇,纯度最高约99.5%。
纯度更高的无水乙醇可用金属镁或金属钠进行处理。
(1) 无水乙醇(含量99.5%)的制备在圆底烧瓶中,放置95%乙醇和生石灰,装上回流冷凝管,其上端接一氯化钙干燥管,在水浴上回流加热2~3 h,稍冷后取下冷凝管,改成蒸馏装置。
蒸去前馏分后,用干燥的吸滤瓶或蒸馏瓶作接受器,其支管接一氯化钙干燥管,使与大气相通。
(2) 无水乙醇(含量99 .95%)的制备①用金属镁制取:在圆底烧瓶中,放置干燥纯净的镁条,小量99.5 %乙醇,装上回流冷凝管,并在冷凝管上端加一只无水氯化钙干燥管。
在沸点浴上或用火直接加热使达微沸,移去热源,立刻加入几粒碘片(此时注意不要振荡),顷刻即在碘粒附近发生作用,最后可以达到相当剧烈的程度。
有时作用太慢则需加热,如果在加碘之后,作用仍不开始,则可再加入数粒碘(一般的讲,乙醇与镁的作用是缓慢的,如所用乙醇含水量超过0.596则作用更为困难)。
常用有机溶剂的纯化-苯
沸点80.1℃,折光率1.501 1,相对密度0.87865。
普通苯常含有少量水和噻吩,噻吩和沸点84℃,与苯接近,不能用蒸馏的方法除去。
噻吩的检验:取1mL苯加入2mL溶有2mg吲哚醌的浓硫酸,振荡片刻,若酸层号蓝绿色,即表示有噻吩存在。
噻吩和水的除去:将苯装入分液漏斗中,加入相当于苯体积七分之一的浓硫酸,振摇使噻吩磺化,弃去酸液,再加入新的浓硫酸,重复操作几次,直到酸层呈现无色或淡黄色并检验无噻吩为止。
将上述无噻吩的苯依次用10%碳酸钠溶液和水洗至中性,再用氯化钙干燥,进行蒸馏,收集80℃的馏分,最后用金属钠脱去微量的水得无水苯。