医学免疫学-第4讲--免疫球蛋白PPT课件
- 格式:ppt
- 大小:2.87 MB
- 文档页数:45





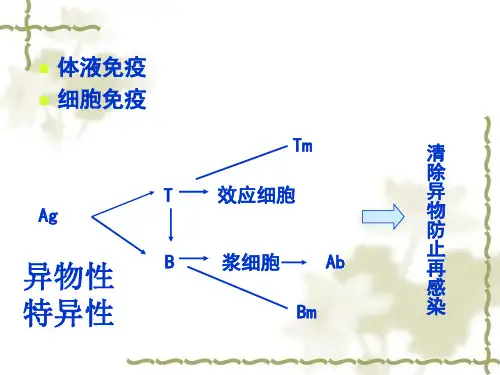



第四章免疫球蛋白抗体与免疫球蛋白的概念抗体(antibody,Ab)分子是能与抗原特异结合的大分子球蛋白。
包括可溶性抗体分子和和膜性抗体分子。
免疫球蛋白分子(immunoglobulin,Ig)具有抗体活性或化学结构与抗体相似的的球蛋白。
抗体的发现及其特性一、发现:1890年德国学者Behring和日本学者北里用白喉杆菌外毒素免疫动物,在其血清中发现一种能中和这种外毒素的组分称为抗毒素。
这是在血清中发现的第一种抗体。
二、抗体的理化性质1、抗体是球蛋白(Globulin)通过电泳证明抗体是两种球蛋白后又经电泳分析,超速离心分析和分子量测定等方法,发现大部分抗体是r球蛋白,小部分是β球蛋白。
所以早期对抗体性质的研究证明抗体不是由均质性球蛋白(γ??β)组成,是异均性的。
2、免疫球蛋白(lmmunoglobulin, Ig)为了准确描述抗体球蛋白的性质,在60年代初提出将具有抗体活性的球蛋白称为免疫球蛋白。
从此r球蛋白则改称为IgG,BIM 称为IgM,而BIA称为IgA,其后又发现IgD和IgE。
抗体主要存在于血清中,但也存在于体液和外分泌液中,所以含有抗体的血清称为免疫血清。
B细胞表面上也存在免疫球蛋白,称为膜表面免疫球蛋白Surface membrane Ig,SmIg。
第一节、免疫球蛋白的结构(一)免疫球蛋白的基本结构Ig分子基本结构是由四个肽链组成的,包括二条较小的轻链和二条较大的重链,轻链与重链之间是由二硫键连接形成Ig分子单体,分为氨基端(N端),羧基端(C端)。
1、重链和轻链(1)重链(heavy chain,H链)450-550个氨基酸残基组成,分子量50-75KD,含糖数量不同,4-5个链内二硫键,可分为5类,μ、γ、α、δ、ε链,不同的H链与L链(κ或λ)组成完整的Ig分子。
分别称为:IgM,IgG,IgA,IgD 和IgE。
(2)轻链(light chain,L链)214个氨基酸残基组成,通常不含碳水化合物,分子量为24KD,有两个由链内二硫键组成的环肽,L链可分为:Kappa(κ)与lambda(λ)2个亚型。
