高中六种有机物的实验室制备简图教学内容
- 格式:doc
- 大小:199.50 KB
- 文档页数:4
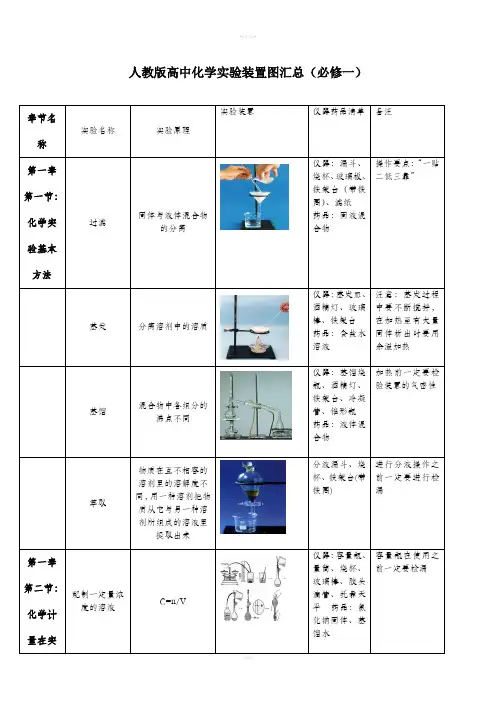

六种有机物的实验室制备简图一、乙烯的制备1、工业制法:石油裂解2、实验原理:CH3-CH2-OH + 浓H2SO4→ CH2=CH2↑+H2O3、注意:(1)温度计的水银球要插于反应物的位置;(2)温度要控制在170℃之间(140℃时生成乙醚);(3)须加入碎瓷片或沸石(防暴沸);(4)浓H2SO4(起催化与脱水作用)与乙醇的体积比为3:1;(5)用排水集气法收集乙烯(乙烯难溶于水);(6)反应液会变黑,有刺激性气味产生的原因:由于有C、SO2的生成。
4、实验装置:二、乙炔的制备乙炔可用电石与水反应制得,因此俗称电石气。
1、原料:电石、水2、实验原理:CaC2 + 2H2O → CH≡CH↑ + Ca(OH)23、反应特点:反应剧烈,放出大量的热;产生糊状的Ca(OH)2。
4、注意:(1)用饱和食盐水代替水,可减小反应速率,得到平稳的乙炔气流(食盐和碳化钙不起反应);(2)若在大试管中制取,则应在管口放一团棉花,避免泡沫从导管中喷出;(3)由电石制得的乙炔中往往含有H2S、PH3等杂质,故须将混合气体通过盛有CuSO4溶液的洗气瓶或通过NaOH溶液的洗气瓶;(4)用排水法收集。
5、实验装置:三、溴苯的制备1、原料:苯、液溴(纯溴)、还原铁粉2、实验原理:3、注意:(1)加药品次序:苯、液溴、铁粉;(2)催化剂实为FeBr3;(3)长导管作用:冷凝、回流;(4)除杂:制得的溴苯常溶有溴而呈褐色,可用稀NaOH洗涤,然后分液得纯溴苯。
发生装置4、实验装置:四、硝基苯的制备1、原料:苯、硝酸、浓硫酸2、实验原理:3、注意:(1)需用浓硫酸与浓硝酸配置混合酸;(2)逐滴加入苯(3)在50-60℃下水浴加热(温度过高会生成二硝基苯);(4)除去混合酸后,用蒸馏水与NaOH溶液洗涤,最后再用蒸馏水洗涤;(5)用无水CaCl2干燥、分离后得到纯产品。
4、实验装置:五、银镜反应1、原料:硝酸银溶液、氨水、乙醛2、反应方程式:AgOH + 2NH3·H2O = [Ag(NH3)2]+ OH- + 2H2OCH3CHO + 2[Ag(NH3)2] + 2OH-→ CH3COO- + NH4+ + 2Ag↓ + 3NH3+ H2O3、注意:(1)银氨溶液的配制:AgNO3溶液中滴加氨水至沉淀恰好溶;(2)热水浴加热时不可振荡试管;(3)碱性环境,氨水不能过量(防止生成易爆物);(4)银镜的处理:用硝酸溶解。



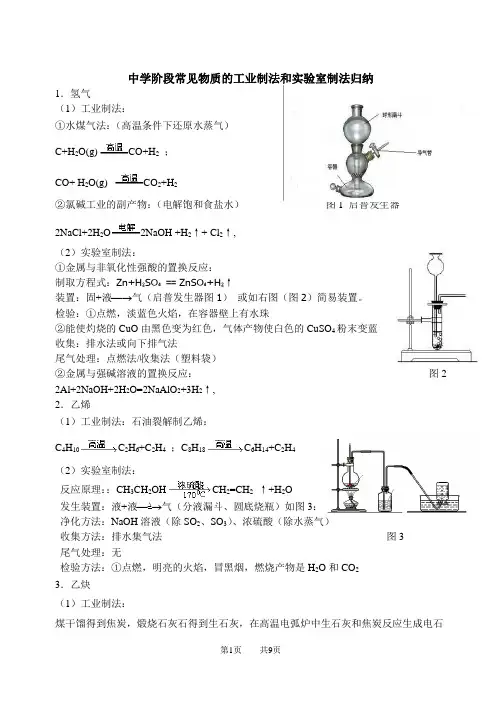
中学阶段常见物质的工业制法和实验室制法归纳1.氢气(1)工业制法:①水煤气法:(高温条件下还原水蒸气)C+H2O(g)CO+H2;CO+ H2O(g) CO2+H2②氯碱工业的副产物:(电解饱和食盐水)图1 启普发生器2NaCl+2H2O2NaOH +H2↑+ Cl2↑,(2)实验室制法:①金属与非氧化性强酸的置换反应:制取方程式:Zn+H₂SO₄== ZnSO₄+H₂↑装置:固+液−→气(启普发生器图1)或如右图(图2)简易装置。
检验:①点燃,淡蓝色火焰,在容器壁上有水珠②能使灼烧的CuO由黑色变为红色,气体产物使白色的CuSO4粉末变蓝收集:排水法或向下排气法尾气处理:点燃法/收集法(塑料袋)②金属与强碱溶液的置换反应:图2 2Al+2NaOH+2H2O=2NaAlO2+3H2↑,2.乙烯(1)工业制法:石油裂解制乙烯:C4H10C2H6+C2H4;C8H18C6H14+C2H4(2)实验室制法:反应原理::CH3CH2OH CH2=CH2↑+H2O发生装置:液+液−∆→气(分液漏斗、圆底烧瓶)如图3:净化方法:NaOH溶液(除SO2、SO3)、浓硫酸(除水蒸气)收集方法:排水集气法图3尾气处理:无检验方法:①点燃,明亮的火焰,冒黑烟,燃烧产物是H2O和CO23.乙炔(1)工业制法:煤干馏得到焦炭,煅烧石灰石得到生石灰,在高温电弧炉中生石灰和焦炭反应生成电石和一氧化碳,电石和饱和食盐水反应生成熟石灰和乙炔。
3C+CaO CaC2+CO↑;CaC2+2H2O Ca(OH)2+C2H2↑(2)实验室制法:反应原理:CaC2+2H2O −→ CH≡CH↑+Ca(OH)2发生装置:固+液−→气(分液漏斗、圆底烧瓶)如图4净化方法:CuSO4溶液、浓硫酸(除水蒸气)收集方法:排水集气法/向上排空气法尾气处理:无图4 4.一氧化碳(1)工业制法:①水煤气法:(高温条件下还原水蒸气)C+H2O(g)CO+H2;②焦炭还原二氧化硅(工业制备粗硅的副产物):2C+SiO2Si+2CO↑③工业制备电石的副产物:3C+CaO CaC2+CO↑;(2)实验室制法:制取原理:浓硫酸对有机物的脱水作用在蒸馏烧瓶里加入浓硫酸,在分液漏斗里盛放甲酸①甲酸分解法:HCOOH CO↑+H2O装置:分液漏斗,圆底烧瓶(图5)检验:燃烧,蓝色火焰,无水珠,产生气体能使澄清石灰水变浑浊除杂:通入浓硫酸(除水蒸气)收集:排水法尾气处理:点燃法/收集法(塑料袋)②草酸分解法:H2C2O4 CO↑+CO2↑+H2O ;混合气体通过碱石灰得到一氧化碳。

第三章有机化合物的制备实验实验十环己烯的制备一、实验目的1.学习环己醇在酸催化作用下分子内脱水制备环己烯的原理和方法。
2.了解分馏原理及其基本操作。
二、实验原理醇在脱水剂作用下分子内脱去一分子水而形成烯烃。
主反应:OH85%+H O342副反应:OH34+H O22O三、仪器与试剂仪器:图1.8分馏装置和图1.6普通蒸馏装置。
试剂:环己醇 10g(10.4mL,0.1mol),85% 磷酸 5mL,氯化钠 1g,无水氯化钙 1~2g,5%碳酸钠溶液 4mL 。
四、实验步骤在50mL 干燥的圆底烧瓶中,分别加入 10g 环己醇(10.4mL)(1),5mL85% 磷酸(2),充分摇荡使两种液体混合均匀。
投入几粒沸石,按图1.8安装好分馏装置。
用小锥形瓶作接收器,置于冷水浴中。
用小火慢慢加热混合物至沸腾,以较慢速度进行蒸馏,控制分馏柱顶部温度不超过73℃(3)。
当无液体蒸出时,可适当加大火源,继续蒸馏。
当温度达到 85℃时,停止加热,馏出液为环己烯和水的浑浊液。
在馏出液中分批加入约 1g 食盐,使之饱和。
再加入 3~4mL5% 的碳酸钠溶液,以中和其中的微量酸。
然后,将上述液体倒入分液漏斗中,振荡后静止分层。
分出下面的水层,将有机层转入干燥的小锥形瓶中,加入适量无水氯化钙将其干燥(4)。
将干燥后澄清透明的粗环己烯滤入 30mL 蒸馏瓶中,加入几粒沸石,加热蒸馏收集80℃~85℃馏分。
所用的蒸馏装置必须是干燥的。
产量:4~5g 。
纯环己烯为无色透明液体,沸点 83℃,n201.4465。
环己烯的红外光谱图见图3.1。
D本实验约需 4h 。
有 机 化 学 实 验图3.1 环己烯的红外光谱图五、注释(1)环己醇在常温下是粘稠液体,如果用量筒量取,约 12.4mL ,应注意转移过程中的损失。
也可用称量法称取。
(2)脱水剂用磷酸或硫酸均可。
磷酸的用量是硫酸用量的 2 倍。
但用磷酸的好处一是反应中不生成碳渣,二是反应中无刺激性气体生成。


![有机重要实验装置图(乙烯、乙炔、溴苯、硝基苯、石油分馏、乙酸乙酯的制备代[二次])](https://uimg.taocdn.com/bebedd3c5022aaea998f0feb.webp)
一、乙烯的制备(1酸(2)原理:C 2H 5CH 2=CH 2H 2O + 副反映:C 2H 52H 5OC 2H 5H 2O+ ,(3)注意:①反映进程中浓硫酸起催化剂和脱水剂的作用 ②浓硫酸和乙醇的体积比为3:1 ③温度计水银求插入混合液液面以下,但不要触及瓶底,控制温度170℃ ④避免暴沸,加入碎瓷片 ⑤由于温度控制不妥,可能产生CO 2,SO 2。
可通过氢氧化钠除杂,注意C 2H 4不能用浓硫酸干燥二、乙炔的制备:(1)原料:电石、水(2)原理:(3)注意:H2+ CaC2+CH CH Ca(OH)2①不能用启普发生器:a、反映放出大量的热易炸裂启普发生器b、反映生成氢氧化钙是糊状物,使反映无法控制c、生成的氢氧化钙糊状易堵塞反映器②为取得平稳的乙炔气流,用饱和食盐水代替水,同时用分液漏斗以控制水的流速③制取的乙炔里常混有H2S和PH3等杂质而产生难闻的气味,用硫酸铜溶液除杂三、溴苯的制备:(1液溴、铁粉(2)原理:+Br2Fe Br H Br+(3)注意:①能用溴水。
②反映进程中加入铁粉,起催化作用。
③苯的溴代反映较猛烈,液体微微沸腾,反映放出的热使苯和液溴气化,整个烧瓶内充满红棕色气体,利用长玻璃管起到:导气、冷凝、回流的作用 ④长玻璃管口应接近锥形瓶液面(水),而不能插入液面以下,不然会产生倒吸现象,会观察到液面上有白雾生成 ⑤反映完毕后反映完毕后把反映液倒入水中,可看到有褐色不容于水的液体在烧瓶底部生成,这是因为溶解了液溴的粗溴苯,把粗溴苯依次用水洗、氢氧化钠溶液洗、水洗、干燥、蒸馏的方式可取得无色密度大于水的溴苯。
四、硝基苯的制备:(1酸、浓硫酸(2)原理浓H 2SO 4++HNO 55℃----60℃NO 2H 2O(3)注意:①浓硫酸起催化剂和吸水剂的作用 ②配制浑酸时,现将浓硝酸注入容器中,再慢慢注入浓硫酸,同时不断搅拌 ③冷却到室温加入苯,水浴加热 ④制取的硝基苯通常呈黄色,因为容有了NO 2,将所得的粗硝基苯依次用水洗、氢氧化钠溶液洗、水洗、干燥、蒸馏的方式可取得有苦杏仁味、比水重的油状液体硝基苯五、乙酸乙酯的制备:(1醋酸、无水乙醇、浓硫酸(2)原理C H 3C OOH C 2H 5OH C H 3C OOC 2H 5H 2O 浓H 2SO 4++(3)注意:①此反映是可逆反映②浓硫酸的作用:催化剂(提高反映速度)、吸水剂(提高乙酸乙醇的转化率) ③加热的目的:提高反映速度,第二使生成的乙酸乙酯挥发而搜集,提高乙酸乙醇的转化率 ④用饱和碳酸钠溶液的目的:a 、降低乙酸乙酯在水中的溶解度,使其分层析出 b、除去挥发出的乙酸,生成乙酸钠,便于闻到乙酸乙酯的气味 c、溶解挥发出的乙醇⑤反映原理:酸脱羟基醇脱氢28.溴苯是一种化工原料,实验室合成溴苯的装置示用意及有关数据如下:按下列合成步骤回答问题:(1)在a中加入15 mL无水苯和少量铁屑。

高考化学实验有机物的制备
有机物的制备实验可以涉及很多不同种类的有机化合物,以下是一些常见的有机物制备实验:
1.苯甲酸的制备实验:将苯基甲酸钠与盐酸反应,再用醋酸酸化得到苯甲酸。
2.二苯甲酮的制备实验:将苯甲酸和乙酰氯反应,再用碱性溶液水解得到二苯甲酮。
3.苯胺的制备实验:将苯硝基与铁和盐酸反应得到苯胺。
4.甲苯的制备实验:将异丙苯和甲酸钠反应得到甲苯。
5.2-溴-2-甲基丙烷的制备实验:将2-氯-2-甲基丙烷与溴反应得到2-溴-2-甲基丙烷。
以上是一些有机物制备实验的举例,具体的实验步骤和操作细节可以根据不同有机物进行调整和改进。
高中六种有机物的实验室制备简图
六种有机物的实验室制备简图
一、乙烯的制备
1、工业制法:石油裂解
2、实验原理:
CH
3-CH
2
-OH + 浓H
2
SO
4
→ CH
2
=CH
2
↑+H
2
O
3、注意:
(1)温度计的水银球要插于反应物的位置;
(2)温度要控制在170℃之间(140℃时生成乙醚);(3)须加入碎瓷片或沸石(防暴沸);
(4)浓H
2SO
4
(起催化与脱水作用)与乙醇的体积比为3:1;
(5)用排水集气法收集乙烯(乙烯难溶于水);
(6)反应液会变黑,有刺激性气味产生的原因:由于有C、SO
2
的生成。
4、实验装置:
二、乙炔的制备
乙炔可用电石与水反应制得,因此俗称电石气。
1、原料:电石、水
2、实验原理:
CaC
2 + 2H
2
O → CH≡CH↑+ Ca(OH)
2
3、反应特点:反应剧烈,放出大量的热;产生糊状的Ca(OH)
2。
4、注意:
(1)用饱和食盐水代替水,可减小反应速率,得到平稳的乙炔气流(食盐和碳化钙不起反应);(2)若在大试管中制取,则应在管口放一团棉花,避免泡沫从导管中喷出;
(3)由电石制得的乙炔中往往含有H
2S、PH
3
等杂质,故须将混合气体通过盛有CuSO
4
溶液的洗气瓶或
通过NaOH溶液的洗气瓶;
(4)用排水法收集。
5、实验装置:
三、溴苯的制备
1、原料:苯、液溴(纯溴)、还原铁粉
2、实验原理:
3、注意:
(1)加药品次序:苯、液溴、铁粉;
(2)催化剂实为FeBr
3
;
(3)长导管作用:冷凝、回流;
(4)除杂:制得的溴苯常溶有溴而呈褐色,可用稀NaOH洗涤,然后分液得纯溴苯。
发生装置
4、实验装置:
四、硝基苯的制备
1、原料:苯、硝酸、浓硫酸
2、实验原理:
3、注意:
(1)需用浓硫酸与浓硝酸配置混合酸;
(2)逐滴加入苯
(3)在50-60℃下水浴加热(温度过高会生成二硝基苯);
(4)除去混合酸后,用蒸馏水与NaOH溶液洗涤,最后再用蒸馏水洗涤;(5)用无水CaCl
2
干燥、分离后得到纯产品。
4、实验装置:
五、银镜反应
1、原料:硝酸银溶液、氨水、乙醛
2、反应方程式:
AgOH + 2NH
3·H
2
O = [Ag(NH
3
)
2
]+ OH- + 2H
2
O
CH
3CHO + 2[Ag(NH
3
)
2
] + 2OH-→ CH
3
COO- + NH
4
+ + 2Ag↓ + 3NH
3
+ H
2
O
3、注意:
(1)银氨溶液的配制:AgNO
3
溶液中滴加氨水至沉淀恰好溶;
(2)热水浴加热时不可振荡试管;
(3)碱性环境,氨水不能过量(防止生成易爆物);
(4)银镜的处理:用硝酸溶解。
4、实验装置:
六、乙酸乙酯的制备
1、原料:无水乙醇、冰醋酸、浓硫酸、饱和碳酸
钠溶液
2、实验原理
3、注意:
(1)加入药品的次序:乙醇、浓硫酸、醋酸;
(2)导管的气体出口位置在饱和碳酸钠溶液液面上;
(3)加碎瓷片防止暴沸;
(4)饱和碳酸钠溶液可除去未反应的乙醇、乙酸,并降低乙酸乙酯的溶解度;
(5)装置中的长导管的作用是:导气兼冷凝回流,防止未反应的乙酸、乙醇因蒸发而损耗;
(6)导气管不宜伸入饱和Na
2CO
3
溶液可防止倒吸。
4、实验装置:。