金属凝固原理第2液态金属的结构和性质
- 格式:pptx
- 大小:1.85 MB
- 文档页数:80



液态金属的结构与性质液态金属是一种特殊的物质,其结构与性质具有独特的特点。
本文将对液态金属的结构与性质进行详细介绍。
首先,液态金属的结构与固态金属有一些相似之处,但也有一些不同之处。
固态金属由由排列紧密的原子晶格构成,而液态金属的原子结构则更加随意和无规则。
液态金属中的原子没有固定的位置,它们以无序方式排列,形成一个非晶态结构,没有明确的晶体面,没有长程有序。
液态金属的性质也有一些独特之处。
首先是液态金属的流动性。
由于其无规则的原子结构,液态金属的原子之间没有明确的位置限制,因此可以自由流动。
这使得液态金属可以被容器中的任何形状所包裹,也使得液态金属可以通过一些制作工艺来制成各种形状的物体。
其次,液态金属具有较高的密度。
液态金属由金属原子组成,金属原子通常比较重。
由于原子之间没有明确的位置限制,因此液态金属可以更紧密地排列,使得其密度相对较高。
液态金属还具有良好的导电性和导热性。
金属中的电子随着原子之间的距离较远,形成自由电子,这些自由电子可以在金属中自由移动,从而实现电流的传导。
液态金属中的自由电子同样可以在液态金属中自由移动,因此液态金属具有良好的导电性。
与此类似,液态金属中的原子之间的距离较近,原子之间的振动更为频繁,从而使得热量在液态金属中得以快速传播,使其具有良好的导热性。
此外,液态金属还具有较高的表面张力。
液态金属原子之间的相互作用力较强,特别是在液体表面,原子受到周围原子的吸引力较大,形成一个表面膜。
由于这个表面膜的存在,液态金属的表面张力较高,使得液态金属在任何其他物体表面上都能形成一个相对稳定的液体球形,这也是为什么液态金属滴在表面上会呈现出球形的原因。
液态金属还具有一些特殊的性质和应用。
首先是其较低的熔点。
与晶体金属相比,液态金属由于无序结构的特殊性质,使得其熔点相对较低。
这使得液态金属在一些特殊工艺中得以应用,例如3D打印中的金属打印。
另外,液态金属还具有极好的流动性和可塑性。



6
Structure and Properties
of Liquid Metals
二
在
在固态
第一章液态金属的结构与性质研究方法
液态金属电阻加大,因原子热振动振幅增大,结构无序性加大;
气、液、固相比较,液态金属结构更接近
衍射图
17液态金属的结构与性质图1-1 700℃液态铝中原子
密
度分布线固态金属:原子在
某一平衡位置热振
动,因此衍射结果
得到的原子密度分
布曲线是一组相距
第一章液态金属的结构与性质20
液态金属的结构与性质其第一峰值与固态时的衍射线(位数与固态时相当。
第二峰值虽仍较明显,但与固
时的峰值偏离增大,而且随
r 的增大,峰值与固态时的偏
也越来越大。
当它
定邻
近。




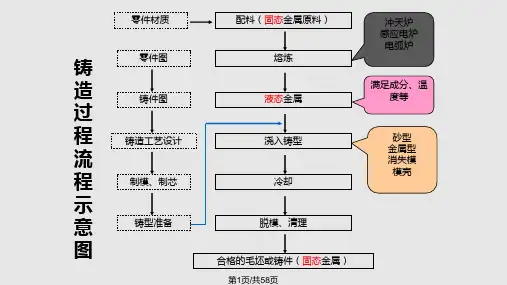
铸造:一种液态金属生产制品的工艺方法。
将金属熔化成具有一定化学成分和一定温度的液体,然后在重力或外力(压力、离心力、电磁力等)作用下将其浇注到铸型型腔中,充满型腔(良好流动性的液态)经凝固和冷却后便形成具有铸型型腔形状的制品—铸件特点:①使用范围广,可生产各种形状和大小的铸件②较高的尺寸精度③成本低廉。
一.液态金属的结构与性质1.固体金属的加热、熔化:⑴晶体中的原子结合:1)在一定条件下,金属中的原子具有一定排列的原因:①引力:异性电荷间的库仑引力;②斥力:同性电荷间的库仑斥力与泡利原理引起的斥力之和。
⑵原子间距离为R0时,F(R0)=0,平衡态,W极小值,状态稳定,原子之间保持一定间距F(R)=-əW(R)/əR ⑵金属的加热膨胀:晶体中的原子不是固定不动,只要温度高于热力学温度,原子在平衡位置附近热振动热膨胀:温度升高,振动频率、振幅加大,原子间距离增加原因:①原子间距增大:势能曲线不对称性;斥力>引力②空穴产生:熔点附近,1%空穴数;离子间相互作用——能垒——平衡位置振动;温度升高—部分原子能量>能垒—原子迁移到表面or原子间隙—留下空穴—vacancy产生;空穴形成—能垒下降—其它原子进入—空穴流动⑶金属的熔化:①熔点附近:离位原子多;熔化始于晶界,晶界原子排列相对不规则,势能高,离位原子多,空穴数目可达到原子总数10% ②熔点:外界能量足够大时——熔化潜热,原子间距离大于R1,原子结合键破坏,固态——液态;固态——液态状态突变;性质突变:体积突变;电阻、粘性突变②熔化实质:规则的原子排列突变为紊乱的非晶质结构的过程2.液态金属的结构:⑴液态金属的热物理性质:①体积:S-L:体积增加3~5%,原子平均间距增加1~1.5%;S-g:体积无限膨胀②熔化潜热:S-L(熔化潜热):原子结合键破坏百分之几;S-g(汽化潜热):原子间结合键全部破坏③熵:S-L:熵增加不大⑵液态与固态结构相似,尤在金属过热度不太高(熔点以上100~300℃)的铸造条件下更是如此⑶液体状态的结构特点(熔化-熔点以上不高的温度范围内):①原子间结合能较强、平均原子间距增加不大、原子排列在较小距离内具有规律性②原子间结合部分破坏,原子集团,近程有序(原子在十几~几百个原子组成的集团内规则排列) ③由于能量起伏,原子集团处于瞬息万变状态④原子集团内,公有电子,金属导电;空穴间,自由电子跟随正离子运动,离子导电;most金属熔化时电阻率能突然增加约1~2倍(半导体金属则减小)⑤温度高——原子集团平均尺寸小、“游动”速度快⑷金属液态结构的理论:①空穴理论:由原子集团(规则排列、近程有序)、空穴组成,能量起伏大、热运动激烈②紊乱排列的密集球堆理论(贝纳尔):液体金属是均质、密集、紊乱排列的原子集合体⑸实际金属的液态结构:1)微观上:①游动原子集团:成分和结构不同,近程有序②空穴③游离原子④许多固态、气态或液态的化合物组成,是一种“混浊”的液体2)化学键:金属键、其它多种类型的化学键⑹①能量起伏②结构起伏:液体中大量不停“游动”着的局域有序原子团簇时聚时散、此起彼伏③浓度起伏:同种元素及不同元素之间的原子间结合力存在差别,结合力较强的原子容易聚集在一起,把别的原于排挤到别处,表现为游动原子团簇之间存在着成分差异。