简单分类法及其应用一
- 格式:docx
- 大小:24.40 KB
- 文档页数:3






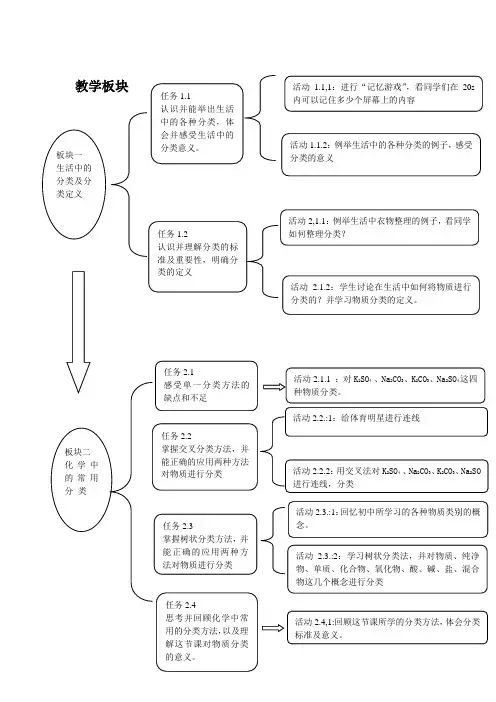
教学板块人板块一 生活中的分类及分类定义任务1.1认识并能举出生活中的各种分类,体会并感受生活中的分类意义。
任务1.2认识并理解分类的标准及重要性,明确分类的定义活动1.1,1:进行“记忆游戏”,看同学们在20s 内可以记住多少个屏幕上的内容活动1.1.2:例举生活中的各种分类的例子,感受分类的意义活动2,1.1:例举生活中衣物整理的例子,看同学如何整理分类?活动 2.1.2:学生讨论在生活中如何将物质进行分类的?并学习物质分类的定义。
板块二 化学中的常用分 类 任务2.1感受单一分类方法的缺点和不足任务2.2掌握交叉分类方法,并能正确的应用两种方法对物质进行分类任务2.4思考并回顾化学中常用的分类方法,以及理解这节课对物质分类活动2.1.1 :对K 2SO 4 、Na 2CO 3、K 2CO 3、Na 2SO 4这四种物质分类。
活动2.2.:1:给体育明星进行连线活动2.2.2:用交叉法对K 2SO 4 、Na 2CO 3、K 2CO 3、Na 2SO 进行连线,分类活动2.4,1:回顾这节课所学的分类方法,体会分类标准及意义。
任务2.3掌握树状分类方法,并能正确的应用两种方法对物质进行分类活动2.3.:1:回忆初中所学习的各种物质类别的概念。
活动 2.3.:2:学习树状分类法,并对物质、纯净物、单质、化合物、氧化物、酸、碱、盐、混合物这几个概念进行分类物质的分类(课时一)§2.1物质的分类——简单分类法及其应用教学设计课题简单分类法及其应用课型新知识课授课人授课班级教材分析本节教学内容位于新课标人教版高中化学必修1第二章《化学物质及其变化》第一节《物质的分类》。
课标在本节的要求是“能根据物质的组成和性质对物质进行分类,并尝试用不同的方法对物质进行分类”。
简单分类法是新课程背景下化学教学教材所增添的“新”内容之一。
在初高中的学习中,贯穿中学化学的学习,对中学化学的教学起到了“承前启后”的作用。

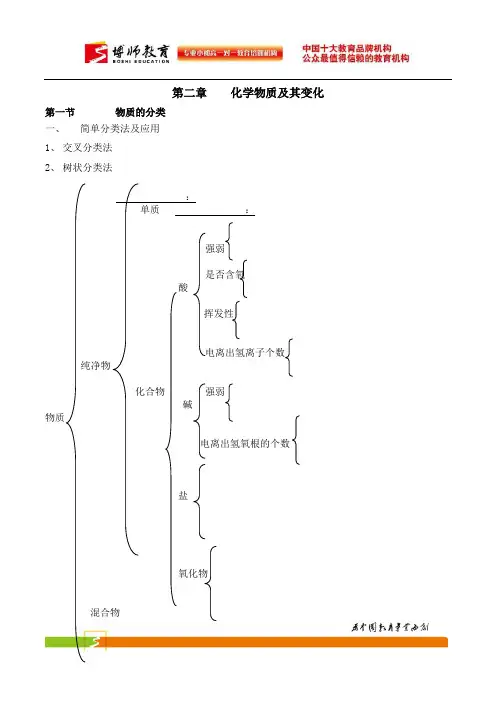
第二章化学物质及其变化第一节物质的分类一、简单分类法及应用1、交叉分类法2、树状分类法:单质:强弱是否含氧酸挥发性电离出氢离子个数纯净物化合物强弱碱物质电离出氢氧根的个数盐氧化物混合物二、分散系及其分类1. 分散系(1)定义:一种物质(或几种物质)以粒子形式分散到另一种物质里所形成的混合物,统称为分散系。
(2)分散质:分散系中分散成粒子的物质。
分散剂:分散质分散在其中的物质。
(3)分散系的分类:当分散剂是水或其他液体时,如果按照分散质粒子的大小来分类,可以把分散系分为:溶液、胶体和浊液。
分散质粒子直径小于1nm的分散系叫溶液,在1nm-100nm 之间的分散系称为胶体,而分散质粒子直径大于100nm的分散系叫做浊液。
2、胶体(1)胶体的定义:分散质粒子直径大小在10-9~10-7m之间的分散系。
(2)胶体的分类:a 根据分散质微粒组成的状况分类:粒子胶体分子胶体。
b 根据分散剂的状态划分:气溶胶液溶胶固溶胶。
(3)胶体的制备:实验:注意:abc原理:(4)胶体的性质:a 丁达尔效应——粒子对光散射作用的结果,是一种物理现象。
鉴别胶体和其他分散系。
b布朗运动——无规则的运动,称为布朗运动。
c电泳——在外加电场的作用下,胶体的微粒在分散剂里向阴极(或阳极)作定向移动的现象。
△常见胶体的胶粒所带电性带正电的胶粒胶体:金属氢氧化物、金属氧化物。
带负电的胶粒胶体:非金属氧化物、金属硫化物As2S3胶体、硅酸胶体、土壤胶体特殊:AgI胶粒随着AgNO3和KI相对量不同,而可带正电或负电。
不带电:蛋白质溶液、淀粉溶液d聚沉——胶体分散系中,分散系微粒相互聚集而下沉的现象称为胶体的聚沉。
△胶体凝聚的方法:(1)加入电解质:电解质电离出的阴、阳离子与胶粒所带的电荷发生电性中和,使胶粒间的排斥力下降,胶粒相互结合,导致颗粒直径>10-7m,从而沉降。
(2)加入带异性电荷胶粒的胶体:(3)加热、光照或射线等:加热可加快胶粒运动速率,增大胶粒之间的碰撞机会。

第二章 化学物质及其变化第一节 物质的分类第 1 课时 简单分类法及其应用一、常见的分类法1.分类及其意义 把大量的事物按照事先设定的__________进行分类,是人们最熟悉,也是最方便的一种工作方法。
这样, 当分类标准确定之后,__________中的事物在某些方面的相似性可以帮助我们做到举一反三;对__________ 事物的了解使我们有可能做到由此及彼。
2.常见分类法含义 根据________的分类标准,对同一事物进行多种分类的一种分类方法交叉 分类法 举例 Na2CO3_____盐(根据阳离子) _____盐(根据阴离子)_____盐(根据溶解性)含义 对________事物按照某种属性进行________的分类法树状 分类法 举例 物质纯净物 _______单质 _______二、分类法的应用分类可以帮助我们更好地认识物质的性质,找出各类物质之间的关系。
如:Ca ① CaO ② Ca(OH)2 ③ CaCO3C ④ CO2 ⑤ H2CO3 ⑥ CaCO3化学方程式分别为: ①___________________________________; ②___________________________________; ③___________________________________; ④___________________________________; ⑤___________________________________;⑥___________________________________。
【答案】一、1.标准 同类 不同类 2.不同 钠 碳酸 易溶 同类 再分类 化合物 混合物 二、①2Ca+O2 2CaO②CaO+ H2O Ca(OH)2③Ca(OH)2+CO2 CaCO3 ↓ +H2O点燃④C+O2CO2⑤CO2 + H2OH2CO3⑥Ca(OH)2 + H2CO3 CaCO3 ↓ +2H2O一、根据纯净物的组成与性质对其进行分类【总结归纳】二、单质、酸、碱、盐、氧化物之间的转化关系有关化学方程式举例: ①Mg+Cl2 MgCl2 ②Fe+CuSO4 FeSO4+Cu ③Zn+H2SO4 ZnSO4+H2↑ ④CaO+SiO2 CaSiO3 ⑤CO2+Ca(OH)2 CaCO3↓+H2O ⑥CuO+H2SO4 CuSO4+H2O ⑦NaOH+HCl NaCl+H2O⑧3NaOH+FeCl3 Fe(OH)3↓+3NaCl⑨AgNO3+HCl AgCl↓+HNO3⑩Na2SO4+BaCl2 BaSO4↓+2NaCl典例 1 (浙江省温州市十五校联合体 2017−2018 学年高一下学期期中联考)下列物质属于碱性氧化物的是A.Na2OB.SO2C.KOHD.H2SO4【答案】A 【解析】碱性氧化物是指溶于水而成碱或与酸反应而成盐的氧化物。
第一节物质的分类第1课时简单分类法及其应用学习目标:1.学会从多角度,依据不同标准对物质进行分类;了解“交叉分类法”和“树状分类法”,感受分类是学习和研究化学物质及其变化的一种重要科学方法。
2.掌握用不同的方法对化学物质及其化学反应进行分类。
3.初步了解分散系的概念和分类。
学习重点:学会根据物质的组成和性质对物质进行分类,初步了解分散系的概念。
学习难点:分类法的应用及常见化学物质及其化学反应的分类方法。
教学过程:一、导入新课[引入]我们知道分类如果从不同角度入手就会有很多不同方法,例如,人类按照年龄分可以分为老年、中年、青年、少年、儿童;按性别分分为男性和女性;按职业分为教师、医生、工程师等等。
同样的道理,化学物质从不同角度有很多不同的分类方法。
[板书]第二章化学物质及变化第一节物质的分类(一)二、推进新课教学环节一:简单分类法及其应用[板书]一、简单分类法及其应用[思考与交流]请尝试对HCl、SO2、CaO、KOH、Na2SO4、H2SO3进行分类。
(氧化物:SO2、CaO 酸:HCl、H2SO3碱:KOH 盐:Na2SO4 )(固体:CaO、KOH、Na2SO4 气体:HCl、SO2液体:H2SO3 )[讲解]在分类的标准确定之后,同类中的事物在某些方面的相似性可以帮助我们做到举一反三;对于不同事物的了解使我们有可能做到由此及彼。
所以,分类法是一种行之有效、简单易行的科学方法。
运用分类的方法不仅能使有关化学物质及其变化的知识系统化,还可以通过分门别类的研究,发现物质及其变化的规律。
[提问]对于Na2CO3,如果从其阳离子来看,它属于什么盐?从阴离子来看,又属于什么盐?( 从阳离子来看,属于钠盐,从阴离子来看,属于碳酸盐。
)[讲解]由于一种分类方法所依据的标准有一定局限,所能提供的信息较少,因此,人们在认识事物的时候往往采取多种分类方法,比如交叉分类法,就像我们刚才举的Na2CO3的例子。
[板书]1.交叉分类法Na2CO3钠盐Na2SO4钾盐K2SO4硫酸盐K2CO3碳酸盐[讲解](1)将事物进行分类时,按照不同的分类标准进行分类会产生不同的分类结果。
第二章化学物质及其变化第一节物质的分类学习目标1、了解物质分类的方法和依据,认识分类方法的应用。
2、了解分散系的含义及分类,知道胶体是一种常见的分散系。
3、了解胶体的特性及其应用。
4、感受分类方法对化学学科研究和化学学习的重要应用。
知识点一简单分类法及其应用一、纯净物的分类1、交叉分类法(1)含义:根据不同的分类标准,对同一事物进行多种分类的一种分类方法。
(2)举例Ⅰ、碳酸钠的交叉分类:2、树状分类法(1)含义:对同类事物按照某些属性进行再分类的分类方法,即对同类事物进行再分类。
(2)举例规律总结:1、纯净物的一般分类2、两种分类方法的特点与区别例题1、分类法是一种行之有效,简单易行的科学方法,人们在认识事物时可以采取多种分类方法,下列关于“Na2CO3”的分类不正确的是( B)A、化合物B、氧化物C、碳酸盐D、钠盐例题2、根据某种共性,可将CO2、SO2归为一类氧化物。
下列物质也属于同类氧化物的是( B)A.CaCO3B.SO3C.CuO D.KMnO4例题3、按照物质的树状分类法和交叉分类法,HNO3应属于( D)①酸②氢化物③氧化物④含氧酸⑤难挥发性酸⑥一元酸⑦化合物⑧混合物A.①②③④⑤⑥⑦B.①④⑤⑥C.①⑧D.①④⑥⑦例题4、从对化合物的分类方法出发,指出下列各组物质中与其他类型不同的一种物质是(1)Na2O CaO SO2 CuO ______ SO2___________(2)NaCl KCl NaClO3CaCl2 _____ NaClO3_________(3)HClO3KClO3HCl NaClO3 _____ HCl _________(4)NaHCO3Ca(HCO3)2NH4HCO3K2CO3 ____ K2CO3______例题5、利用交叉分类法,请你说出Na2SO4可能属于的类型名称是____硫酸盐、钠盐________。
例题6、请尝试对你所学过的化学物质和化学反应进行分类,并与同学交流。