人教版高中化学选修四酸碱中和滴定——专题训练
- 格式:doc
- 大小:90.50 KB
- 文档页数:7

(人教版选修4)3.2.3《酸碱中和滴定》课时训练试题(时间:40分钟满分:100分)一、单项选择题:本题包括12小题,每小题5分,共60分。
1.准确移取20.00 mL某待测HCl溶液于锥形瓶中,用0.100 0 mol·L-1NaOH溶液滴定。
下列说法正确的是()A.滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定B.随着NaOH溶液滴入,锥形瓶中溶液pH由小变大C.用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定D.滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏小【答案】 B【解析】A项,滴定管用蒸馏水洗涤后,还要用待装NaOH溶液润洗,否则将要引起误差,错误;B项,在用NaOH溶液滴定盐酸的过程中,锥形瓶内溶液由酸性逐渐变为中性,溶液的pH由小变大,正确;C项,用酚酞作指示剂,锥形瓶中溶液应由无色变为浅红色,且半分钟内不恢复原色时才能停止滴定,错误;D项,滴定达终点时,发现滴定管尖嘴部分有悬滴,则碱液的体积偏大,测定结果偏大,错误。
2.下列某种仪器中盛有一定量KMnO4溶液,甲同学平视读数为n mL,乙同学仰视读数为x mL,丙同学俯视读数为y mL,若x>n>y,则该仪器是()A.量筒B.酸式滴定管C.容量瓶D.碱式滴定管【答案】 B【解析】量取KMnO4溶液,应该用量筒或酸式滴定管,不能用碱式滴定管,因其有强氧化性。
根据读数,应为酸式滴定管,因其零刻度在上。
3.在一支25 mL的酸式滴定管中盛入0.1 mol·L-1的盐酸,其液面的最低点恰好在5 mL 的刻度处,若把滴定管中的溶液全部放入锥形瓶中,然后用0.1 mol·L-1的NaOH进行中和滴定,消耗NaOH溶液的体积为()A.等于20 mL B.小于20 mLC.大于20 mL D.等于5 mL【答案】 C【解析】酸碱式滴定管中刻度线下有一部分容积没有算在体积内,所以V(HCl)>20 mL,则中和酸消耗的NaOH溶液的体积应大于20 mL。

高中化学学习材料唐玲出品一、选择题(本题包括7小题,每小题3分,共21分)1.在25 mL的碱式滴定管中盛有溶液,液面恰好在20 mL刻度处,现将滴定管内溶液全部放出,流入量筒内,所得溶液的体积为( )A.5 mL B.20 mLC.大于5 mL D.小于5 mL解析:滴定管“0”刻度在上方,滴定管25 mL的刻度在下面,刻度线以下仍有一部分体积,所以流出液体体积大于5 mL。
答案:C2.下列有关叙述中正确的是( )A.滴定管下端连有橡皮管的为酸式滴定管B.在滴定时,左手操作锥形瓶,右手操作滴定管开关C.滴定前应首先排除尖嘴部分的气泡D.滴定过程中两眼应注视滴定管内液面的变化解析:A是碱式滴定管,B右手操作锥形瓶,D两眼观察锥形瓶内颜色变化。
答案:C3.常温下,用0.1 mol·L-1的HCl溶液滴定a mL NaOH稀溶液。
反应恰好完全时,消耗HCl溶液b mL。
此时溶液中c(OH-)是( )A.1×10-7 mol·L-1B.0 mol·L-1C.无法计算 D.0.1bamol·L-1解析:由于此题是酸碱中和滴定,且是一元强酸与一元强碱的中和,当恰好完全反应时,溶液的pH为7,溶液呈中性,常温下c(OH-)=1×10-7mol·L-1。
答案:A4.[双选题]某同学在实验报告中有以下实验数据,其中数据合理的是( )A.用托盘天平称取11.7 g食盐B.用量筒量取5.26 mL盐酸C.用广泛pH试纸测得溶液的pH是3.5D.用标准NaOH溶液滴定未知浓度的盐酸用去23.10 mL溶液解析:托盘天平的精确度为0.1 g;量筒应保留小数点后一位有效数字;滴定管的精确度为0.01 mL;而广泛pH试纸只能粗略测知溶液的pH范围,不能精确测量溶液的pH,记录为整数。
答案:AD5.(2012·皖南八校联考)如图为室温下,用一定物质的量浓度的NaOH溶液滴定20 mL 一定物质的量浓度的盐酸的图示,据图推出盐酸和NaOH溶液的物质的量浓度(mol·L-1)分别是( )A B C Dc(HCl)/(mol·L-1) 0.06 0.04 0.03 0.09c(NaOH)/(mol·L-1) 0.04 0.06 0.09 0.03解析:根据加入20 mL NaOH溶液时,溶液pH=2,推知20 mL×c(HCl)-20 mL×c(NaOH)20 mL+20 mL=10-2 mol/L①;根据加入30 mL NaOH溶液时,溶液pH=7,推知20 mL×c(HCl)=30 mL×c(NaOH)②;解①②组成的方程组得c(HCl)=0.06 mol/L,c(NaOH)=0.04mol/L。

高中化学学习资料金戈铁骑整理制作专题七酸碱中和滴定考纲解读:1、掌握酸碱中和滴定的仪器2、掌握酸碱中和滴定的原理3、认识酸碱中和滴定的操作知识精讲:1、中和滴定的原理:2、酸碱中和滴定的仪器:3、酸碱中和滴定的操作4、酸碱中和滴定的数据办理典型例题:例 1:填空( 1)图 1 表示 10mL 量筒中液面的地址, A 与 B,B 与 C 刻度间相差1mL,若是刻度 A 为 4,量简中液体的体积是____mL 。
( 2)图 II 表示 50mL 滴定管中液面的地址,若是液面处的读数是 a ,则滴定管中液体的体积(填代号)______________。
A.是amLB. 是( 50-a)mLC.必然大于amL D .必然大于( 50-a)mL例 2:常温下酸和碱恰好完好中和时,溶液的pH 是()A 、等于 7B、大于 7C、小于 7D、无法确定例 3、用标准氢氧化钠溶液中和醋酸溶液,当溶液的pH 值等于 7,则此时( )A. 醋酸和氢氧化钠物质的量相等B.醋酸和氢氧化钠恰好中和C.氢氧化钠过分D.醋酸有节余增强训练:1、有一支50 毫升的酸式滴定管,其中盛有溶液,液面恰幸好10 毫升刻度处,现把管内液体全部流下排出,用量筒接收,获取溶液的体积是()A. 不能够确定B.为 40 毫升C.为 10 毫升D.大于 40 毫升2、进行中和滴准时,早先不应当用所盛溶液冲洗的仪器是()A. 酸式滴定管B. 碱式滴定管C.锥形瓶D. 移液管3、在室温下进行中和滴定,酸和碱恰好完好反应时,以下说法必然正确的选项是( )A.. 参加反应的酸和碱的物质的量相等B.参加反应的酸中的氢离子总量和碱中氢氧根离子总量相等C.反应混杂液的 pH=7D. 能用合适的酸碱指示剂来判断4、已知 pH=3 的酸溶液和 pH=11 的碱溶液等体积混杂后的溶液呈酸性,则发生的反应是( )A. 强碱和弱酸溶液之间的反应B 强碱和强酸溶液之间的反应 C.较浓酸溶液和较稀碱溶液之间的反应 D.多元强酸和一元强碱之间的反应5、有甲、乙、丙三瓶等体积等物质的量浓度的NaOH 溶液,若将甲蒸发掉一半水,在乙中通入少量CO 2 ,丙不变,尔后用同浓度的 H 2SO 4 溶液滴定至完好反应后,所需溶液的体积()A. 甲=丙>乙B.丙>乙 > 甲C. 乙 >丙>甲D. 甲=丙=乙6、.以下是几种酸碱指示剂变色的pH 范围:①甲基橙②甲基红 4.4~6.2 ③酚酞 8.2~10,- 1)现用·LNaOH 溶液滴定浓度周边的甲酸时,上述指示剂(A .都能够用B .只能用③C .能够用①或②D .能够用②或③7、 .正确量取 25.00ml KMnO 4 溶液,可采纳的仪器是()A. 25ml 量筒B . 25ml 酸式滴定管 C. 25ml 碱式滴定管 D. 有刻度的 50ml 烧杯8、用溶液滴定盐酸,如达到滴定的终点时不慎多加了1 滴 NaOH 溶液( 1 滴溶液的体积约为 0.05mL ),连续加水到50mL ,所得溶液的 pH 是()A .4B .C . 10D .9、以下实验能达到测量要求的是( )A. 用托盘天平称取35.20g NaClB. 用 10ml 量筒量取 8.50ml 盐酸C. 用 25ml 滴定管量取15.80ml 溶液D. 用 PH 试纸测得溶液pH 值为10、某学生欲用已知物质的量浓度的盐酸来滴定测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂。

第三章水溶液中的离子平衡第二节水的电离和溶液的酸碱性第2课时酸碱中和滴定1.准确量取25.00 mL的KMnO4溶液,可选用的仪器为() A.500 mL量筒B.10 mL移液管C.50 mL酸式滴定管D.50 mL碱式滴定管解析:准确量取25.00 mL溶液应用滴定管或移液管,因KMnO4能腐蚀碱式滴定管的橡胶管,故应用50 mL酸式滴定管。
答案:C2.下列某种仪器中盛有一定量的高锰酸钾溶液,甲同学平视读数为n mL,乙同学仰视读数为x mL,丙同学俯视读数为y mL。
若x>n>y,则该仪器是()A.酸式滴定管B.量筒C.容量瓶D.碱式滴定管解析:仰视读数时数值偏大,俯视读数时数值偏小,即小刻度在上,大刻度在下,因此该仪器是滴定管。
又因为盛放的高锰酸钾溶液具有氧化性,故应是酸式滴定管。
答案:A3.下列有关滴定操作的顺序正确的是()①检查滴定管是否漏水②用蒸馏水洗涤玻璃仪器③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管④装标准溶液和待测液并调整液面(记录初读数)⑤取一定体积的待测液于锥形瓶中⑥滴定操作A.①③②④⑤⑥B.①②③④⑤⑥C.②③①④⑤⑥D.④⑤①②③⑥解析:中和滴定按照检漏、洗涤、润洗、装液、取待测液、滴定等顺序操作,则操作顺序为:①②③④⑤⑥。
答案:B4.用标准盐酸溶液滴定待测浓度的碱溶液时,下列操作中会引起碱溶液浓度的测定值偏大的是()A.锥形瓶中的溶液在滴定过程中溅出B.滴定管装液后尖嘴部位有气泡,滴定后气泡消失C.指示剂变色15 s后又恢复为原来的颜色便停止滴定D.锥形瓶用蒸馏水冲洗后未用待测液润洗解析:根据c(B)=c(A)·V(A)V(B)判断,A项中,V(B)的实际量减少,导致V(A)减少,测定值偏小;B项使液体充满气泡,导致V(A)增大,测定值偏大;C项未到滴定终点,偏小;D项,不影响测定结果。
答案:B5.向盛有10 mL NaOH稀溶液的烧杯中逐滴滴加稀盐酸,并边加边振荡,下列图象中能体现溶液pH变化情况的是()解析:滴加盐酸之前,稀NaOH溶液pH>7,则A和B不正确。

第二节水的电离和溶液的酸碱性第3课时pH的应用酸碱中和滴定1.某同学在实验报告中记录了下列数据,其中正确的是()A.用25 mL量筒量取12.36 mL盐酸B.用pH试纸测出某溶液pH为3.5C.用托盘天平称取8.75 g食盐D.用酸式滴定管测出消耗盐酸的体积为15.60 mL2.下面是中学化学实验室中几种常见的玻璃仪器,在仪器上标明具体使用温度的是()A.圆底烧瓶B.滴定管C.烧杯D.锥形瓶3.用已知物质的量浓度的盐酸滴定未知物质的量浓度的NaOH溶液时,下列操作中不正确的是()A.酸式滴定管用蒸馏水洗净后,直接加入已知物质的量浓度的盐酸B.锥形瓶用蒸馏水洗净后,直接加入一定体积的未知物质的量浓度的NaOH溶液C.滴定时,应左手控制活塞,右手摇动锥形瓶,眼睛时刻注视着锥形瓶内颜色的变化D.读数时,视线与滴定管内液体的凹液面最低处保持水平4.一支规格为a mL的滴定管,其尖嘴部分充满溶液,管内液面在m mL处,当液面降到n mL处时,下列判断正确的是()A.流出溶液的体积为(m-n)mLB.流出溶液的体积为(n-m)mLC.管内溶液体积等于(a-n)mLD.管内溶液体积多于n mL5.用标准的KOH溶液滴定未知浓度的盐酸,若测定结果偏低,其原因可能是()A.配制标准溶液的固体KOH中混有NaOH杂质B.滴定终点读数时,仰视滴定管的刻度,其他操作正确C.盛装待测液的锥形瓶用蒸馏水洗过后再用待测液润洗D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液6.在中和滴定操作过程中,用标准液滴定待测液,有以下各项因操作不当而引起的实验误差,用“偏高”“偏低”或“无影响”等填空:(1)滴定管用蒸馏水洗净后,未用已知浓度的标准溶液润洗,使滴定结果_________________。
(2)锥形瓶用蒸馏水洗净后,又用待测溶液润洗,使滴定结果_________________。
(3)滴定管在滴定前尖嘴处有气泡,滴定过程中气泡消失,使滴定结果_________________。
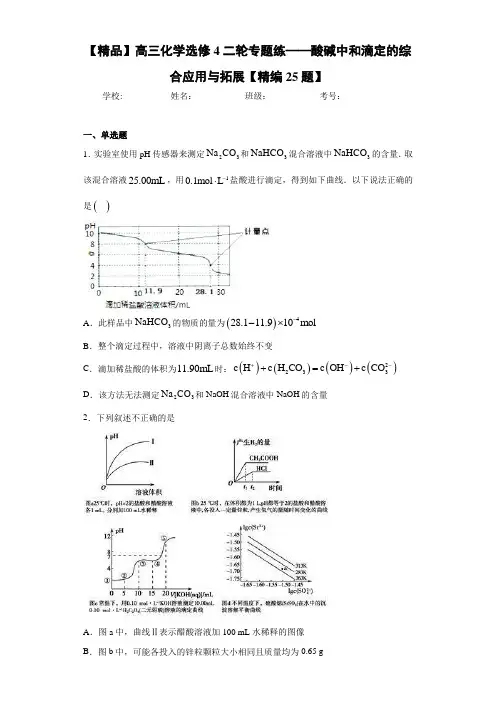
【精品】高三化学选修4二轮专题练——酸碱中和滴定的综合应用与拓展【精编25题】学校:___________姓名:___________班级:___________考号:___________一、单选题1.实验室使用pH 传感器来测定23Na CO 和3NaHCO 混合溶液中3NaHCO 的含量.取该混合溶液25.00mL ,用10.1mol L -⋅盐酸进行滴定,得到如下曲线.以下说法正确的是()A .此样品中3NaHCO 的物质的量为()428.111.910mol --⨯B .整个滴定过程中,溶液中阴离子总数始终不变C .滴加稀盐酸的体积为11.90mL 时:()()()()2233c Hc H CO c OH c CO +--+=+D .该方法无法测定23Na CO 和NaOH 混合溶液中NaOH 的含量 2.下列叙述不正确的是A .图a 中,曲线Ⅱ表示醋酸溶液加100 mL 水稀释的图像B .图b 中,可能各投入的锌粒颗粒大小相同且质量均为0.65 gC .图c 中,在①、②、③、④、⑤各点的溶液中所含阴离子种类不同D .图d 中,三个不同温度中,313 K 时K sp (SrSO 4)最大;且283 K 时,图中a 点对应的溶液是不饱和溶液3.取5.0 mL 18 1mol L -⋅硫酸配制100 mL 0.9 1mol L -⋅的硫酸溶液,并用23Na CO 准确标定稀硫酸浓度。
下列图示对应的操作不正确的是()A .量取B .转移C .定容D .标定4.下列有关实验操作、现象、解释或结论都正确的是()10.10mol L NaOH -⋅A .AB .BC .CD .D5.下列关于中和滴定的操作错误的是( ) A .滴定前需要检查滴定管是否漏水B .用对应加入的溶液润洗的仪器有:酸式滴定管、锥形瓶C .用标准盐酸测定氨水的浓度,最适宜使用的指示剂是甲基橙D .已知浓度的酸滴定未知碱液,终点读数时俯视滴定管的刻度,会造成计算值偏低 6.莫尔盐(]42422[(NH )Fe SO )8H O ⋅溶液经常用于定量滴定实验。

专题三酸碱中和滴定【例1】中和相同体积、相同pH的Ba(OH)2、NaOH和NH3·H2O三种稀溶液,所用相同浓度的盐酸的体积分别为V1、V2、V3,则三者的大小关系为( ) A.V3>V2>V1 B.V3=V2>V1 C.V3>V2=V1 D.V1=V2>V3【巩固练习1】用0.01mol/L H2SO4溶液滴定0.01mol/L NaOH的溶液,中和后加水到100mL。
若滴定时终点判断有误差:①多加了一滴H2SO4;②少加了一滴H2SO4。
(设1滴为0.05mL),则①和②溶液中c(H+)之比值是( ) A.1 B.10-4 C.104D.4×104【例2】取体积相同(0.025L)的两份0.10 mol/L NaOH溶液,把其中一份放在空气中一段时间后,溶液的pH (填“增大”、“减小”或“不变”),其原因是。
用已知浓度的盐酸溶液中和上述两份溶液,若中和第一份(在空气中放置一段时间)所消耗盐酸溶液的体积为V A,另一份消耗盐酸溶液的体积为V B,则:(已知甲基橙pH变色范围为3.1~ 4.4)(1) 以甲基橙为指示剂时,V A与V B的关系是;(2) 以酚酞为指示剂时,V A与V B的关系是。
【巩固练习2】已知c(NH4Cl)<0.1mol/L时,溶液pH>5.1,现在用0.1mol/LHCl滴定10mL0.05mol/L的氨水,用甲基橙作指示剂,达到终点时所用HCl的量应是()A.10 mL B.5 mL C.小于5 mL D.大于5 mL【巩固练习3】实验室为测定一新配制的盐酸的准确浓度,通常用纯净的无水Na2CO3配成标准溶液进行滴定。
具体操作是:称取W g纯净的Na2CO3装入锥形瓶中,加适量蒸馏水溶解,在酸式滴定管中加入待测盐酸滴定。
(1)锥形瓶中应加入几滴指示剂,由于CO2溶解在溶液中会影响pH,为准确滴定终点,宜选在pH为4~5之间,那么中学学过的指示剂宜选,当滴定至溶液由色变成色,即表示到达终点。

学业分层测评(十四) 酸碱中和滴定(建议用时:40分钟)[基础达标练]1.有一支50 mL的酸式滴定管,其中盛有溶液,液面恰好在10 mL刻线处,把管中的溶液全部排出盛接在量筒中,量筒内溶液体积是( )【导学号:80192196】A.大于40 mL B.小于40 mLC.等于40 mL D.10 mLA[因该滴定管50 mL刻度线以下还有液体,因此管中的溶液全部排出盛接在量筒中,量筒内溶液体积将大于50 mL-10 mL=40 mL。
]2.下列有关中和滴定的操作:①用标准液润洗滴定管;②向滴定管内注入标准溶液;③检查滴定管是否漏水;④滴定;⑤滴加指示剂于待测液;⑥洗涤。
正确的操作顺序是( )【导学号:80192197】A.③⑥①②⑤④B.⑤①②⑥④③C.⑤④③②①⑥D.③①②④⑤⑥A[有关中和滴定的实验操作,首先是检查滴定管是否漏水,然后是洗涤滴定管,再润洗,向滴定管中注入标准溶液,然后向待测溶液中滴加指示剂,最后滴定。
因此顺序是③⑥①②⑤④。
] 3.用标准的NaOH溶液滴定未知浓度的盐酸,若测定结果偏低,其原因可能是( )【导学号:80192198】A.盛装标准液的滴定管未用标准液润洗B.滴定终点读数时,仰视滴定管的刻度,其他操作正确C.盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗D.滴定前无气泡,滴定到终点时,发现尖嘴处有气泡D[A项,盛装标准液的滴定管未用标准液润洗,使碱的浓度偏小,则消耗碱液的体积偏大,导致测得酸的浓度偏高,不正确;B项,滴定终点读数时,仰视滴定管的刻度,造成V(碱)偏大,导致测得c(酸)偏高,不正确;C项,盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗,待测液的物质的量偏多,造成V(碱)偏大,导致测得c(酸)偏高,不正确;D项,滴定前无气泡,滴定到终点时,发现尖嘴处有气泡,造成V(碱)偏小,导致测得c(酸)偏低,正确。
]4.下列有关叙述正确的是( )【导学号:80192199】A.下端连有橡皮管的滴定管为酸式滴定管B.在进行滴定时,左手操作锥形瓶,右手操作滴定管C.滴定前应排除滴定管尖嘴部分的气泡D.滴定过程中两眼应注意滴定管内液面的变化C[A选项中所指滴定管是碱式滴定管;B选项中应右手操作锥形瓶,左手操作滴定管;D选项,滴定过程中两眼应观察锥形瓶内颜色变化。

专题08 酸碱中和滴定一、盐类水解实质及水解离子方程式的书写1.在盐类发生水解的过程中,正确的说法是( ) A .盐的电离平衡被破坏 B .水的电离程度逐渐增大 C .溶液的pH 发生了较大改变 D .水解后溶液一定呈酸性或碱性 【答案】B2.下列反应不属于水解反应或水解方程式不正确的是( ) ①HCl +H 2OH 3O ++Cl -②AlCl 3+3H 2O===Al(OH)3+3HCl ③Na 2CO 3+2H 2OH 2CO 3+2NaOH④碳酸氢钠溶液:HCO -3+H 2O CO 2-3+H 3O +⑤NH 4Cl 溶于D 2O 中:NH +4+D 2O NH 3·D 2O +H +⑥HS -的水解:HS -+H 2OS 2-+H 3O +⑦将饱和FeCl 3溶液滴入沸腾的水中:FeCl 3+3H 2OFe(OH)3(胶体)+3HCl A .①②③④ B .①②③ C .②③⑤⑥⑦ D .全部【答案】D【解析】①④⑥是电离方程式且①应用“===”;②是水解反应方程式,但应用“”;③的水解方程式错误,应分步进行;⑤应为NH +4+D 2ONH 3·HDO+D +;⑦应用“===”。
二、盐类水解的影响因素3.在一定条件下,Na 2S 溶液中存在水解平衡:S 2-+H 2O HS -+OH -。
下列说法正确的是( )A .稀释溶液,水解平衡常数增大B .通入H 2S ,HS -浓度减小C .升高温度,c HS -c S 2-增大D .加入NaOH 固体,溶液pH 减小【答案】C【解析】水解平衡常数只与温度有关,因此稀释溶液,水解平衡常数不变,A 项错误;通入H 2S ,HS -浓度增大,B 项错误;升高温度,水解平衡向右移动,溶液中c (HS -)增大、c (S 2-)减小,故c HS -c S 2-增大,C 项正确;加入NaOH 固体,溶液碱性增强,pH 增大,D 项错误。


第三章第二节第三课时中和滴定一、选择题1.下列有关滴定操作的顺序正确的是( )①用标准溶液润洗滴定管 ②往滴定管内注入标准溶液③检查滴定管是否漏水④滴定 ⑤洗涤A .⑤①②③④ B.③⑤①②④C.⑤②③①④D.②①③⑤④2.某冋学在实验报告中记录了下列数据,其中正确的是()A. 用25 mL 量筒量取12.36 mL 盐酸B. 用pH 试纸测出某溶液 pH 为3.5C. 用托盘天平称取 8.75 g 食盐D.用酸式滴定管测出消耗盐酸的体积为 15.60 mL3.(双选)下面是化学实验室中几种常见的玻璃仪器 ,在仪器上标明具体使用温度的是( )4.下列操作错误的是( )①取一锥形瓶,用待测NaOH 溶液润洗两次②在一锥形瓶中加入 25 mL 待测NaOH 溶液 ③加入几滴石蕊溶液作指示剂 ④取一支酸式滴定管,洗涤干净⑤直接往酸式滴定管中注入标准酸溶液,进行滴定 ⑥左手旋转滴定管的玻璃活塞 ,右手不停摇动锥形瓶 盐酸液面下降,直至滴定终点。
A.④⑥⑦B.①⑤⑥⑦C.③⑤⑦D.①③⑤⑦5.以下是几种酸碱指示剂变色的 p H 范围:①甲基橙3.1〜4.4 :②甲基红4.4〜6.2 ;③酚酞8.210,现用0.1000 mol •L — 1NaOH 溶液滴定浓度相近的乙酸时,上述指示剂 ( )A.都可以用 B .只能用③C.可以用①或②如下图所示,图中K 点代表的pH 为(A.容量瓶B.滴定管C.烧杯D.锥形瓶⑦两眼注视着滴定管内D.可以用②或③6.在 25 C 时,用 0.125 molL -1的标准盐酸滴定 25.00 mL 未知浓度的NaOH 溶液所得滴定曲线A.13B.12C.10D.11)30 00 VKlTClymL7. 如下图是常温下向20.0 mL的盐酸中,逐滴加入0.10 mol NaOH溶液时,溶液的pH随NaOH溶液的体积V(mL)变化的曲线,根据图像所得的下列结论中正确的是()A.原盐酸的浓度为0.10 mol •L-B.x 的值为2.0C. 当pH= 12 时,V值为20.4D. 原盐酸的浓度为1.0 mol/L8. 称取一定质量的NaOH来测定未知浓度的盐酸时(NaOH放在锥形瓶内,盐酸放在滴定管中)。
高中化学《酸碱中和滴定》专项训练一、选择题1、用标准盐酸滴定未知浓度的氨水,下列操作引起实验误差分析不正确的是()A. 用蒸馏水洗净碱式滴定管后,装入未知浓度的氨水,再移取10.00 mL氨水至锥形瓶,最终会使实验结果偏低。
B. 用蒸馏水洗净锥形瓶后,再用氨水润洗,后装入氨水,然后进行滴定,最终会使实验结果偏高。
C. 用酸式滴定管盛放盐酸溶液,滴定前开始调节液面时,仰视读数,最终会使实验结果偏低。
D. 用酚酞作指示剂滴至红色刚变无色后,要等半分钟,若溶液红色不褪去,表明达到滴定终点。
2、一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验。
某研究性学习小组在实验室中配制1 mol/L的稀硫酸标准溶液,然后用其滴定某未知浓度的NaOH溶液。
下列有关说法中正确的是()A.如果实验中需用60mL的稀硫酸标准溶液,配制时应选用100mL容量瓶B.容量瓶中含有少量蒸馏水,会导致所配标准溶液的浓度偏小C.酸式滴定管用蒸馏水洗涤后,即装入标准稀硫酸,则测得的NaOH溶液的浓度将偏小D.配制溶液时,定容时俯视读数,则导致实验结果偏大3、用标准盐酸滴定未知浓度的NaOH溶液时,下列操作对滴定结果无影响的是()A.用碱式滴定管量取10.00mLNaOH溶液放入只用蒸馏水洗净的锥形瓶中B.滴定前对酸式滴定管仰视读数C.用蒸馏水洗净酸式滴定管后,直接装入标准盐酸进行滴定D.滴定结束后,酸式滴定管尖嘴处悬挂一滴溶液4、用0.1000mol·L-1NaOH溶液滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是()A.盛装待测液的锥形瓶用蒸馏水洗过,没用待测液润洗B.酸式滴定管在使用前未用待测液盐酸润洗C.滴定前碱式滴定管尖嘴中有气泡,滴定后气泡消失D.滴定前读数平视,滴定终点读数时俯视碱式滴定管的刻度5、室温下,用0.10mol/L的盐酸分别滴定20.00mL浓度均为0.10mol/L氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积的变化关系如图所示。
高中化学第三章水溶液中的离子平衡2第2课时酸碱中和滴定练习(含解析)新人教版选修4一、选择题1.NaOH溶液滴定盐酸实验中,不必用到的是( )A.酚酞B.圆底烧瓶C.锥形瓶D.碱式滴定管解析:选B。
在酸碱中和滴定中要用滴定管滴加试剂,待测溶液或标准溶液要盛装在锥形瓶中,用指示剂酚酞来判断滴定终点。
因此不必使用的仪器是圆底烧瓶。
2.如图表示50.00 mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积是( )A.a mLB.(50.00-a) mLC.一定大于a mLD.一定大于(50.00-a) mL解析:选D。
滴定管的零刻度在上面,50.00 mL的刻度在下面,但刻度线以下仍有一部分容积,因此液体体积一定是大于(50.00-a) mL。
3.现用0.10 mol·L-1 HCl溶液滴定10 mL 0.05 mol·L-1 NaOH溶液,若酸式滴定管未润洗,达到终点时所用盐酸的体积应是( )A.10 mL B.5 mLC.大于5 mL D.小于5 mL解析:选C。
用0.10 mol·L-1HCl溶液滴定10 mL 0.05 mol·L-1NaOH溶液正好需要5 mL HCl 溶液。
酸式滴定管未润洗相当于盐酸被稀释,其浓度小于0.10 mol·L-1,中和NaOH所需体积大于5 mL。
4.(2019·益阳高二期末)用0.010 0 mol/L的KMnO4标准溶液滴定某未知浓度的H2C2O4溶液,下列说法错误的是( )A.该滴定实验不需要指示剂B.该实验用到的玻璃仪器有酸式滴定管、碱式滴定管、锥形瓶C.滴定管使用前需检验是否漏液D.若滴定终止时,仰视读数,所测H2C2O4浓度偏高解析:选B。
A.滴定终点,溶液由无色变为浅红色,不需要指示剂,故A正确;B.该实验用到的玻璃仪器有酸式滴定管、锥形瓶,用不到碱式滴定管,故B错误;C.滴定管使用前需检验是否漏液,故C正确;D.若滴定终止时,仰视读数,读取的标准溶液的体积偏大,所测H2C2O4浓度偏高,故D正确。
酸碱中和滴定【巩固练习】1.酸与碱完全中和时()。
A.酸与碱的物质的量一定相等B.酸所能提供的H+与碱所能提供的OH-的物质的量相等C.酸与碱的质量相等D.溶液呈中性2.现用0.1 mol·L-1 HCl滴定10 mL 0.05 mol·L-1 NaOH,若酸式滴定管未润洗,达到终点时所用盐酸的体积应是()。
A.10 mL B.5 mL C.大于5 mL D.小于5 mL3.在室温下等体积的酸和碱的溶液混合后pH一定小于7的是()A.pH=3的硝酸跟pH=11的氢氧化钠溶液B.pH=3的盐酸跟pH=11的氨水C.pH=3的硫酸跟pH=11的氢氧化钡溶液D.pH=3的醋酸与pH=11的氢氧化钠溶液4.室温下,下列溶液等体积混合后,所得溶液的pH一定大于7的是()A.0.1 mol·L―1的盐酸和0.1 mol·L―1的氢氧化钠溶液B.0.1 mol·L―1的盐酸和0.1 mol·L―1的氢氧化钡溶液C.pH=4的醋酸溶液和pH=10的氢氧化钠溶液D.pH=4的盐酸和pH=10的氨水5.右图中,曲线a和b是盐酸与氢氧化钠的相互滴定的滴定曲线,下列叙述正确的是()A.盐酸的物质的量浓度为1 mol/LB.P点时反应恰好完全,溶液呈中性C.曲线a是盐酸滴定氢氧化钠的滴定曲线D.酚酞不能用作本实验的指示剂6.将氢氧化钠稀溶液滴加到醋酸稀溶液中,如图示意混合溶液有关量或性质的变化趋势,其中错误的是()7.某研究小组为测定食用白醋中醋酸的含量进行如下操作,其中正确的是()A.用碱式滴定管量取一定体积的待测白醋放入锥形瓶中B.称取4.0 g NaOH固体放入1000 mL容量瓶中,然后加水至刻度,配成1.00 mol·L―1 NaOH标准溶液C.用NaOH溶液滴定白醋,使用酚酞作指示剂,溶液颜色恰好由无色变为浅红色,且半分钟内不褪色时,为滴定终点D.滴定时眼睛要注意着滴定管内NaOH溶液的液面变化,防止滴定过量8.对于常温下pH为1的硝酸溶液,下列叙述正确的是()A.该溶液1 mL稀释至100 mL后,pH等于3B.向该溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和C.该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为10―12D.该溶液中水电离出的c(H+)是pH为3的硝酸中水电离出的c(H+)的100倍9.已知常温、常压下,饱和CO2的水溶液的pH=3.9,则可推断用标准的盐酸溶液滴定NaHCO3水溶液时,适宜选用的指示剂及滴定终点时颜色变化的情况是()A、石蕊,由蓝变红B、甲基橙,由橙变黄C、酚酞,红色褪去D、甲基橙,由黄变橙二、填空题【高清课堂:酸碱中和滴定】1.(1)图Ⅰ表示10 mL量筒中液面的位置,A与B,B与C刻度间相差1 mL,如果刻度A为4,量筒中液体的体积为________mL。
专题2018——2019学年北京高二期末复习酸碱中和滴定的问题专题训练(尖子生培优)(人教版选修4)1、室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol·L-1的三种酸(HA、HB和HD)溶液,滴定曲线如图所示。
下列判断错误的是()A.三种酸的电离常数关系:K HA>K HB>K HDB.滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)C.pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)D.当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)2、在25℃时,用0.125mol·L-1的标准盐酸滴定25.00mL未知浓度的NaOH溶液所得滴定曲线如图所示。
图中K点代表的pH为()A.13B.12C.10D.113室温时,往20mL0.1mol·L-1的HM酸溶液中逐滴滴入0.1mol·L-1的ROH碱溶液,溶液的pH与所加ROH 溶液的体积关系如图所示。
下列说法正确的是()A.V(ROH)<20mL时,随着V(ROH)增大,HM的电离程度减小B.K(HM)=K(ROH)C.RM不能发生水解反应D.V(ROH)>20mL时,溶液中c(R+)<c(M-)4室温下,将0.10mol·L-1的盐酸滴入20.00mL0.10mol·L-1氨水中,溶液的pH和pOH随加入盐酸体积的变化曲线如图所示。
已知pOH=-lg c(OH-)。
下列说法正确的是()A.M点所示溶液中c(NH+4)+c(NH3·H2O)=c(Cl-)B.N点所示溶液中c(NH+4)>c(Cl-)C.Q点消耗盐酸的体积等于氨水的体积D.M点和N点所示溶液中水的电离程度相同5.常温下,向10mL0.1mol·L-1的HR溶液中逐滴滴入0.1mol·L-1的NH3·H2O溶液,所得溶液pH及导电性变化如图所示。
2021年高中化学 3.2.3酸碱中和滴定同步练习(含解析)新人教版选修4一、非标准1.酸碱恰好完全中和时( )A.酸与碱的物质的量一定相等B.溶液呈现中性C.酸与碱的物质的量浓度相等D.酸所能提供的H+与碱所能提供的OH-的物质的量相等解析:根据酸碱中和反应的实质可知酸碱恰好完全中和时,酸所能提供的H+与碱所能提供的OH-的物质的量相等。
答案:D2.下列有关滴定操作的顺序正确的是( )①用标准溶液润洗滴定管②往滴定管内注入标准溶液③检查滴定管是否漏水④滴定⑤洗涤A.⑤①②③④B.③⑤①②④C.⑤②③①④D.②①③⑤④答案:B3.实验室现有3种酸碱指示剂,其pH变色范围如下甲基橙:3.1~4.4石蕊:5.0~8.0酚酞:8.2~10.0用0.100 0 mol·L-1 NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述中正确的是( )A.溶液呈中性,可选用甲基橙或酚酞作指示剂B.溶液呈中性,只能选用石蕊作指示剂C.溶液呈碱性,可选用甲基橙或酚酞作指示剂D.溶液呈碱性,只能选用酚酞作指示剂解析:NaOH溶液和CH3COOH溶液恰好反应生成CH3COONa时,CH3COO-水解显碱性,而酚酞的变色范围为8.2~10.0,比较接近,因此答案为D。
答案:D4.某学生用碱式滴定管量取0.1 mol·L-1的NaOH溶液,开始时仰视液面读数为1.00 mL,取出部分溶液后,俯视液面,读数为11.00 mL,该同学在操作中实际取出的液体体积为( )A.大于10.00 mLB.小于10.00 mLC.等于10.00 mLD.等于11.00 mL解析:滴定管的“0”刻度在上,量取NaOH溶液,开始时仰视液面使读数偏大,取出部分溶液后,俯视液面使读数偏小,滴定前后刻度差为10.00 mL,但实际取出的液体体积偏大。
答案:A5.用NaOH滴定pH相同、体积相同的H2SO4、HCl、CH3COOH三种溶液,恰好中和时,所用相同浓度NaOH溶液的体积依次为V1、V2、V3,则这三者的关系是( )A.V1>V2>V3B.V1<V2<V3C.V1=V2>V3D.V1=V2<V3解析:pH相同、体积相同的H2SO4、HCl溶液中所含有氢离子的物质的量相等,恰好中和时,所用相同浓度NaOH溶液的体积相等。
第2节水的电离和溶液的酸碱性第3课时酸碱中和滴定1.下列实验误差分析错误的是()A.用湿润的pH试纸测稀碱液的pH,测定值偏小B.用容量瓶配置溶液,定容时俯视刻度线,所配溶液浓度偏小C.滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小D.测定中和反应反的应热时,将碱缓慢倒入酸中,所测温度值偏小2.下列仪器中使用前不需要检验是否漏水的是()A.滴定管B.分液漏斗C.过滤漏斗D.容量瓶3.用0.01 mol/L NaOH溶液完全中和pH=3的下列溶液各100 mL,需NaOH溶液体积最大的是()A.盐酸B.硫酸C.高氯酸D.醋酸4.以酚酞试液作指示剂,对某新制NaOH溶液进行中和滴定实验,数据记录如下表:则该新制的NaOH溶液的浓度c( mol·L-1)合理的是()A.c=0.01×(V1+V2+V3)/(3×20)B.c=0.01×(V1+V2)/(2×20)C.c=0.01×(V1+V3)/(2×20)D.c=0.01×V1/205.下列有关滴定操作的顺序正确的是()①用标准溶液润洗滴定管②往滴定管内注入标准溶液③检查滴定管是否漏水④滴定⑤洗涤A.⑤①②③④B.③⑤①②④C.⑤②③①④D.②①③⑤④6.实验室中有一未知浓度的稀盐酸,某学生测定盐酸的浓度在实验室中进行实验。
请完成下列填空:(1)配制100 mL 0.10 mol/LNaOH 标准溶液。
①主要操作步骤:计算→称量→溶解→(冷却后)→洗涤(并将洗涤液移入容量瓶)→__________→__________→________→将配制好的溶液倒入试剂瓶中,贴上标签。
②称量________g 氢氧化钠固体所需仪器有:天平(带砝码、镊子)、________、________。
(2)取20.00 mL 待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的NaOH 标准溶液进行滴定。
高中化学学习材料(精心收集**整理制作)酸碱中和滴定——专题训练例1.某学生做中和滴定实验的过程如下:(a)取一支碱式滴定管,(b)用蒸馏水洗净,(c)加入待测的NaOH溶液,(d)记录液面刻度读数,(e)用酸式滴定管精确放出一定量标准酸液,(f)置于未经标准酸液润洗的洁净锥形瓶中,(g)加入适量蒸馏水,(h)加入酚酞试液2滴,(i)滴定时,边滴边摇荡,(j)边注视滴定管内液面的变化,(k)当小心地滴到溶液由无色变成粉红色时,即停止滴定。
(l)记录液面刻度读数。
(m)根据滴定管的两次读数得出NaOH溶液体积为22 mL。
指出上述实验过程中的错误之处(用编号表示)。
例2. 用标准的NaOH溶液滴定未知浓度的盐酸,选用酚酞作为指示剂,造成测定结果偏高的原因可能是()A. 配制标准溶液的NaOH中混有Na2CO3杂质B. 滴定终点读数时,俯视滴定管的刻度,其他操作正确C. 盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗D. 滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液例3. 用NaOH滴定pH相同、体积相同的H2SO4、HCl、CH3COOH三种溶液,恰好中和时,所用相同浓度NaOH溶液的体积依次为V1、V2、V3,则这三者的关系是()(A)V1>V2>V3(B)V1<V2<V3(C)V1=V2>V3(D)V1=V2<V3 例4. 用0.01 mol/L H2SO4滴定0.01mol/L NaOH溶液,中和后加水至100ml,(设1滴为0.05ml)若滴定时终点判断有误差:①多加1滴H2SO4;②少加1滴H2SO4;则①和②[H+]的比值是()A. 10B. 50C. 5×103D. 104例5. 草酸晶体的组成可用H2C2O4·xH2O表示,为了测定x值,进行如下实验:称取Wg草酸晶体,配成100.00mL水溶液。
称25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amol·L-1的KMnO4溶液滴定到KMnO4不再褪色为止,所发生的反应: 2KMnO4+5H2C2O4+3H2SO4 = K2SO4+10CO2↑+2MnSO4+8H2O试回答:(1)实验中不需要的仪器有(填序号),还缺少的仪器有(填名称)_ 。
a.托盘天平(带砝码,镊子)b.滴定管c.100mL量筒d.100mL容量瓶e.烧杯f.漏斗g.锥形瓶h.玻璃棒球i.药匙j.烧瓶(2)实验中,标准液KMnO4溶液应装在________式滴定管中,因为________。
(3)若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,则所测得的x值会__________________________(偏大、偏小、无影响)(4)在滴定过程中若用amol·L-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为____________mol·L-1,由此可计算x的值是____________。
分析:该题涉及到氧化还原滴定,虽然基于反应原理与中和滴定不同,但实验原理及操作和所用仪器等类似。
由于该反应有明显的颜色变化,故可不用指示剂。
(1)c,f,j;还缺少铁架台(带滴定管夹),胶头滴管(定容时用)(2)用酸式滴定管,因KMnO4溶液有强氧化性,能腐蚀橡皮管。
(3)无影响。
因当初所取的待测液的物质的量一定。
(4) H2C2O4·xH2O ~ H2C2O4 ~ xH2O巩固练习:1. 在下列叙述仪器“0”刻度位置正确的是()A. 在量筒的上端B. 在滴定管上端C. 在托盘天平刻度尺的正中D. 在托盘天平刻度尺的右边2. 准确量取25.00ml KMnO4溶液,可选用的仪器是()A. 25ml量筒B. 25ml酸式滴定管C. 25ml碱式滴定管D. 有刻度的50ml烧杯3. 下列实验中,由于错误操作导致所测出的数据一定偏低的是()A. 用量筒量取一定体积液体时,俯视读出的读数B. 用标准盐酸滴定氢氧化钠溶液测碱液浓度时,酸式滴定管洗净后,没有用标准盐酸润洗,直接装标准盐酸滴定碱液,所测出的碱液的浓度值C. 测定硫酸铜晶体结晶水含量时,加热温度太高使一部分硫酸铜发生分解,所测出的结晶水的含量D. 做中和热测定时,在大小烧杯之间没有垫碎泡沫塑料(或纸条)所测出的中和热数值4. 酸碱中和反应属于放热反应,酸碱中和生成1mol水时所放出的热量称为中和热。
放下列浓度均为0.1mol/L的溶液混合时,相关说法中正确的是()A. 与NaOH反应时,HCL的中和热小于CH3COOH的中和热B. 与NaOH反应时,HCL的中和热大于CH3COOH的中和热C. 与NaOH反应时,H2SO4的中和热大于HCL的中和热D. 与H2SO4反应时,Ba(OH)2的中和热等于NaOH的中和热的2倍5. 下列关于等体积、等pH的NaOH和氨溶液的说法正确的是()A. 两种溶液中OH-的浓度相同B. 需要等浓度、等体积的盐酸中和C. 温度升高10℃,两溶液的pH仍相等D. 两种溶液中溶质的物质的量浓度相同6. 下列有关中和滴定的操作:①用标准液润洗滴定管;②往滴定管内注入标准溶液;③检查滴定管是否漏水;④滴定;⑤滴加指示剂于待测液;⑥洗涤。
正确的操作顺序是()A. ⑥③①②⑤④B. ⑤①②⑥④③C. ⑤④③②①⑥D. ③①②④⑤⑥7. 某学生用碱式滴定管量取0.1mol·L-1的NaOH溶液,开始时仰视液面读数为1.0mL,取出部分溶液后,俯视液面,读数为11.0mL,该同学在操作中实际取出的液体体积为()A. 大于10.0mLB. 小于10.0mLC. 等于10.0mLD. 等于11.0mL8. 已知次碘酸(HIO)既能和酸又能和碱发生中和反应。
它与盐酸发生反应将生成()A. HIB. IOClC. HClOD. ICl9. 有等体积、等pH的Ba(OH)2、NaOH和NH3·H2O三种碱溶液,滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为V1、V2、V3,则三者的大小关系正确的是A. V3>V2>V1B. V3=V2=V1C. V3>V2=V1D. V1=V2>V310. 用标准的盐酸滴定未知浓度的NaOH溶液时,下列各操作中,无误差的是()A. 用蒸馏水洗净酸式滴定管后,注入标准溶液盐酸进行滴定B. 用蒸馏水洗涤锥形瓶后,再用NaOH溶液润洗,而后装入一定体积的NaOH 溶液进行滴定C. 用碱式滴定管量取10.00mLNaOH溶液放入用蒸馏水洗涤后的锥形瓶中,再加入适量蒸馏水和2滴甲基橙试液后进行滴定D. 若改用移液管取待测液10.00mLNaOH溶液放入锥形瓶后,把留在移液管尖嘴处的液体吹入锥形瓶内,再加入1mL 甲基橙指示剂后进行滴定11. 用已知浓度的NaOH 溶液测定某H 2SO 4溶液的浓度,参考右图,从表中选出正确选项( )锥形瓶 中溶液 滴定管中溶液 选用 指示剂 选用 滴定管 A碱 酸 石蕊 (乙) B酸 碱 酚酞 (甲) C碱 酸 甲基橙 (甲) D酸 碱 酚酞 (乙)12. 用已知浓度的酸滴定未知浓度的碱时,会导致待测碱液的浓度偏低的操作是①酸式滴定管用蒸馏水洗后,未用标准液润洗②碱式滴定管用蒸馏水洗后,未用待测液润洗③配制碱液时,称量的固体吸潮④滴定前酸式滴定管尖嘴部分未充满溶液⑤滴定中不慎将锥形瓶内液体摇出少量于瓶外A. ①③④B. ②⑤C. ②③⑤D. ①③ 13. 某学生用0.1mol/L KOH 溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:(A )移取20.00mL 待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞(B )用标准溶液润洗滴定管2-3次(C )把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液(D )取标准KOH 溶液注入碱式滴定管至0刻度以上2-3cm(E )调节液面至0或0刻度以下,记下读数(F )把锥形瓶放在滴定管的下面,用标准KOH 溶液滴定至终点,记下滴定管液面的刻度完成以下填空:(1)正确操作的顺序是(用序号字母填写)______________________.(2)上述(B )操作的目的是___________________________________。
(3)上述(A )操作之前,如先用待测液润洗锥形瓶,则对测定结果的影响是(填偏大、偏小、不变,下同)_________________________。
(4)实验中用左手控制_________(填仪器及部位),眼睛注视_______,直至滴定终点。
判断到达终点的现象是___________。
(5)若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,则对测定结果的影响是___________________________________。
(6)滴定结束后如仰视观察滴定管中液面刻度,则对滴定结果的影响是______。
14. 某一种胃药片的制酸剂为碳酸钙,其中所含的制酸剂质量的测定如下:①需配制0.1mol/L的HCl的溶液和0.1mol/L的NaOH溶液②每次取一粒(药片质量均相同)0.2g的此胃药片,磨碎后加入20mL蒸馏水③以酚酞为指示剂,用0.1mol/L的NaOH溶液滴定,需用V x mL达滴定终点,④加入25mL0.1mol/L的HCl 溶液(1)写出全部实验过程的步骤 _____(写编号顺序)(2)下图所示的仪器中配制0.1mol/L的HCl溶液和0.1mol/L的NaOH溶液肯定不需要的仪器是(填序号),配制上述溶液还需用到的玻璃仪器是 ______(填仪器名称)(3)配制上述溶液应选用的容量瓶规格分别为(填字母)A. 50mL 50mLB. 100 mL 100 mLC. 100 mL 150 mLD. 250 mL 250 mL(4)写出相关的化学反应方程式:__________________________-(5)胃药中含碳酸钙的质量为 _____________g,(写出计算式并加以文字说明)15. 用滴定的方法来测定盐酸的浓度,实验数据如下所示:实验编号待测HCl溶液的体积/mL滴入Na2CO3溶液的体积/mL1 20.0 24.82 20.0 23.13 20.0 22.9(1)滴定中误差较大的是()次实验,造成这种误差的三个可能原因是:.(2)计算未知盐酸的浓度(数据精确到0.1)。
[参考答案]1. B2. B3. D4. B5. A6. A、B7. A8. D9. C10. C11. C、D 12. C13. (1)BDCEAF(2)防止将标准液稀释(3)偏大(4)滴定管活塞;锥形瓶中溶液的颜色变化;锥形瓶中溶液的颜色由无色变浅红且保持30秒内不褪色。