测定蛋白酶活力实验
- 格式:doc
- 大小:22.00 KB
- 文档页数:5

蛋白酶活力测定实验报告
实验目的:
通过测定蛋白酶的活力,了解其功能和活性。
实验原理:
蛋白酶是一类能够水解蛋白质的酶,可以将蛋白质分解为多肽和氨基酸。
蛋白酶活力是指单位时间内酶水解蛋白质的能力,通常以单位时间内水解的底物的量来表示。
本实验使用的方法是酶促反应测定法。
首先,将待测蛋白酶与底物混合,反应一定时间后,停止反应并添加淀粉溶液产生反应终止剂,最后用碘化钾溶液滴定反应产物。
实验步骤:
1. 预备试剂:制备蛋白酶和底物的工作液,制备淀粉溶液和反应终止剂,制备碘化钾溶液。
2. 实验装置:准备滴定装置和试管架。
3. 设置实验条件:保持温度恒定,控制pH值。
4. 实验操作:在试管中加入待测蛋白酶和底物工作液,反应一定时间后,加入淀粉溶液和反应终止剂,最后用碘化钾溶液滴定。
5. 记录数据:记录滴定所需碘化钾的体积,计算出酶活力。
实验结果:
根据实验数据,计算出蛋白酶的活力,通常以单位时间内水解的底物的量来表示。
实验讨论:
分析实验结果,比较不同条件下蛋白酶的活力差异,并讨论影响蛋白酶活力的因素。
实验结论:
通过分析实验结果,得出结论,总结蛋白酶活力与其他因素之间的关系,并提出可能的应用前景。
实验总结:
总结实验过程,评价实验结果及数据,提出改进意见,并对今后可能的研究方向进行展望。
参考文献:
列出所参考的文献。

蛋白酶活性的测定方法
蛋白酶活性的测定方法有多种,常见的方法包括:
1. 比色法:基于酶催化底物的产物与染色剂之间发生化学反应的原理。
测定过程中,酶水解底物产生的产物与染色剂发生反应形成有色产物,通过测定产物的吸光度来估计酶活性的强弱。
2. 荧光法:利用荧光底物的酶催化产物发出的荧光信号来测定酶活性。
荧光强度与酶催化产物的浓度成正比,通过测定荧光强度来分析酶活性。
3. 放射性标记法:将底物标记上放射性同位素,使其具有放射性。
通过测定底物放射性崩解的程度来估计酶活性的大小。
4. 免疫学方法:利用特异性抗体与酶结合形成抗原-抗体-酶复合物,测定抗原-抗体-酶复合物的活性来检测酶活性的强弱。
5. 吸收光谱法:利用特定的酶底物,通过测量其吸收光谱的变化来分析酶活性的强弱。
需要根据具体实验目的和条件选择适合的测定方法。

一、实验目的1. 掌握蛋白酶活力的测定原理和方法。
2. 学习酶促反应动力学的基本知识。
3. 了解蛋白酶在不同条件下的活性变化。
二、实验原理蛋白酶是一种催化蛋白质水解的酶,其活性可通过测定在一定条件下水解底物产生氨的速率来表示。
本实验采用紫外分光光度法测定蛋白酶活力,通过测定反应体系中氨的生成速率,间接反映蛋白酶的活力。
三、实验材料与试剂1. 实验材料:- 酪蛋白:1g- 胰蛋白酶:适量- 磷酸氢二钠溶液(0.1mol/L)- 磷酸二氢钠溶液(0.1mol/L)- 氢氧化钠溶液(0.1mol/L)- 蒸馏水- 紫外分光光度计2. 试剂:- Folin试剂:1.25g钼酸铵溶于50ml水中,加入25ml硫酸,混匀,用蒸馏水定容至100ml- 草酸溶液:7.5g草酸溶于100ml水中- 硫酸铜溶液:5g硫酸铜溶于50ml水中,用蒸馏水定容至100ml- 酶标液:1mg/mL四、实验步骤1. 准备反应体系:取0.5g酪蛋白,加入5ml磷酸氢二钠溶液(0.1mol/L)和5ml 磷酸二氢钠溶液(0.1mol/L),混匀后加入适量的胰蛋白酶,使酶与底物比例约为1:100。
2. 预热反应体系:将反应体系放入水浴锅中,恒温40℃。
3. 启动反应:每隔一定时间(如30秒)取样,立即加入0.5ml氢氧化钠溶液(0.1mol/L)终止反应。
4. 测定氨含量:将终止反应后的样品加入0.5ml Folin试剂,混匀后加入0.5ml 硫酸铜溶液,再加入0.5ml草酸溶液,混匀后放入紫外分光光度计中,于波长620nm处测定吸光度。
5. 计算蛋白酶活力:根据标准曲线计算样品中氨的浓度,进而计算蛋白酶活力。
五、实验结果与分析1. 标准曲线绘制:以不同浓度的氨溶液为标准品,绘制标准曲线。
2. 蛋白酶活力计算:根据样品的吸光度值,从标准曲线中查找对应的氨浓度,计算蛋白酶活力。
3. 分析不同条件对蛋白酶活性的影响:通过改变温度、pH值、底物浓度等条件,观察蛋白酶活性的变化。

蛋白酶酶活测定方法一、实验原理:一定条件下不仅能够水解蛋白质中的肽键,也能够水解酰胺键和酯键,因此可用蛋白质或人工合成的酰胺及脂类化合物作为底物来测定蛋白酶的活力。
本实验选用酪蛋白为底物,测定微生物蛋白酶水解肽键的活力。
酪蛋白经蛋白酶作用后,降解成相对分子质量较小的肽和氨基酸,在反应混合物中加入三氯醋酸溶液,相对分子质量较大的蛋白质和肽沉淀下来,相对分子质量较小的肽和氨基酸仍留在溶液中,溶解于三氯醋酸(TCA)溶液的肽的数量与酶的数量和反应时间成正比。
在280nm波长下测定溶液吸光度的增加,计算酶的活力。
一分钟内1mg牛血清蛋白(BSA)相当的非蛋白性Lowry试液显色物质的增量值定义为一个蛋白酶活性单位(IU)。
二、试剂配制:A溶液:含2%KCl,1%TrltonX-100的50mM磷酸盐缓冲溶液(pH 6.0)试样TG酶溶液:直接取发酵样12000rpm离心5min,取上清测定。
底物溶液:精确称取底物二甲基酪蛋白0.250g,加入50mM PB缓冲溶液(pH 6.0)10mL,常温搅拌30min使其溶解后备用。
三、操作步骤:1. 试样1)将底物溶液放入37℃恒温水浴中预热备用2)试管中加入试样TG酶溶液0.2mL后放入恒温水浴中,10min后加入已预热的底物溶液1mL,立即振荡混合,于37℃反应60min3)反应结束后,加入12% TCA溶液1mL,再于37℃反应30min,使反应终止4)20℃,3000rpm,20min离心后取上清备用。
2.空白1)试管中加入已预热底物溶液1mL,再加入12% TCA溶液1mL,振荡混合后,于37℃反应60min2)加入试样TG酶溶液0.2mL,振荡混合后,于37℃反应30min3)20℃,3000rpm,20min离心后取上清备用。
四、Lowry法显色反应试管中分别加入试样清液和空白清液各0.2mL,加入A溶液1mL,振荡混合后室温下放置10min,然后加入试剂B 0.1mL,振荡混合后,于37℃反,空白的吸应30min。

实验四、蛋白酶酶活力的测定一、原理以酪蛋白为反应底物,令蛋白酶在其最适宜条件下反应一定时间,用三氯乙酸终止反应后过滤或离心得上清液,用Folin比色法测上清液中蛋白酶解物的浓度,计算蛋白酶活力。
蛋白酶活力定义:在一定的条件下,每分钟水解酪蛋白生成与1μg酪氨酸相当的三氯醋酸可溶物所需的木瓜蛋白酶的量,为1个酶活力单位(u)。
二、材料、仪器与试剂(一)材料:木瓜蛋白酶(二)仪器:可见-紫外分光光度计、水浴锅、天平、具塞刻度试管(10、15ml)、漏斗、滤纸、试管架,容量瓶、移液管(1、10ml)、烧杯(25ml)、玻璃棒。
(三)试剂:1福林试剂(Folin试剂)市场购买的Folin试剂。
此溶液使用时加2倍蒸馏水稀释,即成已稀释3倍的福林试剂。
2、中性稀释液-pH7.2磷酸盐缓冲液称取磷酸二氢钠(NaH2PO4·2H2O)31.2g,定容至1000mL,即成0.2mol/L溶液(A液)。
称取磷酸氢二钠(Na2HPO4·12H2O)71.63g,定容至1000mL,即成0.2mol/L 溶液(B液)。
取A 液28mL 和B 液72mL,再用蒸馏水稀释1倍,即成0.1mol pH7.2的磷酸盐缓冲液。
3、酪蛋白溶液2g恒重的酪蛋白,用0.5mol/LNaOH溶液润湿后加入80ml pH7.2磷酸盐缓冲液,沸水浴溶解,冷却后,用1 mol/L盐酸调至pH 7.0,再用磷酸盐缓冲液定容至100ml,得浓度为2%的酪蛋白溶液。
临用现配。
4、三氯醋酸溶液称取三氯乙酸(CCL3COOH)65.4g,定容至1000mL,得0.4mol/L三氯乙酸(TCA)溶液5、酪氨酸标准溶液精确称取精确称取在105℃烘箱中烘至恒重的酪氨酸0.1000g,逐步加入6mL 1N盐酸使溶解,用0.2N盐酸定容至100mL,其浓度为1000μg/mL,再用水稀释5倍,得到200μg/mL的酪氨酸标准溶液。
取200μg/mL的标准酪氨酸溶液,配成不同浓度的溶液(0、20、40、60、80、100μg/mL)6、样品溶液称取木瓜蛋白酶0.100g, 置于研钵中,加入相应的缓冲液定容至50mL,得到稀释500倍的酶液(当天配制、稀释)。
实验四、蛋白酶活力的测定1.实验目的掌握用Folin-酚法测定蛋白酶活力的方法,与Azocasein(偶氮酪蛋白)法作为比较。
2.实验原理蛋白酶在一定的温度和pH下,水解酪素底物产生含有酚基的氨基酸(如酪氨酸、色氨酸),在碱性条件下,将福林试剂还原,生成钼蓝和钨蓝,其颜色的深浅与酚基氨基酸含量成正比,通过在660nm测定其吸光度,可得到酶解产生的酚基氨基酸的量,计算出蛋白酶活力,以此代表蛋白酶的总酶活力。
酶活单位定义:在37℃、相应的pH条件下,在1min内水解酪蛋白底物,产生相当于1µg酚类化合物(由酪氨酸等同物表示)的酶量,为1个酶活单位。
3.主要仪器和试剂试剂:0.1mg/mL L-酪氨酸标准贮备溶液、0.55mol/LNa2CO3、福林试剂、Casein溶液、TCA 溶液仪器设备:恒温水浴锅、分光光度计、pH计,分析天平、秒表。
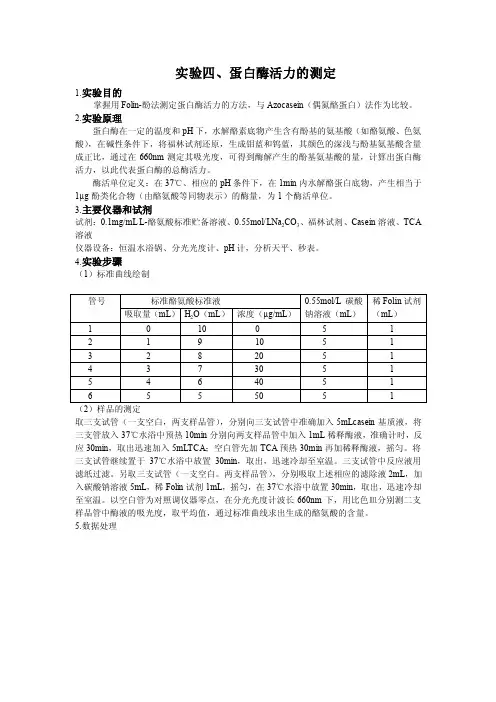
4.实验步骤(1)标准曲线绘制取三支试管(一支空白,两支样品管),分别向三支试管中准确加入5mLcasein基质液,将三支管放入37℃水浴中预热10min分别向两支样品管中加入1mL稀释酶液,准确计时,反应30min,取出迅速加入5mLTCA;空白管先加TCA预热30min再加稀释酶液,摇匀。
将三支试管继续置于37℃水浴中放置30min,取出,迅速冷却至室温。
三支试管中反应液用滤纸过滤。
另取三支试管(一支空白。
两支样品管),分别吸取上述相应的滤除液2mL,加入碳酸钠溶液5mL,稀Folin试剂1mL,摇匀,在37℃水浴中放置30min,取出,迅速冷却至室温。
以空白管为对照调仪器零点,在分光光度计波长660nm下,用比色皿分别测二支样品管中酶液的吸光度,取平均值,通过标准曲线求出生成的酪氨酸的含量。
5.数据处理。


蛋白酶活性检验方法1 定义1g固体酶粉(或1mL液体酶),在一定温度和P H值条件下,1min水解酪素产生1ug酪氨酸为一个酶活力单位,以(u/ mL)表示。
2 福林法(第一法)2、1 原理蛋白酶在一珲的温度与P H条件下,水解底物,产生含有酚基的氨基酸(如:酪氨酸、色氨酸等),在碱性条件下,将福林试剂(Folin)还原,生成钼蓝与钨蓝,用分光度法测定,计算其酶活力。
2、2 试剂和溶液2、2、1 福林试剂的制备于2000mL磨口回流装置中加入钨酸钠(Na2Wo4·2H2O)100g、钼酸钠(Na2MoO4·2H2O)25g、水700mL、85%磷酸50mL、浓盐酸100mL,水火沸腾回流10h,取下回流冷却器,在通风橱中加入硫酸锂(Li2SO4)50g、水50mL和数滴浓溴水(99%),再微沸15min,以除去多余的溴(冷后人有绿色需再加溴水,再煮沸除去过量的溴),冷却,见水定溶至1000ml。
混匀,过滤。
制得的试剂应呈金黄色,贮存于棕色瓶内。
使用溶液:一份福林试剂与二份水混合,摇匀。
2、2、2 碳酸钠溶液c(Na2CO3)=0.4mol/L称取无水碳酸钠(Na2CO3)42.4g,用水溶解并定容至1000 mL。
2、2、3 三氯乙酸c(CCl3·COOH)=0.4mol/L称取三氯乙酸65.4g,用水溶解并定容至1000 mL。
2、2、4 氢氧化钠溶液c(NaOH)=0.5mol/L按GB601配制。
2、2、5 盐酸溶液c(HCI)=1 mol/L及0.1 mol/L按GB601配制。
2、2、6 缓冲溶液a、磷酸缓冲液(P H=7.5)适用于中性蛋白酶称取磷酸氢二钠(Na2HPO4·12H2O)6.02g和磷酸二氢钠(NaH2PO4·12H2O)0.5g,加水溶解并定容至1000mL。
b、乳酸缓冲液(P H=3.0)适用于酸性蛋白酶甲液称取乳酸(80%~90%)10.6g,加水溶解并定容至1000 mL。

一、实验目的1. 了解蛋白酶比活力的概念及测定方法。
2. 掌握利用比色法测定蛋白酶比活力的原理和操作步骤。
3. 通过实验,了解蛋白酶在不同条件下的活性变化,为实际应用提供参考。
二、实验原理蛋白酶比活力是指单位质量的蛋白质所具有的酶活性。
在实验中,通过测定蛋白酶在一定条件下对底物(如酪蛋白)的水解程度,可以计算出蛋白酶的比活力。
本实验采用比色法,通过测定底物水解产生的产物(如酪氨酸)的吸光度变化,间接反映蛋白酶的活性。
三、实验材料与仪器1. 实验材料:- 蛋白酶样品- 酪蛋白- 0.02mol/L pH7.5磷酸盐缓冲液- 0.1mol/L Folin-酚试剂- 0.4mol/L三氯乙酸- 0.05mol/L氢氧化钠溶液- 2.5mol/L硼砂缓冲溶液(pH10.5)- 680nm比色计2. 实验仪器:- 磁力搅拌器- 移液器- 电子天平- 恒温水浴锅- 10mL具塞试管- 50mL容量瓶- 试管架四、实验步骤1. 准备实验试剂:- 配制0.1mol/L Folin-酚试剂:将钨酸钠、钼酸钠、磷酸、盐酸、硫酸锂、液溴等试剂按比例混合,微火回流加热10小时,加入碳酸钠和蒸馏水,定容至1000mL。
- 配制0.4mol/L三氯乙酸溶液:称取三氯乙酸16.34g,用水溶解并定容至500mL。
- 配制0.05mol/L氢氧化钠溶液:按GB601配制。
- 配制2.5mol/L硼砂缓冲溶液(pH10.5):称取硼酸钠19.08g,加水溶解并定容至1000mL,称取氢氧化钠4.0g,加水溶解并定容至1000mL,取甲液500mL乙液400mL混合,用水稀释至1000mL。
2. 实验操作:- 将酪蛋白溶解于0.02mol/L pH7.5磷酸盐缓冲液中,配制成2%酪蛋白溶液。
- 将蛋白酶样品用0.02mol/L pH7.5磷酸盐缓冲液稀释至适宜浓度。
- 取10mL具塞试管,加入2%酪蛋白溶液1mL,然后加入蛋白酶溶液1mL,置于37℃恒温水浴锅中反应30分钟。

蛋白酶比活力实验报告蛋白酶比活力实验报告引言:蛋白酶是一类能够水解蛋白质的酶,广泛存在于生物体内。
通过测定蛋白酶的比活力,可以评估其催化反应的速率和效率。
本实验旨在通过比较不同条件下蛋白酶的活力,探究影响蛋白酶活性的因素。
实验方法:1. 实验材料准备:- 蛋白酶溶液:从动物组织中提取的蛋白酶溶液,浓度为10 mg/mL。
- 底物溶液:使用明胶作为蛋白酶的底物,浓度为1%。
- 缓冲液:pH值为7.4的磷酸盐缓冲液。
- 试管:用于混合反应液的透明试管。
- 恒温水浴:用于控制反应温度的设备。
2. 实验步骤:- 步骤一:在不同温度下测定蛋白酶的活力。
- 将5 mL蛋白酶溶液和5 mL底物溶液混合,并放置于恒温水浴中,分别设置不同温度条件(如25℃、37℃、50℃)。
- 在反应开始后的1分钟、2分钟、3分钟等时间点,取出一定量的反应液,立即停止反应。
- 使用布拉德福法测定反应液中未被水解的底物浓度,计算蛋白酶的比活力。
- 步骤二:在不同pH条件下测定蛋白酶的活力。
- 在不同pH值的缓冲液中,重复上述步骤一的实验操作。
- 测定不同pH条件下蛋白酶的比活力,并比较其差异。
实验结果:1. 温度对蛋白酶活力的影响:- 在25℃、37℃和50℃下进行实验,测得蛋白酶的比活力分别为0.05 U/mg、0.1 U/mg和0.02 U/mg。
- 结果显示,蛋白酶的活力随着温度的升高而增加,但当温度过高时(如50℃),蛋白酶的活力反而下降。
2. pH值对蛋白酶活力的影响:- 在pH为7.4、8.0和9.0的缓冲液中进行实验,测得蛋白酶的比活力分别为0.08 U/mg、0.06 U/mg和0.04 U/mg。
- 结果显示,蛋白酶的活力在中性条件下(pH 7.4)最高,而在酸性和碱性条件下,蛋白酶的活力均降低。
讨论与结论:通过本实验,我们可以得出以下结论:1. 温度对蛋白酶活力有显著影响,适宜的温度可以提高蛋白酶的催化效率,但过高的温度会导致酶的变性,从而降低活力。

一、实验目的1. 学习和掌握蛋白酶活性检测的基本原理和方法。
2. 了解蛋白酶的特性和作用。
3. 通过实验,学会使用相关仪器和操作技能。
二、实验原理蛋白酶是一种能够水解蛋白质的酶,其活性是指在一定条件下,蛋白酶催化蛋白质水解的能力。
蛋白酶活性检测通常采用紫外分光光度法,通过测定反应体系中蛋白质的降解程度来评估蛋白酶的活性。
三、实验材料与仪器1. 实验材料:(1)蛋白酶样品(2)底物:酪蛋白(3)缓冲液:磷酸盐缓冲液(pH 7.0)(4)其他试剂:硫酸铜、碘化钾、氢氧化钠等2. 实验仪器:(1)紫外分光光度计(2)恒温水浴锅(3)电子天平(4)移液器(5)试管(6)烧杯四、实验步骤1. 准备实验试剂和仪器。
2. 配制底物溶液:称取一定量的酪蛋白,加入适量磷酸盐缓冲液,溶解后备用。
3. 设置实验组:(1)取若干个试管,分别加入不同浓度的蛋白酶样品。
(2)在每个试管中加入相同体积的底物溶液。
(3)将试管放入恒温水浴锅中,设定温度为37℃,反应一定时间。
4. 设置对照组:(1)取若干个试管,分别加入相同体积的蛋白酶样品和底物溶液。
(2)将试管放入恒温水浴锅中,设定温度为37℃,反应一定时间。
5. 测定反应体系中蛋白质的降解程度:(1)取一定体积的反应体系,加入硫酸铜和碘化钾溶液。
(2)用紫外分光光度计测定反应体系的吸光度。
(3)根据吸光度计算蛋白质的降解程度。
6. 数据处理和分析:(1)绘制蛋白酶活性与酶浓度、反应时间的关系曲线。
(2)分析蛋白酶的特性和作用。
五、实验结果与分析1. 实验结果:(1)不同浓度的蛋白酶样品对底物溶液的降解程度不同。
(2)随着反应时间的延长,蛋白质的降解程度逐渐增加。
2. 分析:(1)蛋白酶的活性与酶浓度呈正相关,即酶浓度越高,活性越强。
(2)在一定反应时间内,蛋白酶活性随着反应时间的延长而增加,但当反应时间过长时,活性逐渐降低,可能是因为蛋白酶自身发生降解。
六、实验结论1. 通过本实验,掌握了蛋白酶活性检测的基本原理和方法。
实验:蛋白酶的活力测定一、实验目的1、学习蛋白酶活力的测定方法。
2、深入了解酶的活力和比活力的概念。
二、实验原理1、酶活力的大小,是以该酶在适宜的温度和pH下,酶催化一定时间后,反应底物的减少量或者反应产物的增加量来表示。
2、本实验蛋白酶的活力大小是以分解出的酪氨酸的量来表示,其单位为:每分钟内分解出1微克酪氨酸的酶量称为1单位。
3、本实验采用福林-酚与蛋白质水解出的酪氨酸生成兰色物,从兰色的深浅程度可以求知酪氨酸的多少,从而确定酶活力的大小。
4、在测酶活力前,先用福林-酚与用已知的不同浓度的酪氨酸作用,作出兰色深浅程度(用光密度表示)与酪氨酸浓度关系的标准曲线。
5、将酶与底物反应产生的产物与福林-酚试剂作用后测光密度,从标准曲线上查出相当于多少微克的酪氨酸,就可以计算出酶的单位了。
三、实验材料、仪器和试剂1.实验材料1398中性蛋白酶粗酶粉(上海新型发酵厂)、滤纸2.仪器(1)试管(1.5*15cm*24) (2)移液管(3)电热恒温水浴(4)721型分光光度计3.试剂(1)福林-酚试剂B(2)标准酪氨酸溶液称取50毫克酪氨酸(预先在105摄氏度烘至恒重),加0.2MHCL溶液后定容至100ml,在加水稀释5倍得到100微克/毫升的酪氨酸溶液。
(3)酪蛋白溶液称取酪蛋白2克,置150ml三角烧瓶中,加入0.2M磷酸氢二钠61ml,在水浴上搅拌使溶解,再加入39ml0.2M磷酸二氢钠,得到pH7的酪蛋白液,倾出上清液备用。
(4)0.4M三氯醋酸溶液(TCA)(5)0.4M碳酸钠溶液四、操作步骤1、酪氨酸标准曲线制作:按下列次序加入试剂,混合均匀,保温,然后在分光光度计上进行比色,测出650nm处的光密度值。
以酪氨酸浓度为横坐标,光密度值为纵坐标,作出标准曲线。
管号 1 2 3 4 5 62、蛋白酶活力测定 (1)浸出酶液称取0.5克酶粉加入40ml 水,在室温下放置1小时并时加搅动。
将酶浸出液过滤,取滤液1ml 用水稀释至20ml ,即为稀释1600倍的酶液。
实验三蛋白酶活力的测定一、目的掌握用分光光度计法测定蛋白酶活力的原理与操作技术。
二、原理蛋白酶水解酪蛋白,其产物酪氨酸能在碱性条件下使福林——酚试剂还原,生成鉬蓝与钨蓝,以比色法测定。
三、试剂及仪器1.福林—酚试剂称取50g钨酸钠(Na2WO4•2H2O),12.5g钼酸钠(Na2MoO4•2H2O),置入1000mL原底烧瓶中,加350mL水,25mL85%磷酸,50mL浓盐酸,文火微沸回流10h,取下回流冷凝器,加50g硫酸锂(Li2SO4)和25mL水,混匀后,加溴水脱色,直至溶液呈金黄色,再微沸15min,驱除残余的溴,冷却,用4号耐酸玻璃过滤器抽滤,滤液用水稀释至500mL。
使用时用2倍体积的水稀释。
2.0.4mol/L碳酸钠溶液:称取42.4g碳酸钠,用水溶解并定容至1000mL。
3.0.4mol/L三氯乙酸溶液:称取65.5g三氯乙酸,用水溶解并定容至1000mL。
4.2%酪蛋白溶液称取2.00g酪蛋白(又名干酪素),加约40mL水和2~3滴浓氨水,于沸水浴中加热溶解,冷却后,用pH7.2磷酸缓冲溶液稀释定容至100mL,贮存于冰箱中。
5.pH7.2磷酸缓冲液0.2mol/L 磷酸二氢钠溶液:称取31.2g磷酸二氢钠(NaH2PO4•2H2O),用水溶解稀释至1000mL;0.2mol/L 磷酸氢二钠溶液:称取71.6g磷酸氢二钠(Na2HPO4•12H2O),用水溶解稀释至1000mL;pH7.2磷酸缓冲溶液:取28mL 0.2mol/L磷酸二氢钠溶液和72mL 0.2mol/L磷酸氢二钠溶液,用水稀释至1000mL。
6.标准酪氨酸溶液:准确称取0.1g DL-酪氨酸,加少量0.2mol/L盐酸溶液(取1.7mL浓盐酸,用水稀释至100mL),加热溶解,用水定容至1000mL,每毫升含DL-酪氨酸100微克。
7.仪器:分光光度计、试管四、操作步骤1.标准曲线绘制编号0 1 2 3 4 5 6 7 80 1 2 3 4 5 6 7 8标准酪氨酸溶液(mL)[100g/mL]水(mL) 10 9 8 7 6 5 4 3 2稀释酪氨酸溶液浓度(g/mL) 0 10 20 30 40 50 60 70 80在上述各管中各取1mL,分别加入5mL 0.4mol/L碳酸钠溶液,1mL福林—酚试剂,于400C水浴显色20min,在680nm波长下测吸光度,绘制标准曲线,在标准曲线上求得吸光度为1时相当的酪氨酸g数,即为K值。
测定蛋白酶活力实验一、实验目的1.加深了解酶活力的概念。
2.学习掌握测定蛋白酶活力的方法。
二、实验原理酶活力指酶催化某一特定反应的能力。
其大小可用在一定条件下酶催化反应进行一定时间后,反应体系中底物的减少量或产物的生成量来表示。
酶活力单位是表示酶活力大小的重要指标。
本实验规定酶活力单位(U)为一定条件下每分钟分解1μg 酪氨酸所需的酶量。
实验选用枯草杆菌蛋白酶水解酪蛋白产生酪氨酸的反应体系。
产物酪氨酸在碱性条件下与Folin-酚试剂反应生成蓝色化合物,该蓝色化合物在680nm 处有最大光吸收,其吸光值与酪氨酸含量呈正比。
因此通过测定一定条件下产物酪氨酸的含量变化,可计算出蛋白酶的活力。
三、仪器和试剂仪器:恒温水浴锅、分光光度计、试管及试管架、干燥滤纸、玻璃漏斗。
原料枯草杆菌蛋白酶:称取1g 枯草杆菌蛋白酶粉,用少量0.02mol/L,pH7.5磷酸缓冲液溶解并定容至100mL,震荡15分钟,使充分溶解,干纱布过滤,取滤液冰箱备用。
使用时视酶活力高低用缓冲液适当稀释。
试剂1. Folin-酚试剂:在2L 磨口回流瓶中加入钨酸钠(Na2WoO4. 2H2O)100g,钼酸钠(Na2WoO4. 2H2O)25g,蒸馏水700mL,85%磷酸50mL 以及浓盐酸100mL,充分混匀后,微火回流加热10小时。
再加入硫酸锂150g,蒸馏水50mL 和液溴数滴,摇匀后开口继续煮沸15min,以驱赶过剩的溴。
冷却后加蒸馏水定容至1000mL,过滤,溶液呈黄绿色,置于棕色试剂瓶中暗处贮藏。
使用前用标准NaOH 溶液、酚酞为指示剂标定酸度(约为2mol/L),然后加水稀释至1mol/L,即可使用。
2. 0.2mol/L 盐酸溶液3. 0.04mol/L 氢氧化钠溶液4. 0.55mol/L 碳酸钠溶液5. 10%三氯乙酸溶液6. 0.02mol/LpH7.5磷酸缓冲液:称取磷酸氢二钠(Na2HPO4 . 12H2O)7.16g,用水定容至100mL(A 液);称取磷酸二氢钠(Na2HPO4 .12H2O)3.12g,用水定容至100mL(B 液)。
测定蛋白酶活力实验
一、实验目的
1.加深了解酶活力的概念。
2.学习掌握测定蛋白酶活力的方法。
二、实验原理
酶活力指酶催化某一特定反应的能力。
其大小可用在一定条件下酶催化反应进行一定时间后,反应体系中底物的减少量或产物的生成量来表示。
酶活力单位是表示酶活力大小的重要指标。
本实验规定酶活力单位(U)为一定条件下每分钟分解1μg 酪氨酸所需的酶量。
实验选用枯草杆菌蛋白酶水解酪蛋白产生酪氨酸的反应体系。
产物酪氨酸在碱性条件下与Folin-酚试剂反应生成蓝色化合物,该蓝色化合物在680nm 处有最大光吸收,其吸光值与酪氨酸含量呈正比。
因此通过测定一定条件下产物酪氨酸的含量变化,可计算出蛋白酶的活力。
三、仪器和试剂
仪器:
恒温水浴锅、分光光度计、试管及试管架、干燥滤纸、玻璃漏斗。
原料
枯草杆菌蛋白酶:称取1g 枯草杆菌蛋白酶粉,用少量L,磷酸缓冲液溶解并定容至100mL,震荡15分钟,使充分溶解,干纱布过滤,取滤液冰箱备用。
使用时视酶活力高低用缓冲液适当稀释。
试剂
1. Folin-酚试剂:
在2L 磨口
回流瓶中加入钨酸钠(Na2WoO4 . 2H2O)100g,钼酸钠(Na2WoO4 .
2H2O)25g,蒸馏水700mL,85%磷酸50mL 以及浓盐酸100mL,充分混匀后,微火回流加热10小时。
再加入硫酸锂150g,蒸馏水50mL 和液溴数滴,摇匀后开口继续煮沸15min,以驱赶过剩的溴。
冷却后加蒸馏水定容至1000mL,过滤,溶液呈黄绿色,置于棕色试剂瓶中暗处贮藏。
使用前用标准NaOH 溶液、酚酞为指示剂标定酸度(约为
2mol/L),然后加水稀释至1mol/L,即可使用。
2. 0.2mol/L 盐酸溶液
3. L 氢氧化钠溶液
4. L 碳酸钠溶液
5. 10%三氯乙酸溶液
6. 磷酸缓冲液:
称取磷酸氢二钠(Na2HPO4 . 12H2O)7.16g,用水定容至100mL(A 液);称取磷酸二氢钠(Na2HPO4.12H2O)3.12g,用水定容至100mL(B 液)。
取A 液84mL,B 液16mL 混合后,得到磷酸缓冲液,可长期存放。
临用时稀释10倍即可。
7. 标准酪氨酸溶液(50μg/mL):称取以烘干至恒重的酪氨酸,用L 盐酸约30mL 溶解后,蒸馏水定容至250mL。
8. 酪蛋白溶液%):称取1.25g 酪蛋白,用L 氢氧化钠溶液(20mL)溶解,再用磷酸缓冲液定容到250mL。
四、操作步骤
(一)酪氨酸标准曲线的制作
取6支试管(标号0,1~5),按顺序分别加入,,,,和标准酪氨酸溶液,再用水
补足到,摇匀后各加入L 碳酸钠,摇匀。
依次加入Folin—酚试剂,摇匀并计时,于30℃水浴锅中保温15min。
然后680nm 处测定吸光值(以0号管作对照)。
以酪氨酸含量(μg)作横坐标,吸光值为纵坐标绘制标准曲线。
(二)酶活力测定
1.酶反应:取一支试管,加入的酪蛋白溶液,于30℃水浴中预热5分钟,再加入已预热好的枯草杆菌蛋白酶液,立即计时,水浴中准确保温10min,从水浴中取出后,立即加入的10%三氯醋酸溶液,摇匀静置数分钟,干滤纸过滤,收集滤液(样品液)。
另取一试管,先加入已预热好的枯草杆菌蛋白酶液和的10%三氯醋酸溶液,摇匀,放置数分钟,再加入的酪蛋白溶液,然后于30℃水浴保温10min,同样干滤纸过滤,收集滤液(对照液)。
以上两过程,应各做一次平行实验。
2.滤液中酪氨酸含量的测定
取3支试管,分别加入水、A 液、B 液,然后各加入 mL L 碳酸钠溶液和酚试剂,摇匀按标准曲线制作方法保温并测吸光度值。
根据吸光度值,由标准曲线查出A、B 液中酪氨酸含量差值,即可推算出酶的活力单位。
五、计算
A 样品—样品液的吸光度值
A 对照—对照液的吸光度值
K—标准曲线上A=1时对应的酪氨酸μg 数
V—酶促反应液的体积(本实验为5mL)
T—酶促反应时间(本实验为10min)
N—酶溶液稀释倍数。