高一化学必修一第二章第一节讲解
- 格式:ppt
- 大小:1.55 MB
- 文档页数:70



高中化学必修一第二章知识点总结在高中化学的教学中注重学生学习兴趣的培养,不仅可以提高课堂教学的效率,而且有利于促进学生的个性发展。
接下来店铺为你整理了高中化学必修一第二章知识点总结,一起来看看吧。
高中化学必修一第二章知识点总结第一节物质的分类1、掌握两种常见的分类方法:交叉分类法和树状分类法。
2、分散系及其分类:(1)分散系组成:分散剂和分散质,按照分散质和分散剂所处的状态,分散系可以有9种组合方式。
(2)当分散剂为液体时,根据分散质粒子大小可以将分散系分为溶液、胶体、浊液。
分散系溶液胶体浊液分散粒子直径<1nm1~100nm>100nm 外观均一,透明,稳定均一,透明,介稳体系不均一,不透明,不稳定能否透过滤纸能能不能能否透过半透膜能不能不能实例食盐水Fe(OH)3胶体泥浆水3、胶体:(1)常见胶体:Fe(OH)3胶体、Al(OH)3胶体、血液、豆浆、淀粉溶液、蛋白质溶液、有色玻璃、墨水等。
(2)胶体的特性:能产生丁达尔效应。
区别胶体与其他分散系常用方法丁达尔效应。
胶体与其他分散系的本质区别是分散质粒子大小。
(3)Fe(OH)3胶体的制备方法:将饱和FeCl3溶液滴入沸水中,继续加热至体系呈红褐色,停止加热,得Fe(OH)3胶体。
高中化学必修一第二章知识点总结第二节离子反应一、电解质和非电解质电解质:在水溶液里或熔融状态下能导电的化合物。
1、化合物非电解质:在水溶液中和熔融状态下都不能导电的化合物。
(如:酒精[乙醇]、蔗糖、SO2、SO3、NH3、CO2等是非电解质。
)(1)电解质和非电解质都是化合物,单质和混合物既不是电解质也不是非电解质。
(2)酸、碱、盐和水都是电解质(特殊:盐酸(混合物)电解质溶液)。
(3)能导电的物质不一定是电解质。
能导电的物质:电解质溶液、熔融的碱和盐、金属单质和石墨。
电解质需在水溶液里或熔融状态下才能导电。
固态电解质(如:NaCl晶体)不导电,液态酸(如:液态HCl)不导电。

高中化学必修一第二章知识点第一节:物质的量和摩尔质量化学中的基本概念之一就是物质的量,而物质的量是使用摩尔(mol)来表示的。
如果我们拿一摩尔的物质,它的质量就是我们所定义的摩尔质量。
摩尔质量可以通过元素的相对原子质量或者化合物的相对分子质量来计算。
第二节:分子式和结构式分子式是用元素符号表示化合物当中各种元素的种类和数量的方法,而结构式则更加详细地展示了各个元素之间的联结方式。
通过分子式和结构式,我们可以进一步了解和研究分子的性质以及它们之间的相互作用。
第三节:摩尔质量与理论计算通过摩尔质量的概念,我们可以进行理论上的计算。
例如,知道了一种物质的摩尔质量,我们就可以通过称量来确定实际的质量。
通过这种方式,我们可以在实验室中精确测量化学物质的摩尔质量,从而得到更加精确的数据。
第四节:化学反应与化学方程式化学反应是物质之间发生的变化,而化学方程式则是将化学反应以化学式的形式表示出来。
通过化学方程式,我们可以清楚地了解反应物和生成物之间的摩尔比例,以及反应物和生成物之间的相对质量关系。
第五节:氧化还原反应氧化还原反应是化学中非常重要的反应类型之一。
在氧化还原反应中,发生电子的转移,其中一个物质失去电子被氧化,而另一个物质获得电子被还原。
通过氧化还原反应,我们可以了解到电子转移过程中的能量变化以及反应物之间的关系。
第六节:质量守恒定律和化学计算质量守恒定律是化学中最基本也是最重要的定律之一。
质量守恒定律告诉我们任何化学反应中,质量都是不会发生变化的。
通过质量守恒定律,我们可以进行化学计算,例如计算反应物和生成物之间的摩尔比例、质量比例等等。
第七节:浓度和溶液的稀释浓度是溶液中溶质的含量与溶剂或溶液总体积之间的比值。
通过浓度,我们可以量化地了解溶液的性质和浓度的变化。
而溶液的稀释则是指通过增加溶剂的量来减少溶质的浓度,这样可以改变溶液的性质和浓度。
结尾:高中化学必修一第二章的知识点涵盖了物质的量和摩尔质量、分子式和结构式、摩尔质量与理论计算、化学反应与化学方程式、氧化还原反应、质量守恒定律和化学计算、浓度和溶液的稀释等内容。

第二章化学反应速率与化学平衡第一节化学反应速率第1课时化学反应速率知|识|梳|理知识点一化学反应速率1.定义。
用来描述化学反应过程进行快慢的物理量。
2.表示方法。
(1)可用单位时间、单位体积中反应物或生成物的物质的量变化来表示。
(2)如果反应体系的体积是恒定的,通常用单位时间内反应物浓度的减小或生成物浓度的增加来表示。
3.表达式及其单位。
(1)表达式:v=ΔcΔt。
(2)常用单位:mol·L-1·min-1[或mol/(L·min)]、mol·L-1·s-1[或mol/(L·s)]。
(3)对于一个化学反应:m A+n B===p C+q D,用不同的物质的物质的量浓度变化表示的该反应的反应速率存在的关系为v(A) m=v(B)n=v(C)p=v(D)q。
【微思考】(1)同一化学反应,用不同物质表示其反应速率时,数值相同吗?提示:不一定相同,若化学计量数相同,则反应速率相同,否则,不相同。
(2)在C(s)+H2O(g)CO(g)+H2(g)的反应中,可用哪些物质表示反应速率?提示:在C(s)+H2O(g)CO(g)+H2(g)反应中,可以用H2O(g)、CO(g)、H2(g)的浓度变化来表示反应速率,但不能用固体或纯液体来表示反应速率,因为固体或纯液体的浓度视为常数。
知识点二化学反应速率的测定化学反应速率是可以通过实验测定的。
根据化学反应速率表达式,实验中需要测定不同反应时刻反应物(或生成物)的浓度。
利用任何一种与物质浓度有关的可观测量都可以进行测定,如气体的体积、体系的压强、颜色的深浅、光的吸收、导电能力等。
微训练1.下列对“化学反应速率”的理解正确的是()A.化学反应速率表示的是化学反应进行的程度B.化学反应速率可以用单位时间内反应物浓度的变化来表示C.化学反应速率可以用任何一种反应物或生成物的浓度变化来表示D.化学反应速率可以是正值,也可以是负值解析化学反应速率表示化学反应进行的快慢,不表示反应进行的程度,A项错误;化学反应速率可以用单位时间内反应物浓度的减少来表示,也可以用单位时间内生成物浓度的增加来表示,B项正确;反应速率不能用纯液体或纯固体来表示,C项错误;化学反应速率都是正值、无负值,D项错误。

高一化学必修一第二章知识点第一节:物质的组成与性质化学对我们生活的影响无处不在。
从我们所处的自然环境到我们所习惯的日常用品,都离不开化学。
本章将介绍化学的基础知识和概念,帮助我们更好地理解和应用化学。
一、物质的分类物质是由不同种类的化学元素组成的。
化学元素是由相同类型的原子组成的物质,目前已知的化学元素有118种。
通过各种实验和研究方法,科学家们将这些元素按照一定的规律进行分类,形成了元素周期表。
二、化学符号与化学式为了便于描述和表示化学元素和化合物,科学家们发明了化学符号和化学式。
化学符号是用拉丁字母缩写表示一个元素的符号,如氢元素的符号为H,氧元素的符号为O。
化学式是用化学符号表示化合物的组成,如水的化学式是H2O。
三、化学反应化学反应是物质之间发生变化的过程。
在化学反应中,产生了新的物质(产物),同时消耗了原有的物质(反应物)。
化学反应可以分为合成反应、分解反应、置换反应和化合反应等。
四、物质的性质物质的性质是指物质本身所具有的特点和表现。
物质的性质可以分为物理性质和化学性质两类。
1.物理性质是指与物质的组成和结构无关的性质,例如颜色、形状、密度、熔点、沸点等。
物理性质可以通过观察和测量进行确定。
2.化学性质是指与物质的组成和结构相关的性质,例如可燃性、氧化性、酸碱性等。
化学性质需要通过化学反应进行测试和验证。
第二节:原子结构与元素周期表了解物质的基本组成——原子结构,对理解化学现象和性质变化至关重要。
一、原子的组成原子是构成物质的基本微粒。
原子由原子核和电子云组成。
原子核由质子和中子组成,质子带正电荷,中子不带电。
电子云是由电子构成,电子带负电荷。
二、元素周期表元素周期表是根据元素的原子序数和元素性质进行排列的一种化学工具。
元素周期表可以帮助我们系统地了解元素的特性和变化规律。
元素周期表按照一定的规则和模式排列,分为周期和族。
三、原子结构与元素周期表的关系原子结构与元素周期表的关系是一个基本的化学原理。




高一年级化学必修一第二章说课稿《物质的分类》
世界上的物质都是化学物质,或者是由化学物质所组成的混合物,小编准备了高一年级化学必修一第二章说课稿,具体请看以下内容。
一、说教材
(一)教材分析
《物质的分类》选自新课标人教版高中化学必修1 第二章第一节。
本节主要介绍化学物质及其变化的分类;是连接初中化学和高中化学的纽带客桥梁;为以后章节的学习做了很好的铺垫;因此,本节在全章中占有特殊的地位,学好本节课具有非常重要的意义。
刚上高一的学生处于初高中的过渡时期,对化学物质和化学反应有了一定的基础,但对物质的组成及分类方法还有待于加强,对化学基础实验还需要提高;这一阶段的学生正处在抽象思维向逻辑思维的过渡时期,能较客观的看待问题和解决问题,但独立分析解决问题的能力还有待加强,因此,要多为学生提供自主学习的机会,激发其独立思考的能力和培养科学探究的兴趣。
(二)教学目标
根据对教材地位和作用的分析,在新课改理念的指导下,我确定如下三维教学目标:。
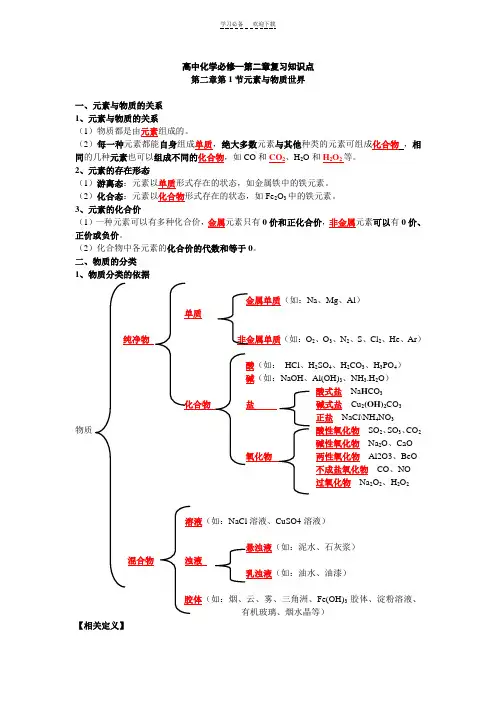
高中化学必修一第二章复习知识点第二章第1节元素与物质世界一、元素与物质的关系1、元素与物质的关系(1)物质都是由元素组成的。
(2)每一种元素都能自身组成单质,绝大多数元素与其他种类的元素可组成化合物,相同的几种元素也可以组成不同的化合物,如CO和CO2、H2O和H2O2等。
2、元素的存在形态(1)游离态:元素以单质形式存在的状态,如金属铁中的铁元素。
(2)化合态:元素以化合物形式存在的状态,如Fe2O3中的铁元素。
3、元素的化合价(1)一种元素可以有多种化合价,金属元素只有0价和正化合价,非金属元素可以有0价、正价或负价。
(2)化合物中各元素的化合价的代数和等于0。
二、物质的分类1、物质分类的依据金属单质(如:Na、Mg、Al)单质纯净物非金属单质(如:O2、O3、N2、S、Cl2、He、Ar)酸(如:HCl、H2SO4、H2CO3、H3PO4)碱(如:NaOH、Al(OH)3、NH3.H2O)酸式盐Na H CO3化合物盐碱式盐Cu2(OH)2CO3正盐NaCl\NH4NO3物质酸性氧化物SO2、SO3、CO2碱性氧化物Na2O、CaO氧化物两性氧化物Al2O3、BeO不成盐氧化物CO、NO过氧化物Na2O2、H2O2溶液(如:NaCl溶液、CuSO4溶液)悬浊液(如:泥水、石灰浆)混合物浊液乳浊液(如:油水、油漆)胶体(如:烟、云、雾、三角洲、Fe(OH)3胶体、淀粉溶液、有机玻璃、烟水晶等)【相关定义】(1)酸性氧化物:能和碱反应(不能跟酸反应),只生成盐和水的氧化物。
(判断酸性氧化物时,看面相,大多数非金属氧化物属于酸性氧化物,例外的见注意部分)(2)碱性氧化物:能和酸反应(不能跟碱反应),只生成盐和水的氧化物。
(判断碱性氧化物时,也看面相,大多数金属氧化物属于碱性氧化物,例外的见注意部分)(3)两性氧化物:既能和酸又能和碱反应的氧化物。
(只需要记住Al2O3这个例子)(4)不成盐氧化物:不能与酸或碱反应生成相应价态的盐和水的氧化物叫做不成盐氧化物。