【人教版】高中化学必修1知识点总结:第三章金属及其化合物
- 格式:pdf
- 大小:2.71 MB
- 文档页数:5

第三章铁金属材料第一节铁及其化合物1.了解单质铁、铁的氧化物的性质及用途。
2.认识铁单质与水蒸气反应的条件,通过实验掌握Fe(OH)2、Fe(OH)3的制备原理及化学性质。
3.掌握Fe、Fe2+、Fe3+相互转化的途径,通过实验探究学会Fe2+、Fe3+的检验方法。
4.掌握实现铁及其化合物之间转化的试剂和条件。
知识点一铁的单质知识点二铁的氧化物和氢氧化物知识点一铁的单质1.铁的存在和冶炼(1)存在铁在自然界中可以以单质形态(如陨铁)存在,但主要以+2价和+3价化合物的形态存在于矿石中,在地壳中的含量居第四位,仅次于氧、硅和铝。
(2)冶炼工业炼铁的原理是利用还原的方法把铁从铁矿石中提炼出来,化学方程式:3CO+Fe2O3=====高温2Fe+3CO2(以Fe2O3为例)。
2.铁的物理性质铁有延展性、导热性。
铁能导电,但其导电性不如铜和铝,铁还能被磁体吸引,其熔、沸点较高。
3.铁的化学性质(1)与某些非金属单质、酸和盐溶液反应①Fe与非金属单质反应②Fe与非氧化性酸反应(稀H2SO4)Fe+2H+===Fe2++H2↑。
③Fe与盐溶液反应(CuSO4)Fe+Cu2+===Cu+Fe2+。
(2)实验探究铁粉与水蒸气的反应实验装置操作现象用火柴点燃肥皂液,听到爆鸣声,证明生成了H 2实验结论在高温下,铁能与水蒸气反应,化学方程式为3Fe +4H 2O(g)=====高温Fe 3O 4+4H 21.下列物质在氧气中燃烧,现象为火星四射,有黑色固体生成的是A .红磷B .木炭C .铁丝D .酒精【答案】C【解析】红磷在氧气中燃烧时会产生大量的白烟,生成白色固体,A 错误;木炭在氧气中燃烧时会发出白光,生成无色气体,B 错误;铁丝在氧气中燃烧时火星四射,生成黑色固体,C 正确;酒精在氧气中燃烧时火焰为淡蓝色,生成无色气体,D 错误。
2.(2023桂林高一检测)下列各项物质间的转化不能通过反应一步完成的是()A .Fe→Fe 3O 4B .3C .Fe→FeCl 2D .Fe→Fe(OH)3【答案】D【解析】Fe 与O 2点燃可得到Fe 3O 4,能一步反应完成,A 不符合题意;Fe 与Cl 2点燃可得到FeCl 3,能一步反应完成,B 不符合题意;Fe 与盐酸反应可得到FeCl 2,能一步反应完成,C 不符合题意;Fe 不能一步反应生成Fe(OH)3,D 符合题意。
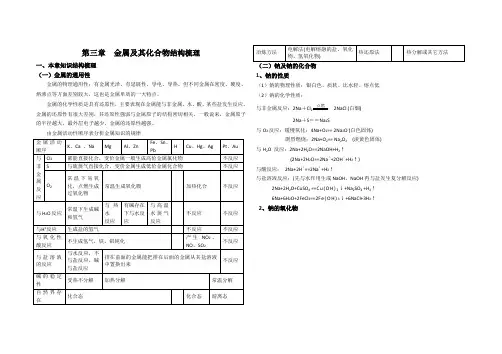
第三章金属及其化合物结构梳理一、本章知识结构梳理(一)金属的通用性金属的物理通用性:有金属光泽、有延展性、导电、导热。
但不同金属在密度、硬度、熔沸点等方面差别较大,这也是金属单质的一大特点。
金属的化学性质是具有还原性,主要表现在金属能与非金属、水、酸、某些盐发生反应。
金属的还原性有很大差别,其还原性强弱与金属原子的结构密切相关,一般说来,金属原子的半径越大,最外层电子越少,金属的还原性越强。
由金属活动性顺序表分析金属知识的规律(二)钠及钠的化合物1、钠的性质(1)钠的物理性质:银白色、质软、比水轻、熔点低(2)钠的化学性质:与非金属反应:2Na+Cl2点燃2NaCl (白烟)2Na+S==Na2S与O2反应:缓慢氧化:4Na+O2== 2Na2O (白色固体)剧烈燃烧:2Na+O2== Na2O2(淡黄色固体)与H2O 反应:2Na+2H2O==2NaOH+H2↑(2Na+2H2O==2Na++2OH―+H2↑)与酸反应:2Na+2H+==2Na++H2↑与盐溶液反应:(先与水作用生成NaOH,NaOH再与盐发生复分解反应) 2Na+2H2O+CuSO4 ==C u(O H)2↓+Na2SO4 +H2↑6Na+6H2O+2FeCl3==2Fe(O H)3↓+6NaCl+3H2↑2、钠的氧化物3、碱------氢氧化钠白色固体,易潮解。
俗名苛性钠,烧碱,火碱。
一元强碱,具有碱的通性,即: 能与酸反应生成盐和水,例:NaOH+HCl==NaCl+H 2O能与酸性氧化物反应生成盐和水,例:2NaOH+CO 2==Na 2CO 3+H 2O 能与某些盐发生复分解反应,例:2NaOH+CuCl 2==C u (O H )2↓+2NaCl4、盐------碳酸钠和碳酸氢钠1、铁的氧化物的转化34.铁三角二、本章知识综合应用1、滴加顺序不同,实验现象不同(1)稀Na2CO3溶液与稀盐酸间的反应向Na2CO3溶液中逐滴加入稀盐酸,开始时无气体产生,达到一定量后才有气泡冒出,由少到多的过程中依次发生下列反应:Na2CO3+HCl==NaCl+NaHCO3NaHCO3+HCl==NaCl+CO2↑+H2O向稀盐酸中逐滴加入稀Na2CO3溶液立即有气泡冒出,由少到多只发生下列反应:2HCl+Na2CO3==2NaCl+CO2↑+H2O(2) 稀AlCl3溶液与稀NaOH溶液间的反应向AlCl3溶液中滴加NaOH溶液直至过量时发生的反应依次为:Al3++3OH―==A l(O H)3↓A l(O H)3+OH―==AlO2―+2H2O现象:白色沉淀逐渐增多,继续加NaOH溶液沉淀逐渐溶解,直至完全消失。

高中化学必修一第三章知识点总结一、金属及其化合物(一)金属的化学性质1. 金属与非金属的反应- 钠与氧气反应- 常温下:4Na + O_{2}=2Na_{2}O,氧化钠为白色固体。
- 加热时:2Na+O_{2}{}{=!=!=}Na_{2}O_{2},过氧化钠为淡黄色固体。
- 铝与氧气反应- 在常温下,铝能与空气中的氧气反应,表面生成一层致密的氧化铝薄膜,4Al + 3O_{2}=2Al_{2}O_{3}。
这层薄膜可以阻止内部的铝进一步被氧化。
2. 金属与酸和水的反应- 钠与水反应- 化学方程式:2Na + 2H_{2}O = 2NaOH+H_{2}↑。
- 现象:“浮(钠的密度比水小)、熔(反应放热,钠的熔点低)、游(有气体生成)、响(反应剧烈)、红(溶液呈碱性,使酚酞变红)”。
- 铁与水蒸气反应- 化学方程式:3Fe + 4H_{2}O(g){高温}{=!=!=}Fe_{3}O_{4}+4H_{2}。
3. 铝与氢氧化钠溶液反应- 化学方程式:2Al+2NaOH + 2H_{2}O=2NaAlO_{2}+3H_{2}↑。
(二)几种重要的金属化合物1. 氧化物- 氧化钠和过氧化钠- 氧化钠(Na_{2}O)- 属于碱性氧化物,与水反应:Na_{2}O + H_{2}O = 2NaOH;与酸反应:Na_{2}O+2HCl = 2NaCl + H_{2}O。
- 过氧化钠(Na_{2}O_{2})- 与水反应:2Na_{2}O_{2}+2H_{2}O = 4NaOH+O_{2}↑。
- 与二氧化碳反应:2Na_{2}O_{2}+2CO_{2}=2Na_{2}CO_{3}+O_{2},因此过氧化钠可用于呼吸面具和潜水艇中作为氧气的来源。
- 氧化铝(Al_{2}O_{3})- 两性氧化物,既能与酸反应:Al_{2}O_{3}+6HCl = 2AlCl_{3}+3H_{2}O,又能与碱反应:Al_{2}O_{3}+2NaOH = 2NaAlO_{2}+H_{2}O。
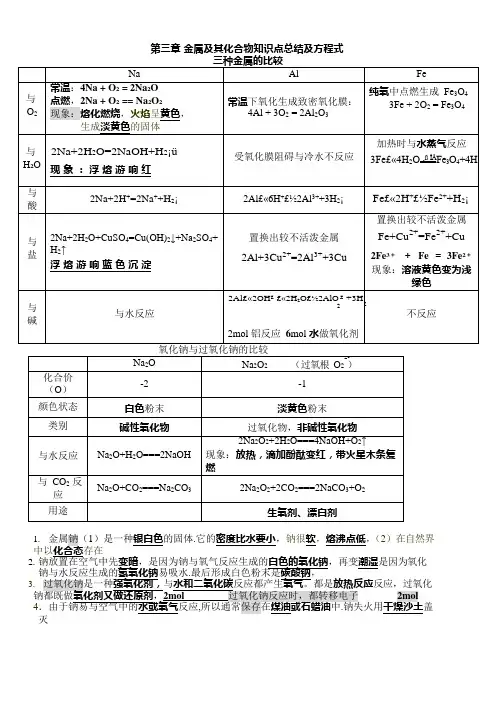
第三章金属及其化合物知识点总结及方程式1.金属钠(1)是一种银白色的固体.它的密度比水要小,钠很软,熔沸点低,(2)在自然界中以化合态存在2.钠放置在空气中先变暗,是因为钠与氧气反应生成的白色的氧化钠,再变潮湿是因为氧化钠与水反应生成的氢氧化钠最后形成白色粉末是碳酸钠,3.反应,过氧化2mol4钠失火用干燥沙土盖风化是化学变化区别碳酸钠与碳酸氢钠可用1.与CaCl2 反应有无沉淀2.与酸反应剧烈程度3 碱性强弱4 稳定性2.碳酸钠与盐酸互滴时现象不同,碳酸钠滴到盐酸中马上有气泡,盐酸滴到碳酸钠中刚开始无现象,后有气泡3 除杂:Na2CO3固体(NaHCO3)加热;Na2CO3溶液(NaHCO3)适量NaOHNaHCO3溶液(Na2CO3)足量CO22 2 1. Al 3+和 OH -互滴现象不同:OH -滴到 Al 3+中先沉淀后澄清;Al 3+到 OH -中先澄清后沉淀Al 3++3 OH -=Al(OH)3 ↓ Al(OH)3 + OH - = AlO -2+2 H 2OAl 3++4OH -= AlO - +2 H O 2. NaAlO 2 和盐酸-互滴现象不同:盐酸滴到 NaAlO2 中先沉淀后澄清; NaAlO 2 滴到盐酸中先澄清后沉淀AlO -+H ++H O=Al(OH) ↓ Al(OH) + 3H + = Al 3+ + 3H O .AlO -+4H + = Al 3+ + 2H O22332222. 实验室制取 Al(OH)3 碱须用氨水3. 铝,氧化铝,氢氧化铝与碱反应,碱必须是强碱4.明矾的化学式 KAl(SO 4)2·12 H 2O,可做净水剂原因是Al 3+ + 3 H 2O = Al(OH)3( 胶 体 )+ 3H +5. 焰色反应:是元素的性质,是物理变化;钠的焰色是黄色,钾的焰色是紫色(透过蓝色钴玻璃)实验中用盐酸洗铂丝;实验步骤:烧,蘸,烧,洗33△3 3点燃2422 23 31制备Fe(OH)2注意:亚铁盐溶液必须新制,保证无氧氛围2铁盐可做净水剂原因是Fe3与水反应形成Fe(OH)胶体:Fe3++3 H2O =Fe(OH)3(胶体)+3H+3.合金的硬度一般高于各成分金属,熔点一般低于各成分金属;铁合金可分为生铁和钢第三章化学反应归纳1、钠在空气中燃烧2Na +O2Na2O2钠块在空气中变暗4Na+O2=2Na2O2 、2Na +2H2O =2 NaOH +H2↑2Na +2H2O =2Na++2OH-+H2↑3 、2Na2O2+2H2O =4NaOH +O2↑2Na2O2+2H2O =4Na++4OH -+O2↑Na2O+H2O=2NaOH4、2Na2O2+2CO2=2Na2CO3+O25、苏打(纯碱)与盐酸反应①盐酸中滴加纯碱溶液Na2CO3+2HCl =2NaCl +H2O+CO2↑CO 2-+2H+=H2O+CO2↑②纯碱溶液中滴加盐酸,至过量Na2CO3+HCl =NaHCO3+NaCl CO 2-+H+=HCO -NaHCO3+HCl=NaCl+H2O+CO2↑HCO -+H+=H2O +CO2↑6、2NaHCO3Na2CO3+H2O +CO2↑7 、NaHCO3+NaOH = Na2CO3+H2O HCO -+OH -=H2O +CO 2-8.Na2CO3+H2O+CO2 = 2NaHCO39.2NaHCO3+Ca(OH)2====CaCO3 + 2H2O+Na2CO3NaHCO3+Ca(OH)2====CaCO3+H2O+NaOH10.2Na+2H2O+CuSO4=Cu(OH)2↓+Na2SO4+H2↑1、铝箔在氧气中剧烈燃烧4Al +3O22Al2O32. 2Al +6HCl =2AlCl3+3H2↑2Al +6H+=2Al3++3H2↑3. 2Al+2NaOH +2H2O =2NaAlO2+3H2↑2Al +2OH -+2H2O =2AlO -+23H2↑4.Al2O3+2NaOH 2NaAlO2+H2O Al2O3+2OH -=2AlO -+H2O5.Al2(SO4)3+6NH3·H2O=2Al(OH)3↓+(NH4)2SO4Al3++3 NH3·H2O =Al(OH)3↓+3NH +6.Al(OH)3+3HCl =AlCl3+3H2O Al(OH)3+3H+=Al3++3H2O7.Al(OH)3+NaOH NaAlO2+2 H2O Al(OH)3+OH-=AlO -+2 H O8 2Al(OH)3=Al2O3+3H2O9.Al3++3 H2O =Al(OH)3( 胶体)+3H+11.Al3++3 OH-=Al(OH)3↓Al(OH)3+OH-=AlO -+2 H2OAl3++4OH-= AlO -+2 H O2 212.AlO2-+H++H2O=Al(OH)3↓Al(OH)3+3H+=Al3++3H2O.AlO2-+4H+ = Al3++2H2O13.2AlO2-+CO2+3H2O=2 Al(OH)3+ CO32-1. 高温下铁与水反应3Fe +高温4H2O(g) Fe3O4+4H22. 铁与盐酸反应Fe +2HCl =FeCl2+H2↑Fe +2H+=Fe2++H2↑3. 氧化铁溶于盐酸中Fe2O3+6HCl =2FeCl3+3H2O Fe2O3+6H+=2Fe3++3H2O4.Fe3O4+8H+=Fe2++2Fe3++4H2O5.Fe2O3+3CO=2Fe+3CO26.FeCl3+3NaOH =Fe(OH)3↓+3NaCl Fe3++3OH -=Fe(OH)3↓7.FeCl2+2NaOH =Fe(OH)2↓+2NaCl Fe2++2OH -=Fe(OH)2↓8.氢氧化亚铁在空气中被氧化4Fe (OH)2+O2+2H2O =4Fe (OH)39.Fe(OH)2+2HCl=FeCl2+2H2O10.Fe(OH)3+3HCl=FeCl3+3H2O11.氯化亚铁溶液中通入氯气2FeCl2+Cl2=2FeCl3 2 Fe2++Cl2=2 Fe3++2Cl-12.氯化铁溶液中加入铁粉2FeCl3+Fe =3FeCl22Fe3++Fe =3Fe2+13.2Fe3++Cu=2Fe2++ Cu2+14.3SCN- + Fe3+=Fe(SCN)3“”“”At the end, Xiao Bian gives you a passage. Minand once said, "people who learn to learn are very happy people.". In every wonderful life, learning is an eternal theme. As a professional clerical and teaching position, I understand the importance of continuous learning, "life is diligent, nothing can be gained", only continuous learning can achieve better self. Only by constantly learning and mastering the latest relevant knowledge, can employees from all walks of life keep up with the pace of enterprise development and innovate to meet the needs of the market. This document is also edited by my studio professionals, there may be errors in the document, if there are errors, please correct, thank you!。




【人教版】高中化学必修1知识点总结:第三章金属及其化合物【人教版】高中化学必修1知识点总结:第三章金属及其化合物第三章金属及其化合物课标要求1.了解钠、铝、铁、铜与氧气、水、盐酸、氢氧化钠溶液的反应情况,了解金属共性,掌握个性。
2.初步学会根据铁与水蒸汽反应的原理设计实验装置。
3.运用氧化还原反应知识,分析金属单质在各种反应中所表现的还原性。
4.了解钠、铝、铁、铜等金属的主要物理性质及金属钠的保存。
5.掌握钠及其化合物之间的转化关系(包括碳酸钠溶液与碳酸氢钠溶液的相互转化。
6.掌握铝及其重要化合物之间的转化关系。
7.掌握铁及其重要化合物之间的转化关系。
8.知道合金的一般特性。
9.能列举铜合金、钢等合金材料的重要应用。
10.能说出青铜的主要成分,钢的主要成分。
要点精讲一、金属的物理通性:常温下,金属一般为银白色晶体(汞常温下为液体),具有良好的导电性、导热性、延展性。
二、金属的化学性质:多数金属的化学性质比较活泼,具有较强的还原性,在自然界多数以化合态形式存在。
三、金属化合物的性质:1、氧化物2、氢氧化物3、盐四、金属及其化合物之间的相互转化1、铝及其重要化合物之间的转化关系。
2、铁及其重要化合物之间的转化关系。
3、钠及其化合物之间的相互转化。
附:1、焰色反应:用于在火焰上呈现特殊颜色的金属或它们的化合物的检验。
注:观察钾焰色反应时,应透过蓝色钴玻璃,以便滤去杂质钠的黄光。
2、碳酸钠、碳酸氢钠:Na2CO3又叫纯碱,俗称苏打。
无水碳酸钠是白色粉末。
NaHCO3俗称小苏打,也叫酸式碳酸钠。
它是白色粉末,在水中的溶解度比碳酸钠略小,水溶液呈微碱性,固体碳酸氢钠受热即分解。
NaHCO3是发酵粉的主要成分,也用于制灭火剂、焙粉或清凉饮料等方面的原料,在橡胶工业中作发泡剂。
将碳酸钠溶液或结晶碳酸钠吸收CO2可制得碳酸氢钠。
3、氧化铝、氢氧化铝(1)Al2O3俗名矾土,是一种难熔又不溶于水的白色粉末。
它的熔点、沸点都高于201某度。

高一化学金属及其化合物知识点总结1 .元素的存在形式有两种:游离态和化合态。
(1 )钠镁铝只以化合态形式存在:钠元素的主要存在形式是氯化钠,镁元素的存在形式有菱镁矿,铝元素的存在形式有铝土矿。
(2)铁元素有两种存在形式:游离态的陨铁和化合态的铁矿石。
2.金属单质的用途:(1 )利用钠元素的特征焰色(黄色)制高压钠灯,高压钠灯的透雾力强,可以做航标灯;利用钠单质的熔点低,钠钾合金常温下呈液态,做原子反应堆的导热剂;利用钠单质制备过氧化钠,利用钠单质还原熔融态的四氯化钛制备金属钛。
(2)镁条燃烧发出耀眼的白光,用来做照明弹。
(3)利用铝的良好导电性,做导线。
利用铝块和铝粉的颜色都是银白色,铝粉制成银粉(白色涂料)。
3.金属化合物的用途:(1 )过氧化钠做漂白剂,过氧化钠做水下作业、坑道下作业的供氧剂;氯化钠、碳酸钠、碳酸氢钠做食品添加剂;氯化钠做为制备单质钠和氯气的原料,氯化钠做为制备氢氧化钠、氢气、氯气的原料。
(2)氧化镁的熔点高,做耐高温的材料:耐火管、耐火坩埚、耐高温的实验仪器。
(3)明矾做净水剂。
4.金属的分类:(1 )根据冶金工业标准分类:铁(铬、锰)为黑色金属,其余金属(钠镁铝等)为有色金属。
(2)根据密度分类:密度大于4.5g/cm3的金属是重金属:如铁、铜、铅、银,密度小于4.5g/cm3 的金属是轻金属:如钠、镁、铝。
5.氧化物的分类:二元化合物,其中一种元素是氧元素,并且氧元素呈负二价的化合物是氧化物。
1 )氧化物(根据氧化物中非氧元素的种类)分为金属氧化物和非金属氧化物。
2)金属氧化物分为酸性氧化物、碱性氧化物、两性氧化物。
3)非金属氧化物分为酸性氧化物、不成盐氧化物。
4)氧化物(根据氧化物是否与碱或酸反应生成盐)分为成盐氧化物和不成盐氧化物(CO 、NO)。
(5)成盐氧化物分为酸性氧化物、碱性氧化物、两性氧化物。
(6)酸性氧化物分为高价态的金属氧化物(Mn2O7)和非金属氧化物(CO2)。


高一化学必修(bìxiū)一第三章总结高一化学必修(bìxiū)一第三章总结第三章金属(jīnshǔ)及其化合物一、金属(jīnshǔ)的物理通性:常温下,金属一般为银白色晶体〔汞常温下为液体(yètǐ)〕,具有良好的导电性、导热性、延展性。
二、金属的化学性质:多数金属的化学性质比拟活泼,具有较强的复原性,在自然界多数以化合态形式存在。
物质保存化性与O2Na煤油〔或石蜡油〕中常温下氧化成Na2O:4Na+O2=2Na2O点燃生成Na2O2点燃2Na+O2==Na2O2Al直接在试剂瓶中即可常温下生成致密氧化膜:4Al+3O2=2Al2O3致密氧化膜使铝耐腐蚀。
纯氧中可燃,生成氧化铝:点燃4Al+3O2==2Al2O3点燃2Al+3Cl2==2AlCl3Fe直接在试剂瓶中潮湿空气中易受腐蚀:铁锈:主要成分Fe2O3纯氧中点燃生成:点燃3Fe+2O2==Fe3O4与Cl2与S2Na+Cl2==2NaCl点燃常温下即可反响:2Na+S=Na2S常温与冷水剧烈反响:2Na+2H2O=2NaOH+H2↑2Na+2HCl=2NaCl+H2↑----------------------与硫酸铜溶液:2Na+2H2O+CuSO4=Cu(OH)2↓+Na2SO4+H2↑与氯化铁溶液:6Na+6H2O+2FeCl3=2Fe(OH)3↓+6NaCl+3H2↑----------------------2Fe+3Cl2==2FeCl3点燃加热只能生成亚铁盐:Fe+S==FeS△常温下纯铁不与水反响。
加热时才与水蒸气反响:3Fe+4H2O(g)==Fe3O△4+4H2Fe+2HCl=FeCl2+H2↑---------------------加热时才能反响:2Al+3S==Al△2S3去膜后与热水反响:2Al+6H2O==2Al(OH)3↓+3H2↑△与水与酸溶液与碱溶液2Al+6HCl==2AlCl3+3H2↑2Al+2NaOH+2H2O=2NaAlO2+3H2↑与盐溶液置换出较不活泼的金属单质置换出较不活泼的金属单质与氧化物镁条引燃时铝热反响:2Al+Fe2O3==Al2O3+2Fe点燃金属活泼性逐渐减弱---------------------三、金属化合物的性质:1、氧化物性质Na2O碱性氧化物Na2O2非碱性氧化物淡黄色固体2Na2O2+2H2O=4NaOH+O2↑2Na2O2+4HCl=4NaCl+2H2O+O2↑Al2O3两性氧化物白色固体----------------Al2O3+6HCl=2AlCl3+3H2OFe2O3碱性氧化物赤红色固体----------------Fe2O3+6HCl=2FeCl3+3H2O〔溶液黄色〕颜色状态白色固体与水反响Na2O+H2O=2NaOH与酸溶液Na2O+2HCl=2NaCl+H2O〔溶液无色〕与碱溶液----------------其他Na2O+CO2=Na2CO3----------------2Na2O2+2CO2=2Na2CO3+O2Al2O3+2NaOH=2NaAlO2+H2O------------------------------------------------2、氢氧化物化性属性NaOH碱性氢氧化物Al(OH)3两性氢氧化物Al(OH)3+3HCl=AlCl3+3H2OFe(OH)2碱性氢氧化物Fe(OH)2+2HCl=FeCl2+2H2OFe(OH)3碱性氢氧化物Fe(OH)3+3HCl=FeCl3+3H2O---------------- △与酸溶液NaOH+HCl=NaCl+H2O与碱溶液----------------稳定性其他稳定2NaOH+CO2=Na2CO3+H2ONaOH+CO2(过量)=NaHCO3金属钠与水即可Al(OH)3+NaOH=NaAlO2+2H2O----------------△2Al(OH)3==Al2O3+3H2O----------------4Fe(OH)2+O2+2H2O=4Fe(OH)32Fe(OH)3==Fe2O3+3H2O----------------亚铁盐溶液与氢氧化钠溶液〔液面下〕----------------铁盐溶液滴加氢氧化钠溶液制备3、盐溶解度溶液碱性与酸与碱稳定性铝盐溶液与过量浓氨水Na2CO3较大使酚酞变红,溶液呈碱性。
高中化学必修一知识点(第三章)学习高中化学要学会总结,最好一个章节一次总结,最后再来个大总结,那么化学必修一第三章知识点有哪些呢?今天小编在这给大家整理了高中化学必修一知识点(第三章),接下来随着小编一起来看看吧!高中化学必修一知识点(第三章)第三章金属及其化合物第一节金属的化学性质1.金属的物理通性有哪些?(1)金属在常温下的状态除汞是液体外,其他在常温下是固体。
(2)金属的颜色、光泽绝大多数金属都是银白色,具有金属光泽,少数金属是特殊颜色如铜是紫红色,金是金黄色。
(3)良好的导电、导热性。
(4)延展性延性:拉成细丝的性质。
展性:压成薄片的性质。
2.化学通性有哪些?(1)化合态金属元素只有正化合价(2)金属单质易失电子,表现还原性(3)易与氧气反应,得到氧化物(4)活动性排在氢前的金属元素与酸反应得到盐和氢气(5)与盐反应,置换出活动性弱的金属单质3.金属钠的性质有哪些?(1)物理性质有哪些?钠银白色、质软、熔点低、密度比水的小但比煤油的大。
(2)化学性质有哪些?①很活泼,常温下:4Na + O2=2Na2O(新切开的钠放在空气中容易变暗)②加热条件下:2Na+O2Na2O2(先熔化成小球,后燃烧产生黄色火焰,生成淡黄色固体Na2O2。
)钠在空气中的变化过程:Na―→Na2O―→NaOH―→Na2CO3·10H2O(结晶)―→Na2CO3(风化),最终得到是一种白色粉末。
一小块钠置露在空气中的现象:银白色的钠很快变暗(生成Na2O),跟着变成白色固体(NaOH),然后在固体表面出现小液滴(NaOH易潮解),最终变成白色粉未(最终产物是Na2CO3)。
③钠与水的反应与H2O反应2Na+2H2O=2NaOH+H2↑离子方程式:2Na++2H2O=2Na++2OH-+H2↑(注意配平)实验现象:钠浮在水面上,熔成小球,在水面上游动,有哧哧的声音,最后消失,在反应后的溶液中滴加酚酞,溶液变红。
化学必修一第三章《金属及其化合物》主要知识及化学方程式总结材料科学必修一第三章《金属及其化合物》主要知识及化学方程式总结高一化学必修I第三章主要知识及化学方程式一、钠及其化合物的性质:1.钠在空气中缓慢氧化:4Na+O2==2Na2O2.钠在空气中燃烧:2Na+O2====Na2O23.钠与水反应:2Na+2H2O=2NaOH+H2↑现象:①钠浮在水面上;②熔化为银白色小球;③在水面上四处爬行;④伴有响声;⑤滴有磷化的水变红色。
4.过氧化钠与水水解:2Na2O2+2H2O=4NaOH+O2↑5.过氧化钠与二氧化碳反应:2Na2O2+2CO2=2Na2CO3+O26.碳酸氢钠受浓硫酸:2NaHCO3==Na2CO3+H2O+CO2↑7.氢氧化钠与碳酸氢钠反应:NaOH+NaHCO3=Na2CO3+H2O8.在碳酸钠溶液中通入二氧化碳:Na2CO3+CO2+H2O=2NaHCO39.苏打(纯碱)与盐酸反应①盐酸中滴加纯碱溶剂Na2CO3+2HCl=2NaCl+H2O+CO2↑CO32-+2H+=H2O+CO2↑②纯碱氯化钠中滴加盐酸,至过量Na2CO3+HCl=NaHCO3+NaClCO32-+H+=HCO3-NaHCO3+HCl=NaCl+H2O+CO2↑HCO3-+H+=H2O+CO2↑10.小苏打与盐酸反应NaHCO3+HCl=NaCl+H2O+CO2↑HCO3-+H+=H2O+CO2↑二、铝及其化合物的物理性质1.铝与盐酸的反应:2Al+6HCl=2AlCl3+3H2↑2.铝与强碱的反应:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑3.铝在空气中氧化:4Al+3O2==2Al2O34.氧化铝与酸反应:Al2O3+6HCl=2AlCl3+3H2O5.铋与强碱反应:Al2O3+2NaOH+3H2O=2Na[Al(OH)4]6.氢氧化铝与强酸加成反应:Al(OH)3+3HCl=AlCl3+3H2O7.氢铋与强碱反应:Al(OH)3+NaOH=Na[Al(OH)4]8.实验室二甲醚氢氧化铝沉淀:Al3++3NH3H2O=Al(OH)3↓+3NH4+9.NaAlO2与强酸反应:NaAlO2+HCl+H2O=Al(OH)3↓+NaClAlO2-+H++H2O=Al(OH)3↓10.NaAlO2与弱酸反应(以CO2为例)△点燃CO2少量:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-CO2过量:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-三、铁及其化合物性质1.Fe2+及Fe3+离子的检验:①Fe2+的检验:(浅绿色溶液)a)加氢氧化钠溶液,产生白色沉淀,继而变灰绿色,最后变红褐色。
人教版高一化学第三章金属及其化合物知识点金属是一种拥有光彩、富裕延展性、简单导电、导热等性质的物质。
查词典化学网为您供给的是高一化学第三章金属及其化合物知识点,希望对你有帮助!金属及其化合物知识点一、金属活动性NaAlFe 。
二、金属一般比较开朗,简单与O2 反响而生成氧化物,可以与酸溶液反响而生成 H2 ,特别开朗的如 Na 等能够与 H2O 发生反响置换出 H2,特别金属如 Al 能够与碱溶液反响而得到 H2。
三、 A12O3 为两性氧化物, Al(OH)3 为两性氢氧化物,都既能够与强酸反响生成盐和水,也能够与强碱反响生成盐和水。
五、 Na2CO3 和 NaHCO3 比较碳酸钠碳酸氢钠俗名纯碱或苏打小苏打色态白色晶体渺小白色晶体水溶性易溶于水,溶液呈碱性使酚酞变红易溶于水 (但比Na2CO3 溶解度小 )溶液呈碱性 (酚酞变浅红 )热稳固性较稳固,受热难分解受热易分解2NaHCO3 Na2CO3+CO2↑ +H2O与酸反响CO32— +H+ H CO3 —H CO3 — +H+ CO2↑ +H2OH CO3 — +H+ CO2↑ +H2O同样条件下放出 CO2 的速度 NaHCO3 比 Na2CO3 快与碱反响 Na2CO3+Ca(OH)2 CaCO3 ↓+2NaOH反响本质: CO32—与金属阳离子的复分解反响NaHCO3+NaOH Na2CO3+H2O反响本质: H CO3 — +OH- H2O+CO32 —与 H2O 和 CO2 的反响 Na2CO3+CO2+H2O 2NaHCO3CO32— +H2O+CO2 H CO3 —不反响与盐反响CaCl2+Na2CO3 CaCO3↓+2NaClCa2++CO32 — CaCO3↓不反响主要用途玻璃、造纸、制皂、清洗发酵、医药、灭火器转变关系六、 .合金:两种或两种以上的金属(或金属与非金属)熔合在一同而形成的拥有金属特征的物质。
合金的特色 ;硬度一般比成分金属大而熔点比成分金属低,用途比纯金属要宽泛。
化学必修一第三章《金属及其化合物》知识点简单整理1.了解钠、铝、铁、铜等金属及其重要化合物的主要物理性质(1).钠、铝、铁、铜在自然界中的存在形式。
(2)钠、铝、铁、铜单质的物理性质①.颜色:块状钠铝铁单质是银白色金属,纯铜是紫红色金属;粉末状的铝和铜颜色不变,粉末状的铁屑是黑色,没有粉末状的钠,钠在空气中马上氧化成白色的氧化钠,最终氧化成碳酸钠;冶金工业中铁属于黑色金属,钠、铝、铜属于有色金属。
③.熔点:钠的熔点低,钠与水反应产生的热量就可以使其熔化成小球;铝、铁、铜的熔点很高。
④.共性:不透明,有导电性、导热性、延展性;钠钾合金做原子反应堆的导热剂;铝、铁、铜可以做导线,金属的导电性:Ag>Cu>Al ;铝的延展性可以制成包装用的铝箔;铝、铁、铜可以制成各种容器等。
⑤.硬度:钠的硬度很小,可以用小刀切割;纯铝的硬度较小,铁和铜的硬度较大。
(3)钠、铝、铁、铜的重要化合物的物理性质①.氧化物的颜色:白色:Na2O 、Al2O3;黑色:FeO 、Fe3O4、CuO;淡黄色:Na2O2;红棕色:Fe2O3。
②.氧化物的溶解性:Na2O 、Na2O2溶于水生成强碱发生化学变化;Al2O3、FeO 、Fe2O3、Fe3O4、CuO不溶水。
③.氢氧化物的颜色:白色:NaOH 、Al(OH)3、Fe(OH)2;红褐色:Fe(OH)3;蓝色:Cu(OH)2。
④.氢氧化物的溶解性:溶于水的:NaOH;不溶于水的:Al(OH)3、Fe(OH)2、Fe(OH)3、Cu(OH)2;其中Fe(OH)2溶于水变色:先变成灰绿色,再变成红褐色Fe(OH)3。
(4)钠、铝、铁、铜重要化合物的物理性质的用途②.为离子共存提供判断依据:ⅰ、有颜色的离子不能大量共存:黄色:Fe3+,浅绿色:Fe2+,蓝色:Cu2+;ⅱ、强碱性条件下不能共存的离子:Fe3+、Fe2+ 、Cu2+、Al3+;ⅲ、与HCO 不能大量共存(发生双水解反应)的离子:Fe3+、Fe2+、Cu2+、Al3+。
第三章金属及其化合物
课标要求
1. 了解钠、铝、铁、铜与氧气、水、盐酸、氢氧化钠溶液的反应情况,了解金属共性,
掌握个性。
2.初步学会根据铁与水蒸汽反应的原理设计实验装置。
3. 运用氧化还原反应知识,分析金属单质在各种反应中所表现的还原性。
4.了解钠、铝、铁、铜等金属的主要物理性质及金属钠的保存。
5.掌握钠及其化合物之间的转化关系(包括碳酸钠溶液与碳酸氢钠溶液的相互转化。
6.掌握铝及其重要化合物之间的转化关系。
7.掌握铁及其重要化合物之间的转化关系。
8.知道合金的一般特性。
9.能列举铜合金、钢等合金材料的重要应用。
10.能说出青铜的主要成分,钢的主要成分。
要点精讲
一、金属的物理通性:常温下,金属一般为银白色晶体(汞常温下为液体),具有良好的导电性、导热性、延展性。
二、金属的化学性质:
多数金属的化学性质比较活泼,具有较强的还原性,在自然界多数以化合态形式存在。
三、金属化合物的性质:
1、氧化物
2、氢氧化物
3、盐
四、金属及其化合物之间的相互转化
1、铝及其重要化合物之间的转化关系。
2、铁及其重要化合物之间的转化关系。
3、钠及其化合物之间的相互转化。
附: 1、焰色反应:用于在火焰上呈现特殊颜色的金属或它们的化合物的检验。
注:观察钾焰色反应时,应透过蓝色钴玻璃,以便滤去杂质钠的黄光。
2、碳酸钠、碳酸氢钠: Na2CO3又叫纯碱,俗称苏打。
无水碳酸钠是白色粉末。
NaHCO3俗称小苏打,也叫酸式碳酸钠。
它是白色粉末,在水中的溶解度比碳酸钠略小,水溶液呈微碱性,固体碳酸氢钠受热即分解。
NaHCO3是发酵粉的主要成分,也用于制灭火剂、焙粉或
清凉饮料等方面的原料,在橡胶工业中作发泡剂。
将碳酸钠溶液或结晶碳酸钠吸收
得碳酸氢钠。
3、氧化铝、氢氧化铝
(1)Al2O3俗名矾土,是一种难熔又不溶于水的白色粉末。
它的熔点、沸点都高于
CO2可制2000 度。
(2)氢氧化铝是典型的两性氢氧化物,它既能溶于强酸生成铝盐溶液,又能溶于强碱
生成偏铝酸盐溶液。
氢氧化铝可用来制备铝盐,作吸附剂等的原料。
氢氧化铝凝胶有中和胃酸和保护溃疡面的作用,可用于治疗胃和十二指肠溃疡、胃酸过多等。
10、合金:。