《溶液配制记录》
- 格式:doc
- 大小:46.50 KB
- 文档页数:1

标准溶液配制记录 Company number:【WTUT-WT88Y-W8BBGB-BWYTT-19998】
标准溶液配制记录第页共页
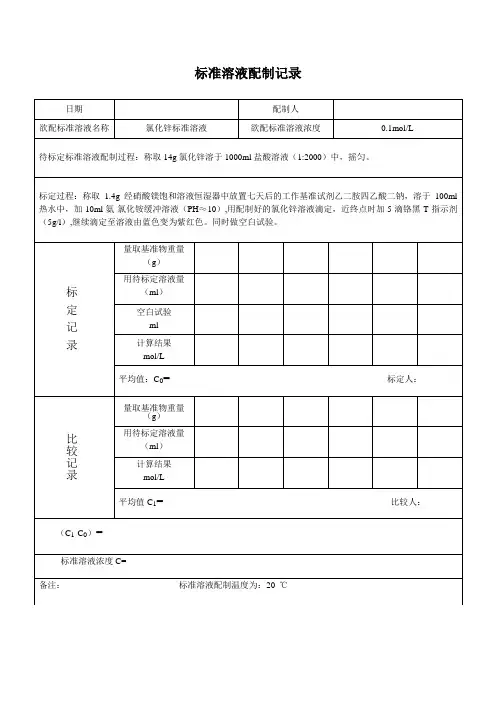
内蒙古工大华远工程技术有限公司标准溶液配制记录
内蒙古工大华远工程技术有限公司标准物质领用记录
标准物质领用记录第页共页
内蒙古工大华远工程技术有限公司标准物质登记表
GDHY-ZP/CX-24-6 标准物质登记表第页共页
编号:GDHY-ZP-YS-001 气相色谱法原始记录第页共页
分析者:审核者:
光度法原始记录
编号:GDHY-ZP-YS-003 第页共页
分析者:审核者:
第页共页
分析者:审核者:
第页共页
分析者:审核者:
编号:GDHY-ZP-YS-002 光谱法原始记录第页共页
分析者:审核者:。

标准溶液配制记录一、前言。
标准溶液是化学分析中常用的一种溶液,它的浓度和成分都是经过严格计算和实验确定的。
正确、精确地配制标准溶液对化学分析结果的准确性和可靠性至关重要。
本文档旨在记录标准溶液的配制过程,以供参考和借鉴。
二、配制目的。
本次配制的标准溶液是XXX试剂,其主要用途是作为XXX分析的定量标准品。
通过配制标准溶液,可以确保在化学分析中得到准确的定量结果。
三、实验步骤。
1. 确定溶液浓度。
首先,根据实验需要和已知的化学反应式,计算出所需的标准溶液的浓度。
在确定浓度的过程中,需要考虑到实验的精确度和所需的最终结果。
2. 准备试剂和仪器。
在配制标准溶液之前,需要准备好所需的试剂和仪器。
试剂的纯度和仪器的准确度对标准溶液的配制至关重要。
3. 溶解试剂。
按照计算得出的配方,将所需的试剂溶解在适量的溶剂中。
在溶解过程中,需要充分搅拌并保持恒温,以确保试剂充分溶解。
4. 调整溶液体积。
根据需要,将溶解好的试剂溶液调整至所需的体积。
在调整体积时,需要使用准确的容量瓶或移液器,并注意避免气泡的产生。
5. 校正浓度。
配制好标准溶液后,需要进行浓度的校正。
校正的方法可以是比色法、滴定法或仪器分析法,根据实际情况选择合适的方法进行校正。
6. 记录实验数据。
在配制标准溶液的整个过程中,需要准确记录每一步的操作和实验数据。
这些数据将作为实验结果的依据,并在实验后的数据分析中起到重要的作用。
四、实验结果。
经过以上步骤,我们成功配制出了XXX浓度为XXX的标准溶液。
经过校正后,其浓度符合实验要求,可以用于后续的化学分析实验。
五、结论。
本次标准溶液配制实验成功完成,得到了符合要求的标准溶液。
在实验过程中,我们严格按照操作规程进行操作,严格控制试剂的纯度和仪器的准确度,最终取得了满意的实验结果。
六、致谢。
在实验过程中,得到了实验室老师和同事们的帮助和支持,在此表示衷心的感谢。
七、参考文献。
[1] XXX. 化学分析实验指导. 化学出版社, 20XX.[2] XXX. 分析化学. 化学工业出版社, 20XX.以上就是本次标准溶液配制的记录,希望对您有所帮助。
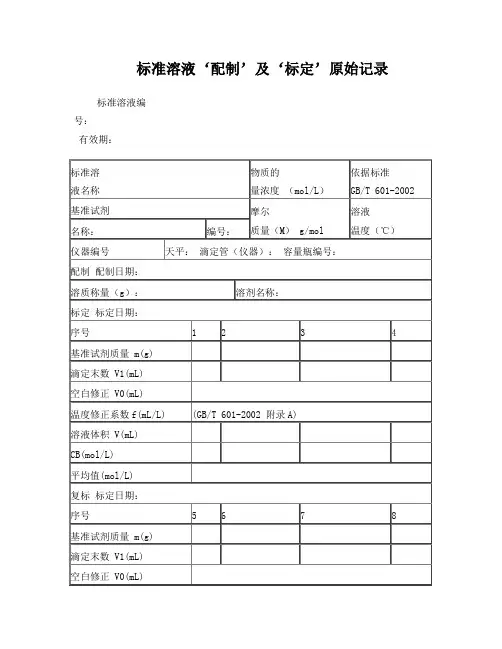
标准溶液‘配制’及‘标定’原始记录标准溶液编号:有效期:温度修正系数f(mL/L) (GB/T 601-2002 附录A)溶液体积 V(mL)CB(mol/L)平均值(mol/L)计算式:V=(V1-V0)×(1+f/1000)CB=1000m/(M×V)说明:每次滴定必须从“0”开始备注:配制人:标定:复标:审核:标准物质配制(标定)记录编号: CHEC/QBG-075名称:、配制方法:使用天平型号编号室温℃、湿度 %RH配制:取定溶 mL标定:取份:⑴⑵⑶⑷用溶液滴定,滴定消耗量(mL)V1= 、V2= 、V3= 、V4= 、V0= 。
标准溶液浓度计算公式:C=计算结果():C1= C2= C3= C4= C =相对偏差(%):S1= S2= S3= S4=备注:。
配制人:复核人:配制日期:年月日有效期年月日标准溶液配制记录编号: CHEC/QBG-147标准溶液名称:规格:配制方法:仪器名称:溯源标准:温度:℃ 、湿度: %RH 标准溶液拟配浓度:配制或稀释过程:配制日期:年月日有效期:年月日配制人:复核人:0.1mol/L盐酸标准滴定溶液的标定编号:JL/LJ-001-01一、标定方法:GB/T5009.1-2003二、使用仪器:AEL-200电子天平(仪器编号:JYB001)马弗炉(仪器编号:JYC009)三、操作1、量取9ml盐酸,加适量水并稀释至1000ml。
混匀,待标定。
2、标定:精密称取约0.15g在270~300℃干燥至恒量的基准无水碳酸钠,加50ml水使之溶解,加10滴溴甲酚绿-甲基红混合指示液,用本溶液滴定至溶液由绿色转变为紫红色,煮沸2min,冷却至室温,继续滴定至溶液由绿色变为暗紫色。
四、记录和结果1、计算公式:c(HCl)=m/[(V1-V2)×0.0530]0.0530……与1.00ml盐酸标准滴定溶液[c(HCl)=1mol/L]相当的基准无水碳酸钠的质量,g2、数据配制人:复核人:配制日期:复核日期:稀释记录表标准溶液(滴定液)管理工作的基本要求关键词(必填项目):标准溶液、滴定液目的(必填项目):对标准溶液的使用等制定统一的要求,便于统一的管理。
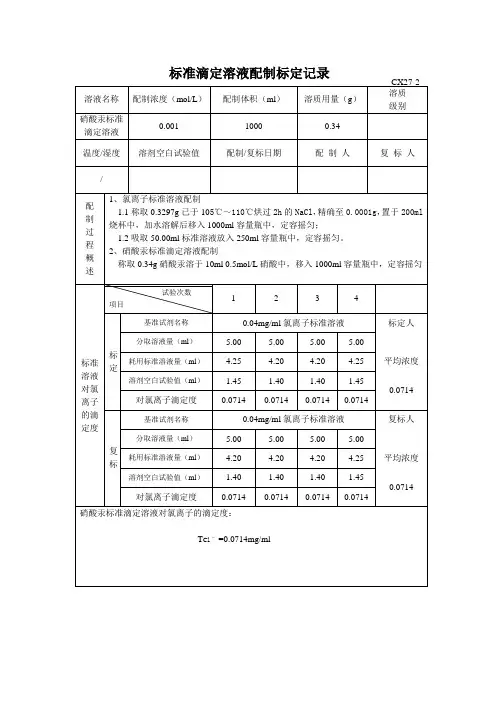
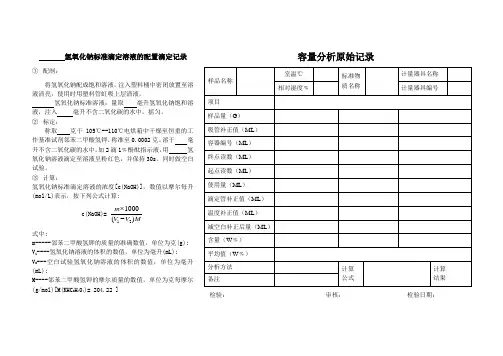
氢氧化钠标准滴定溶液的配置滴定记录 ① 配制:将氢氧化钠配成饱和溶液,注入塑料桶中密闭放置至溶液清亮,使用时用塑料管虹吸上层清液。
氢氧化钠标准溶液:量取 毫升氢氧化钠饱和溶液,注入 毫升不含二氧化碳的水中,摇匀。
② 标定:称取 克于105℃--110℃电烘箱中干燥至恒重的工作基准试剂邻苯二甲酸氢钾,称准至0.0002克。
溶于 毫升不含二氧化碳的水中,加2滴1﹪酚酞指示液,用 氢氧化钠溶液滴定至溶液呈粉红色,并保持30s 。
同时做空白试验。
③ 计算:氢氧化钠标准滴定溶液的浓度[c(NaOH)],数值以摩尔每升(mol/L)表示,按下列公式计算:c(NaOH)=121000()m V V M⨯-式中:m-----邻苯二甲酸氢钾的质量的准确数值,单位为克(g); V 1----氢氧化钠溶液的体积的数值,单位为毫升(mL); V 2---空白试验氢氧化钠溶液的体积的数值,单位为毫升(mL);M----邻苯二甲酸氢钾的摩尔质量的数值,单位为克每摩尔(g/mol)[M(KHC 8H 404)= 204.22 ]容量分析原始记录检验: 审核: 检验日期:盐酸标准滴定溶液的配置滴定记录① 配制:盐酸标准溶液,量取 毫升盐酸,注入 毫升水中。
② 标定:称取 克于270℃--300℃高温炉中灼烧至恒重的工作基准试剂无水碳酸钠,称准至0.0002克。
,溶于50mL 水中,加10滴溴甲酚绿一甲基红指示液,用配制好的盐酸溶液滴定至溶液由绿色变为暗红色,煮沸2min ,冷却后继续滴定至溶液再呈暗红色,同时做空白试验。
③ 计算:盐酸标准滴定溶液的浓度[c(HCl)]数值以摩尔每升(mol/L)表示,按下列公式计算:c(HCl)=121000()m V V M⨯-式中:m----无水碳酸钠的质量的准确数值,单位为克(g) V 1---盐酸溶液的体积的数值,单位为毫升(mL)V 2---空白试验盐酸溶液的体积的数值,单位为毫升(mL) M---无水碳酸钠的摩尔质量的数值,单位为克每摩尔(g/mol)[M (12Na 2CO 3)=52.994]容量分析原始记录检验: 审核: 检验日期:硫酸标准滴定溶液的配置滴定记录①配制:硫酸标准溶液,量取毫升硫酸,注入毫升水中。


标准溶液配制记录一、实验目的。
本实验旨在记录标准溶液的配制过程,以及相关实验数据,为后续实验提供准确可靠的参考依据。
二、实验原理。
标准溶液是已知浓度的溶液,通常用于分析化学中的定量分析。
在配制标准溶液时,需要根据溶质的化学性质和实验要求,选择适当的溶剂和溶质的质量,按照一定的比例配制而成。
三、实验步骤。
1. 准备实验所需的试剂和仪器设备,包括天平、容量瓶、移液管等。
2. 根据实验要求,选择合适的溶剂和溶质,并按照所需的浓度比例进行称量。
3. 将称量好的溶质溶解于适量的溶剂中,摇匀使其充分溶解。
4. 用容量瓶将溶液定容至刻度线,摇匀混合。
5. 将配制好的标准溶液转移至干净的密封瓶中,标注好溶液的名称、浓度、配制日期等信息。
四、实验数据记录。
| 溶质 | 质量/g | 溶剂 | 体积/mL | 浓度/mol/L | 配制日期 |。
|------|--------|------|---------|------------|----------|。
| NaCl | 5.85 | 水 | 1000 | 0.1 |2022/03/15|。
| KCl | 7.20 | 水 | 1000 | 0.2 |2022/03/16|。
五、实验结果分析。
通过本次实验的记录数据,我们成功配制出了两种浓度不同的标准溶液,分别为0.1mol/L的NaCl溶液和0.2mol/L的KCl溶液。
在实验过程中,我们严格按照配制步骤进行操作,确保了实验结果的准确性和可靠性。
六、实验总结。
本次实验记录了标准溶液的配制过程和相关数据,为后续实验提供了重要的参考依据。
在实验中,我们需要严格按照配制步骤进行操作,确保实验结果的准确性和可靠性。
同时,对于配制好的标准溶液,我们也需要做好标注和保存工作,以便后续实验的使用。
七、实验注意事项。
1. 在配制标准溶液时,需要准确称量溶质和溶剂,严格按照比例进行配制。
2. 配制好的标准溶液需要标注清楚名称、浓度、配制日期等信息,并保存在干净的密封瓶中。

溶液配制记录范文实验目的:本实验旨在通过溶液配制的方式,熟悉溶液的配制过程,并掌握配制过程中的操作技巧。
实验原理:溶液配制是将溶质溶解于溶剂中的过程。
通常情况下,配制溶液的方法有称量法和稀释法两种。
称量法是根据溶质的质量比例精确配制溶液,而稀释法是在已有溶液的基础上,用溶剂将其稀释至所需浓度。
实验仪器与试剂:1.磁力搅拌器2.称量瓶3.手持式电子天平4.三角底容量瓶5.各种试剂(如NaCl、NaOH、HCl等)实验步骤:1.准备工作a.清洗并消毒所需试剂容器。
b.检查瓶盖、瓶塞是否紧密,容器是否存在破损。
c.称量所需试剂前先校准电子天平。
d.检查溶剂是否过期,若过期则需更换新溶剂。
2.根据实验要求,决定所需溶质和溶剂,计算所需质量和体积。
3.称重试剂a.清洁并校准电子天平。
b.纳入干净的称量瓶中。
4.配制溶液a.根据所需质量或体积,向三角底容量瓶中加入适量的溶质。
b.用溶剂将溶质溶解至一定体积。
c.摇匀溶液直至充分溶解。
5.检验溶液浓度a.取适量溶液放入试管中。
b.使用合适的检测方法,如比色法、滴定法等,检测溶液的浓度。
c.如浓度不符合要求,根据需要进行稀释或浓缩。
6.记录所配制的溶液信息a.按照实验要求,记录有关溶液的相关信息,如浓度、溶质、溶剂、配制日期等。
实验注意事项:1.在称量试剂之前,保持天平干燥、清洁。
2.配制液体时,使用洁净、干燥的工具。
3.配制过程中,及时记录操作及所得结果。
4.每次操作后,清洗工具和容器,避免交叉污染。
实验结果与分析:本次实验中,成功配制了若干溶液,并通过浓度检测方法验证了其浓度。
每一步操作都严格按照实验步骤进行,并注意了各项注意事项。
实验结果表明所配制的溶液符合预期要求,操作过程中未出现明显误差。
通过本次实验,我对溶液配制有了更深入的理解,提高了实验操作的熟练度。
实验总结:通过本次溶液配制实验,我进一步理解了溶液配制的原理和方法,掌握了实验中的一些操作技巧。
在实验过程中,我加深了对操作的认识,提高了操作的精确性和独立性。