拜耳法生产氧化铝工艺设计计算
- 格式:doc
- 大小:2.17 MB
- 文档页数:25
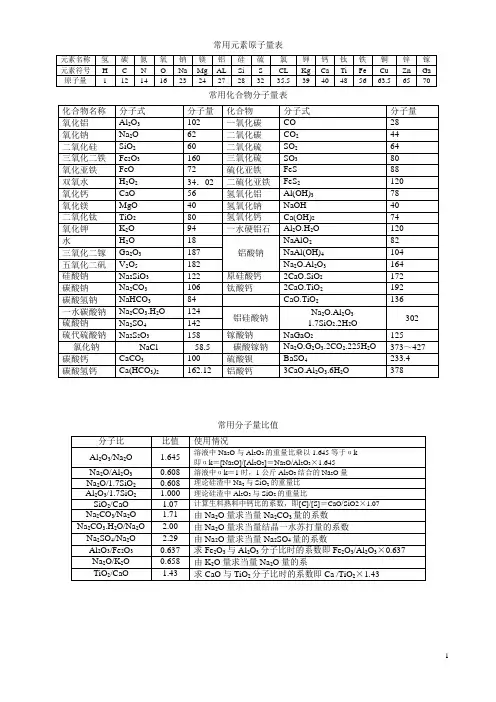
常用元素原子量表常用化合物分子量表常用分子量比值碱赤泥浆水份、比重对照表实测各种固体物料比重表* ---为跑浑期间测定值** ---测定时使用溶剂为苯,比重0.877~0.879计算时按0.88计。
生料浆水份、比重对照表生料浆的水份和比重的关系可用下列方程式表示:γ=2.106-0.012×Wγ---生料浆的比重W---生料浆的水份(%)生料浆水份与熟料折合比对照表注:此表为未掺煤时之定值生产上各种铝酸钠溶液的比重及粘度注:* 假定值,末实际测定;** 按公式(6)计算,并作Ns考虑。
饱和水蒸汽表(按压力编排)过热蒸汽焓表(千卡/公斤)第 二 章 技术指标与工艺计算(1) αK: 苛性比值。
是铝酸钠溶液的重要特性函数之一,是溶液稳定程度的参数,与碳分分解和种分分解密切关系。
它是溶液中所含的苛性氧化钠( Na 2O 苛 )与氧化铝分子数的比值。
645.1102/62/322322⨯==O AL ONa O AL O Na ak 荷 式中 Na 2O 苛, Al 2O 3 -- 分别为溶液中Na 2O 苛与Al 2O 3的含量,克/升; 式中 Na 2O 苛, Al 2O 3 -- 分别为溶液中Na 2O 苛与Al 2O 3的含量,克/升; 62 . 102 --- 分别为Na 2O 与Al 2O 3分子量。
从公式可见,苛性比值在数量上等于溶液中的Na 2O 苛和Al 2O 3的重量比与系数1.645的乘 积。
(2) A/S:铝硅比。
铝土矿、赤泥等固体物料或各种溶液中所含Al 2O 3和SiO 2 重量比。
在固体物料中%100(%)(%)232⨯=SiO O AL S A 在各种溶液中%100)/()/(232⨯=L g SiO L g O AL S A式中:Al 2O 3 (%) 、SiO 2 (%) ---分别为各种物料中Al 2O 3和SiO 2的百分含量,%; Al 2O 3 (g/l)、SiO 2 (g/l)---分别为各种溶液中Al 2O 3和SiO 2的浓度,g/l 。


拜耳法生产氧化铝工艺流程简介拜耳法适于处理高品位铝土矿,这是用苛性碱溶液在一定的温度下溶出铝土矿中的氧化铝的生产方法,具有工艺简单、产品纯度高、经济效益好等优点。
基本原理拜耳法的基本原理有两个。
一个是铝土矿的溶出;一个是铝酸钠溶液的分解。
溶出是用苛性碱溶液在一定的条件下(加石灰、碱浓度、温度、时间及搅拌等)溶出铝土矿中的氧化铝,反应为Al2O3·H2O+2NaOH=2NaAlO2+2H2OAl2O3·3H2O+2NaOH=2NaAlO2+4H2OSiO2+NaOH+NaAlO2=Na2O·Al2O3·2SiO 2·2H2O+H2O一水铝石或三水铝石溶解形成铝酸钠进入碱液中,而其它杂质不进入溶液中,呈固相存在,称赤泥。
三水铝石(Al2O3·3H2O)的溶解温度为105℃,一水硬铝石(α-Al2O3·H2O)为220℃,一水软铝石(γ-Al2O3·H2O)为190℃。
分解是利用NaAlO2溶液在降低温度、加入种子及搅拌的条件下析出固相Al(OH)3,分解反应为NaAlO2+2H2O=Al(OH)3↓+NaOH 种子即为Al(OH)3,加入量(以Al2O3量计算)为溶液中Al2O3含量的一倍以上;温度控制为从75℃降到55℃;搅拌时间为60h左右。
所得Al(OH)3再经焙烧脱水变成Al2O3;并使Al2O3晶型转变,满足铝电解的要求,焙烧反应为Al2O3·3H2O 225℃γ-Al2O3·H2O + 2H2Oγ-Al2O3·H2O 500℃γ-Al2O3 + H2Oγ-Al2O3 900~1200℃α-Al2O3工艺流程及主要技术条件拜耳法的生产工艺主要由溶出、分解和焙烧三个阶段组成。
全流程主要加工工序为:矿石的破碎、均化及湿磨、高温高压溶出、赤泥分离洗涤、叶滤、种子分解、母液蒸发及氢氧化铝焙烧。


拜耳法氧化铝溶出的原理和工艺摘要拜耳法用于生产氧化铝是目前生产氧化铝的主要工业方法,生产氧化铝的工艺有原矿浆制备、高压溶出、压煮矿浆稀释及赤泥分离和洗涤、晶种分解、氢氧化铝分级和洗涤、氢氧化铝焙烧、母液蒸发及苏打苛化等主要生产工序。
关键词拜耳法;氧化铝;原理工艺拜耳法用于氧化铝生产已有近百年的历史,几十年来已经有了很大的发展和改进。
目前仍是世界上生产氧化铝的主要工业方法。
拜耳法用在处理低硅铝土矿(一般要求A/S为7~10),特别是用在处理三水铝石型铝土矿时流程简单,作业方便、能量消耗低,产品质量好等优点。
现在除了受原料条件限制的某些地区外,大多数氧化铝厂都采用拜耳法生产氧化铝。
拜耳法处理一水硬铝石型铝土矿时工艺条件要苛刻一些。
拜耳法最主要的缺点是不能单独地处理氧化硅含量高的矿石。
1 拜耳法生产氧化铝的原理基本原理是拜耳法精心研究出来的。
他在1889年的第一专利谈到用氢氧化铝的晶粒作为种子,使铝酸钠溶液分解,也就是种子分解法。
1892年提出第二个专利系统地闸述了铝土矿所含氧化铝可以在氢氧化钠溶液中溶解成铝酸钠的原理,也就是今天所采用的溶出工艺方法。
此法用在处理低硅铝土矿,特别是处理三水铝石型优质铝土矿,其经济效果远非其他生产方法所能比拟。
直到现在工业生产上实际使用的拜耳法工艺还是以上述两个基本原理为依据。
为了纪念拜耳称之为拜耳法。
原理归纳如下。
用苛性碱溶液溶出铝土矿中氧化铝而制得铝酸钠溶液,采用溶液降温、加晶种、搅拌的条件下,从溶液中分解出氢氧化铝,将分解后母液(主NaOH)经蒸发用来溶出新的一批铝土矿,溶出过程是在加压下进行的。
拜耳法的实质也就是下一反应在不同的条件下交替进行:2 拜耳法生产氧化铝的工艺由于各地铝土矿成份和结构的不同所以采用的技术条件各有特点,各个工厂的具体工艺流程也常有差别。
拜耳法处理一水硬铝石型铝土矿的基本流程如图1所示。
拜耳法生产氧化铝有原矿浆制备,高压溶出,压煮矿浆稀释及赤泥分离和洗涤、晶种分解、氢氧化铝分级和洗涤、氢氧化铝焙烧、母液蒸发及苏打苛化等主要生产工序。
![[方案]拜耳法生产氧化铝工艺流程简介](https://uimg.taocdn.com/5d19abedfbb069dc5022aaea998fcc22bcd143de.webp)
拜耳法生产氧化铝工艺流程简介拜耳法适于处理高品位铝土矿,这是用苛性碱溶液在一定的温度下溶出铝土矿中的氧化铝的生产方法,具有工艺简单、产品纯度高、经济效益好等优点。
基本原理拜耳法的基本原理有两个。
一个是铝土矿的溶出;一个是铝酸钠溶液的分解。
溶出是用苛性碱溶液在一定的条件下(加石灰、碱浓度、温度、时间及搅拌等)溶出铝土矿中的氧化铝,反应为Al2O3〃H2O+2NaOH=2NaAlO2+2H2OAl2O3〃3H2O+2NaOH=2NaAlO2+4H2OSiO2+NaOH+NaAlO2=Na2O〃Al2O3〃2SiO 2〃2H2O+H2O一水铝石或三水铝石溶解形成铝酸钠进入碱液中,而其它杂质不进入溶液中,呈固相存在,称赤泥。
三水铝石(Al2O3〃3H2O)的溶解温度为105℃,一水硬铝石(α-Al2O3〃H2O)为220℃,一水软铝石(γ-Al2O3〃H2O)为190℃。
分解是利用NaAlO2溶液在降低温度、加入种子及搅拌的条件下析出固相Al(OH)3,分解反应为NaAlO2+2H2O=Al(OH)3↓+NaOH 种子即为Al(OH)3,加入量(以Al2O3量计算)为溶液中Al2O3含量的一倍以上;温度控制为从75℃降到55℃;搅拌时间为60h左右。
所得Al(OH)3再经焙烧脱水变成Al2O3;并使Al2O3晶型转变,满足铝电解的要求,焙烧反应为Al2O3〃3H2O 225℃γ-Al2O3〃H2O + 2H2Oγ-Al2O3〃H2O 500℃γ-Al2O3 + H2Oγ-Al2O3 900~1200℃α-Al2O3工艺流程及主要技术条件拜耳法的生产工艺主要由溶出、分解和焙烧三个阶段组成。
全流程主要加工工序为:矿石的破碎、均化及湿磨、高温高压溶出、赤泥分离洗涤、叶滤、种子分解、母液蒸发及氢氧化铝焙烧。
铝矿石进厂后经破碎、均化、贮存,碎矿石送下一工序湿磨。
本工序的目的是使铝矿石破碎至≤15㎜粒度,并且使化学成分均匀地向湿磨供料,控制指标是:每7天的供矿量加权平均值A/S波动在±0.5范围内。

书山有路勤为径,学海无涯苦作舟拜耳法生产氧化铝所谓“拜耳法”系奥地利化学家K·J·Bayer 于1887 年发明的处理优质铝土矿制取氧化铝的一种方法。
拜耳法就是用含有大量游离苛性碱的循环母液处理铝土矿,溶出其中的氧化铝得到铝酸钠溶液,往铝酸钠溶液中添加氢氧化铝晶种,经过一定时间的搅拌分解就可以析出氢氧化铝,分解母液经蒸发后用于溶出下一批铝土矿。
拜耳法生产中经常用到苛性比、硅量指数、循环效率、晶种系数等概念。
拜耳法就是用碱溶出铝土矿中的氧化铝。
工业上把溶液中以NaAlO2 和NaOH 形式存在的Na2O 叫做苛性碱(记作Na2Ok),以Na2CO3 形式存在的Na2O 叫做碳酸碱(记作Na2Oc),以Na2CO4 形式存在的Na2O 叫做硫酸碱(记作Na2O),所有形态的碱的总和称做全碱(记作Na2Ot)。
苛性比就是铝酸钠溶液中的Na2Ok 与Al2O3 的摩尔比,记作αko。
美国习惯用铝酸钠溶液中的Al2O3 与Na2Ok 的质量比表示,符号A/N。
硅量指数指铝酸钠溶液中的Al2O3 与SiO2 含量的比,符号A/S。
循环效率指铝酸钠溶液中的1t Na2O 在一次拜耳法循环中产出的Al2O3 的量(t),用E 表示。
它表明碱的利用率的高低。
晶种系数(种子比)指添加晶种氢氧化铝中的Al2O3 数量与分解原液中的Al2O3 数量之比。
分解离指分解出氢氧化铝中的Al2O3 数量占精液中所含Al2O3 数量之比。
计算式为:η=(1-αa/αm)×100%式中αa,αm-分别表示分解精液和分解母液的苛性比值。
拜耳法生产包括四个过程:(1)用αk=3.4的分解母液溶出铝土矿中的氧化铝,使溶出液的αk=1.6~1.5;(2)稀释溶出液,洗涤分离出精制铝酸溶液(精液);(3)精液加晶种分解;(4)分解母液蒸发浓缩至苛性碱的浓度达到溶出要求(230~280g/L)。
拜耳法生产氧化铝的工艺流程如图1 所示。

目录第一章概述 (2)1、工艺流程描述 (2)2、工艺流程图 (4)3、全厂主要设备表 (6)第二章原料、燃料质量标准 (19)1、进场铝矿石质量要求 (19)2、进场石灰质量要求 (19)3.1、进场固体碱质量要求 (19)3.2、进场液体碱质量要求 (19)4、进场电媒质量要求 (19)5、进场气煤质量要求 (20)第三章产品质量标准 (20)3.1、氢氧化铝质量标准 (20)3.2、氧化铝质量标准 (20)第四章对动力的技术要求 (21)4.1、新蒸汽 (21)4.2、压缩空气 (21)4.3、新水 (21)第五章生产过程主要技术条件 (21)5.1、原料车间 (21)5.2、溶出车间 (22)5.3、沉降车间 (22)5.4、分解车间 (23)5.5、焙烧车间 (24)5.6、蒸发及排盐苛化 (24)5.7、热电站 (24)5.8、煤气站 (26)5.9、设备清洗用碱液和水的要求 (26)第六章主要技术经济指标 (26)6.1、氧化铝产品单耗 (26)6.2、蒸汽单耗 (27)6.3、煤气单耗 (27)6.4、氧化铝总回收率 (27)6.5、产品质量 (27)第七章环境保护 (27)第一章概述1、工艺流程描述1.1 原料车间由汽车运进厂的铝土矿经地磅站称重后和原矿堆场的铝土矿经破碎后一起倒入卸矿站,经胶带输送机送往均化堆场堆存,再经斗轮取料机、胶带输送机将铝土矿送往原料磨的磨头仓。
外购石灰由汽车运进厂,卸入石灰卸矿站,经胶带输送机送往石灰仓,一部分石灰通过胶带输送机送往原料磨磨头仓,另一部分石灰送往石灰消化工段。
在石灰消化工段,石灰与热水一同加入化灰机中,制备的石灰乳流进石灰乳槽,石灰乳用泵送往蒸发车间苛化工序和沉降车间控制过滤工序。
消化渣用胶带输送机送往的消化渣堆场,消化渣最终用汽车运到热电浓缩池一起外排到灰渣坝。
在原料磨工段,铝土矿、石灰及循环母液按比例加入原料磨中磨制原矿浆,原矿浆用水力漩流器进行分级,分级机溢流为合格的原矿浆,送入原矿浆槽,分级机底流返回原料磨。


拜耳法生产氧化铝工艺1。
拜耳法定义所谓“拜耳法”系奥地利化学家K。
J.Bayer于1887年发明的处理优质铝土矿制取氧化铝的一种方法。
100多年来它已经有了许多改进,但仍然习惯地沿用着拜耳法这个名词。
拜耳法在处理低硅铝土矿,特别是用在处理三水铝石型铝土矿时,流程简单,作业方便,产品质量高,其经济效果远非其它方法所能媲美。
目前全世界生产的Al2O3和Al(OH)3,有90%以上是用拜耳法生产的。
拜耳法包括两个主要过程,也就是拜耳提出的两项专利。
(1)一项是他发现Na2O和Al2O3分子比为1.8的铝酸钠溶液在常温下,只要添加Al(OH)3作晶种,不断搅拌,溶液中的Al2O3便可以呈Al(OH)3徐徐析出,直到其中Na2O和Al2O3 的分子比提高到6为止。
这也就是铝酸钠溶液的晶种分解过程。
(2)另一项是他发现,已经析出大部分Al(OH)3的溶液,在加热时,又可以溶出铝土矿中的Al2O3水合物,这也就是利用种分母液溶出铝土矿的过程。
交替使用这两个过程就能够一批批地处理铝土矿,从中得出纯的Al(OH)3产品,构成所谓拜耳法循环。
拜耳法的实质也可用下列反应来表示。
反应在不同条件下的交替进行:Al2O3(1或3)H2O+2NaOH+aq=2NaAl(OH)4+aq2拜耳法基本原理及适用范围2。
1基本原理:(l)用NaOH溶液溶出铝土矿,所得到的铝酸钠溶液在添加晶种、不断搅拌的条件下,溶液中的氧化铝呈氢氧化铝析出,即种分过程。
(2)分解得到的母液,经蒸发浓缩后在高温下可用来溶出新的铝土矿,即溶出过程。
2.2适用范围氧化铝的生产方法有拜耳法、烧结法、拜耳—烧结联合法三种.各种方法的适用范围为:(3)拜耳法:7<A/S;(4)烧结法:3~3.5<A/S〈5;(5)联合法:以拜耳法为主,以烧结法补其不足,处理中间品位的铝土矿。
其中,符号A/S 称为硅量指数,即铝酸钠溶液中的Al2O3与SiO2含量的比。

拜耳法生产氧化铝工艺设计计算拜耳法生产氧化铝工艺设计计算 1 目的与要求通过工艺设计计算,对氧化铝生产工艺工艺流程有更深入全面的了解,培养和训练学生具备解决复杂的工艺问题、管理氧化铝生产、进行物料平衡计算的能力。
在进行冶金计算之前,必须收集有关现场数据,以便于具体计算。
为了计算的方便,下面的物料平衡计算按生产1吨氧化铝为基准进行。
2 主要生产技术指标的选择01)产品为一级氧化铝(国标):含量不低于。
本设98.6AlO0230计取为。
99000) 2)铝土矿的化学组成(表1 铝土矿成分表AlOCOFeOSiOHOTiO成分其他合计附着水 232232220 067.40 11.08 5.45 4.20 10.77 0.52 0.58 100 0.9003)石灰的化学组成()表2 石灰石的成分表成分 AlOCOSiO 其他合计 CaO 2322087.56 3.8 3.27 5.19 0.18 100 0004)氧化铝实际溶出率:89.09,总回收率:87。
0005)石灰添加量占干铝土矿量的8。
06)碱耗: 53kg/t,AlO23补碱组成表3 补碱成分表NaONaOCO成分 2k2c2g/L 438.8 7.2 5.13密度=1440 kg/m7)循环母液的组成表4 循环母液的成分成分 NaOAlONaOCONaO2k232c22Tg/L 240 135.13 20 14.19 2603密度=1358 kg/m,,3K8)稀释后的铝酸钠溶液组成表 5 铝酸钠溶液成分成分 NaONaOCOAlO2k2c223g/L 160 181.52 11.04 7.833g/cm 密度=1315,,1.48K9)沉降分离底流,末次洗涤槽底流。
LS,3.0LS,1.010)弃赤泥液相中的含量(浓度):。
NaO2.25gL211)溶出后赤泥的,。
AS,1.35NS,0.3012) 溶出过程浓缩率:。
80013)晶种分解中种子比为3.0,种子附水率为,分离后氢18.00氧化铝浆液的。
第一章:设计任务书1、云南文山铝业有限公司铝土矿平均品位表1—1铝土矿的化学组成(%)2、石灰的化学组成(%)表1—2石灰的化学组成(%)3、设计年产能:80万吨砂状氧化铝4、设计生产工艺:拜耳法生产工艺第二章技术条件及经济指标2.1原料工序原料工序的技术条件和工艺指标如下表2-1。
表2-1 原料工序技术条件和工艺指标工艺条件技术指标Al2O3含量≥50%A/S(10天内平均波动)±0.2矿石块度≤30mm铝矿石附水率≤5%2.2溶出工序A)铝土矿的理论溶出率和实际溶出率Al2O3的理论溶出率:理论上矿石中可以溶出的Al2O3量(扣除不可避免的化学损失)与矿石中的Al2O3量之比称为Al2O3的理论溶出率(η理)。
Al2O3的实际溶出率:在溶出时,实际溶出的Al2O3量与矿石中的Al2O3量之比称为Al2O3的实际溶出率(η实)。
根据表1-1的数据,该铝土矿的铝硅比:A/S=55.22÷7.34=7.523,故理论溶出率:η理=ASA-×100%=22.5534.722.55-×100%= 86.708%实际溶出率:η实=矿赤矿)/ () /()/(SAS ASA-×100%=523.741 .1523.7-×100%=81.257%式中:η理——理论溶出率,%;η实——实际溶出率,%;Al2O3——铝矿石中Al2O3的百分含量,%;SiO2——铝矿石中SiO2的百分含量,%;(A/S)矿——铝矿石中的铝硅比;(A/S)赤——赤泥中的铝硅比;B)溶出温度温度是影响溶出过程最主要的因素。
随着温度的升高,氧化铝在碱溶液中的溶解度增大,溶出反应速度以及碱溶液与反应产物的扩散速度也增加,当其它溶出条件相同时,提高溶出温度总时使溶出速度加快,溶出设备产能显著提高。
本设计溶出温度定为280℃。
溶出温度对赤泥A/S 的影响如下图2-1。
图2-1溶出温度对赤泥A/S 的影响C )循环母液碱浓度及岢性比值[24]循环母液的岢性碱浓度愈高,其未饱和程度愈大,氧化铝溶出速度及产能越大,得到的溶出液岢性比值越低,碱的循环效率也越高。
氧化铝生产工艺及计算(总16页)--本页仅作为文档封面,使用时请直接删除即可----内页可以根据需求调整合适字体及大小--氧化铝生产工艺及计算第一章氧化铝生产方法简介氧化铝生产方法大致可分为四类,即碱法、酸法、酸碱联合法和热法。
但目前用于工业生产的几乎全属于碱法。
碱法生产氧化铝的基本过程如下:焙烧图1:碱法生产氧化铝基本过程碱法生产氧化铝又分为拜耳法、烧结法和联合法等多种流程。
拜耳法是直接用含有大量游离NaOH的循环母液处理铝矿石,以溶出其中的氧化铝而获得铝酸钠溶液,并用加晶种搅拌分解的方法,使溶液中的氧化铝以Al(OH)3状态结晶析出。
种分母液经蒸发后返回用于浸出另一批铝矿石。
矿石中的主要杂质SiO2是以水合铝硅酸钠(Na2O••••••Al2O3••nH2O)的形式进入赤泥,造成Al2O3和Na2O的损失。
因此,拜耳法适合处理高品位铝矿,铝硅比A/S大于9。
烧结法是将铝矿石配入石灰石(或石灰)、苏打(含有Na2CO3的碳分母液),在高温下烧结得到含固体铝酸钠的物料,用稀碱溶液溶出熟料便得到铝酸钠溶液。
经脱硅后的纯净铝酸钠溶液用碳酸2化分解法使溶液中的氧化铝呈Al(OH)3析出。
碳分母液经蒸发后返回用于配制生料浆。
矿石中的主要杂质SiO2是以原硅酸钙(2CaO•SiO2)的形式进入赤泥,不会造成Al2O3和Na2O的损失。
因此,烧结法适合处理高硅铝矿,铝硅比A/S可以为3-5。
拜耳-烧结联合法兼有拜耳法和烧结法流程,兼收了两个流程的优点,获得更好的经济效果。
它适合处理A/S为6-8的中等品位铝矿。
由于流程较复杂,只有生产规模较大时,采用联合法才是可行和有利的。
酸法是用硝酸、硫酸、盐酸等无机酸处理含铝原料而得到相应的铝盐的酸性水溶液。
然后使这些铝盐成水合物晶体(蒸发结晶)或碱式铝盐(水解结晶)从溶液中析出,亦可用碱中和这些铝盐的水溶液,成氢氧化铝析出,煅烧后得无水氧化铝。
酸法适合处理高硅低铁铝矿,如粘土、高岭土等。
拜耳法生产氧化铝工艺设计计算1 目的与要求通过工艺设计计算,对氧化铝生产工艺工艺流程有更深入全面的了解,培养和训练学生具备解决复杂的工艺问题、管理氧化铝生产、进行物料平衡计算的能力。
在进行冶金计算之前,必须收集有关现场数据,以便于具体计算。
为了计算的方便,下面的物料平衡计算按生产1吨氧化铝为基准进行。
2 主要生产技术指标的选择1)产品为一级氧化铝(国标):32O Al 含量 不低于006.98。
本设计取为0099。
2)铝土矿的化学组成(00)表1 铝土矿成分表 成分32O Al 32O Fe 2SiO 2TiO O H 22CO 其他 合计附着水67.40 11.08 5.45 4.2010.77 0.520.58100 0.93)石灰的化学组成(00)表2 石灰石的成分表成分CaO 32O Al 2SiO2CO 其他合计87.56 3.8 3.27 5.190.181004)氧化铝实际溶出率:0009.89,总回收率:0087。
5)石灰添加量占干铝土矿量的008。
6)碱耗:32/53O Al t kg 补碱组成表3 补碱成分表 成分k O Na 2 c O Na 22COL g /438.87.25.1密度=14403/m kg 7)循环母液的组成表4 循环母液的成分成分k O Na 232O Alc O Na 22COTO Na 2L g /240135.132014.19260密度=13583/m kg3=K α8)稀释后的铝酸钠溶液组成 表 5 铝酸钠溶液成分成分k O Na 232O Alc O Na 22COL g /160181.5211.047.83密度=13153/cm g 48.1=K α9)沉降分离底流0.3=S L ,末次洗涤槽底流0.1=S L 。
10)弃赤泥液相中O Na 2的含量(浓度):L g 25.2。
11)溶出后赤泥的35.1=S A , 3.0=S N 。
12) 溶出过程浓缩率:008。
13)晶种分解中种子比为3.0,种子附水率为000.18,分离后氢氧化铝浆液的0.1=S L 。
14)氢氧化铝洗涤水的消耗量为3)(0.1OH Al t t -,氢氧化铝滤饼的含水量为0010。
15)蒸发中,O H CO Na 232⋅带走的循环母液为湿沉淀质量的0050。
16)苛化时的石灰数量为化学反应计算量的00125,苛化率为0090。
17)苛化时碳酸钠-石灰浆夜得液相中含00210T O Na ,弃石灰渣中含水量0025。
3 物料平衡计算3.1 损失计算根据原始数据,该铝土矿的铝硅比37.12=S A ,故理论溶出率00000091.9110040.6745.540.67100=⨯-=⨯-=A S A 理η 实际溶出率00000009.8910040.6735.137.12100)()()(=⨯-=⨯-=矿赤矿理S A S A S A η因总回收率比实际溶出率低003~2,故本次设计的实际的总回收率取0087。
在氧化铝的产出率为0089的条件下,如果制取1吨含量为0099的成品氧化铝,则需要干铝土矿为:kg 32.1688)6740.089.0(990=⨯÷其中应含有氧化铝:kg 93.11376740.032.1688=⨯ 因而,氧化铝的总损失量:kg 93.14799093.1137=-其中,破碎及储存时氧化铝的损失量为生产一吨氧化铝所需总32O Al 量的003.0,即为:kg 41.393.11373.000=⨯相当于损失干铝土矿:kg 06.56740.041.3=÷则进入湿磨工序的干铝土矿:kg 26.168306.532.1688=- 干石灰添加量为kg 996.100626.168300=⨯湿磨过程中32O Al 的损失与破碎时相同,即有:kg 6.1123.0⨯,相当于干铝土矿为kg 06.527.6741.300=÷则送溶出的原矿浆矿石量为:kg 20.167806.526.1683=- 送溶出的铝土矿中,各成分含量如下表6:表6 送溶出的铝土矿成分成分 含量/kg 32O Al 11.1131674.020.1678=⨯ 32O Fe 94.18511.020.1678=⨯ 2SiO 46.91055.020.1678=⨯ 2TiO 48.70042.020.1678=⨯ 2CO 73.80052.020.1678=⨯O H 274.1801077.020.1678=⨯其它 73.90058.020.1678=⨯合计 1678.20 附着水1.15009.020.1678=⨯而送溶出的石灰成分见表 7:表7 送溶出的石灰化学成分成分含量/kgCaO43.888756.099.100=⨯ 2CO 24.50519.099.100=⨯ 32O Al84.3038.099.100=⨯ 2SiO30.30327.099.100=⨯ 其它 18.00018.099.100=⨯ 合计100.99需要补加的苛碱溶液体积为:312.0)2.78.438(53m =+÷ 质量为:kg 80.172144012.0=⨯ 则补碱溶液中各组分含量见表 8:表8 补碱溶液成分成分 含量/kgO Na 2 53 2CO61.012.01.5=⨯ O H 2(按差值计)75.11761.05336.171=--合计171.36溶出后赤泥的组成如表9:表9 赤泥成分成分含量/kg32O Al )35.1(93.12735.176.94==⨯S A 赤泥 O Na 2)3.0(43.283.076.94==⨯S N 赤泥32O Fe185.94 2SiO94.76 2TiO70.48 CaO88.43 其它 9.91不计灼碱的赤泥127.93+28.43+185.94+94.76+70.48+88.43+9.91=605.88灼碱的计算过程如下:1)若赤泥中的CaO 以O H TiO CaO 22⋅⋅的形式存在,那么248.70kgTiO 结合①CaO :kg 34.49568048.70=⨯ ② O H 2 kg 86.15188048.70=⨯ 2)若赤泥中剩余的CaO 以O H SiO O Al CaO 223263⋅⋅⋅的形式存在,那么kgCaO 09.3934.4943.88=-结合 ① 2S iO :kg 96.14603156/09.39=⨯⨯②O H 2:kg 13.2618256/09.39=⨯⨯3)若2S i O 在赤泥中以O H SiO O Al O Na 2232227.1⋅⋅⋅形式存在,那么28.7996.1476.94kgSiO =-结合O H 2:kg 77.27367.1/50/8.79=⨯4)若008.1的32O Fe 在赤泥中以)3()(2323O H O Fe OH Fe ⋅形式存在,则结合O H 2:kg 13.154150/018.094.185=⨯⨯由此可得灼碱为:80.7113.177.2713.2686.15=+++ 总赤泥量为kg 68.67780.7188.605=+若过程中水解造成氧化铝损失量为生产一吨氧化铝所需总32O Al 量的004.0,则水解损失320055.44.093.1137O kgAl =⨯,因此加上水解损失的氧化铝则赤泥总量应为kg 64.68454102/55.455.468.677=⨯++O Na 2的化学损失稍低于组成为O H SiO O Al O Na 2232222⋅⋅⋅时同239.71kgSiO 相结合的O Na 2,因为水和铝酸钠中有一部分O Na 2会被CaO 所取代。
由于洗涤不完全,故随赤泥损失的O Na 2为:kg 75.100255.00.164.684=⨯⨯上式中:1.0为末次洗涤槽底流S L ,2.55为弃赤泥液相中O Na 2的含量(g/L )。
根据以上计算,得出32O Al 和O Na 2的损失量表,见表10.表10 32O Al 和O Na 2的损失量损失项目 损失32O Al 占总量/00损失的氧化铝质量/kgO Na 2/kg 破碎及储存0.3 3.41 / 湿磨0.3 3.41 1.00 赤泥不溶解形式11.2127.93 28.43 赤泥溶解形式 0.33.2 1.75 水解0.48 4.55 / 分解0.065 0.715 8.60 蒸发及析出苏打0.121.32 6.08 石灰乳渣0.11 1.20 5.80 焙烧0.11 1.21 0.60 合计13 147.93 533.2 循环溶液计算分解过程氧化铝的分解率: 000067.500.348.1-11001==⨯-)(母原αα 因此,进入分解过程的铝酸钠溶液中32O Al 含量为:kg 25.19565067.0)23.1990(=÷+上式中:1.23为焙烧时损失的32O Al (见表10)。
如果分解过程中无机械损失,则留于母液中的32O Al 为:kg 49.99023.199025.1956=--如果考虑到32O Al 分解,蒸发和苏打苛化时的损失,则循环溶液中32O Al 为kg 19.98722.134.174.049.990=---当8.2=母α时,其所含的K O Na 2为kg 35.1800645.18.219.987=÷⨯ c O Na 2量为T O Na 2的008,即: 00002228100=⨯+K c cO Na O Na O Na则L g O Na O Na K C /2192824092822=⨯=⨯= 因此循环母液中2CO 含量为:kg 19.144462/21=⨯循环母液中32O Al 浓度为L g /60.1310.3/240645.1=⨯ 循环母液的体积为:35.724035.1800m =÷ 322/36.1001865.000142.00009.0)2()2(cm g N N A d C K NaOHNaOH=++++=ρρ上式中:NaOH ρ-O Na 2浓度与铝酸钠溶液中T O Na 2浓度相等的NaOH 溶液密度 L g /275.1: A-铝酸钠溶液中32O Al 浓度;K N -铝酸钠溶液中苛碱浓度;C N -铝酸钠溶液中碳碱浓度。
则循环母液的质量为:kg 1018513585.7=⨯ C O Na 2:kg 5.157215.7=⨯2CO :kg 77.11144625.157=⨯÷则O H 2:kg 19.71285.15777.11135.180019.98710185=---- 原矿浆量=铝土矿重量+石灰重量+补碱重量+循环母液 =11018536.17199.100)1.1520.1678(-++++ =kg 65.12149式中1—磨矿时O Na 2的损失,kg溶出时矿浆浓缩率为008,即浓缩水量为kg 97.971865.1214900=⨯根据上述计算得的数据引出高压溶出的平衡表如表11所示:表11 高压溶出平衡表进/kg 出/kg 铝土矿溶出浆液32O Al1131.11 32O Al 2121.14 32O Fe185.94 T O Na 22110.14 2SiO91.46 32O Fe185.94 2TiO70.48 2SiO94.76 2CO8.73 2TiO70.48 其它 9.73 CaO88.43 灼碱 180.74 2CO126.35 附着O H 2 15.1 其它 9.91 总计1693.29灼碱180.74 石灰O H 26289.07 CaO88.43 总计 11178.67 2CO 5.24 湿磨O Na 2的损失1 32O Al3.84 浓缩水量971.97 2SiO3.30其它0.18总计 100.99 苛性碱K O Na 2 52.15 c O Na 2 0.85 2CO0.61 O H 2117.75 总计171.36循环母液32O Al 987.19 K O Na 2 1800.35 c O Na 2 157.5 2CO111.77 O H 27128.19 总计 10185合计12150.6412150.643.3 浆液的稀释与沉降稀释后的赤泥浆液溶液中,K O Na 2浓度为L g /160,当45.1=K α时,其32O Al 浓度为:L g /52.18145.1645.1160=÷⨯当55.1=Tα时,c O Na 2浓度=L g /04.11160645.155.125.181=-⨯2CO 浓度=L g /83.74462037.11=⨯÷322/31.1001865.000142.00009.0)2()2(cm g N N A d C K NaOHNaOH=++++=ρρ上式中:NaOH ρ-O Na 2浓度与铝酸钠溶液中T O Na 2浓度相等的NaOH 溶液密度 ,L g /207.1: A-铝酸钠溶液中32O Al 浓度;K N -铝酸钠溶液中苛碱浓度;C N -铝酸钠溶液中碳碱浓度。