(方案)内镜下胃息肉切除术.doc
- 格式:doc
- 大小:56.00 KB
- 文档页数:6

临床路径在内镜下胃息肉切除术的应用研究的开题报告一、研究背景内镜下胃息肉切除术(Endoscopic submucosal dissection,ESD)是治疗消化道早期肿瘤、息肉和其他粘膜病变的根本性方法之一。
其治疗效果得到了广泛认可,但在操作过程中需对病人进行全身麻醉和局部麻醉,术中涉及到多个器械和步骤,手术时间长,术后疼痛和并发症风险较高。
因此,如何在手术中提高效率、减少并发症和术后疼痛成为临床研究的重要方向。
临床路径是对一种疾病的传统治疗过程进行全方位规划和管理的临床管理模式。
在内镜下胃息肉切除术中的临床路径可以大大提高患者的手术安全性、并发症发生率和手术后恢复质量,而且避免了过度治疗和无效治疗,提高了医疗资源利用效率。
因此开展内镜下胃息肉切除术的临床路径研究,对于提高手术效率、减少并发症和提高患者满意度具有重要意义。
二、研究目的本研究旨在探讨内镜下胃息肉切除术的临床路径优化对手术效果的影响,进一步提高手术效率和安全性,减少并发症和术后疼痛,提高患者满意度。
三、研究内容(一)研究对象选取行内镜下胃息肉切除术治疗的患者作为研究对象,排除合并其他重要疾病的患者。
(二)研究方法1.资料收集:对该类患者的临床数据进行统计和整理,包括患者年龄、性别、患者病史、内镜病理学分型、手术方式、术后并发症等,以了解临床路径优化对该类患者手术效果的影响。
2.画出内镜下胃息肉切除术的临床路径:根据手术过程的顺序,对整个治疗过程进行系统规划和安排。
3.实施优化后的临床路径:在医疗院内设立内镜下胃息肉切除术的临床路径,实施旨在提高手术效率和安全性、减少术后疼痛和并发症的优化措施。
4.比较和分析:比较实施临床路径前后的治疗效果,包括手术时间、术中出血量、并发症发生率、术后疼痛和患者满意度,评价实施临床路径的临床价值。
(三)研究进展设计合理的临床路径,提高了内镜下胃息肉切除术的手术效率和安全性,在术后并发症率和手术后疼痛程度方面表现优异,尤其能提高患者的满意度。


内镜下消化道息肉切除术的术中配合摘要】目的讨论内镜下上消化道息肉切除术的术中配合。
方法配合治疗进行护理。
结论电切息肉中的配合:护士应严格按照术者指示进行操作。
首先根据息肉蒂的粗细或广基息肉基底的直径设定电切、电凝指数及决定是否设定混合电流。
然后送入圈套器,随时按术者的指示伸出、回缩、张开、收紧圈套器协助完成电切。
食管贲门、十二指肠部位壁薄、蠕动快,圈套息肉时需与术者密切配合,尽量套进息肉近端,否则易引起穿孔。
【关键词】内镜下上消化道息肉切除术术中配合消化道息肉是临床常见的良性肿瘤,病理组织学上以腺瘤常见且有一定的癌变率,属癌前病变。
随着内镜技术的广泛应用,人们对消化道息肉的认识也不断提高,特别对于广基息肉,为消除隐患更应及早治疗。
内镜下息肉切除术是在内镜直视下借助各种辅助设备和配件切除息肉,不仅有治疗作用,更具有诊断价值。
内镜下上消化道息肉切除术是一种创伤小、方法简便、安全有效的优选治疗方法。
它具有操作方便,定位准确,成功率高,可及时观察和局部镜下处理术中出血等优点,避免了患者开刀的痛苦,损伤小,恢复快,同时也节约了住院费用。
1 临床资料一般资料本组患者12例,其中男性6例,女性6例,年龄18~68岁。
其中食道息肉2例,胃息肉6例,结肠息肉3例,直肠息肉1例。
均采用电子胃镜或者电子肠镜进行电切术。
全部病人手术成功。
2 物品准备2.1 内镜。
2.2 一般胃镜检查的常规设备。
2.3 基本器械高频电发生器、电缆线、把手、圈套器(无齿、带齿及各种型号根据息肉形态选择)是内镜下套切息肉中必不可少的。
2.4 其他相关的或止血的附件高频电凝探头、热探头、透明帽、热活检钳、注射针、止血钛夹等。
为了使手术顺利进行和及时处理并发症,这些都是应该准备好的。
2.5 回收息肉的附件三爪钳、网篮等。
2.6 药物去甲肾上腺素、肾上腺素、生理盐水、浓氯化钠等。
3 术前准备3.1内镜准备3.2圈套器准备3.3高频电发生器的准备3.4患者准备3.4.1 了解患者病情包括既往史及治疗情况,嘱患者把既往内镜及X线检查结果带来,了解息肉的部位、大小及形态,以便选择适当的内镜及圈套器。
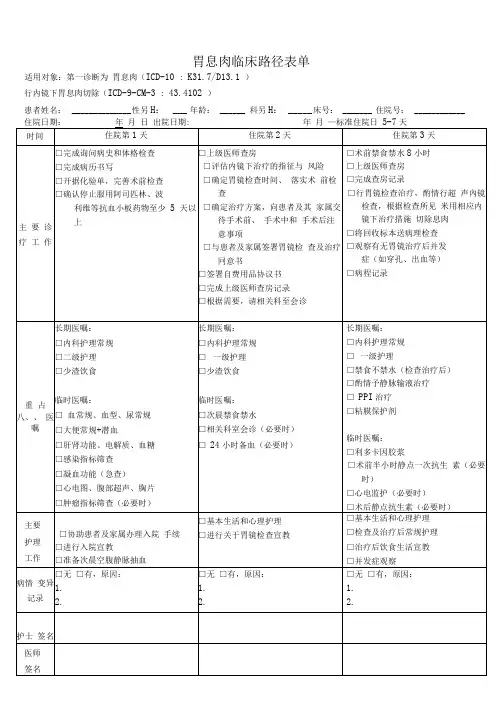
胃息肉临床路径表单适用对象:第一诊断为胃息肉(ICD-10 : K31.7/D13.1 )行内镜下胃息肉切除(ICD-9-CM-3 : 43.4102 )患者姓名:______________ 性另H:___ 年龄:______ 科另H:_____ 床号:_______ 住院号:____________临床路径告知单(胃息肉)患者或亲属签字: _________________ 经治医师签字:______________________________________ 年 ____ 月_____ 日XXXXXXXXXXX)医院胃息肉临床路径内镜下胃息肉切除术临床路径标准住院流程(一)适用对象。
第一诊断为胃息肉(ICD-10:K31.7/D13.1 )。
行内镜下胃息肉切除术(ICD-9-CM-3:43.4102 )。
(二)诊断依据。
根据《实用内科学》(复旦大学医学院编著,人民卫生出版社,2005年9月,第12 版)、《消化内镜学》(李益农、陆星华主编,科学出版社,2004年4月,第2版)等国内、外临床、内镜诊断及治疗指南。
1.胃镜发现胃息肉。
2.钡餐造影检查发现充盈缺损,提示胃息肉。
(三)治疗方案的选择。
根据《实用内科学》(复旦大学医学院编著,人民卫生出版社,2005年9月,第12版)、《消化内镜学》(李益农、陆星华主编,科学出版社,2004年4月,第2版)等国内、外临床、内镜诊断及治疗指南。
1.内科基本治疗(包括生活方式、饮食等)。
2.内镜下治疗。
(四)标准住院日为5 -7天。
(五)进入临床路径标准。
1.第一诊断必须符合ICD-10:K31.7/D13.1 胃息肉疾病编码。
2.符合胃息肉内镜下切除适应证。
3.当患者同时具有其他疾病诊断时,但住院期间不需要特殊处理,也不影响第一诊断的临床路径流程实施时,可以进入路径。
(六)住院期间检查项目。
1.必需的检查项目:(1 )血常规、血型及Rh 因子;(2 )尿常规;(3 )大便常规+潜血;(4 )肝肾功能、电解质、血糖;(5)感染指标筛查(乙型、丙型肝炎病毒、HIV、梅毒);(6 )凝血功能;(7)心电图、腹部超声、胸片。

胃息肉治疗方案1. 胃息肉的定义和类型胃息肉是指胃黏膜局部隆起形成的肿块,可分为以下几种类型:1.腺瘤性息肉:由于胃黏膜腺体增生而形成的息肉,可分为炎性腺瘤性息肉、腺瘤样息肉和腺瘤息肉等不同类型。
2.内襞上皮性息肉:由胃黏膜上皮增生而形成的息肉。
3.异位胃黏膜性息肉:由于异位胃黏膜的存在而形成的息肉,常见的异位胃黏膜有食道黏膜、肠黏膜和胃底黏膜等。
4.浆液囊肿性息肉:由于胃黏膜浆液囊肿形成的息肉。
2. 胃息肉治疗原则胃息肉的治疗目标是彻底切除或控制其生长,防止恶变和症状的加重。
治疗方案应依据息肉的类型、大小、数量、位置、症状等因素进行个体化制定。
一般的治疗原则包括以下几点:1.彻底切除:对于可切除的息肉,应采取手术、内镜下切除或腔内微创手术等方法进行切除,以确保肿块完全去除,减少复发的可能。
2.监测复发:对于具有复发倾向的胃息肉,应定期进行内镜检查,及时发现和处理再次出现的肿块。
3.症状缓解:针对引起症状的胃息肉,可以采取药物治疗、消化道支持治疗等方法进行症状缓解,改善患者的生活质量。
4.恶性变异预防:对于具有恶性变异的胃息肉(如腺瘤性息肉),应密切关注其变异的情况,必要时采取手术或其他治疗手段进行处理。
3. 胃息肉治疗方法3.1 内镜下切除内镜下切除是治疗胃息肉的主要方法之一,通常适用于直径小于2cm的胃息肉。
内镜下切除包括以下几种技术:•切除术:将胃息肉直接切除,并采取各种方式进行止血(如电凝、钳夹等)。
•假扩张术:通过将气体灌入胃腔,使胃黏膜平面上抬,方便切除胃息肉。
•热凝术:利用高频电凝或氩气凝固来切除胃息肉。
•冷冻疗法:使用液态氮或其他冷冻装置,冷冻胃息肉并切除。
•激光烧灼术:采用激光烧灼来切除胃息肉。
3.2 药物治疗胃息肉的药物治疗主要用于缓解炎症、减少胃酸分泌和控制胃息肉生长。
常用的药物包括:•质子泵抑制剂:用于减少胃酸的分泌,保护胃黏膜。
•抗生素:用于控制胃息肉炎症的发生和发展。

胃esd切除标准全文共四篇示例,供读者参考第一篇示例:胃ESD切除是目前治疗早期胃癌和胃息肉的一种有效方法,其在准确诊断和治疗上具有显著优势。
ESD全称为内镜下粘膜切除术(Endoscopic Submucosal Dissection),是一种微创手术技术,可以在不开腹的情况下,通过内窥镜将粘膜肿瘤或息肉完整地切除。
那么,胃ESD切除的适应症是什么呢?适应症包括表面型和隐窝型早期胃癌,即T1a和T1b期病变;适应症还包括直径小于2cm的良性粘膜肿瘤和持续性不变的低级别上皮内瘤变。
对于那些无法通过EMR或手术切除的大型或难以切除的病变,也可以考虑采用ESD切除。
对于胃ESD切除术的操作者来说,其具有一定的技术挑战性,因为需要在内窥镜下进行较为复杂的操作。
在进行ESD切除前,需要进行详细的术前评估,包括肿瘤的大小、位置、形态等,以及术中的镜下观察和处理技术。
在术中应特别注意以下几个方面:一是保持良好的视野,保证切除的完整性和安全性;二是准确切除肿瘤的边缘,避免肿瘤残留;三是控制出血和穿孔的风险,及时处理并避免并发症的发生。
术后,患者需要接受一定的后续治疗和随访。
一般来说,患者需要定期复查内镜,以监测切除部位的愈合情况和发现复发的可能。
患者还需在术后遵守饮食调理和生活方式改变,以预防病情的进一步恶化。
ESD切除虽然是一种微创手术,但对操作者和患者都提出了一定的挑战,需要慎重操作和持续的随访管理。
胃ESD切除作为治疗早期胃癌和胃息肉的一种标准方法,具有显著的优势和应用前景。
通过合理的术前评估、精准的手术操作和细致的术后管理,可以最大限度地提高手术的成功率,减少并发症的发生,从而使患者获得更好的治疗效果和生存质量。
随着技术的不断进步和经验的积累,相信胃ESD切除会在未来的临床实践中发挥更加重要的作用,造福更多需要此项治疗的患者。
第二篇示例:胃ESD(内镜下黏膜切除术)是一种微创手术,用于治疗早期胃癌和其他胃部疾病。

胃息肉治疗方案摘要胃息肉是一种常见的胃部肿瘤病变,可能会引发消化道出血、溃疡和恶变等严重并发症。
本文通过综合分析胃息肉的病因、病理特点和临床表现,探讨了常见的胃息肉治疗方案,包括内镜下治疗、手术治疗和药物治疗等,并对各种治疗方法的适应症和优缺点进行了详细介绍。
1. 胃息肉的病因和病理特点胃息肉是指胃黏膜上的良性病变,其病因与遗传、饮食、环境等因素有关。
常见的胃息肉类型包括息肉状胃炎、颗粒状息肉、息肉样腺瘤等。
不同类型的胃息肉在病理特点上也有所不同。
2. 胃息肉的临床表现胃息肉的临床表现多样,包括上腹疼痛、消化不良、呕吐、黑便等。
有些患者可能无明显症状,仅在体检或内镜检查中发现。
3. 胃息肉的诊断胃息肉的诊断主要依靠内镜检查和病理检查。
内镜检查可观察到胃黏膜上的息肉病变,通过活检可明确病理类型。
4. 胃息肉的治疗方案4.1 内镜下治疗内镜下治疗是目前常用的胃息肉治疗方法之一,主要包括切除、电凝和消融等。
内镜下切除是将胃息肉与黏膜分离并切除的方法,适用于直径较小的息肉。
电凝是利用电热加热或高频电流杀死胃息肉细胞,常用于颗粒状息肉的治疗。
消融是通过冷冻或热蒸汽等方式破坏胃息肉组织,适用于较大的息肉。
4.2 手术治疗对于直径较大的息肉或出血、溃疡、恶变等严重并发症的胃息肉,手术治疗是更有效的选择。
手术治疗包括开腹手术和腔镜手术两种,根据实际情况选择合适的手术方式。
4.3 药物治疗药物治疗主要针对具有刺激性活性的胃息肉,如胃酸分泌过多的胃息肉。
常用的药物包括质子泵抑制剂、抗酸剂和抗生素等。
药物治疗适合直径较小、无明显症状的胃息肉。
5. 治疗方案的选择选择合适的治疗方案取决于胃息肉的类型、大小、位置、临床表现和患者的整体状况。
对于直径较小、无症状的胃息肉,内镜下治疗和药物治疗是较为合适的选择。
对于直径较大、临床表现明显的胃息肉,手术治疗可能更为有效。
治疗过程中需密切监测患者病情,并随时调整治疗方案。
结论胃息肉是一种常见的胃部肿瘤病变,治疗方案的选择需根据胃息肉的病理特点和临床表现。

治疗胃息肉的最佳方法
胃息肉是胃黏膜上的良性病变,治疗方法主要包括药物治疗、内镜治疗和手术治疗。
1. 药物治疗:对于小型、无症状的胃息肉,可以采用药物治疗来缓解症状和预防病变进展。
常用的药物包括抗酸药,如质子泵抑制剂,可以降低胃酸分泌,减少息肉的刺激和炎症反应。
另外,还可以使用抗生素药物,如替硝唑和克林霉素等,用于治疗与幽门螺杆菌感染相关的胃息肉。
2. 内镜治疗:对于较大、具有出血风险或可疑恶性变的息肉,可以采用内镜切除术进行治疗。
内镜切除术通过内镜将切除器械送入胃腔,直接切除息肉或进行电凝止血。
常用的内镜治疗方法包括内镜下黏膜剥除术(EMR)和内镜下微创手术(ESD),这些方法可以有效切除息肉并减少复发风险。
3. 手术治疗:对于较大、合并恶性变的息肉,或者内镜治疗失败的患者,需要考虑手术治疗。
手术治疗主要通过开腹手术或腹腔镜手术进行,将整个病变的胃部切除,并进行组织病理学检查,以确保完全切除病变。
总之,治疗胃息肉的最佳方法应根据患者的具体情况来确定,对于大部分小型胃息肉,药物治疗和内镜治疗是较为常用的方法,而手术治疗主要适用于大型胃息肉或合并恶性变的情况。
对于任何治疗方法,患者应密切关注病情变化,定期进行复查和随访。


内镜下息肉电凝电切术操作规范1、目标:内镜下高频电刀诊疗消化道息肉2、适应症:经内镜下确诊为消化道息肉;禁忌症:严重心脏病患者;已安装心脏起搏器患者;有出血倾向患者。
3、仪器:日本产Olympus-70型电子胃镜. Olympus-V70型电子肠镜ERBEIcc80高频电发生器、电凝切圈套器、活检钳、内镜注射针等.4、术前准备全部病例术前检验血Rt ,肝功、凝血酶原时间、ECG、胃息肉常规胃镜检验,肠息肉使用硫酸镁清洁肠道(禁用甘露醇)。
5、操作方法插入内镜找到息肉后,依据息肉大小和有没有蒂来决定手术方法,由助手帮助插入圈套器或活检钳,对直径小于0.5厘米息肉,通常采取活检钳咬除或电凝灼除,使息肉发白,电凝指数为1.2、通电时间为3-4秒即可。
直径小于2厘米亚蒂或无蒂息肉,多采取圈套+电凝切除法;圈套器钢丝在息肉基底稍上方为息肉切除最好部位,或在基底部注射盐水,使形成蒂,再切除;有蒂息肉采取圈套器+电凝切除法,尽可能保留残蒂1厘米左右长;直径大于2厘米无蒂息肉可采取圈套器法,但需先将高渗盐水或1:10000肾上腺素溶液在息肉基底部粘膜下注射2-4 点,每点0.5-1毫升,然后再行圈套电凝切除;凝切指数均为30-35,先行电凝再行电切,每次凝切时间均为3-4秒。
大息肉也可分块分期切除,2-3周后行第二次切除。
切除息肉用异物钳或经活检孔负压吸引连同内镜一块拔出后送病理检验。
6、并发症及注意事项一、消化道息肉出血是最常见并发症,迟发性出血是指发生于术后二十四小时出血,文件报道迟发性出血发生率为1%-2%,常见原因因为操作者经验不足相关,迟发性出血原因和下列原因相关(1)、电凝不充足,电凝指数过小或电凝时间不足;(2)、电凝过分,电凝指数过高或电凝时间过长使创面过大过深,结痂脱落后出血;(3)、套切不根本,残蒂过长;(4)、套切面在大血管处;(5)、患者血管弹性差,PT降低;(6)、创面继发感染;(7)、术后患者饮食运动未严格控制。

内镜下高频电切术治疗胃息肉503例临床应用体会【摘要】目的:总结内镜下高频电切术治疗胃息肉的临床应用体会。
方法:回顾性分析503例内镜下高频电切术治疗胃息肉患者资料。
结果:治疗503例共978 粒息肉,活检钳或圈套一次性完整摘除893粒,另85粒需要分次切除。
术后出现腹痛19例,呕吐7例,畏寒6例,经对症治疗后症状消失,术后无胃出血、胃穿孔发生。
结论:内镜下高频电切术治疗胃息肉是一种安全、创伤小、痛苦少、恢复快、并发症少、疗效确切的治疗方法。
【关键词】内镜;高频电切;胃息肉【中图分类号】r735 【文献标识码】b 【文章编号】1004-7484(2012)07-0352-01胃息肉是指呈单发性或多发性的胃黏膜隆起,病变局限在黏膜和黏膜下层,是胃黏膜上皮细胞的一种增生性病变,临床表现无特异性,主要症状以上腹疼痛、腹胀等多见,是较常见的胃良性肿瘤,但也有人认为其是胃的癌前病变。
胃息肉的治疗方法较多,疗效各异。
我院从2006年2月起采用内镜下高频电切治疗胃息肉503例,取得较好效果,现报告如下。
1 资料与方法1.1 临床资料2006年2月至2012年3月,在本院进行胃镜检查患者5743例,503例胃镜下诊断为胃息肉,其中男270例,女233例,年龄20~73岁,平均( 39.23 ±4.68) 岁。
患者无典型临床症状,多数表现为上腹不适、恶心、呕吐、上腹部闷痛、腹胀、嗳气、纳差等慢性胃炎症状,少数可有呕血、黑便。
1.2 治疗方法1.2.1 治疗仪器日本奥林巴斯(olmpus evis-v)电子胃镜、高频电发生器和电圈套器、活检钳、抓钳。
1.2.2 治疗方法与常规胃镜检查要求相同,术前常规查血常规和出凝血时间,排除高血压或心脏病,45岁以上者常规进行心电图检查。
术前禁食水12 h ,术前半小时肌注阿托品0.5 mg,鲁米那100 mg,按常规胃镜进镜到胃部,先观察胃各部位病变情况和息肉粒数、分布、大小、部位、息肉是否有水肿、充血、糜烂、溃疡、是有蒂或无蒂。
胃息肉切除的标准主要取决于息肉的大小、数量、位置以及患者的具体情况。
一般来说,以下几种情况下可能需要考虑进行胃息肉切除手术:
1. 息肉较大:如果息肉的直径超过2cm,可能会对胃部造成较大的压力,引发不适症状。
在这种情况下,切除息肉可以减轻症状,防止息肉进一步增大。
2. 息肉数量较多:如果患者的胃部存在多个息肉,可能会影响胃部的正常功能。
为了保障患者的健康,医生会根据息肉的数量和位置进行手术切除。
3. 息肉生长位置:位于贲门、幽门附近或者容易出血的息肉需要手术切除。
这些部位发生息肉可能会引起一系列并发症,如出血、梗阻等,严重影响患者的健康和生活质量。
4. 考虑癌变风险:对于有恶变风险的息肉,如腺瘤性息肉、增生性息肉等,需要尽早切除,以防止癌变的发生。
在手术过程中,医生通常会采用内镜下切除或手术切除两种方式。
内镜下切除是一种微创手术,通过胃镜将息肉从根部夹住,然后切除。
这种手术方法具有创伤小、恢复快等优点,是目前胃息肉切除术的主要方式。
手术切除则是在全身麻醉下,通过腹部切口进行息肉切除。
这种方式适用于息肉较大、数量较多或存在恶变风险的病例。
需要注意的是,胃息肉切除手术并不是简单的操作,具有一定的风险和并发症。
如术中出血、穿孔、感染等。
因此,患者在决定进行手术前应充分了解手术风险,并与医生进行沟通。
同时,患者在术后应遵医嘱进行护理,定期复查,以防止息肉的复发。
总的来说,胃息肉切除的标准需要根据具体情况而定,患者如有疑虑,应及时就医,听从医生的建议。
胃镜下息肉切除术80例病例分析目的分析探讨胃镜下息肉切除术在胃息肉、十二指肠球部息肉治疗中的临床应用价值。
方法回顾2010年~2013年胃息肉切除病例80例临床资料,结合近年来文献资料,综述胃镜下息肉切除术的新进展。
结果一次性完全切除74例(92.5%);分两次手术6例(7.5%)。
重度不典型增生9例(11.25%),中度不典型增生19例(23.75%),单纯腺瘤21例(26.25%),非腺瘤性息肉31例(38.75%)。
术前病理与术后病理对照相符者71例,占88.75%,不相符者占12.25%。
所有病例均未发生大出血或穿孔等严重并发症,有14例切除后出现少量渗血。
结论内镜下黏膜切除术已经成为一项成熟、安全的技术方法。
标签:胃镜;胃息肉;切除术随着胃镜检查的广泛开展,镜下息肉的检出率也随之升高,胃镜下息肉切除术目前已成为国内外广泛开展的治疗胃、十二指肠息肉的的方法。
常用的方法有电凝电切、圈套器、氩气刀、热活检钳等等,许多医院开展了无痛苦胃镜下息肉切除,使用异丙酚联合瑞芬太尼麻醉[1,2],大大减轻了患者的痛苦。
现收集我院2010年~2013年胃息肉切除病例80例资料,报道操作体会并结合今年来文献资料展开综述。
1资料与方法1.1一般资料病例选择均符合下列条件:①息肉直径小于3cm;②病理证实为非肿瘤性增生。
其中,男性47例,女性33例,年龄22~71岁,平均年龄45岁;多发性息肉35例(43.75%),单发息肉45例(56.25)。
炎性息肉19例(23.75%),增生型息肉28例(35%),腺瘤33例(41.25%)。
1.2器械电子胃镜:日本富士99型;高频电刀:氩气刀:圈套器:1.3方法术前常规进行胃镜检查,并取活检送病理检查,癌变者除外。
术前查血常规、凝血四项,有凝血异常的患者给内科治疗,至出凝血时间正常[3]。
签署手术治疗同意书,禁食8h[4],准备8%去甲肾上腺素溶液、钛夹等止血用品。
对于情绪紧张的患者可给予少量镇静剂、阿托品,并给予适当解释和安慰[3]。
胃息肉的治疗方法
胃息肉的治疗方法通常根据息肉的性质和大小来决定。
常见的治疗方法包括:
1. 观察和随访:对于小型息肉,尤其是良性息肉,如果没有任何不适症状,医生可能会建议观察和随访,定期复查胃镜检查来评估息肉的生长变化。
2. 冻融治疗:冻融治疗是一种常见的治疗方法,通过利用低温冷冻或高温热灼烧来消融和切除息肉组织。
3. 切除手术:对于较大的息肉,或者有明显症状(如出血、溃疡)的息肉,常常需要通过手术切除。
4. 内镜下黏膜剥离术:对于表面平坦、无蒂的息肉,内镜下黏膜剥离术是一种有效的治疗方法。
通过内镜下操作,将息肉隆起剥离到正常黏膜下。
5. 放射治疗:对于恶性息肉或复杂的息肉情况,放射治疗可能会作为辅助治疗方法。
需要注意的是,不同类型的息肉可能需要不同的治疗方法,因此治疗方案应由医生根据患者具体情况来制定。
同时,治疗结束后需要定期随访,以监测息肉的复发情况。
胃息肉内镜下切除术护理常规一.定义胃息肉是指胃黏膜面突出的一种赘生物,包括增生性、炎症性、错构瘤、腺瘤及其他肿瘤等。
胃息肉内镜下切除术是通过胃镜进行的一种安全有效的微创手术,具有患者痛苦轻、创伤少、并发症少、操作简单、术后康复快等优点。
二.症状体征本病早期或无并发症时多无症状。
出现症状时常表现为上腹隐痛、腹胀不适,少数可出现恶心、呕吐。
合并糜烂或溃疡者可有上消化道出血,多表现为粪潜血试验阳性或黑便,呕血少见。
位于幽门部的带蒂息肉,可脱入幽门管或十二指肠,而出现幽门梗阻的表现。
息肉生长于贲门附近时可有吞咽困难。
三.护理问题(一)出血危险与胃息肉切除有关。
(二)跌倒的危险与中深度镇静有关。
(三)知识缺乏缺乏疾病相关知识。
四.护理措施(一)休息/体位病室环境保持整洁、舒适、安静,空气新鲜。
卧床休息,避免劳累。
(二)术前护理前一天禁止吸烟,以免检查时因咳嗽影响插管;禁烟还可减少胃酸分泌,便于医生观察。
检查前至少要空腹 8 小时以上。
重症及体质虚弱禁食后体力难以支持者,检查前应适当补液。
做胃镜检查前必须做心电图、血常规、凝血常规、感染性指标检查。
向医生讲明药物过敏史。
与医生要合作,检查前病人先排出小便,进入检查室后,松开领口及裤带,取下假牙及眼镜,取左侧卧位,或根据需要改用其他体位。
入镜后,不能用牙齿咬镜,以防咬破镜身的塑管。
身体及头部不能转动,以防损坏镜子并伤害内脏。
如有不适情况,病人忍耐一段时间,实在不能忍受,可用手势向施术者示意,以便采取必要措施。
接受钡餐检查三日内不宜做胃镜检查,以免影响观察。
口服阿司匹林、华法林等药物时一周内不宜做胃镜下治疗。
(三)术后护理术后禁食。
如无不适反应,次日可给适量流质饮食,50ml~80ml/次。
第 3 日给全量流质,每次 100~150ml。
每日 6~7 餐,饮食原则为:食物无刺激性,呈液性,少食多餐,每 2~3 小时进食一次,宜选不宜胀气,不过甜的食物,如鸡蛋汤、米汤、菜汤、藕粉等。
内镜下胃息肉切除术临床路径
(2011年版)
一、内镜下胃息肉切除术临床路径标准住院流程
(一)适用对象。
第一诊断为胃息肉(ICD-10:K31.7/D13.1)。
行内镜下胃息肉切除术(ICD-9-CM-3:43.4102)。
(二)诊断依据。
根据《实用内科学》(复旦大学医学院编著,人民卫生出版社,2005年9月,第12版)、《消化内镜学》(李益农、陆星华主编,科学出版社,2004年4月,第2版)等国内、外临床、内镜诊断及治疗指南。
1.胃镜发现胃息肉。
2.钡餐造影检查发现充盈缺损,提示胃息肉。
(三)治疗方案的选择。
根据《实用内科学》(复旦大学医学院编著,人民卫生出版社,2005年9月,第12版)、《消化内镜学》(李益农、陆星华主编,科学出版社,2004年4月,第2版)等国内、外临床、内镜诊断及治疗指南。
1.内科基本治疗(包括生活方式、饮食等)。
2.内镜下治疗。
(四)标准住院日为5–7天。
(五)进入临床路径标准。
1.第一诊断必须符合ICD-10:K31.7/D13.1胃息肉疾病编码。
2.符合胃息肉内镜下切除适应证。
3.当患者同时具有其他疾病诊断时,但住院期间不需要特殊处理,也不影响第一诊断的临床路径流程实施时,可以进入路径。
(六)住院期间检查项目。
1.必需的检查项目:
(1)血常规、血型及Rh因子;
(2)尿常规;
(3)大便常规+潜血;
(4)肝肾功能、电解质、血糖;
(5)感染指标筛查(乙型、丙型肝炎病毒、HIV、梅毒);
(6)凝血功能;
(7)心电图、腹部超声、胸片。
2.根据患者情况可选择的检查项目:
(1)消化道肿瘤指标筛查(CA199、CA242、CEA等);
(2)超声内镜;
(3)结肠镜检查。
(七)内镜下治疗为住院后第3天。
1.术前完成胃镜检查和治疗同意书。
2.可使用镇静或麻醉药:术中需监测生命体征,术后要在内镜室观察至清醒后返回病房。
3.按顺序进行常规胃镜检查。
4.根据术中所见息肉形态、大小、数目等决定内镜下治疗方案并按胃息肉内镜治疗规范实施治疗,围手术期采用适当措施避免可能的治疗并发症。
5.抗血小板药物停用5天或以上。
6.尽可能回收切除标本送病理检查。
7.术后密切观察病情,及时发现并处理可能的并发症。
(八)选择用药。
1.使用抑酸剂(如PPI/H2RA)。
2.用粘膜保护剂。
3.必要时抗生素。
(九)出院标准。
1.无出血、穿孔、感染等并发症。
2.患者一般情况允许。
(十)变异及原因分析。
1.患者年龄小于18岁,或大于65岁者,进入特殊人群临床路径。
2.具有胃镜操作禁忌证的患者进入特殊人群临床路径:如心肺等重要脏器功能障碍及凝血功能障碍,有精神疾患不能配合者,上消化道穿孔的急性期或消化道手术的围手术
期,严重咽喉部疾患内镜不能插入,腐蚀性食管损伤的急性期等。
3.应用影响血小板及凝血功能药物者,进入特殊人群临床路径。
4.息肉不符合内镜治疗指征,或患者存在内镜治疗禁忌证,出院或转外科,进入胃肿瘤外科治疗临床路径。
5.合并急性消化道大出血,进入消化道出血临床路径,进行内镜下止血,必要转外科手术。
6.合并感染,需要继续抗感染治疗,进入消化道感染临床路径。
7.合并消化道穿孔,转外科手术,进入相应临床路径。
8.病理提示恶性,转外科手术,进入其他路径。
9.多发息肉、大息肉或复杂情况:多发大于3枚,或息肉直径≥2cm或广基息肉或粗蒂息肉(蒂直径≥1cm)。
二、内镜下胃息肉切除术临床路径表单
适用对象:第一诊断为胃息肉(ICD-10:K31.7/D13.1)
行内镜下胃息肉切除(ICD-9-CM-3:43.4102)
患者姓名:性别:年龄:门诊号:住院号:。