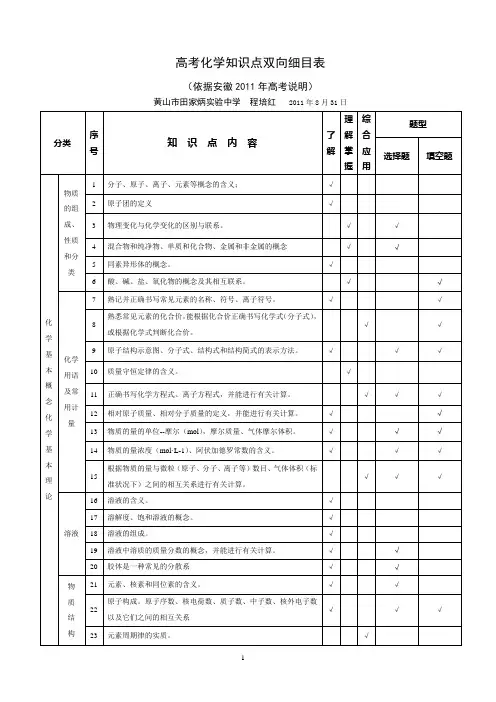
高考化学知识点双向细目表
- 格式:doc
- 大小:243.00 KB
- 文档页数:5


高中化学必修1双向细目表
高中化学必修2双向细目表
高一历史人教版必修二知识细目表
中国史(一、三、四、五单元)
第一单元古代中国经济的基本结构与特点
第三单元近代中国经济结构的变动与资本主义的曲折发展
第四单元中国特色社会主义建设的道路
第五单元中国近现代社会生活的变迁
世界史(二、六、七、八单元)
第二单元资本主义世界市场的形成和发展
第六单元世界资本主义经济政策的调整
第七单元苏联的社会主义建设
第八单元世界经济的全球化趋势
高一历史必修二教学进度表
2021-----2021学年第二学期高一化学教学进度表。

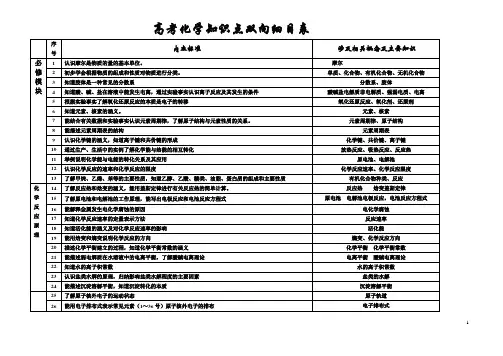
高一化学必修双向细目表1. 化学基础知识- 原子结构和元素周期表- 化学键和化合物的分类- 化学反应和化学方程式- 酸碱中和和中性化学反应- 物质的状态变化和相变- 化学量和化学计算- 元素周期表中的主要元素和其特性- 元素的周期性和趋势- 物质的分子结构和化学键的类型2. 化学实验技能- 实验室安全和实验室设备的使用- 常用实验方法和仪器的操作- 实验数据的记录和处理- 实验结果的分析和解释- 实验原理和实验设计3. 化学反应与能量变化- 化学反应的能量变化- 燃烧反应和氧化还原反应- 酸碱中和反应和热化学方程式- 粒子间的引力作用和化学反应的速率- 化学反应的平衡和平衡常数- 溶液中的溶解度和溶液的浓度4. 化学物质的构成与结构- 元素和化合物的构成- 原子和分子的结构- 组成物质的化学键- 元素周期表中元素的结构特性- 金属和非金属元素的性质- 化合物的分子结构和性质- 傅里叶光谱和分子结构分析5. 化学周期律与离子反应- 元素周期表和周期律规律- 同一周期和同一族的元素特性- 阴离子与阳离子的结构和特性- 离子反应的性质和反应方程式- 酸碱反应和生成离子的化学方程式- 离子溶液中的电离反应和电导率6. 环境与持续发展化学- 化学物质对环境的影响- 大气污染和水污染的原因和防治- 可持续发展和绿色化学的概念- 环境友好的化学产品和过程- 生物质资源的利用和能源转化- 化学垃圾处理和废物回收利用的方法7. 高分子物质与生物化学- 高分子物质的结构和性质- 聚合反应与高分子合成- 塑料和纤维的生产和应用- 生物大分子的结构和功能- 生物有机物的合成和代谢- 酶的催化作用和生物化学反应以上是高一化学必修双向细目表的主要内容。
这份文档包含了学习该科目所需的基础知识、实验技能以及各个单元的重点内容。
希望能对你的学习和备考有所帮助。

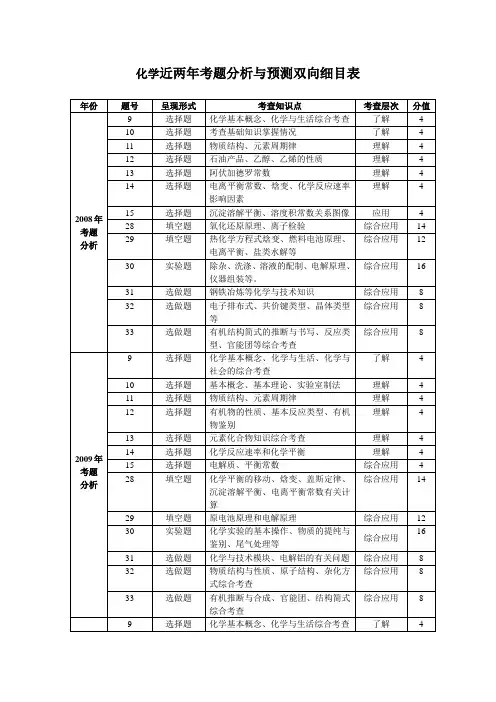
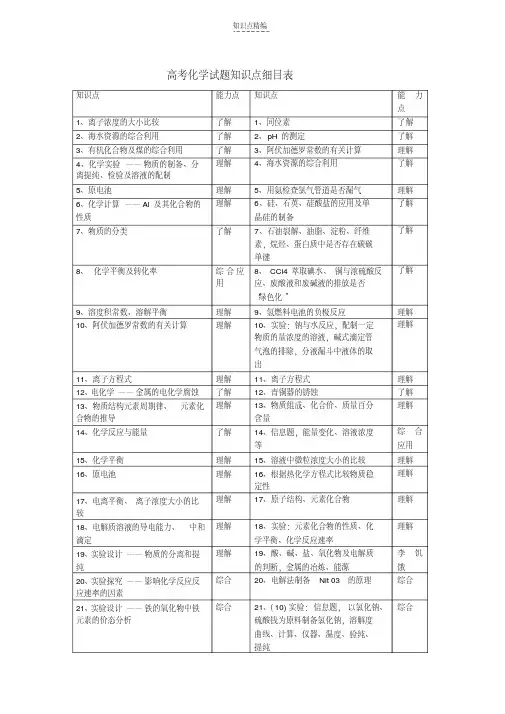
化学近两年考题分析与预测双向细目表
重点分析与思考:
1.三年都考查的知识点有:物质的量浓度,氧化还原反应,离子方程式的书写,化学基本操作,物质的检验、分离和提纯,常见物质的实验室制法,化学键,盖斯定律,原电池工作原理,平衡常数,弱电解质的电离平衡,盐类水解,铁及其化合物,铜及其化合物,氯气,二氧化硫与硫酸,环境污染与环境保护,石油、煤的加工,乙醇、乙酸的性质,以“mol”为核心的换算(含N A)。
2.近三年未考查的主干知识点有:等效平衡,烷烃的取代反应
3.近年考查的热点知识有:电离常数的计算,杂化轨道,金属的腐蚀
4.新考纲增加的知识点有:沉淀转化的本质,有机物的同分异构现象,有机反应类型,电负性,杂化轨道类型,推测简单分子或离子的空间结构
5.分析学生(特别是目标生)缺漏的知识点有:金属的腐蚀,杂化轨道类型判断,电离常数的计算
6.下段复习重点有:物质的量、氧化还原反应、物质结构与元素周期表、热化学、电化学、化学平衡、电解质溶液、常见金属元素及化合物、常见非金属元素及化合物、化学基本实验原理及操作、化学基本计算、有机化学基础知识等这些主干知识。
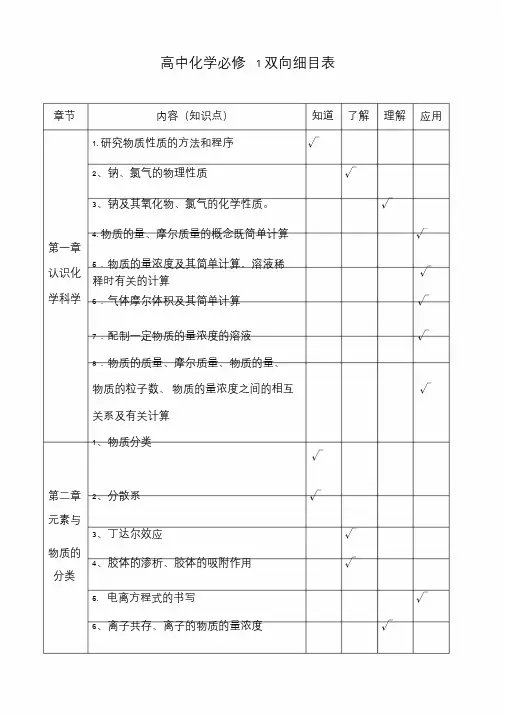
高中化学必修 1 双向细目表章节内容(知识点)知道了解理解应用1. 研究物质性质的方法和程序√2、钠、氯气的物理性质√3、钠及其氧化物、氯气的化学性质。
√第一章4. 物质的量、摩尔质量的概念既简单计算√认识化5.物质的量浓度及其简单计算,溶液稀释时有关的计算√学科学6.气体摩尔体积及其简单计算√7.配制一定物质的量浓度的溶液√8.物质的质量、摩尔质量、物质的量、物质的粒子数、物质的量浓度之间的相互√关系及有关计算1、物质分类√第二章2、分散系√元素与3、丁达尔效应√物质的分类4、胶体的渗析、胶体的吸附作用√5. 电离方程式的书写√6、离子共存、离子的物质的量浓度√7、Cl - 、SO2- 、CO2- 的检验方法√4 38.氧化还原反应、氧化、还原、氧化剂、√ 还原剂等概念9.简单的氧化还原反应方程式的配平、√标出电子转移的方向和数目1、同素异形体的概念,√2、碳酸钠和碳酸氢钠的主要性质。
√3、碳单质、一氧化碳、二氧化碳、碳酸√ 盐、碳酸氢盐之间的转化。
4.自然界中的氮循环及人类活动对氮循第三章√环的影响;自然界5、生物固氮和人工固氮形式,认识N2 、中的元√NO 、NO2 的性质;素6、NH3 性质及制取、铵盐的性质及铵态氮√ 肥的使用问题;7、HNO3 的性质。
√8、硫的主要性质;√9、不同价态硫元素之间的相互转化√10、二氧化硫和浓硫酸的主要性质。
√11、硫及其化合物在生产中的应用及酸雨√ 的危害12、镁单质的还原性和重要用途。
√13、氯、溴、碘单质的氧化性和氧化性递变顺序及溴单质和溴的化合物的重要用√途。
14、海水中微量元素的存在和应用及在工业生产和高科技领域的潜在价值,认识到√综合开发利用海水化学资源的重要意义。
1、硅的存在及用途。
√2、二氧化硅的物理、化学性质及其用途。
√3、硅酸的性质(弱酸性、水溶性、硅胶√第四章的吸水性)及制备方法。
元素与材4.硅酸钠(Na2SiO3)的性质、用途。
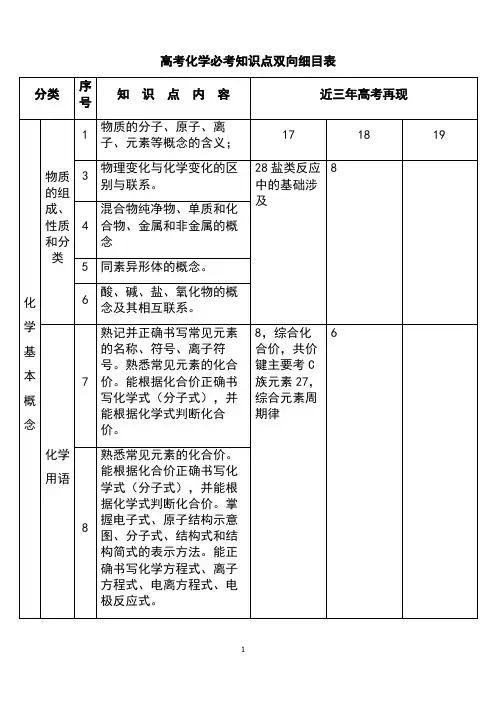
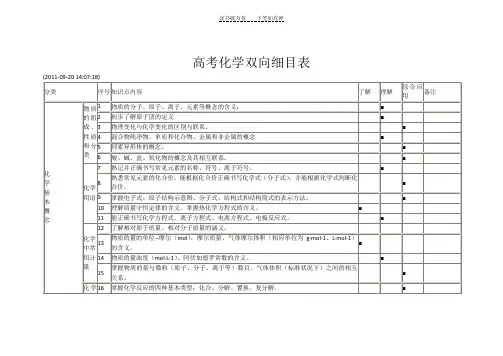
高中化学双向细目表高考化学双向细目表分类序号知识点内容1 物质的组成、性质和分类2 化学基本概念3 物质的分子、原子、离子、元素等概念的含义;初步了解原子团的定义4 物理变化与化学变化的区别与联系5 混合物、纯净物、单质和化合物、金属和非金属的概念6 同素异形体的概念7 酸、碱、盐、氧化物的概念及其相互联系8 熟记并正确书写常见元素的名称、符号、离子符号9 熟悉常见元素的化合价;能根据化合价正确书写化学式(分子式),并能根据化学式判断化合价10 掌握电子式、原子结构示意图、分子式、结构式和结构简式的表示方法;理解质量守恒定律的含义;掌握热化学方程式的含义11 能正确书写化学方程式、离子方程式、电离方程式、电极反应式12 了解相对原子质量、相对分子质量的涵义13 掌握物质的量的单位--摩尔(mol),摩尔质量、气体摩尔体积(相应单位为g·mol-1、L·mol-1)的含义14 物质的量浓度(mol·L-1)、阿伏加德罗常数的含义15 掌握物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)之间的相互关系16 掌握化学反应的四种基本类型:化合、分解、置换、复分解17 理解氧化还原反应,了解氧化剂和还原剂等概念;掌握重要氧化剂、还原剂之间的常见反应18 能判断氧化还原反应中电子转移的方向和数目,并能配平反应方程式19 了解化学反应中的能量变化,吸热反应、放热反应、反应热、燃烧热和中和热及新能源的开发等概念20 了解溶液的涵义21 了解溶液的组成,理解溶质的质量分数的概念22 了解饱和溶液、不饱和溶液的概念;了解溶解度的概念;了解温度对溶解度的影响及溶解度曲线23 初步了解结晶、结晶水、结晶水合物、风化、潮解的概念24 了解胶体的概念及其重要性质和应用25 了解原子的组成及同位素的概念26 掌握原子序数、核电荷数、质子数、中子数、核外电子数,以及质量数与质子数、中子数之间的相互关系注:综合应用部分不在此表中列出。
(原创2023)化学高考双向细目表一、无机化学1. 元素和化合物- 1.1 元素周期表- 1.2 常见元素的性质和应用- 1.3 水和溶液中的离子反应- 1.4 化合物的命名和化学式2. 化学反应- 2.1 燃烧反应- 2.2 氧化还原反应- 2.3 酸碱中和反应- 2.4 沉淀反应- 2.5 气体生成和反应3. 化学原理- 3.1 序列化反应和电位差- 3.2 动态平衡和平衡常数- 3.3 反应速率和速率常数- 3.4 催化剂和化学反应速率二、有机化学1. 有机化合物- 1.1 碳的特性和共价键- 1.2 烃类化合物- 1.3 醇、酚、醚类化合物- 1.4 醛、酮、羧酸类化合物- 1.5 氨基酸和蛋白质2. 有机反应- 2.1 烃类的燃烧反应- 2.2 单官能团化合物的反应- 2.3 多官能团化合物的反应- 2.4 聚合反应和聚合物的合成- 2.5 脂肪酸和酯的反应3. 有机化学原理- 3.1 反应机理和反应路径- 3.2 功能团和化学性质- 3.3 离子和自由基反应- 3.4 共轭系统和共轭反应三、化学实验1. 基本实验操作- 1.1 实验室安全和实验室常识- 1.2 仪器使用和实验操作技巧- 1.3 实验记录和数据处理2. 实验现象和解释- 2.1 气体生成与气体收集- 2.2 溶液中的颜色变化- 2.3 岩石和矿石的检验- 2.4 酸碱中和和中和滴定- 2.5 电解质的电导性实验3. 实验设计和控制变量- 3.1 实验变量和实验因素- 3.2 实验设计和实验步骤- 3.3 实验结果的误差和精度- 3.4 实验报告的撰写和结论以上为高考化学学科的双向细目表,其中包含了无机化学、有机化学和化学实验三个部分的细分内容。
学生可以根据这份细目表来进行有针对性的学习和复习,以便在高考中取得好成绩。