初三化学上学期元素及元素符号-P
- 格式:pdf
- 大小:479.92 KB
- 文档页数:8

九年级化学元素符号
同学,那九年级化学的元素符号可有意思啦。
首先是氢,符号是H,你就想啊,“氢”这个字读音有点像“轻”,氢气很轻嘛,所以是H,简单好记。
氧呢,符号是O,氧气是我们呼吸离不开的,你看这个O,就像一个小嘴巴在呼吸一样。
碳是C,“碳”字的拼音开头就是C呀,而且碳可是组成很多东西的重要元素呢,像我们的铅笔芯主要就是石墨,它是碳的一种形式。
氮是N,氮气在空气中占了很大比例,这个N就像一道闪电,氮元素在自然界中的转化就像闪电那样充满神奇的变化。
钠是Na,这个有点特别,你可以联想一下“那”这个字的拼音,然后稍微变一变就成Na啦,钠可是很活泼的金属元素哦。
镁是Mg,“镁”字有个“美”,就想象镁燃烧的时候发出耀眼的白光,可美了,Mg就是它的符号。
铝是Al,铝制品在我们生活中很常见,你就记这个Al,读起来也很顺口。
硅是Si,硅可是在计算机芯片等高科技产品里很重要的元素,这个Si就像两个小字母凑在一起,很独特。
磷是P,磷有白磷和红磷,这个P就像一个小旗在飘扬,磷在燃烧的时候也很有特点呢。
硫是S,这个S就像弯弯的小蛇,硫也有特殊的气味,就像小蛇一样有点神秘的感觉。
氯是Cl,氯气是黄绿色的气体,这个Cl就像两个小伙伴靠在一起,氯在消毒等方面有很大作用。
钾是K,这个有点特殊,不过你多记几遍就好啦,钾在人体里也很重要呢。
钙是Ca,“钙”字的拼音里有Ca的音,钙对我们的骨骼生长可重要啦,就像建筑的骨架一样。

磷的化学元素-概述说明以及解释1.引言1.1 概述磷是化学元素周期表中的第15号元素,化学符号为P。
它是地球上最常见的元素之一,广泛存在于矿石、土壤、植物和动物体内。
磷在生物体中扮演着重要的角色,是生命体系中的必需元素之一,参与着DNA、RNA、ATP等生物分子的合成,对细胞的结构和功能起着重要作用。
本文将对磷的性质、用途和存在形式进行深入探讨,探讨其在各个领域的重要性。
同时,我们将讨论磷资源的可持续性问题,以及展望未来磷的发展趋势。
通过阐述磷的化学特性和应用价值,希望能够增进对磷这一重要元素的认识,促进其在可持续发展中的合理利用和保护。
1.2 文章结构文章结构部分应该包括对整篇长文的章节安排和内容概述,以便读者能够清晰地了解文章的组织结构和主要内容。
具体内容可以是:文章结构部分将主要分为引言、正文和结论三个部分。
在引言部分中,将简要介绍磷元素的重要性以及本文的目的和意义。
在正文部分,将详细探讨磷的性质、用途和存在形式,为读者提供全面的了解。
最后,在结论部分总结磷元素的重要性,讨论其资源可持续性,并展望未来磷元素的发展方向,以期为磷元素的研究和应用提供一定的参考和启示。
整篇文章的章节安排和内容概述将在文章结构部分中得到详细介绍。
1.3 目的目的部分的内容是为了明确本文撰写的目的和意义。
本文的目的是深入探讨磷这一化学元素的性质、用途和存在形式,了解磷在生活和工业领域的重要性,并探讨磷资源的可持续性以及展望未来磷的发展方向。
通过本文的撰写,旨在帮助读者更全面地了解磷这一元素的重要性,促进对磷资源的合理利用与保护,为未来磷资源的可持续发展提供参考和借鉴。
2.正文2.1 磷的性质磷是一种非金属元素,在化学元素周期表中的原子序数为15,原子量为30.97。
磷在常温常压下是一种白色固体,有两种常见的同素异形体,即红磷和白磷。
红磷是一种暗红色的粉末状物质,稳定性较高,常被用作阻燃剂和橡胶添加剂。
白磷是一种有毒的、可燃的固体,能在空气中燃烧发出荧光。




20个必记:氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷硫氯氩钾钙(5个一记会好记点)一、实验操作1、粉末状药品的取用粉末药品药匙取,也可倒在纸槽里;横放试管送底部,直立试管落到低。
或:一斜二送三直立。
2、块状药品的取用块状药品镊子夹,绝对不能手来拿;横持试管把药放,慢慢竖起向下滑。
或:一横二放三慢竖。
3、液体药品的取用取下瓶塞倒放桌,标签朝心右手握;口口紧挨要倾斜,倒完液体原处搁。
4、液体药品的量取量筒平放实验桌,先倒后滴至刻度;平视凹液最低处,三线一齐为读数。
或:一倒二滴三读数。
5、用滴管取用药品轻拿滴管胶头处,手捏滴管橡胶头;垂直滴入容器中,切忌管头触器口。
或:两管直立,莫触内壁;滴管悬空,滴入正中。
6、托盘天平的使用天平用前调零点,左物右码记心间;砝码要用镊子夹,由大到小顺序拿;一般药品垫纸称,腐蚀药品杯中放;称完天平要复原,游码移回到零点。
或:一放平、二调零,三加砝码四进行;砝码要用镊子取,左物右码须记清。
7、酒精灯的使用酒精不能燃着加,对火可能危险发;酒精灯焰分三层,外焰温度为最大;熄灯要用灯帽盖,切记嘴吹酿火灾;万一失火燃起来,抹布立刻来扑盖。
8、试管中的固体加热药品斜铺试管底,受热均匀面积大;管口略比管底低,防水倒流试管炸;试管夹持中上部,根据外焰定高度;均匀预热试管后,集中外焰把热加。
9、试管中的液体加热加热常用试管夹,夹在试管中上部;试管加液三分一,药液体积不超它;移动试管预热前,应把外壁水擦干;管口不朝你我他,四十五度为最佳。
10、仪器的洗涤一般容器用水洗,内壁附物用刷洗;壁内若有不溶物,盐酸溶碱纯碱脂;仪器洗净有标准,水不成股不聚滴。
二、前二十种元素氢氦锂铍硼,碳氮氧氟氖;钠镁铝硅磷,硫氯氩钾钙。
三、常见元素的化合价(一)钾钠银氢正一价,钙镁钡锌正二价;一二铜汞二三铁,三铝四硅五氮磷;二四六硫二四碳,金正非负单质零。
(二)一价钾钠银氢氟,二价钙镁和钡锌;铝价正三氧负二,以上价态要记真;铜一二来铁二三,碳硅二四要记全;硫显负二正四六,负三正五氮和磷;氯价通常显负一,还有正价一五七;锰显正价二四六,最高价数也是七。


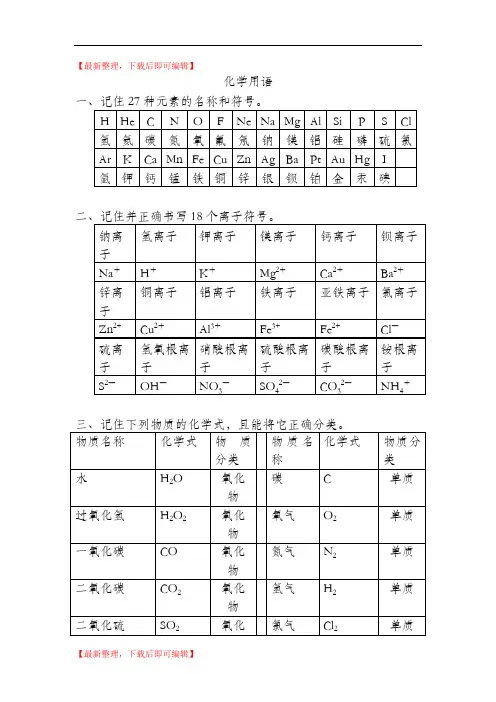
【最新整理,下载后即可编辑】化学用语四、记住下列反应的化学方程式。
1.木炭在空气中充分燃烧C+O2CO22.硫在空气中燃烧S+O2SO23.红磷在空气中燃烧4P+5O22P2O54.铁在氧气中燃烧3Fe +2O2Fe3O4点燃点燃点燃点燃5. 镁带在空气中燃烧2 Mg +O 2 2MgO 6. 铝在空气中被氧化 4Al +3O 2 =2Al 2O 37. 铜在空气中加热(现象:红色固体变黑) 2Cu+O 22CuO 8. 氢气在空气里燃烧2H 2 +O 2 2H 2O 9. 碳在空气中不充分燃烧 2C+O 2 2CO10. 一氧化碳燃烧2CO+O 2 2CO 211. 甲烷燃烧CH 4 +2O 2 CO 2 +2H 2O 12. 乙醇燃烧C 2H 5OH +3O 2 2CO 2 +3H 2O13. 实验室用过氧化氢和二氧化锰的混合物制氧气 2 H 2O 2 2H 2O +O 2 ↑14. 实验室用加热氯酸钾和二氧化锰的混合物制氧气2 KClO 32 KCl +3O 2 ↑ 15. 实验室用加热高锰酸钾的方法制氧气 2KMnO 4 K 2MnO 4 +MnO 2+O 2 ↑16. 实验室用大理石(或石灰石)与稀盐酸反应制二氧化碳气体 CaCO 3 +2HCl =CaCl 2 +H 2O +CO 2 ↑ 17. 实验室用锌粒与稀硫酸反应来制氢气 Zn +H 2SO 4 =ZnSO 4 +H 2 ↑ 18. 水通电分解2H 2O 2H 2↑+O 2↑ 19. 氢气还原氧化铜 H 2+CuO Cu +H 2O 20. 碳还原氧化铜MnO 2 MnO 2△通电 高温点燃点燃 点燃 点燃点燃 点燃C+2CuO 2 Cu +CO 2 ↑ 21. 碳还原氧化铁3C+2Fe 2O 3 4Fe +3CO 2 ↑ 22. 碳还原二氧化碳C+CO 2 2CO23. 一氧化碳还原氧化铁(炼铁原理)3CO +Fe 2O 3 2 Fe +3CO 2 24. 一氧化碳还原氧化铜 CO +CuO Cu +CO 2 25. 二氧化碳通入澄清的石灰水CO 2 +Ca(OH)2 =CaCO 3 ↓+H 2O 26. 二氧化碳与水反应 CO 2 +H 2O =H 2CO 3 27. 碳酸分解H 2CO 3 =H 2O +CO 2 ↑ 28. 碳酸钙高温分解 CaCO 3 CaO +CO 2 ↑ 29. 铁丝伸入硫酸铜溶液中 Fe +CuSO 4 = FeSO 4 +Cu30. 金属与盐酸(或稀硫酸)反应Mg +2HCl =MgCl 2 +H 2 ↑ Mg+H 2SO 4=MgSO 4 +H 2 ↑ Zn +2HCl =ZnCl 2 +H 2 ↑ Zn+H 2SO 4=ZnSO 4 +H 2 ↑ Fe +2HCl =FeCl 2 +H 2 ↑ Fe +H 2SO 4 =FeSO 4 +H 2 ↑ 31. 金属氧化物与盐酸(或稀硫酸)反应 Fe 2O 3+6HCl=2FeCl 3+3H 2O Fe 2O 3+3H 2SO 4=Fe 2(SO 4)3+3H 2OCuO+2HCl=CuCl 2+H 2O CuO+H 2SO 4=CuSO 4+H 2O 32. 碱与酸发生中和反应NaOH+HCl=NaCl+H 2O 2NaOH+H 2SO 4=Na 2SO 4+2H 2O Ca(OH)2+2HCl=CaCl 2+2H 2O高温高温 高温高温33. 碳酸钠中加入稀盐酸Na 2CO 3 +2HCl =2NaCl +H 2O +CO 2 ↑ (CO 32― 的检验) 34. 非金属氧化物与碱反应CO 2+2NaOH=Na 2CO 3+H 2O SO 2+2NaOH=Na 2SO 3+H 2O 35. 盐与碱反应Ca(OH)2+Na 2CO 3=CaCO 3↓+2NaOH2NaOH +CuSO 4 =Cu(OH)2↓+Na 2SO 4 (氢氧化铜是蓝色沉淀)3NaOH+FeCl 3=Fe(OH)3↓+3NaCl (氢氧化铁是红褐色沉淀)36. 盐与盐反应AgNO 3+NaCl=AgCl ↓+NaNO 3 (Cl ―的检验)Ba(NO 3)2+Na 2SO 4=BaSO 4↓+2NaNO 3 (SO 42― 的检验) Ba(NO 3)2+Na 2CO 3=BaCO 3 ↓+2NaNO 3 (BaCO 3 溶于稀硝酸)。

初三化学上册必背知识点(精华)-初中化学上册必背知识点一、化学用语1、前二十号元素、符号及其原子序数:氢(H)、氦(He)、锂(Li)、铍(Be)、硼(B)、碳(C)、氮(N)、氧(O)、氟(F)、氖(Ne)、钠(Na)、镁(Mg)、铝(Al)、硅(Si)、磷(P)、硫(S)、氯(Cl)、氩(Ar)、钾(K)、钙(Ca)2、常见元素及原子团的名称和符号非金属:O氧、H氢、N氮、Cl氯、C碳、P磷、S硫金属:K钾、Ca钙、Na钠、Mg镁、Al铝、Zn锌、Fe铁、Cu铜、Hg汞、Ag银、Mn锰、Ba钡原子团(根):氢氧根、硝酸根、碳酸根、硫酸根、磷酸根、铵根3、化合价口诀1).常见单质化合价:钾钠银氢正一价、钙镁钡锌正二价、氟氯溴碘负一价、铝三、硅四、氧负二、铜有一二、铁二三、单质零价要牢记2).常见原子团化合价:一价铵根、氢氧根、另外还有硝酸根、二价硫酸、碳酸根、三价只有磷酸根、除了铵根皆为负、常用须记住3)熟练默写常见元素的常用的化合价:K、Na、H、Ag、Ca2、Ba2、Mg2、Zn2、Cu2、+1价、+2价、+++NH4、Hg2、亚Fe2、-1价Cl、OH、NO3、---、++++++++++3价Fe3、Al3+、-2价O2、S2、CO32、SO42----、-3价PO43-4、必须熟记的常见物质的俗称、化学名称、化学式、用途俗称 | 化学名称 | 化学式 | 用途 |金刚石、石墨、木炭等 | 碳单质 | C | 金刚石做钻头、切割玻璃;石墨做铅笔芯、电极 |水银 | 汞 | Hg | 温度计 |干冰 | 二氧化碳固体 | CO2 | 致冷剂 |水 | 水 | H2O | 最常见溶剂 |双氧水 | 过氧化氢 | H2O2 | 消毒剂 |铁锈 | 氧化铁 | Fe2O3 | 除铁锈 |生石灰 | 氧化钙 | CaO | 熟石灰、消石灰(澄清石灰水)氢氧化钙 |石灰石 | 碳酸钙 | CaCO3 | 建筑材料、制水泥 |盐酸 | 氢氯酸(氯化氢) | HCl | |天然气、沼气、瓦斯 | 甲烷 | CH4 | 燃料 |酒精 | 乙醇 | C2H5OH | 燃料、乙醇汽油 |5、必须熟记的制取物质的化学方程式1)实验室制取氧气2KMnO4 === K2MnO4 + MnO2 + O2实验室制取氧气的方法有三种:第一种是2H2O2→2H2O+O2,第二种是2KClO3→2KCl+3O2,第三种是XXX制取氢气的方法有两种:一种是Zn+H2SO4→ZnSO4+H2,另一种是电解水,2H2O→2H2+O2.湿法炼铜术是通过铁置换出铜,Fe+CuSO4→FeSO4+Cu。

氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷硫氯氩钾钙氢H 氦He 锂Li 铍Be 硼B 碳C 氮N 氧O 氟F 氖Ne 钠Na 镁Mg 铝Al 硅Si 磷P 硫S 氯Cl 氩Ar 钾K 钙Ca序号元素名称符号1 铬Cr 铌Nb 铝Pb2 镍Ni 钽Ta 铋Bi3 硅Si 氢H 锕Ac4 锰Mn 碳C 铈Ce5 铝Al 氧O 铍Be6 磷P 钠Na 铯Se7 钨W 镁Mg 锆Zr8 钼Mo 硫S 镧La9 钒V 氯Cl 钡Ba10 钛T 钾K 汞Hg11 铜Cu 锌Zn 钙Ca12 铁Fe 银Ag 碘I13 硼B 锡Sn 溴Br14 钴Co 锑Sb 氟F15 氮N 金Au 烯土Re1 铬铌铝2 镍钽铋3 硅氢锕4 锰碳铈5 铝氧铍6 磷钠铯7 钨镁锆8 钼硫镧9 钒氯钡10 钛钾汞11 铜锌钙12 铁银碘13 硼锡溴14 钴锑氟15 氮金烯土常用化学元素符号表序号元素名称符号1 Cr Nb Pb2 Ni Ta Bi3 Si H Ac4 Mn C Ce5 Al O Be6 P Na Se7 W Mg Zr8 Mo S La9 V Cl Ba10 T K Hg11 Cu Zn Ca12 Fe Ag I13 B Sn Br14 Co Sb F15 N Au Re初中化学基础知识总结和常用口诀一、物质的学名、俗名及化学式⑴金刚石、石墨:C⑵水银、汞:Hg(3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2(5)盐酸、氢氯酸:HCl(6)亚硫酸:H2SO3(7)氢硫酸:H2S(8)熟石灰、消石灰:Ca(OH)2(9)苛性钠、火碱、烧碱:NaOH(10)纯碱:Na2CO3 碳酸钠晶体、纯碱晶体:Na2CO3·10H2O(11)碳酸氢钠、酸式碳酸钠:NaHCO3 (也叫小苏打)(12)胆矾、蓝矾、硫酸铜晶体:CuSO4·5H2O(13)铜绿、孔雀石:Cu2(OH)2CO3(分解生成三种氧化物的物质)(14)甲醇:CH3OH 有毒、失明、死亡(15)酒精、乙醇:C2H5OH(16)醋酸、乙酸(16.6℃冰醋酸)CH3COOH(CH3COO- 醋酸根离子)具有酸的通性(17)氨气:NH3 (碱性气体)(18)氨水、一水合氨:NH3·H2O(为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19)亚硝酸钠:NaNO2 (工业用盐、有毒)。
初中化学上册必背知识点一、化学用语1、常见元素及原子团的名称和符号非金属:O氧H氢N氮Cl氯C碳P磷S硫金属:K钾Ca钙Na钠Mg镁Al铝Zn锌Fe铁Cu铜Hg汞Ag银Mn锰Ba钡原子团(根):氢氧根硝酸根碳酸根硫酸根磷酸根铵根OH-NO3-CO32-SO4 2-PO43-NH4+2、化合价口诀(1) 常见元素化合价口诀:一价氢氯钾钠银;二价氧钙钡镁锌;三五氮磷三价铝;铜汞一二铁二三;二、四、六硫四价碳; 许多元素有变价,条件不同价不同.(2) 常见原子团(根)化学价口诀:一价硝酸氢氧根;二价硫酸碳酸根;三价常见磷酸根;通常负价除铵根。
4、必须熟记的制取物质的化学方程式(1)实验室制取氧气一:2KMnO4===K2MnO4+MnO2+O2↑(2)实验室制取氧气二:2H2O2 ===2H2O+O2↑(3)实验室制取氧气三: 2KClO3===2KCl+3O2↑(4)实验室制法CO2:CaCO3+2HCl==CaCl2+H2O+CO2↑(5)实验室制取氢气:Zn+H2SO4==ZnSO4+H2↑(6)电解水制取氢气:2H2O===2H2↑+O2↑(7)湿法炼铜术(铁置换出铜):Fe+CuSO4==FeSO4+Cu(8)炼铁原理:3CO+Fe2O3===2Fe+3CO2(9)生灰水[Ca(OH)2 ]的制取方法:CaO+H2O==Ca(OH)2(10)生石灰(氧化钙)制取方法:CaCO3 ===CaO+CO2↑二.金属活动性顺序:金属活动性由强至弱:K Ca Na Mg Al ,Zn Fe Sn Pb (H),Cu Hg Ag Pt Au。
(按5个一句顺序背诵)钾钙钠镁铝,锌铁锡铅(氢),铜汞银铂金。
三、常见物质的颜色、状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态),除了有颜色的固体,其他固体一般为白色。