微课:化学方程式的配平之定一法
- 格式:ppt
- 大小:1.87 MB
- 文档页数:6

化学方程式配平方法总结化学方程式配平方法总结第一篇找到化学方程式中关键的化学式,定其化学式前计量数为1,然后依据关键化学式去配平其他化学式前的化学计量数。
若出现计量数为分数,再将各计量数同乘以同一整数,化分数为整数,这种先定关键化学式计量数为1的配平方法,称为归一法。
例如:甲醇(ch3oh)燃烧化学方程式配平可采纳此法:ch3oh+o2――h2o+co2,明显决定生成h2o与co2的多少的关键是甲醇的组成,因此定其计量数为1,这样可得其燃烧后生成h2o与co2的分子个数:ch3oh+o2――2h2o+co2。
然后配平氧原子:ch3oh+3/2o2===2h2o+co2,将各计量数同乘以2化分为整数:2ch3oh+3o2==4h2o+2co2。
化学方程式配平方法总结第二篇用奇数配偶数法去配平化学反应方程式的原理是:一、两个奇数或两个偶数之和为偶数;奇数与偶数之和则为奇数——简称加法则。
奇数与偶数或两个偶数之积为偶数;两个奇数之积则仍为奇数——简称乘法则。
二、依质量守恒定律,反应前后各元素的原子总数相等。
其配平方法可按以下步骤进行:找出化学反应式左右两边出现次数较多的元素,且该元素的原子个数在反应式左右两边有奇数也有偶数;选定含该元素奇数个原子的化学式,作为配乎起点,选配适当系数,使之偶数化;由已推得的系数,来确定其它物质的系数。
最终,验证方程式是否正确:[例1]配平FeS2十O2——Fe2O3十SO2[分析](1)从反应方程式可知,氧元素在两边出现的次数较多,且其原子个数在两边有奇数亦有偶数。
(2)反应式左边有O2,由“乘法则〞可知,其系数无论为何,O原子总数必为偶,而由“加法则〞可知,要使右边O原子总数亦为偶,就必需给右边含奇数个氧原子的Fe2O3系数选配2,使之偶数化,则:FeS2十O2——2 Fe2O3十SO2(3)由已确定的系数,推出与此有关的其它物质的系数。
反应式右边有4个Fe原子,故左边FeS2的系数须配4,则:4FeS2十O2——2 Fe2O3十SO2然后以左边的S原子数,推得右边应有8SO2,即:4FeS2十O2——2 Fe2O3十8SO2最终配平O原子,当左边有11O2时,反应式则可配平为:4FeS2十11O2——2 Fe2O3十8SO2代数法——待定系数法代数法也叫待定系数法,其方法步骤如下:设a、b、c、d等未知数,分别作为待配平的化学方程式两端各项化学式的系数。


化学方程式配平方法讲解化学方程式配平方法讲解学习化学的过程当中经常要去配平很多的方程式,但是具体要怎么做?下面是店铺整理的化学方程式配平方法讲解,希望可以很好的帮助大家对化学知识的学习。
化学方程式配平方法讲解篇1一、原理遵循两个原则①质量守恒定律(在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变。
)②客观事实二、配平方法通常考试配平题所给方程式等号写的是短线,需要考生把短线改为等号,否则是没有分的。
1、配平系数,配平化学方程式中各化学式的系数,有些地方的系数1不能省略;2、将单线改为双线,此为化学方程式中最容易忽略的地方;3、如果是溶液中发生反应,反应物中无固体,而生成物中有沉淀的,在生成的沉淀化学式右侧用“ ”号表示反应物中无气体,而生成物中有气体产生的则在生成的气体右侧用“↑”号表示;反应物和生成物都有气体,则不用加任何符号。
(1)悠然观察便配齐:意思是说将约简后的系数代入反应式后,悠然自在地观察一下就可以配平。
观察可知:右边为6个K,所以KOH前应加6,加6后左边为6个H,所以H2O前应加3,于是得到配平后的化学反应方程式:3S+6KOH=2K2S+K2SO3+3H2O说明:只要将这种方法掌握后,在“实战”时,仅需几秒钟便可完成配平过程啦,大家快试试吧。
(2)双水解反应简捷配平法谁弱选谁切记清,添加系数电荷等。
反应式中常加水,质量守恒即配平。
说明:双水解反应,是指由一种强酸弱碱盐与另一种强碱弱酸盐作用,由于相互促进,从而使水解反应进行到底的反应。
如:AI2(SO4)3和Na2CO3反应。
该法的特点是可以直接写系数,可在瞬间完成配平过程。
解释:1、谁弱选谁切记清:“谁弱选谁”的意思是说,在两种盐中要选择弱碱对应的金属离子(如AI3+是弱碱AI(OH)3对应的金属阳离子;NH4+离子是特例)和弱酸对应的酸根阴离子(如CO32—是弱酸H2CO3对应的酸根阴离子)作为添加系数(配平)的对象。


化学方程式的配平方法一、最小公倍法1、找出式子两边各出现一次且原子数相差较大的元素;2、找出上述元素在式子两边原子数的最小公倍数;3、用最小公倍数分别除以所选定元素的原子数,所得的商写在相应化学式的前面;4、配平其他元素的原子。
例:P + O2——P2O5KClO₃——KCl + O₂二、奇数配偶法口诀:一找元素见面多,二将奇数变成偶,三按连锁先配法,四用观察配其它。
1、先找出式子两边出现次数较多且两边原子数一奇一偶的元素;2、在上述元素的原子数为奇数的化学式前配上偶数“2”(或其它偶数);3、配平其他元素的原子;4、最后配平所选定元素的原子。
例:C2H6 + O2 —点燃—CO2 + H2OFeS2+ O2 —高温—Fe2O3+ SO2三、观察法1、先从化学式比较复杂的一种反应物或生成物入手,确定与之相关的各生成物或反应物的化学计量数;2、根据求得的化学式前的化学计量数,推出其他化学式前的化学计量数。
例:H2+Fe3O4—高温—Fe+H2O【4H2+Fe3O4=高温=3Fe+4 H2O 】Al +CuSO4——Cu+Al2(SO4)3【2Al +3 CuSO4 = 3Cu+Al2(SO4)3 】四、有双原子分子的单质参加或生成的反应1、先配平其他元素的原子;2、配平单质中元素的原子(若单质化学式前的化学计量数为分数,则在式子两边该分数的分母。
)(练习):C2H6 + O2—点燃—CO2 + H2OCl2+Ca(OH)2—— CaCl2+Ca(ClO)2+H2ONH3 + O2——NO+ H2OC2H8N2 +N2O4——N2+CO2+H2O五、化合价升降法1、先找出式子两边化合价有改变的元素,并标出相应的化合价;2、根据化合价升高的数与化合价降低的数相等,找出正价与负价的最小公倍数,用这个数分别除以正价与负价的改变数,所得的商写在相应化学式前面;3、最后配平所选定元素的原子例1:Cu + HNO3(稀)——Cu(NO3)2+ NO + H2O例2 :NH3 + O2——NO+ H2O六、待定系数法1、现在各化学式前写上字母;2、根据反应前后各原子数相等,写出各元素在式子两边原子数的关系式;3、找出上述几个关系式中出现次数较多的字母,令其为“1”,再根据关系式推出其他字母的数值。
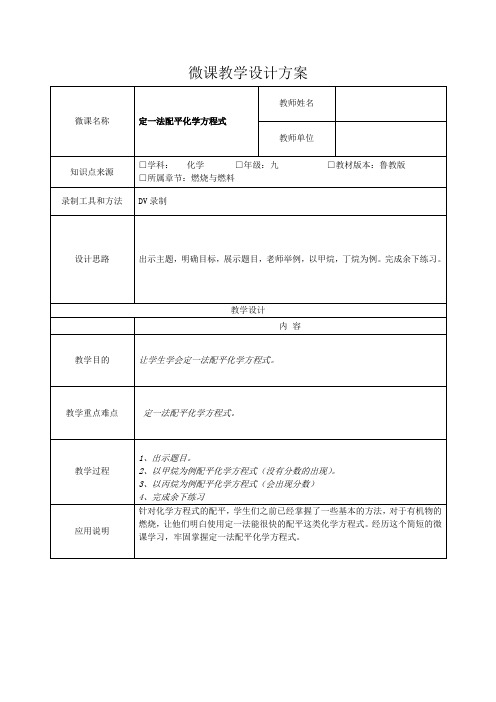
微课教学设计方案微课名称定一法配平化学方程式
教师姓名
教师单位
知识点来源□学科:化学□年级:九□教材版本:鲁教版□所属章节:燃烧与燃料
录制工具和方法DV录制
设计思路出示主题,明确目标,展示题目,老师举例,以甲烷,丁烷为例。
完成余下练习。
教学设计
内容
教学目的让学生学会定一法配平化学方程式。
教学重点难点定一法配平化学方程式。
教学过程1、出示题目。
2、以甲烷为例配平化学方程式(没有分数的出现)。
3、以丙烷为例配平化学方程式(会出现分数)
4、完成余下练习
应用说明针对化学方程式的配平,学生们之前已经掌握了一些基本的方法,对于有机物的燃烧,让他们明白使用定一法能很快的配平这类化学方程式。
经历这个简短的微课学习,牢固掌握定一法配平化学方程式。
化学配平方法定一法
化学配平方法之一:定一法
化学配平是在化学反应中确定反应物和生成物之间的摩尔比例的过程。
化学配平方法有多种,其中之一是定一法。
定一法是一种常用的基础配平方法,适用于一些简单的化学反应。
在使用定一法进行化学配平时,首先需要确定反应中的主要反应物和生成物。
然后,根据反应物和生成物之间的化学方程式,将反应物和生成物的系数进行调整,使其满足摩尔比例。
举例来说,考虑以下化学反应:
H2+O2→H2O
在该反应中,氢气和氧气是反应物,水是生成物。
根据该方程式,我们可以确定氢气和氧气的系数都是1,水的系数是2。
根据定一法,我们可以假设氢气的系数是x,氧气的系数是y。
然后,我们根据方程式中氢气和氧气的原子数量,建立以下方程:
x(H2)+y(O2)→2(H2O)
根据这个方程式,我们可以得到两个方程:
氢的原子数:2x=2
氧的原子数:2y=2
解这个方程组,我们可以得到:
x=1
y=1
因此,根据定一法,反应式为:
H2+O2→2H2O
通过定一法,我们可以确定反应物和生成物的系数,从而了解反应物和生成物之间的摩尔比例。
总结一下,化学配平方法之一是定一法。
使用定一法进行化学配平时,需要根据化学方程式确定反应物和生成物的系数,然后通过解方程组得到正确的系数。
通过使用合适的配平方法,我们可以保证文章的清晰思路和流畅表达,并且避免包含任何负面影响的元素,如不符合标题、广告信息、版权争议、敏感词和不良信息。
此外,文章的正文应该是完整的,没有缺失语句、丢失序号或不完整的段落。