山东省泰安市201X中考化学复习 第一部分 基础过关 第七单元 溶液 第2课时 物质的溶解性课件
- 格式:ppt
- 大小:910.50 KB
- 文档页数:15


第七单元 常见的酸和碱第一节酸及其性质(第一课时)一、学习目标:1.知道盐酸、硫酸的主要性质和用途;2.认识浓硫酸的腐蚀性和稀释方法;3.掌握酸的化学性质,知道酸具有相似化学性质的原因。
学习重点:盐酸、硫酸的物理性质 难点:浓硫酸的特性【情境导入】人们在购买葡萄、橘子等水果时,常习惯的问“酸不酸?”。
的确,许多未成熟的水果是很酸的,这是因为里面含有很多的有机酸,如苹果酸,柠檬酸,酒石酸等,随着水果的成熟有些酸会逐渐分解,酸味也随之减轻。
二、自主探究:展示观察浓盐酸浓硫酸试剂瓶:识记浓盐酸的质量分数为35%-37%,密度1.097g/cm 3,浓硫酸的质量分数为98%,密度为1.84g/cm 3。
阅读课本【讨论】白雾说明什么?【观察】【讨论】1.如果不慎将浓硫酸溅在皮肤或者衣物上会有什么结果?应该怎么处理?说明浓硫酸具有什么性质?2.如果将稀硫酸不慎溅在衣物上,应该怎么处理?3.在稀释浓硫酸时应该怎样操作?为什么要这样做?【归纳】一、浓盐酸、浓硫酸的物理性质、特性及用途:1.盐酸——氯化氢气体的水溶液2.浓盐酸和浓硫酸的物理性颜色、状态打开瓶盖现象原因气味敞口久置质量及P% 原因用途3.浓硫酸的特性:⑴脱水性:能够将纸张、木材、布料、皮肤里氢、氧元素按水的组成比夺去,使它们脱水生成黑色的炭,发生炭化。
(思考:脱水性是什么性质?)⑵:浓硫酸跟空气接触,能够空气里的水分,可用作某些气体的。
⑶强烈的。
⑷强氧化性:与金属反应时一般不生成氢气,而生成水。
4.浓硫酸的稀释:稀释浓硫酸时,应将其沿杯壁慢慢倒入中,且边倒边搅拌。
而不能把往里倒,以免水沸腾将硫酸带出,造成危险。
(因为硫酸溶于水时放出大量的热)万一浓硫酸洒在皮肤上,请立即,然后涂3%-5%的溶液。
【巧学妙记】浓硫酸的稀释:“酸入水,沿内壁,慢慢倒,不断搅”。
当堂达标1.下列物质敞口放一段时间,质量会减少的是 ( )A.浓硫酸 B.大理石 C.稀硫酸 D.浓盐酸2.下列叙述错误的是 ( )A.打开浓盐酸的试剂瓶盖,瓶口出现白烟B.用浓硫酸在白纸上写字,白纸上的字迹慢慢变黑C.稀释浓硫酸时,应将浓硫酸沿器壁慢慢注入水中,并用玻璃棒不断搅拌D.稀硫酸、稀盐酸都可以用于金属表面除锈3.下列关于物质的用途的叙述不正确的是( )A.盐酸可用来除铁锈 B.稀硫酸在实验室里常用作干燥剂C.硫酸可用于精炼石油和金属除锈 D.盐酸是重要化工产品4.如图该装置被誉为“万用瓶”。

山东省泰安市2019中考化学复习第一部分基础过关第八单元常见的酸和碱第2课时溶液的酸碱性酸碱中和反应练习(含解析)编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(山东省泰安市2019中考化学复习第一部分基础过关第八单元常见的酸和碱第2课时溶液的酸碱性酸碱中和反应练习(含解析))的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为山东省泰安市2019中考化学复习第一部分基础过关第八单元常见的酸和碱第2课时溶液的酸碱性酸碱中和反应练习(含解析)的全部内容。
/ 22 1 / 221第八单元常见的酸和碱第2课时溶液的酸碱性酸碱中和反应夯基提能作业一、选择题1。
(2018四川成都中考)下图为物质经一步反应转化的两种途径,相关说法正确的是( )A。
氧化物为SO2B。
X只能是硫酸C.②可能有沉淀生成/ 22 2 / 222D。
①、②属于复分解反应2。
(2018辽宁沈阳中考)下列描述属于氢氧化钙化学性质的是()A。
白色固体B.微溶于水C。
溶液有滑腻感D.能与CO2反应3。
(2018辽宁沈阳中考)测得生活中一些物质的pH如下表,下列说法正确的是()物质胃液人体血液肥皂水洗涤剂pH0.8~1.57。
35~7.4510.212.2A。
人体血液显酸性B.用NaOH可以治疗胃酸过多C.洗涤剂比肥皂水的碱性强D.肥皂水能使蓝色石蕊试纸变红4。
(2018北京中考)一些物质的pH范围如下,其中呈碱性的是()A。
油污净(12~13)/ 22 3 / 223B.西瓜汁(5~6)C.洁厕灵(1~2)D。
橘子汁(3~4)5。
(2018北京中考)下列物质能与NaOH反应的是()A.FeB.CO2C.Fe2O3D.NaCl6.(2018重庆中考)食醋里通常含有3%~5%的醋酸(CH3COOH),食醋与鸡蛋壳反应产生能使澄清石灰水变浑浊的气体。

2024年中考化学一轮复习知识点总结—溶液(含解析)知识点一、溶液1.定义:一种或几种物质分散到另一种物质里,形成均一、稳定的混合物。
2.溶液的组成及其特征:溶液由溶质和溶剂,最常用的溶剂是水;另外常用的溶剂还有酒精、汽油。
溶液的基本特征是均一、稳定、混合物。
3.溶解过程:物质在溶解过程中发生了两种变化,一种是扩散过程,此过程吸收热量,另一种是水合过程,此过程放出热量,氢氧化钠、浓硫酸、生石灰等物质溶于水放热,硝酸铵等物质溶于水吸热,食盐、蔗糖等物质溶于水温度不变。
4.乳化现象:洗洁精、洗发液等因为具有乳化作用,所以可去油污,它们使油类物质以细小的液滴的形态分散在水中,形成不易分层、比较稳定的混合物这种现象叫做乳化现象。
(用汽油洗掉油污是溶解作用,形成溶液;用洗涤剂洗油污是乳化作用,形成乳浊液。
)5.饱和溶液和不饱和溶液(1)定义:在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,叫这种溶质的饱和溶液;还能继续溶解某种溶质的溶液的溶液,叫这种溶质的的不饱和溶液。
(2)饱和溶液与不饱和溶液之间的转化方法:(对大多数固体物质)a针对大多数溶解度随温度升高而增大的物质:b对于Ca(OH)2等溶解度随温度升高而减小的物质:知识点二、溶液组成的定量表示1.溶质质量分数定义:定量表示溶液组成的方法很多,化学上常用溶质质量分数来表示溶液的组成。
它是溶质与溶液的质量之比。
2.其定义公式为:溶质的质量分数=溶液质量溶质质量×100%。
3.变形公式:溶质质量=溶液质量×溶质质量分数;溶剂质量=溶液的质量—溶质的质量4.溶液的稀释问题(1)通过向一定溶质质量分数的溶液中加入水或蒸发水,改变其溶质质量分数,在此过程中,浓稀溶液中溶质的质量不变。
(2)稀释前浓溶液质量×浓溶液溶质质量分数=稀释后稀溶液质量×稀溶液溶质质量分数知识点三、配制溶液1.步骤(1)计算;需要食盐8克;需要水42克;即42毫升。
![【配套K12】[学习]山东省泰安市2019中考化学复习 第一部分 基础过关 第七单元 溶液 第1课时](https://uimg.taocdn.com/6f47fe3e6edb6f1aff001fa4.webp)
第七单元溶液第1课时溶液的形成和定量表示夯基提能作业一、选择题1.(2018江苏泰州中考)下列厨房用品中,易溶于水形成溶液的是( )A.花生油B.面粉C.白糖D.辣椒粉2.下列有关溶液的叙述错误的是( )A.长期放置后不会分层的液体一定是溶液B.衣服上的油污用汽油或用加了洗涤剂的水可除去C.一瓶合格的生理盐水密封一段时间后,不会出现浑浊D.实验室常将固体药品配制成溶液进行化学反应,以提高反应速率3.(2017辽宁沈阳中考)按下列方法配制的溶液,其溶质质量分数为5%的是( )A.称取5.0 g氯化钾,溶解在95 mL水中,充分搅拌B.称取5.0 g生石灰,放入95 mL水中,充分搅拌C.量取5.0 mL浓盐酸,倒入95 mL水中,充分搅拌D.称取5.0 g二氧化锰,放入95 mL水中,充分搅拌4.(2018山东滨州中考)小芳在配制一定溶质质量分数的氯化钠溶液时,没有按照正确的称量氯化钠、量取水的操作规程进行操作(图示为小芳操作时的读数,其他操作都正确)。
小芳实际配制的氯化钠溶液的溶质质量分数(水的密度为1 g/cm3)约为( )A.12.4%B.17.2%C.16.9%D.12.5%5.(2018江苏宿迁中考)如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )A.甲的溶解度大于乙的溶解度B.降温可使接近饱和的丙溶液变为饱和溶液C.将t2℃甲、乙、丙的饱和溶液降温至t1℃,所得溶液的溶质质量分数:乙>甲=丙D.P点表示t1℃时甲、丙两种物质的溶解度都是25 g6.(2018山东菏泽中考)对下列实验事实的解释错误的是( )A.硫在空气和氧气中燃烧现象不同——氧气浓度不同B.硝酸钾在热水和冷水中溶解的快慢不同——温度不同,硝酸钾的溶解度不同C.酒精和食醋的气味不同——不同分子性质不同D.金刚石和石墨硬度不同——碳原子的排列方式不同7.(2017新疆乌鲁木齐中考)如图所示,将液体X加入到集气瓶中与固体Y作用,观察到气球逐渐变大。

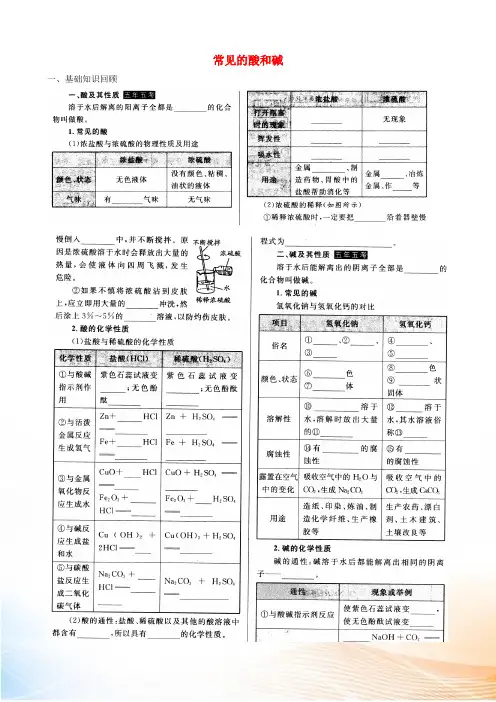
常见的酸和碱一、基础知识回顾二、典型例题考点1 酸碱指示剂和pH用滤纸折成蝴蝶并喷洒某种溶液或试剂后,悬挂于铁架台上.另取一只盛有某未知溶液的烧杯,放在纸蝴蝶的下方(见右图).一会儿,纸蝴蝶的颜色发生变化,请回答:(1)若纸蝴蝶上喷洒的是酚酞试液,纸蝴蝶变红色,烧杯中的溶液是______;(2)若纸蝴蝶上喷洒的是石蕊试液,纸蝴蝶变红色,烧杯中的溶液是______,若纸蝴蝶变蓝色,烧杯中的溶液是________;(3)试分析产生以上现象的原因是__________________________.考点2 酸、碱的化学性质(1)为探究盐酸与氢氧化钠溶液的反应,设计下列实验方案(如图1):向5mL稀氢氧化钠溶液中滴加3滴酚酞溶液,然后逐滴加入稀盐酸,并用玻璃棒不断搅拌.①实验过程中观察到的现象是。
②向稀氢氧化钠溶液滴加稀盐酸至过量,溶液pH变化的曲线正确的是(如图3)(填写字母标号).(2)实验室可以利用稀盐酸等药品,通过连接图2装置制取二氧化碳、氢气。
①制取二氧化碳气体装置的连接顺序是(填写字母,下同),制取氢气装置的连接顺序是____.②块状固体加入试管中的方法是.③检查发生装置气密性的方法是。
考点3 中和反应(2022.山东滨州)在研究酸和碱的化学性质时,某小组想证明稀硫酸与氢氧化钠溶液混合后,虽然无明显现象,但确实发生了化学反应,试与他们一起完成实验方案的设计,实施和评价,并得出有关结论.(1)探究稀硫酸与氢氧化钠溶液的反应:当滴入几滴酚酞试液后,溶液由无色变为红色,根据上述实验中颜色变化,可确定稀硫酸与氢氧化钠溶液发生了化学变化,反应的化学方程式为:.(2)探究上述稀硫酸与氢氧化钠溶液反应后烧杯中的硫酸是否过量:根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量,同学们又分别选取氯化钡溶液、紫色石蕊试液设计实验方案,请你判断并分析:实验方案实验步骤实验现象实验结论方案二取样,滴入几滴紫色石蕊试液溶液变红稀硫酸过量上述设计的实验方案中,正确的是(填“方案一”或“方案二”)另外一个实验方案错误的原因是;请你设计一个确定稀硫酸是否过量的实验方案,你选用的药品是,实验现象及结论是。