2020年高考化学工艺流程试题汇编
- 格式:doc
- 大小:223.00 KB
- 文档页数:8
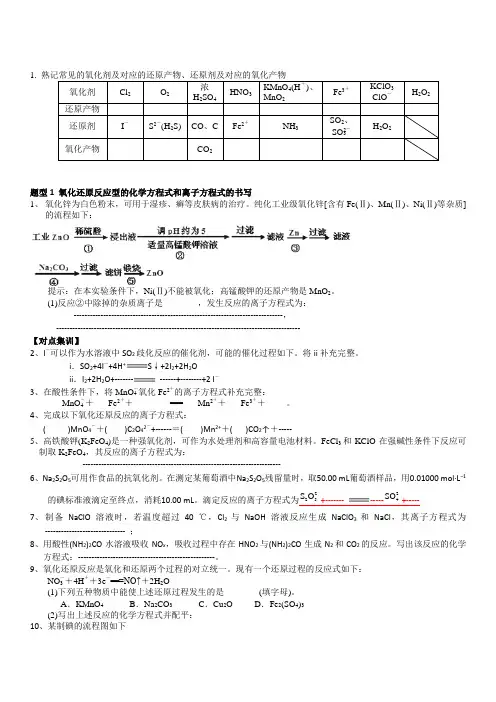
1. 熟记常见的氧化剂及对应的还原产物、还原剂及对应的氧化产物氧化剂Cl2O2浓H2SO4HNO3KMnO4(H+)、MnO2Fe3+KClO3ClO-H2O2还原产物还原剂I-S2-(H2S) CO、C Fe2+NH3SO2、SO2-3H2O2氧化产物CO2题型1 氧化还原反应型的化学方程式和离子方程式的书写1、氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。
纯化工业级氧化锌[含有Fe(Ⅱ)、Mn(Ⅱ)、Ni(Ⅱ)等杂质]的流程如下:提示:在本实验条件下,Ni(Ⅱ)不能被氧化;高锰酸钾的还原产物是MnO2。
(1)反应②中除掉的杂质离子是__ ,发生反应的离子方程式为:------------------------------------------------------------------------------,-------------------------------------------------------------------------------------------【对点集训】2、I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。
将ii补充完整。
i.SO2+4I-+4H+S↓+2I2+2H2Oii.I2+2H2O+-------------+--------+2 I-3、在酸性条件下,将MnO-4氧化Fe2+的离子方程式补充完整:-----MnO-4+-----Fe2++___-----__===-----Mn2++-----Fe3++-------。
4、完成以下氧化还原反应的离子方程式:( )MnO4-+()C2O42-+------=( )Mn2++( )CO2↑+-----5、高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。
FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为:--------------------------------------------------------------------------6、Na2S2O5可用作食品的抗氧化剂。

全国新课标三卷高考化学工艺流程试题汇编(新课标Ⅲ)2020新课标Ⅲ.某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni 、Al 、Fe 及其氧化物,还有少量其他不溶性物质。
采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO 4·7H 2O):溶液中金属离子开始沉淀和完全沉淀的pH 如下表所示:回答下列问题:(1)“碱浸”中NaOH 的两个作用分别是______________。
为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。
写出该反应的离子方程式______________。
(2)“滤液②”中含有的金属离子是______________。
(3)“转化”中可替代H 2O 2的物质是______________。
若工艺流程改为先“调pH”后“转化”,即“滤液③”中可能含有的杂质离子为______________。
(4)利用上述表格数据,计算Ni(OH)2的K sp =______________(列出计算式)。
如果“转化”后的溶液中Ni 2+浓度为1.0 mol·L −1,则“调pH”应控制的pH 范围是______________。
(5)硫酸镍在强碱溶液中用NaClO 氧化,可沉淀出能用作镍镉电池正极材料的NiOOH 。
写出该反应的离子方程式______________。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是______________。
2020新课标Ⅲ.高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。
回答下列问题:相关金属离子[c0(Mn+)=0.1 mol·L−1]形成氢氧化物沉淀的pH范围如下:(1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式____________________________________________________。

2020年高考复习化学工艺流程题题型特点本题型以现代工业生产为基础,与化工生产成本、产品提纯、环境保护等相融合,考查物质的制备、检验、分离、提纯等基本实验原理在化工生产中的实际应用,要求考生依据流程图分析原理、紧扣信息、抓住关键、准确答题。
这类试题具有较强的实用性和综合性,能较好地考查学生信息获取能力、分析问题能力、语言表达能力和计算能力等。
突破点一化工工艺流程题的分析【解题策略】1.粗读试题(1)读题头,得目的。
题头一般是简单介绍该工艺生产的原材料和工艺生产的目的(包括副产品),以及提供需要用到的信息。
(2)读题干、析过程。
题干部分主要用框图形式将原料到产品的主要生产工艺流程表示出来。
题干信息有三个层次:读得懂的;读得不太懂但根据上下文可以勉强懂的;完全读不懂的。
关键是突破第二层次,对于读得不太懂但根据上下文可以勉强懂的部分需要学生运用已有的基础知识,根据学习过的化学反应原理,联系实际工业生产及题目信息等进行知识的整合,最终得到结论。
(3)读题尾、看措施:题尾主要是根据生产过程中涉及的化学知识设计成系列问题,构成一道完整的化学试题。
阅读题尾时要将设问中的提示性信息,用笔画出来,以便在后面精读试题时随时提醒自己与之联系。
2.精读试题在粗读试题的基础上,结合流程图以外的文字描述、表格信息、后续设问中的提示性信息,在流程图上随手画出相关信息,以便在解题时随时进行联系和调用;同时思考几个问题:从原料到产品依次进行了什么反应,利用了什么原理(氧化还原?溶解度?溶液中的平衡?),每一步操作进行到什么程度最佳,每一步除目标物质外还产生了什么杂质或副产物,杂质或副产物用什么方法除去等等,体会出题者设问的角度、意图。
只要掌握了这一题型的一般特点和解题策略,无论流程如何陌生复杂,在高考中即使遇到情境陌生的流程图题,也能够驾驭自如,迎刃而解。
1[2019·全国卷Ⅲ]高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如图G2-1所示。
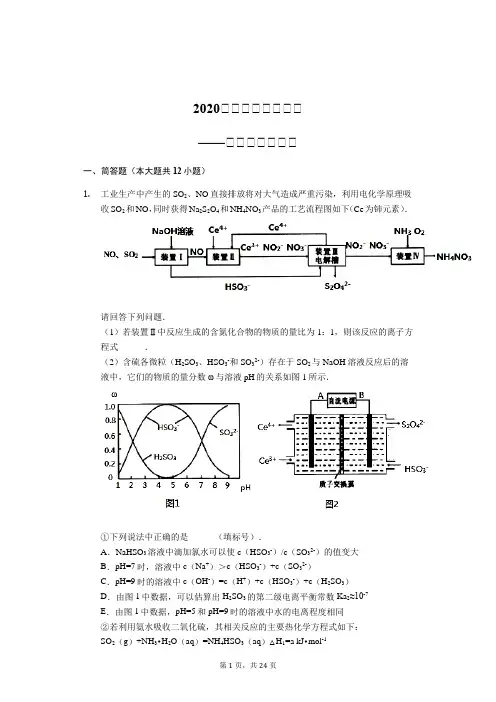
2020届届届届届届届届——届届届届届届届一、简答题(本大题共12小题)1.工业生产中产生的SO2、NO直接排放将对大气造成严重污染,利用电化学原理吸收SO2和NO,同时获得Na2S2O4和NH4NO3产品的工艺流程图如下(Ce为铈元素).请回答下列问题.(1)若装置Ⅱ中反应生成的含氮化合物的物质的量比为1:1,则该反应的离子方程式______.(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数ω与溶液pH的关系如图1所示.①下列说法中正确的是______(填标号).A.NaHSO3溶液中滴加氯水可以使c(HSO3-)/c(SO32-)的值变大B.pH=7时,溶液中c(Na+)>c(HSO3-)+c(SO32-)C.pH=9时的溶液中c(OH-)=c(H+)+c(HSO3-)+c(H2SO3)D.由图1中数据,可以估算出H2SO3的第二级电离平衡常数Ka2≈10-7E.由图1中数据,pH=5和pH=9时的溶液中水的电离程度相同②若利用氨水吸收二氧化硫,其相关反应的主要热化学方程式如下:SO2(g)+NH3•H2O(aq)=NH4HSO3(aq)△H1=a kJ•mol-1NH3•H2O (aq)+NH4HSO3(aq)=(NH4)2SO3(aq)+H2O(l)△H2=b kJ•mol-1 2(NH4)2SO3(aq)+O2(g)=2(NH4)2SO4(aq)△H3=c kJ•mol-1反应2SO2(g)+4NH3•H2O(aq)+O2(g)=2(NH4)2SO4(aq)+2H2O(l)△H=______kJ•mol-1.③取装置Ⅰ中的吸收液VmL,用cmol/L的酸性高锰酸钾溶液滴定.吸收液溶液应装在______(填“酸式”或“碱式”)滴定管中,判断滴定终点的方法______.(3)装置Ⅲ的作用之一是再生Ce4+,其原理如图2所示.图中B为电源的______(填“正”或“负”)极.左侧反应室中发生的主要电极反应式为______.(4)已知进入装置Ⅳ的溶液中NO2-的浓度为0.4mol/L,要使1m3该溶液中的NO2-完全转化为NH4NO3,该过程中转移电子数目为______.2.2015年2月16日李克强总理到东北调研经济情况,重点走访了钢铁厂,鼓励钢铁厂提高钢铁质量和产量,铁及其化合物在日常生活中应用广泛.(1)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理.已知含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,则另一反应的离子方程式为______;(2)氧化铁是重要工业颜料,下面是制备氧化铁的一种方法,其流程如下:①操作Ⅰ的名称是______;操作Ⅱ为洗涤,洗涤操作的具体方法为______;②滤液A中加入稍过量的NH4HCO3溶液生成沉淀同时有一种气体产生,写出其化学方程式:______;(3)如果煅烧不充分,产品中将有FeO存在,称取3.0g氧化铁产品,溶解,在250mL 容量瓶中定容;量取25.00mL待测溶液于锥形瓶中,用酸化的0.01000mol/L KMnO4溶液滴定至终点,重复滴定2-3次,消耗KMnO4溶液体积的平均值为20.00mL,①该实验中的KMnO4溶液需要酸化,用于酸化的酸是______(填字母序号).a.稀硝酸 b.稀盐酸 c.稀硫酸 d.浓硝酸②计算上述产品中Fe2O3的质量分数为______.3.某学习小组利用废旧电池拆解后的碳包滤渣(含MnO2、C、Hg2+等)制取硫酸锰晶体( MnSO4•H2O ),实验流程如下:已知:(1)25℃时,几种硫化物的溶度积常数如下:物质 FeS MnS HgS 溶度积 5×10-18 4.6×10-14 2×10-54(2)25℃时,几种金属氢氧化物沉淀时的PH 如下:Fe (OH )2 Fe (OH )3Mn (OH )2 开始沉淀时的PH 6.3 2.78.3 沉淀完全时的PH 8.43.7 9.8 请回答下列问题:(1)“浸取”时加热的作用是______;写出“浸取”时生成MnSO 4、Fe 2(SO 4)3 反应的离子方程式:______.(2)若“浸取”在25℃时进行,加入足量FeS ,则FeS (s )+Hg 2+(aq )⇌HgS (s )+Fe 2+ (aq )的平衡常数K 为______.(3)过滤I 过程中,需要使用的玻璃仪器有烧杯、______,滤渣I 的主要成分为FeS 、S 和______(化学式).(4)“氧化”时加入MnO 2 的作用是______,也可用H 2O 2 代替MnO 2 ,H 2O 2 的电子式为______.(5)“中和”过程,应该调节溶液PH 为______,写出该过程产生滤渣II 的离子方程式:______(6)获得MnSO 4•H 2O 的“一系列操作”是______、过滤、洗涤、干燥.(7)1150℃时,MnSO 4•H 2O 在氩气氛围中进行焙烧的分解产物是Mn 3O 4、硫的氧化物等,分解反应的化学方程式是:______,在MnSO 4•H 2O 进行焙烧时,除加热仪器外,还需要的仪器中主要成分属硅酸盐的有______.4. 草酸钴用途广泛,可用于指示剂和催化剂制备.一种利用水钴矿[主要成分为Co 2O 3,含少量Fe 2O 3、Al 2O 3、MnO 、MgO 、CaO 等]制取CoC 2O 4•2H 2O 工艺流程如图1:已知:①浸出液含有的阳离子主要有H +、Co 2+、Fe 2+、Mn 2+、Ca 2+、Mg 2+、Al 3+等; ②部分阳离子以氢氧化物形式沉淀时溶液的pH 见表:沉淀物 Fe (OH )3 Fe (OH )2 Co (OH )2 Al (OH )3 Mn (OH )2完全沉淀的pH3.79.69.2 5.29.8(1)浸出过程中加入Na2SO3的目的是将______还原(填离子符号).(2)NaClO3的作用是将浸出液中的Fe2+氧化成Fe3+,产物中氯元素处于最低化合价.该反应的离子方程式为______.(3)请用平衡移动原理分析加Na2CO3能使浸出液中Fe3+、Al3+转化成氢氧化物沉淀的原因是:______.(4)萃取剂对金属离子的萃取率与pH的关系如图2所示.滤液Ⅱ中加入萃取剂的作用是______;使用萃取剂适宜的pH是______.A.接近2.0 B.接近3.0 C.接近4.0(5)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀.已知K sp(MgF2)=______.=7.35×10-11、K sp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液c(Mg2+)c(Ca2+)(6)为测定制得的无水草酸钴样品的纯度,现称取样品mg,先用适当试剂将其转化,得到纯净的草酸铵溶液,再用过量的稀硫酸酸化,用cmol/L高锰酸钾溶液去滴定,当溶液由______(填颜色变化),共用去高锰酸钾溶液VmL(CoC2O4的摩尔质量147g/mol),计算草酸钴样品的纯度为______.5.图l表示“侯氏制碱法”工业流程,图2表示各物质的溶解度曲线.回答下列问题:(1)图中X的化学式为______ .(2)沉淀池中发生反应的化学方程式为______ ,该反应先向饱和食盐水中通入______ (填化学式)至饱和,再通入另一种气体,若顺序颠倒,后果是______ .(3)沉淀池的反应温度控制在30~35℃,原因是______ .(4)母液中加入CaO后生成Y的化学方程式为______ .(5)氯碱工业是指电解饱和食盐水,这里的碱是指______ (填化学式),其另外两种气体产物可以用于工业上制取纯硅,流程如图3:①整个制备过程必须严格控制无水无氧.SiHCl3遇水剧烈反应,写出该反应的化学方程式______ .②假设每一轮次制备1mol纯硅,且生产过程中硅元素没有损失,反应I中HCl的利用率为90%,反应II中H2的利用率为93.75%.则在第二轮次的生产中,补充投入HCl 和H2的物质的量之比是______ .6.Ⅰ.工业上常利用电解含有铁、钯、铜等金属的粗银棒精炼银,示意图如下:(1)阴极反应式为______。

2020年高考化学一模、二模试题分类汇编专题十一工艺流程综合题(A型题组)
高考命题动向预测:T
3、T5、T10
1.(东北三省三校2020届高三一模)工业上以钒钛磁铁矿为原料,在炼铁的同时还可以制备钒的最高价氧化物V2O5,其主要流程如下:
已知:①VO3-+2H+ VO2++H2O
②NH4VO3微溶于冷水,易溶于热水,不溶于乙醇
(1)高炉炼铁应用的冶炼方法是____(填标号)
A.热分解法B.热还原法C.电解法
(2)钒渣中的V2O3在焙烧时转化为Ca(VO3)2,写出该反应的化学方程式____________
(3)Ca(VO3)2难溶于水但能溶于稀硫酸,试用平衡移动原理分析其原因____,浸出液中含钒物质的化学式为____________________________
(4)沉钒过程有气体生成,其反应的离子方程式为
_________________
(5)过滤后用乙醇代替水来洗涤沉淀的原因是__________________
(6)煅烧NH4VO3时,固体质量随温度变化的曲线如图所示。
加热到200℃时,得到的固体物质化学式为____,300~350℃放出的气态物质化学式为____。
【答案】(1)B
(2)V2O3+O2+CaCO3Ca(VO3)2+CO2
(3)加入硫酸使VO3-+2H+ VO2++H2O中c(VO3-)降低,Ca(VO3)2溶解平衡
Ca(VO3)2(s)Ca2+(aq)+VO3-(aq)正向移动,Ca(VO3)2溶解(VO2)2SO4
1。
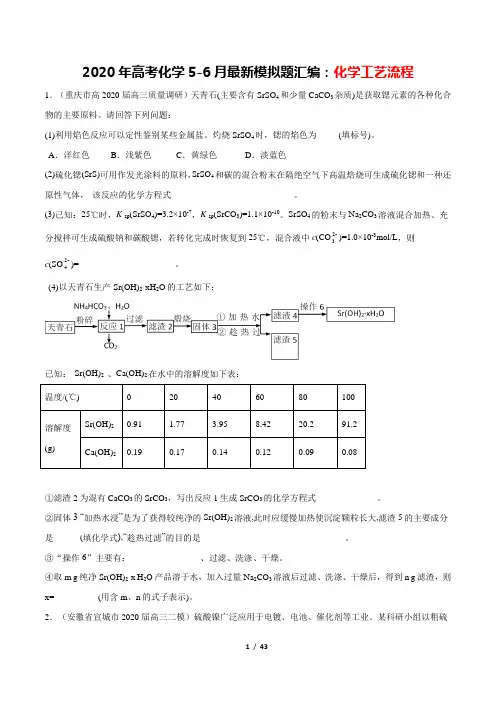
2020年高考化学5-6月最新模拟题汇编:化学工艺流程1.(重庆市高2020届高三质量调研)天青石(主要含有SrSO4和少量CaCO3杂质)是获取锶元素的各种化合物的主要原料。
请回答下列问题:(1)利用焰色反应可以定性鉴别某些金属盐。
灼烧SrSO4时,锶的焰色为_____(填标号)。
A.洋红色B.浅紫色C.黄绿色D.淡蓝色(2)硫化锶(SrS)可用作发光涂料的原料,SrSO4和碳的混合粉末在隔绝空气下高温焙烧可生成硫化锶和一种还原性气体,该反应的化学方程式____________________________。
(3)已知:25℃时,K sp(SrSO4)=3.2×10-7,K sp(SrCO3)=1.1×10-10。
SrSO4的粉末与Na2CO3溶液混合加热、充分搅拌可生成硫酸钠和碳酸锶,若转化完成时恢复到25℃,混合液中c(CO2-3)=1.0×10-3mol/L,则c(SO2-4)=______________________。
(4)以天青石生产Sr(OH)2·xH2O的工艺如下:已知:Sr(OH)2、Ca(OH)2在水中的溶解度如下表:温度/(℃) 0 20 40 60 80 100溶解度(g) Sr(OH)20.91 1.77 3.95 8.42 20.2 91.2 Ca(OH)20.19 0.17 0.14 0.12 0.09 0.08①滤渣2为混有CaCO3的SrCO3,写出反应1生成SrCO3的化学方程式______________。
②固体3 “加热水浸”是为了获得较纯净的Sr(OH)2溶液,此时应缓慢加热使沉淀颗粒长大,滤渣5的主要成分是______(填化学式),“趁热过滤”的目的是_________________________________。
③“操作6”主要有:________________、过滤、洗涤、干燥。
④取m g纯净Sr(OH)2·x H2O产品溶于水,加入过量Na2CO3溶液后过滤、洗涤、干燥后,得到n g滤渣,则x=__________(用含m、n的式子表示)。
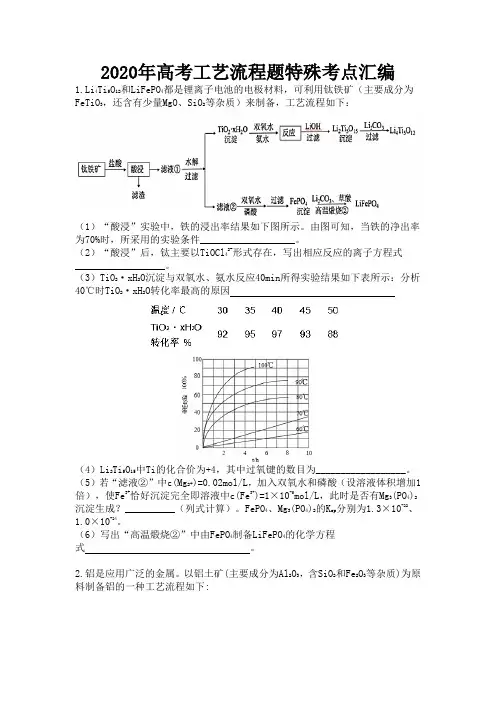
2020年高考工艺流程题特殊考点汇编1.Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:(1)“酸浸”实验中,铁的浸出率结果如下图所示。
由图可知,当铁的净出率为70%时,所采用的实验条件___________________。
(2)“酸浸”后,钛主要以TiOCl42-形式存在,写出相应反应的离子方程式__________________。
(3)TiO2·xH2O沉淀与双氧水、氨水反应40min所得实验结果如下表所示:分析40℃时TiO2·xH2O转化率最高的原因(4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为__________________。
(5)若“滤液②”中c(Mg2+)=0.02mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1×10-5mol/L,此时是否有Mg3(PO4)2沉淀生成?__________(列式计算)。
FePO4、Mg3(PO4)2的K sp分别为1.3×10-22、1.0×10-24。
(6)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式。
2.铝是应用广泛的金属。
以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为_____________________。
(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,溶液的pH_________(填“增大”、“不变”或“减小”)。
(3)“电解Ⅰ”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是___________。
(4)“电解Ⅱ”是电解Na2CO3溶液,原理如图所示。
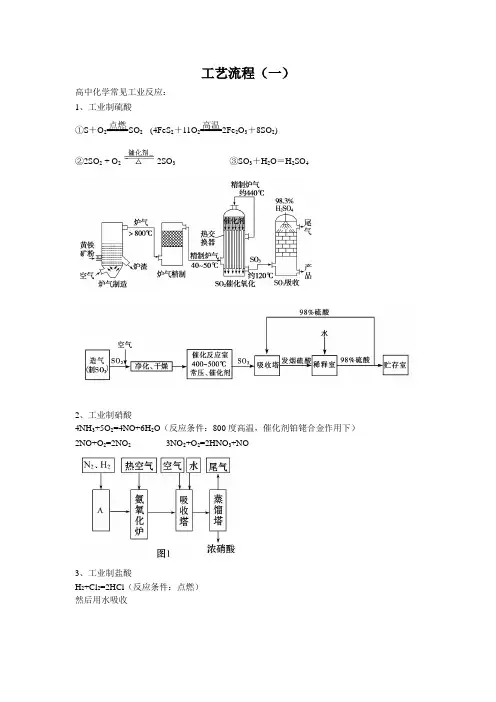
工艺流程(一)高中化学常见工业反应: 1、工业制硫酸①S +O 2=====点燃SO 2 (4FeS 2+11O 2=====高温2Fe 2O 3+8SO 2) ②2SO 2 + O 22SO 3 ③SO 3+H 2O =H 2SO 42、工业制硝酸4NH 3+5O 2=4NO+6H 2O (反应条件:800度高温,催化剂铂铑合金作用下) 2NO+O 2=2NO 2 3NO 2+O 2=2HNO 3+NO3、工业制盐酸H 2+Cl 2=2HCl (反应条件:点燃) 然后用水吸收4、工业制烧碱(氯碱工业)2NaCl+2H 2O=H 2+Cl 2+2NaOH (电解饱和食盐水)5、工业制取漂白粉(漂粉精)、漂白液 2Ca(OH)2+2Cl 2=CaCl 2+Ca(ClO)2+2H 2O 2 NaOH +Cl 2=NaCl+NaClO+H 2O6、工业制纯碱(侯氏).侯氏制碱法 NaCl +NH 3+CO 2+H 2O =NaHCO 3+NH 4Cl 1)NH 3+H 2O+CO 2=NH 4HCO 32)NH 4HCO 3+NaCl=NaHCO 3+NH 4Cl (NaHCO 3结晶析出) 3)2NaHCO 3=====△Na 2CO 3+CO 2↑+H 2O7、工业制金属铝2Al 2O 3===========950~970 ℃通电,Na 3AlF 64Al +3O 2↑利用反应 SiO 2+2C=====高温Si+2CO↑能得到不纯的粗硅。
粗硅需进行精制,才能得到高纯度硅。
首先,使Si 跟Cl 2起反应: Si+2Cl 2=SiCl 4(400 ℃~500 ℃)生成的SiCl4液体通过精馏,除去其中的硼、砷等杂质。
然后,用H 2还原SiCl 4: SiCl 4+2H 2=====高温Si+4HCl 这样就可得到纯度较高的多晶硅。
9.硅酸盐工业(制普通玻璃)生石灰 (高温煅烧石灰石) CaCO 3=====高温CaO+CO 2↑玻璃工业(玻璃窑法) Na 2CO 3 + SiO 2=====高温Na 2SiO 3 +CO 2↑ CaCO 3 + SiO 2=====高温CaSiO 3 +CO 2↑ 10.高炉炼铁3CO +Fe 2O 3=====高温2Fe +3CO 2 11.工业制取水煤气 C+H 2O=====高温CO+H 212.粗铜的精炼 电解:阳极用粗铜阳极:Cu -2e -=Cu 2+阴极:Cu 2++2e -=Cu 13、工业制氨气N 2(g)+3H 2(g) 2NH 3(g)注:催化剂为铁触媒MgCl 2(熔融)Mg +Cl 2↑15.海水提溴Cl 2+2Br -===2Cl -+Br 2Br 2+SO 2+2H 2O===2HBr +H 2SO 416.化石燃料的综合利用石油煤原料 原油煤 原理分馏、裂化、裂解干馏产品溶剂油、汽油、煤油、柴油、重油、润滑油、凡士林、乙烯、丙烯、丁烯等工艺流程(二)1.锌可作为食品锌强化剂的原料。

重要元素为题材的化学工艺流程题汇总1.【锂、铝、铁】磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片(除LiFePO4外,还含有Al箔、少量不溶于酸碱的导电剂)中的资源,部分流程如图:(1)从“正极”可以回收的金属有。
(2)“碱溶”时Al箔溶解的离子方程式。
(3)“酸浸”时产生标准状况下2.24L NO时,则被氧化的LiFePO4为mol。
(其他杂质不与HNO3反应)(4)实验测得滤液②中c(Li+)=4 mol·L-1,加入等体积的Na2CO3溶液后,Li+的沉降率到99%,则滤液③中c(CO32-)=________ mol·L-1。
[K sp(Li2CO3)=1.6×10-3](5)磷酸亚铁锂电池总反应为:LiFePO4+6C Li1-x FePO4+Li x C6,电池中的固体电解质可传导Li+。
充电时,Li+移向(填“阳极”或“阴极”);放电时,正极反应式为。
(6)磷酸亚铁锂电池中铁的含量可通过如下方法测定:称取1.40g试样用盐酸溶解,在溶液中加入稍过量的SnCl2溶液,再加入HgCl2饱和溶液,用二苯胺磺酸钠作指示剂,用0.030 mol·L-1重铬酸钾溶液滴定至溶液由浅绿色变为蓝紫色,消耗重铬酸钾溶液40.00mL。
已知:2Fe3++Sn2++6Cl-===SnCl62-+2Fe2+4Cl -+Sn 2++2HgCl 2===SnCl 62-+Hg 2Cl 26Fe 2++Cr 2O 72-+14H +===6Fe 3++2Cr 3++7H 2O① 实验中加入HgCl 2饱和溶液的目的是 。
② 磷酸亚铁锂电池中铁的含量为 。
1.答案(15分)(1)Li 、Fe 、Al (2分)(答对3个给2分,2个给1分,1个不给分)(2)2Al +2OH -+2H 2O ===2AlO 2-+3H 2↑(2分)(3)0.3(2分)(4)4(2分)(5)阴极(1分) Li 1-x FePO 4+xLi ++xe -===LiFePO 4(2分) (6)①将溶液中过量Sn 2+转化为稳定的SnCl 62-,防止其干扰Fe 2+的测定(2分) ②28.8%(2分)2.【铈】 二氧化铈(CeO 2)是一种重要的稀士氧化物。

高中化学工艺流程100题以下是关于高中化学工艺流程的一些题目,可以根据需要使用:1.化学工艺流程是将原料转化为最终产品的过程。
在石油工业中,下列哪个化学工艺流程被用来将原油分解成不同的组分? a) 裂化 b) 氧化 c) 水解 d) 酯化2.在化工生产中,反应器是一个关键设备,用于控制和促进化学反应。
下列哪个反应器类型广泛应用于液体相反应?a) 塔式反应器 b) 固定床反应器 c) 搅拌反应器 d) 流动床反应器3.化学工艺中的蒸馏是将混合物分离成不同组分的过程。
下列哪种蒸馏技术被用于分离液体混合物,其中组分沸点差异较小? a) 精馏 b) 真空蒸馏 c) 溶剂萃取 d) 分子蒸馏4.在高温下,氧气和氮气可以通过下列哪个工艺流程分离?a) 吸附 b) 含水剂萃取 c) 深冷分馏 d) 汽化凝结5.下列哪个工艺流程广泛应用于金属和合金的提取和纯化?a) 複分解反应 b) 溶剂萃取 c) 水解反应 d) 高温氧化6.下列哪个工艺流程主要用于制造硝酸?a) 溶剂萃取b) 萃取精炼 c) 蒸馏 d) 共沉淀法7.下列哪个工艺流程常用于水处理,用于去除悬浮物和杂质?a) 离子交换 b) 水解 c) 真空蒸馏 d) 逆渗透8.化学工艺流程中,下列哪个过程用于将固体转化为气体状态,以便于进一步处理? a) 溶解 b) 氧化 c) 透析 d) 热分解9.下列哪个化学工艺流程主要用于制备盐酸? a) 离子交换 b)吸附 c) 气相色谱 d) 水解10.化学工艺流程中,下列哪个过程用于将气体转化为液体状态? a) 吸附 b) 液相色谱 c) 精馏 d) 合成11.在某些化学工艺流程中,通过添加催化剂来加速反应速率。
这个过程被称为: a) 离子交换 b) 催化剂还原 c) 催化反应d) 气相析出12.下列哪个工艺流程常用于制备金属粉末?a) 溶解b) 沉淀c) 氧化 d) 高温烧结13.化学工艺流程中,下列哪个过程用于将溶液中的溶质从溶剂中分离出来? a) 热分解 b) 脱水 c) 搅拌 d) 结晶14.下列哪个工艺流程主要用于制造乙醇? a) 裂解 b) 酯化 c)醇醚化 d) 发酵15.化学工艺流程中,下列哪个过程用于将混合物通过电流分解为其组成部分? a) 电沉积 b) 离子交换 c) 沉淀 d) 气体解离16.下列哪个工艺流程广泛用于制造纸张和纤维素制品?a)光合作用 b) 氧化 c) 化学热解 d) 碱法蒸煮17.化学工艺流程中,下列哪个过程用于将金属从矿石中提取出来? a) 酸洗 b) 热解 c) 高温氧化 d) 萃取18.下列哪个工艺流程广泛用于生产塑料和纤维素? a) 氧化 b)高温烧结 c) 聚合 d) 溶剂萃取19.化学工艺流程中,下列哪个过程用于加热和冷却反应器以控制温度? a) 加压 b) 流量控制 c) 冷凝 d) 分馏20.下列哪个工艺流程常用于生产肥料和农药?a) 溶解b) 空气氧化 c) 化学合成 d) 洗涤21.化学工艺流程中,下列哪个过程用于将液体通过蒸发转化为气体? a) 吸附 b) 合成 c) 蒸馏 d) 过滤22.下列哪个工艺流程广泛用于制造肥皂和洗涤剂?a) 离子交换 b) 氧化 c) 溶解 d) 酯化23.化学工艺流程中,下列哪个过程用于将气体通过压缩转化为液体? a) 催化反应 b) 沉淀 c) 吸附 d) 压缩24.下列哪个工艺流程常用于生产纯净水? a) 水解 b) 脱色 c)萃取 d) 蒸馏25.化学工艺流程中,下列哪个过程用于将金属表面涂上一层保护性的金属涂层? a) 电沉积 b) 氧化 c) 合成 d) 分馏26.下列哪个工艺流程广泛应用于制备塑料和橡胶? a) 聚合 b)氧化 c) 合成 d) 溶剂萃取27.化学工艺流程中,下列哪个过程用于将废水中的污染物去除? a) 结晶 b) 分馏 c) 沉淀 d) 离子交换28.下列哪个工艺流程广泛用于制备化学品和药物?a) 晶须结晶 b) 脱色 c) 高温烧结 d) 合成29.化学工艺流程中,下列哪个过程用于将液体通过过滤分离出固体颗粒? a) 溶解 b) 过滤 c) 反应 d) 吸附30.下列哪个工艺流程常用于生产化学肥料?a) 溶剂萃取b)淘汰 c) 高温烧结 d) 合成31.化学工艺流程中,下列哪个过程用于将固体直接转化为气体,跳过液体状态? a) 合成 b) 热分解 c) 燃烧 d) 气体解离32.下列哪个工艺流程广泛用于制造玻璃和陶瓷?a) 溶解b)空气氧化 c) 冷凝 d) 吸附33.化学工艺流程中,下列哪个过程用于使固体颗粒变得均匀分散在液体中? a) 溶剂萃取 b) 超滤 c) 搅拌 d) 结晶34.下列哪个工艺流程广泛应用于制备电池和电器元件?a)电沉积 b) 高温烧结 c) 车窑炉烧制 d) 氧化35.化学工艺流程中,下列哪个过程用于将有机化合物转化为无机化合物? a) 氧化 b) 合成 c) 置换反应 d) 燃烧36.下列哪个工艺流程常用于生产颜料和染料? a) 溶剂萃取 b)氧化 c) 合成 d) 蒸馏37.化学工艺流程中,下列哪个过程用于从液体中蒸发水分,使溶液浓缩? a) 溶解 b) 吸附 c) 蒸馏 d) 沉淀38.下列哪个工艺流程广泛用于制备钢铁? a) 溶解 b) 精炼 c)电沉积 d) 高温煅烧39.化学工艺流程中,下列哪个过程用于将有机溶剂从溶液中去除? a) 水解 b) 细胞液化反应 c) 溶剂萃取 d) 碳化40.下列哪个工艺流程常用于制备香料和精油? a) 离子交换 b)蒸馏 c) 氧化 d) 裂化41.化学工艺流程中,下列哪个过程用于将溶液通过离子交换去除杂质? a) 离子交换 b) 吸附 c) 分离 d) 脱色42.下列哪个工艺流程广泛用于制备涂层和防腐剂? a) 合成 b)表面处理 c) 液相凝聚 d) 化学热解43.化学工艺流程中,下列哪个过程用于将气体从混合物中吸附到固体表面? a) 氧化 b) 吸附 c) 分解 d) 溶解44.下列哪个工艺流程常用于制造玻璃纤维和碳纤维?a) 电沉积 b) 细胞液化反应 c) 焙烧 d) 合成45.化学工艺流程中,下列哪个过程用于将矿石中的金属提取出来? a) 粉末冶金 b) 电解 c) 触媒剂加工 d) 煅烧46.下列哪个工艺流程广泛应用于制备石油产品如汽油和柴油?a) 裂化 b) 氧化 c) 溶剂萃取 d) 酯化47.化学工艺流程中,下列哪个过程用于将气体和液体相分离?a) 真空蒸馏 b) 离子交换 c) 搅拌 d) 超滤48.下列哪个工艺流程常用于生产纸浆和造纸?a) 溶解b) 氧化 c) 高温烧结 d) 碱法蒸煮49.化学工艺流程中,下列哪个过程用于将固体通过加热转化为液体? a) 合成 b) 热分解 c) 冷凝 d) 分馏50.下列哪个工艺流程广泛用于制造玻璃和陶瓷?a) 烧结b)液相色谱 c) 溶解 d) 硝化51.化学工艺流程中,下列哪个过程用于将固体在高温下转化为气体? a) 合成 b) 热分解 c) 反应 d) 过滤52.下列哪个工艺流程广泛用于制备电池和电子元件?a) 电沉积 b) 高温烧结 c) 氧化 d) 合成53.化学工艺流程中,下列哪个过程用于将溶液通过过滤分离出固体颗粒? a) 溶解 b) 过滤 c) 吸附 d) 分馏54.下列哪个工艺流程常用于生产化学肥料和农药?a) 溶剂萃取 b) 淘汰 c) 高温烧结 d) 合成55.化学工艺流程中,下列哪个过程用于将液体通过蒸发转化为气体? a) 吸附 b) 合成 c) 蒸馏 d) 含水剂萃取56.下列哪个工艺流程广泛用于制造颜料和染料?a) 溶剂萃取 b) 氧化 c) 合成 d) 蒸华57.化学工艺流程中,下列哪个过程用于从液体中蒸发水分,使溶液浓缩? a) 溶解 b) 吸附 c) 蒸馏 d) 结晶58.下列哪个工艺流程广泛应用于制备钢铁?a) 溶解b) 复分解反应 c) 电沉积 d) 高温煅烧59.化学工艺流程中,下列哪个过程用于将有机溶剂从溶液中去除? a) 水解 b) 脱色 c) 溶剂萃取 d) 碳化60.下列哪个工艺流程常用于制备香料和精油? a) 离子交换 b)蒸馏 c) 氧化 d) 裂化61.化学工艺流程中,下列哪个过程用于将溶液通过离子交换去除杂质? a) 离子交换 b) 吸附 c) 分离 d) 脱色62.下列哪个工艺流程广泛用于制备涂层和防腐剂? a) 合成 b)表面处理 c) 液相沉淀 d) 化学热解63.化学工艺流程中,下列哪个过程用于将气体从混合物中吸附到固体表面? a) 氧化 b) 吸附 c) 分解 d) 溶解64.下列哪个工艺流程常用于制造玻璃纤维和碳纤维?a) 电沉积 b) 聚合反应 c) 焙烧 d) 合成65.化学工艺流程中,下列哪个过程用于将矿石中的金属提取出来? a) 粉末冶金 b) 电解 c) 焙烧 d) 燃烧66.下列哪个工艺流程广泛应用于制备塑料和橡胶? a) 聚合 b)氧化 c) 合成 d) 溶剂萃取67.化学工艺流程中,下列哪个过程用于将气体和液体相分离?a) 真空蒸馏 b) 离子交换 c) 搅拌 d) 超滤68.下列哪个工艺流程常用于生产纸浆和造纸?a) 溶解b) 氧化 c) 高温烧结 d) 碱法蒸煮69.化学工艺流程中,下列哪个过程用于将固体通过加热转化为液体? a) 合成 b) 热分解 c) 冷凝 d) 分馏70.下列哪个工艺流程广泛用于制造玻璃和陶瓷?a) 烧结b)液相色谱 c) 溶解 d) 硝化71.化学工艺流程中,下列哪个过程用于将固体在高温下转化为气体? a) 合成 b) 热分解 c) 反应 d) 过滤72.下列哪个工艺流程广泛用于制备电池和电子元件?a) 电沉积 b) 高温烧结 c) 氧化 d) 合成73.化学工艺流程中,下列哪个过程用于将溶液通过过滤分离出固体颗粒? a) 溶解 b) 过滤 c) 吸附 d) 分馏74.下列哪个工艺流程常用于生产化学肥料和农药?a) 溶剂萃取 b) 淘汰 c) 高温烧结 d) 合成75.化学工艺流程中,下列哪个过程用于将液体通过蒸发转化为气体? a) 吸附 b) 合成 c) 蒸馏 d) 含水剂萃取76.下列哪个工艺流程广泛用于制造颜料和染料?a) 溶剂萃取 b) 氧化 c) 合成 d) 蒸华77.化学工艺流程中,下列哪个过程用于从液体中蒸发水分,使溶液浓缩? a) 溶解 b) 吸附 c) 蒸馏 d) 结晶78.下列哪个工艺流程广泛应用于制备钢铁?a) 溶解b) 复分解反应 c) 电沉积 d) 高温煅烧79.化学工艺流程中,下列哪个过程用于将有机溶剂从溶液中去除? a) 水解 b) 脱色 c) 溶剂萃取 d) 碳化80.下列哪个工艺流程常用于制备香料和精油? a) 离子交换 b)蒸馏 c) 氧化 d) 裂化81.化学工艺流程中,下列哪个过程用于将溶液通过离子交换去除杂质? a) 离子交换 b) 吸附 c) 分离 d) 脱色82.下列哪个工艺流程广泛用于制备涂层和防腐剂? a) 合成 b)表面处理 c) 液相沉淀 d) 化学热解83.化学工艺流程中,下列哪个过程用于将气体从混合物中吸附到固体表面? a) 氧化 b) 吸附 c) 分解 d) 溶解84.下列哪个工艺流程常用于制造玻璃纤维和碳纤维?a) 电沉积 b) 聚合反应 c) 焙烧 d) 合成85.化学工艺流程中,下列哪个过程用于将矿石中的金属提取出来? a) 粉末冶金 b) 电解 c) 焙烧 d) 燃烧86.下列哪个工艺流程广泛应用于制备石油产品如汽油和柴油?a) 裂化 b) 氧化 c) 溶剂萃取 d) 酯化87.化学工艺流程中,下列哪个过程用于将气体和液体相分离?a) 真空蒸馏 b) 离子交换 c) 搅拌 d) 超滤88.下列哪个工艺流程常用于生产纸浆和造纸?a) 溶解b) 氧化 c) 高温烧结 d) 碱法蒸煮89.化学工艺流程中,下列哪个过程用于将固体通过加热转化为液体? a) 合成 b) 热分解 c) 冷凝 d) 分馏90.下列哪个工艺流程广泛用于制造玻璃和陶瓷?a) 烧结b)液相色谱 c) 溶解 d) 硝化91.化学工艺流程中,下列哪个过程用于将固体在高温下转化为气体? a) 合成 b) 热分解 c) 反应 d) 过滤92.下列哪个工艺流程广泛用于制备电池和电子元件?a) 电沉积 b) 高温烧结 c) 氧化 d) 合成93.化学工艺流程中,下列哪个过程用于将溶液通过过滤分离出固体颗粒? a) 溶解 b) 过滤 c) 吸附 d) 分馏94.下列哪个工艺流程常用于生产化学肥料和农药?a) 溶剂萃取 b) 淘汰 c) 高温烧结 d) 合成95.化学工艺流程中,下列哪个过程用于将液体通过蒸发转化为气体? a) 吸附 b) 合成 c) 蒸馏 d) 含水剂萃取96.下列哪个工艺流程广泛用于制造颜料和染料?a) 溶剂萃取 b) 氧化 c) 合成 d) 蒸华97.化学工艺流程中,下列哪个过程用于从液体中蒸发水分,使溶液浓缩? a) 溶解 b) 吸附 c) 蒸馏 d) 结晶98.下列哪个工艺流程广泛应用于制备钢铁?a) 溶解b) 复分解反应 c) 电沉积 d) 高温煅烧99.化学工艺流程中,下列哪个过程用于将有机溶剂从溶液中去除? a) 水解 b) 脱色 c) 溶剂萃取 d) 碳化100.下列哪个工艺流程常用于制备香料和精油?a) 离子交换 b) 蒸馏 c) 氧化 d) 裂化101.化学工艺流程中,下列哪个过程用于将溶液通过离子交换去除杂质? a) 离子交换 b) 吸附 c) 分离 d) 脱色102.下列哪个工艺流程广泛用于制备涂层和防腐剂?a) 合成 b) 表面处理 c) 液相沉淀 d) 化学热解103.化学工艺流程中,下列哪个过程用于将气体从混合物中吸附到固体表面? a) 氧化 b) 吸附 c) 分解 d) 溶解上述问题能够丰富和加深学生对高中化学工艺流程的了解。

2020 年高考化学大题专项复习:化学工艺流程题1.中南大学郑雅杰等 3 位老师提出“以含砷废水沉淀还原法制备 As2O3”,有较高的实际应用价值。
某工厂含砷废水含有 H3AsO3、H2SO4、Fe2(SO4)3、Bi2(SO4)3 等,利用该废水提取As2O3 的流程如图所示。
表:金属离子沉淀 pH 值表格(20℃)(1)为了加快中和过程的速率,可以采取的措施有______________(施即可)。
(2)沉淀中的成分,除了 Bi(OH)3 沉淀外,还有。
(3)A 可以循环利用,A 的化学式为_________。
在滤液 1 中,加入 NaOH 调节 pH 为 8 的目的是。
(4)Cu3(AsO3)2 沉淀加入一定量的水调成浆料,通入 SO2,该过程的化学反应方程式是。
(5)按照一定的液固比,将水加入 Cu3(AsO3)2 沉淀中,调成浆料。
当反应温度为25℃,SO2 流量为 16L/h,液固比、时间对砷、铜浸出率的影响如图甲、乙所示。
请选择最适宜的液固比、反应时间:______________、_______________。
(6)一定条件下,用雄黄(As4S4)制备 As2O3 的转化关系如图所示。
若反应中,1mol As4S4(其中 As 元素的化合价为+2 价)参加反应时,转移 28mole-,则物质 a 为_______(填化学式)。
【答案】(1)适当增加氢氧化钠溶液的浓度或加热(2)Fe(OH)3(3)CuSO4 完全沉淀 Cu2+,回收利用铜(4)Cu3(AsO3)2+3SO2+6H2O=Cu3(SO3)2·2H2O+2H3AsO3+H2SO4(5)4:1 60min SO2【解析】(1)为了加快中和的速率,可以通过浓度、温度来调节反应的速率。
(2)根据元素守恒进行判断。
(3)Cu3(SO3)2·2H2O 氧化可以得到 CuSO4,在流程中可以循环利用。
(4)根据氧化还原反应中化合价升降守恒可知 S 的化合价升高,根据信息写出反应物和产物并配平方程式。
2020年高三化学工艺流程题专项训练题学校:___________姓名:___________班级:___________考号:___________注意事项:注意事项: 2、请将答案正确填写在答题卡上第1卷一、填空题4。
一种以软锰矿(含2MnO ,及少 量2SiO 杂质)和黄铁矿(主要成分为FeS 2)为原料生产42MnSO H O g 的工艺流程如下:已知:球磨是在封闭的设备中,利用下落的研磨体(如钢球、鹅孵石等)的冲击作用以及研磨体与球磨内壁的研磨作用而将物料粉碎并混合。
回答下列问题: (1)“球磨”的目的是。
(2)通入空气“焙烧”的目的是。
(3)“一系列操作”包括 、过滤等。
结合流程中物质的转化关系,说明“母液A ”不能丟弃的原因是。
(4)“碱浸”中发生的离子反应方程式是,“滤渣B ”的成分是(写方程式),“母液B ”中的盐类溶质是(填名称)。
(4)取一定量母液A 加入43NH HCO 可制得高性能强磁性材料3MnCO ,该反应为2+332Mn +HCO Mn +X H C O O +→↓↑,X 的电子式是。
已知常温时,0.11mol L -g 43NH HCO 溶液中含氮(或含碳)微粒分布分数α与pH 的关系如图所示,则a122(H CO )K 、b 32(NH H O)K g 、a222(H CO )K 的大小关系为.2.镍钴锰酸锂电池是一种高功率动力电池。
采用废旧锂离子电池回收工艺制备镍钴锰酸锂三元正极材料(铝电极表面涂有1x y x y 2LiNi Co Mn O --)的工艺流程如图所示:回答下列问题(1)废旧锂离子电池拆解前进行“放电处理”有利于锂在正极的回收,其原因是_______。
(2)能够提高“碱浸”效率的方法有______(至少写两种)。
(3)“碱浸”过程中,铝溶解,在该反应中每产生1mol 非极性共价键放出133.3Kj 的热量 请写出该反应的热化学方程式 。
2020年高考试题分类汇编化学工艺流程题1.[2019新课标Ⅰ 26](14分)钒具有广泛用途。
黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO 2、Fe 3O 4。
采用以下工艺流程可由黏土钒矿制备NH 4VO 3。
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH 如下表所示:回答下列问题:(1)“酸浸氧化”需要加热,其原因是___________。
(2)“酸浸氧化”中,VO +和VO 2+被氧化成,同时还有___________离子被氧化。
写出VO +转化为反应的离子方程式___________。
(3)“中和沉淀”中,钒水解并沉淀为,随滤液②可除去金属离子K +、Mg 2+、Na +、___________,以及部分的___________。
(4)“沉淀转溶”中,转化为钒酸盐溶解。
滤渣③的主要成分是___________。
(5)“调pH”中有沉淀生产,生成沉淀反应的化学方程式是___________。
(6)“沉钒”中析出NH 4VO 3晶体时,需要加入过量NH 4Cl ,其原因是___________。
【答案】26.(1)加快酸浸和氧化反应速率(促进氧化完全) (2)Fe 2+ VO ++MnO 2 +2H + =2VO ++Mn 2++H 2O(3)Mn 2+ Al 3+和Fe 3+ (4)Fe(OH)3(5)NaAl(OH)4+ HCl= Al(OH)3↓+NaCl+H 2O (6)利用同离子效应,促进NH 4VO 3尽可能析出完全2VO +2VO +252V O H O x ⋅252V O H O x ⋅2.[2020新课标Ⅲ27](15分)某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。
采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:金属离子Ni2+Al3+Fe3+Fe2+开始沉淀时(c=0.01 mol·L−1)的pH 沉淀完全时(c=1.0×10−5 mol·L−1)的pH 7.28.73.74.72.23.27.59.0回答下列问题:(1)“碱浸”中NaOH的两个作用分别是______________。
大题01 化学工艺流程题(一)1.钼酸钠晶体(Na2MoO4·2H2O)是一种金属腐蚀抑制剂。
工业上利用钼精矿(主要成分是不溶于水的MoS2)制备钼酸钠的两种途径如图所示:(1)途径I碱浸时发生反应的化学反应方程式为________________________________________。
(2)途径II氧化时还有Na2SO4生成,则反应的离子方程式为_____________________________。
(3)已知途径I的钼酸钠溶液中c(MoO42-)=0.40 mol/L,c(CO32-)=0.10mol/L。
由钼酸钠溶液制备钼酸钠晶体时,需加入Ba(OH)2固体以除去CO32-。
当BaMoO4开始沉淀时,CO32-的去除率是____________[已知K sp(BaCO3)=1×10-9、K sp(BaMoO4)=4.0×10-8,忽略溶液的体积变化]。
(4)分析纯的钼酸钠常用钼酸铵[(NH4)2MoO4]和氢氧化钠反应来制取,若将该反应产生的气体与途径I所产生的气体一起通入水中,得到正盐的化学式是__________________________。
(5)钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。
常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如下图:①当硫酸的浓度大于90%时,碳素钢腐蚀速率几乎为零,原因是________________________。
②若缓释剂钼酸钠-月桂酸肌氨酸总浓度为300mg·L-1,则缓蚀效果最好时钼酸钠(M=206g/mol) 的物质的量浓度为__________________(计算结果保留3位有效数字)。
(6)二硫化钼用作电池的正极材料时接受Li+的嵌入,锂和二硫化钼形成的二次电池的总反应为:xLi+nMoS2Li x(MoS2)n。
则电池放电时正极的电极反应是:_____________________。