消毒记录登记表.doc
- 格式:doc
- 大小:42.50 KB
- 文档页数:2
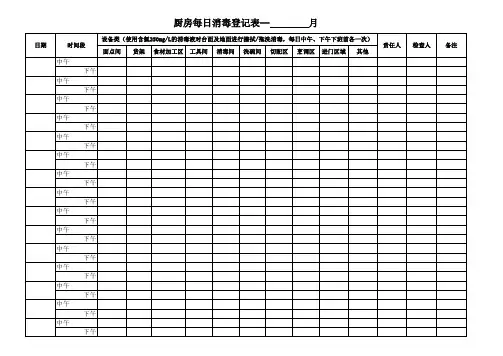

桌面、台面消毒登记表日期消毒1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭签名日期消毒1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭1000mg/L含氯消毒剂擦拭签名xx区中医院桌面、台面消毒登记簿2016年5月至10月科室:肠道门诊。
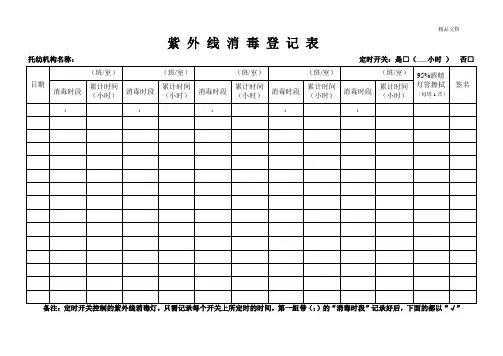
紫外线消毒登记表
托幼机构名称:定时开关:是□(___小时)否□
日期
(班/室)(班/室)(班/室)(班/室)(班/室)95%酒精
灯管擦拭
(每周1次)
签名消毒时段
累计时间
(小时)
消毒时段
累计时间
(小时)
消毒时段
累计时间
(小时)
消毒时段
累计时间
(小时)
消毒时段
累计时间
(小时):::::
备注:定时开关控制的紫外线消毒灯,只需记录每个开关上所定时的时间,第一组带(:)的“消毒时段”记录好后,下面的都以“√”
表示,“累计时间”填写具体数字,如是手动开关的就需详细记录每天的开和关时间,95%酒精灯管擦拭做“△”。
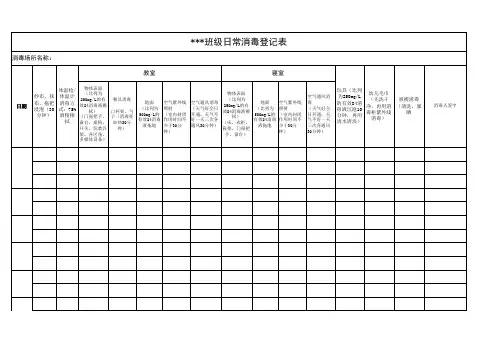

XXXX人民医院检验科消毒记录表(可以直接使用,可编辑实用优秀文档,欢迎下载)
XXXXX人民医院检验科消毒记录表
科室名称:室201 年月日
填表说明:1、工作人员每日以0.2%过氧乙酸或1000㎎/L氯消净抹拭工作台面一次,台面受污染时及时消毒,并按规定浸泡消毒所以消耗品,工作结束后及时清洗。
2、空气消毒,紫外线照射30-60分钟。
3、一次性采血管及其他污染品收集后登记交处理站。
4所有工作结束后工作人员按洗手要求严格洗手。
5、及时检查并更换消毒液。
XXXXXXX医院检验科
标本接收登记表
备注:信息系统故障时使用。
检验科消毒用品有效性监测记录表。

消毒登记表_附件3消毒记录表整理表姓名:职业工种:申请级别:受理机构:填报日期:附件3:消毒记录表消毒记录表表1:场所清洁消毒记录表场所名称:备注:清洗消毒方式包括清扫、冲洗、杀虫、消毒等。
表2:供应商评价表量合格检验报告,其他原辅料的合格供应商还应持有有效的营业执照和生产(流通)许可证(生产许可证仅针对已纳入生产许可证管理产品),否则不得列为合格供应商。
表3:合格供应商汇总表表4:到货通知单到货日期:年月日表5:采购物资检验/验证结果通知单企业采购的物资须有出厂检验合格证或质量检验合格报告。
2、对无法提供合格证明文件的采购物资,应当依照食品安全标准进行检验。
3、对有产品合格证明文件的采购物资,企业可根据管理要求进行必要的检验。
表6:采购物资出入库台账备注:本表用于单一采购物资的管理。
表7:进货台账表8:配料记录表表9:内部学习培训记录学习内容:学习方式:授课人:日期:年月日课时:表10:外出学习情况登记表表11:从业人员健康检查档案表12:不合格品处置记录编号:表13:机器设备维修清洗保养卡设备名称:设备编号:年月表14:投料记录表表15:领料单领料单位:年月日领料:审批:发料:年月日年月日年月日(共三联,第一联:存根,第二联:仓库,第三联:领料单位)表16:成品出入库台账产品名称/代号:包装规格:仓管员:表17:产品销售台账表18:抽检产品留样记录备注:本表仅适用于有对出厂产品进行留样管理的企业。
表19:委托出厂检验登记表时间:年月日备注:本表适用于对出厂产品进行全项目或部分项目委托检验的企业。
表20:成品检验报告单表21:食品安全风险分析记录表表22:不合格品销毁记录表企业名称:表23:食品召回措施报告注:本报告一式两份,一份交食品药品监督管理部门部门,一份企业留存。
表24:食品召回阶段性进展报告注:本报告一式两份,一份交食品药品监督管理部门部门,一份企业留存。
表25:食品召回总结报告注:本报告一式两份,一份交食品药品监督管理部门部门,一份企业留存。