高中化学碳族元素和硼族元素竞赛解析
- 格式:pdf
- 大小:158.25 KB
- 文档页数:7





第十五章 硼族元素Chapter 15 The Boron Family ElementsBoron (B) Aluminum (Al) Gallium (Ga) Indium (In)Thallium (Tl)Electron configuration :n s 2n p 1§15-1 硼及其化合物 Boron and its Compounds一、General Properties1.硼的化学性质与Si 有某些相似之处(对角线相似原则),通常硼呈现+3氧化态,负氧化态的情况很少.硼与金属形成非化学计量的化合物(nonstoichiometric compounds ),M 4B 、M 2B 、MB 、M 3B 4、MB 2、MB 6等.(1) B 2O 3与SiO 2都是固态酸性氧化物,Al 2O 3是两性,CO 2是气态酸性; (2) H 3BO 3与H 4SiO 4都是很好的酸; (3) 多硼酸盐与多硅酸盐结构相似;(4) 硼烷、硅烷可形成多种可燃性气态物质,而AlH 3是固态. 2.在自然界中,硼以硼砂(borax ):Na 2B 4O 7·10H 2O,四水硼砂(kernite ):Na 2B 4O 7·4H 2O,天然硼酸 ( sassolite ):H 3BO 3存在.3.硼在自然界中丰度之所以低,是因为Li He B 734210105+→+n ,所以硼材料可作为核反应堆的减速剂和生物防护. 二、The Simple Substance1.Boron has several allotropic forms. 无定形硼为棕色粉末, The crystals ofboron are black. 高熔沸点(m.p. 2300℃,b.p. 2550℃)单质硼有多种复杂的晶体结构,其中最普通的一种是α - 菱形硼,其基本结构单元为正二十面体的对称几何构型,然后由B 12的这种二十面体的布起来组成六方晶系的α - 菱形硼. 2.Properties(1) 硼和硅一样在常温下较惰性,仅与F 2反应.对于单质硼的同素异构形体而言,结晶状单质硼较惰性,无定形硼则比较活泼,在高温下:(2)单质硼作还原剂: 3SiO 2 + 4B强热3Si + 2B 2O 3 2B + 6H 2O(g)赤热2B(OH)3 + 3H 2↑ (3) 与氧化性的酸反应,生成H 3BO 3 (4) 在有氧化剂存在时,与碱反应:B 2S 3B BCl 3B 2O 3BN O 2S Cl 2N2Fig 15.1 Icosahedral arrangement of B 122B + 2NaOH + 3KNO 3共熔2NaBO 2 + 3KNO 2 + H 2O3.Preparation : (1) 金属还原: B 2O 3 + 3Mg 2B + 3MgO KBF 4 + 3Na3NaF + KF + B(2) 工业上:从硼镁矿 → 单质硼 → 精制硼 a .用浓碱溶液来分解硼镁矿: Mg 2B 2O 5·5H 2O + 2NaOH 2NaBO 2 + 2Mg(OH)2 + 4H 2O b .通入CO 2调节碱度,分离出硼砂 4NaBO 2 + CO 2 + 10H 2O Na 2B 4O 7·10H 2O + Na 2CO 3 c .用H 2SO 4调节酸度,可析出溶解度小的硼酸晶体:Na 2B 4O 7 + H 2SO 4 + 5H 2O 4H 3BO 3 + Na 2SO 4d .加热,脱水: 2H 3BO 3B 2O 3 + 3H 2Oe .用Mg 或Al 还原成粗硼:B 2O 3 + 3Mg 2B + 3MgO f .精制:2B (粗) + 3I 22BI 32BI 31000-1300K钽丝2B(α - 菱形硼) + 3I 2三、Compounds 1.Boron hydrides:(1) 这类氢化物的物理性质相似于烷烃(paraffin ),故称硼烷(Borane ).多数硼烷组成是B n H n + 4、B n H n + 6,少数为B n H n + 8、B n H n + 10.但最简单的硼烷是B 2H 6.BH 3之所以不存在是由于B 的价轨道没有被充分利用,且配位数未达到饱和,又不能形成稳定的sp 2杂化态的离域π键,所以 BH 3(g) + BH 3(g)B 2H 6(g) ∆r G m,298 =-127kJ ·mol -1而BF 3之所以存在,是因为 64Π的存在.(2) preparation : a .质子置换法: ++3H MnB ++362Mn H B 21b .氢化法: 233H BCl +HCl 3H B 2162+ c .氢负离子置换法: 34BF 43LiAlH +ether 362AlF 33LiF H 2B ++ 344BF 3NaBH +ether4623NaBF H 2B +(3) 硼烷的结构特点:它是缺电子化合物(electron deficient compound ),例如B 2H 6中价电子总共只有12个,不足以形成七个二中心二电子单键(2c-2e),B 原子采取sp 3杂化,位于一个平面的BH 2原子团,以二中心二电子键连接,位于该平面上、下且对称的H 原子与硼原子分别形成三中心二电子键,称为氢桥键.其分子轨道能级图为:在各种硼烷中呈现五种成键情况:a . 2c —2e 端侧b . 3c —2e 氢桥键c . 2c —2e 硼硼键d . 开放式 3c —2e 硼桥键e . 闭合式 3c —2e 硼桥键1957-1959年,Lipscomb.W.N 提出了解决硼氢化合物的“三中心键理论”,获得了巨大的成功,荣获1976年Nobel 化学奖. “硼氢化合物拓扑理论”对于B n H n + m :s 表示硼烷分子中氢桥键数目 t 表示硼桥键数目y 表示硼硼(B -B )键数 x 表示(BH)n (端基氢)以外的切向B -H 基团的数目根据守恒原理:氢原子守恒:s + x = m B 原子的价电子守恒:s + 2t + 2y + x = 2nB 原子的轨道守恒:2s + 3t + 2y + x = 3n s + x = m①即 s + 2t + 2y + x = 2n ②2s + 3t + 2y + x = 3n ③由②、③ 得:s + t = n由①、② 得:m n y t 21-=+x = m - s B 4H 10 (4012)∴ t = n - sy = s -21m例: B 2H 6 (2002) (styx ) (4) properties :B 的两个 sp 3杂化轨道H 的 1s 原子轨道三中心二电子键σσnonσ*Fig 15.2 Structure of biborane, B 2H 6实际上 3B 2H 6(g) + 6NH 3(g)2B 3N 3H 6(l) + 12H 2(g) B 3N 3H 6(l) + 3HCl(g)B 3N 3H 9Cl 3(s)NaBH 4B 3N 3H 12(5) applications :a .火箭燃料:B 2H 6(g) + 3O 2(g) B 2O 3(g) + 3H 2O(l) ∆c H m =-2152.5kJ ·mol -1B 2H 6理应是理想的火箭燃料,但由于所有硼烷有很高的毒性(B 2H 6 0.1ppm 致死),且贮存条件苛刻(易燃且水解:B 2H 6 + 6H 2O 2H 3BO 3 + 6H 2),只好暂时放弃.b .万能还原剂(在有机化学上) 2NaH + B 2H 62NaBH 4c .可以制备聚合物,高温稳定,低温保持粘度不变d .硼烷化合物与蛋白质结合,用于肿瘤治疗 2.卤化物(Boron halides )(1) preparation :3CaF 2 + B 2O 3 + 3H 2SO 4(浓)2BF 3↑+ 3CaSO 4 + 3H 2O B 2O 3 + 3C + 3Cl 22BCl 3 + 3CO (2) properties :a .hydrolysis :OH 64BF 23+343B(OH)BF 3O 3H ++-+ BF 3 + 3H 2O 3HF + H 3BO 3BF 3 + HF + H 2O -4BF + H 3O +BCl 3 + 3H 2O B(OH)3 + 3HClb .与碱性物质反应:4BF 3 + 2Na 2CO 3 + 2H 2O 3NaBF 4 + NaB(OH)4 + 2CO 2↑可以看作首先形成HBF 4 + H 3BO 3,再与Na 2CO 3碱性物质反应.3.含氧化物 (1) B 2O 3a .易溶于水:B 2O 3 + 3H 2O 2H 3BO 3 所以它是吸水剂.b .硼珠试验:熔融的B 2O 3可熔解许多金属氧化物反应可得到特征颜色:CuO + B 2O 3Cu(BO 2)2 (蓝色) NiO + B 2O 3Ni(BO 2)2 (绿色)c .与NH 3反应,在500℃生成(BN)n ,与石墨结构相似. B 2O 3(s) + 2NH 3(g) 1000℃2BN(s) + 3H 2O(g)(2) H 3BO 3a .硼酸为一元弱酸,呈片状晶体结构,OH 间以氢键连接OH B(OH)23++-+H B(OH)4在冷水中溶解度小,在热水中因部分氢键断裂而使溶解度增大.b .与碱反应:2NaOH + 4H 3BO 3Na 2B 4O 7 + 7H 2O 过量NaOH 使Na 2B 4O 7变成NaBO 2Na 2B 4O 7 + 2NaOH4NaBO 2 + H 2Oc .H 3BO 3的酸性可因加入甘油或甘露醇等多元醇而大大增强HOBOOH HHOCH 2CHOHCH 2OH+H 3O + H 2O++OCH 2CHOH 2OB O [ ]d .H 3BO 3也表现出微弱的碱性3HCl )B(PO POH B(OH)4433++(3) 一些硼酸盐阴离子结构a .环状 -332)(BO ,在KBO 2,NaBO 2晶体中b .zig —zag chains -n n )(BO 2,在Ca(BO 2)2,LiBO 2中4NaBO 2 + CO 2 + 10H 2O Na 2[B 4O 5(OH)4]·8H 2O + Na 2CO 3 c .硼砂:Na 2B 4O 7·10H 2ONa 2[B 4O 5(OH)4]·8H 2ONa 2B 4O 7 + H 2SO 4(浓) + 5H 2O4H 3BO 3↓+ NaSO 4-2454](OH)O [B :-452O B 焦硼酸盐:d .硼酸盐阴离子结构式的特点: B 原子采取sp 2杂化33BO -:Mg 3(BO 3)2 ,LaBO 3 ; (B 2O 5)4-:Mg 2B 2O 5 ,Fe 2B 2O 5 ; (B 3O 6)3-:K 3B 3O 6 ,Ba 3(B 3O 6)2 (BBO 晶体) ; 2(BO )n n -:Ca(BO 2)2(s)B 原子采取sp 3杂化54BO -:TaBO 4 ; 4B(OH)-:Na 2[B(OH)4]Cl ;Mg[B 2O(OH)6][B 2(O 2)(OH)4]2-:Na 2[B 2(O 2)2(OH)4]·6H 2O B 原子既采取sp 2又采取sp 3杂化K[B 5O 6(OH)4]·2H 2O ,Ca[B 3O 3(OH)5]·H 2O ,Na 2[B 4O 5(OH)4]·8H 2O从上面的各种硼酸盐阴离结构式来看:当B 原子的端基是OH 基团时,硼酸根离子的结构式中,sp 3杂化的硼原子数目等于硼酸根阴离子的电荷数.凡是四个或四个以上硼酸根相连时,绝大多数的结构是B 原子以三配位或四配位同氧原子结合形成的.KB 5O 8·4H 2OKB 5O 6(OH)4·2H 2O煮OB O OB B O O B O O B O O B O OB OOHO B OO B B O OOB OHOHB OO OB OO HOB O B HOO O B OOBB O OH OH-] [硼砂也可以作硼珠试验. Na 2B 4O 7 + CoO 2NaBO 2·Co(BO 2)2 (蓝色) 3Na 2B 4O 7 + Cr 2O 36NaBO 2·2Cr(BO 2)3 (绿色)硼砂除了鉴别金属外,还可以用来焊接金属,因为它可以消除金属表面的氧化物.1971年美国结构化学家K.Wade 在分子轨道理论基础上提出了一个预言硼烷,硼烷衍生物及其它原子簇化合物结构的规则,通常称为“Wade 规则”,其含义是硼烷、硼烷衍生物及其它原子簇化合物的结构是由其骨架成键电子对数决定的.若以b 表示骨架成键电子对数,n 为骨架原子数,则b = n + 1为闭式结构(closo),b = n + 2为巢式结构(nido ),b = n + 3为网式结构(arachno ),b = n + 4为链式结构(hypho ).这意味着随着硼烷骨架上的成键电子对数目增加,其完整程度逐一降低,开口程度不断增加.对于中性硼烷、硼烷阴离子,碳硼烷的结构均可用下式表示:[(CH)a (BH)p H q ]d -CH 提供给骨架3个电子,BH 提供给骨架2个电子,S 提供给骨架4个电子,P 提供给骨架3个电子给骨架,因为当硫原子和磷原子取代硼烷中的硼原子时,S 、P 原子上必有一对价电子指向骨架外侧,成为孤对电子对,所以键合时,S 原子提供4个电子,P 原子提供3个电子.则多面体骨架成键电子数 d q p a M +++=23,由于n p a =+,则:d q a n M +++=2 ∴b (骨架成键电子对数))(21d q a n +++=对于-2H B n n :a = 0,q = 0,d = 2,,所以b = n + 1,为闭式结构B 11SH 11,B 10CPH 11为闭式,B 3C 2H 7,B 5SH 10为巢式.Practice Exercise :应用Wade 规则,指出下列物质所属的结构类型:14108362421129112926695H B H B H C B H C B H C B H B H B ,,,,,,--- 11972318101510SH B H C B H B H B ,,,-。

化学竞赛无机化学绝密课件硼族元素-(含多场合)化学竞赛无机化学绝密课件硼族元素摘要:本文主要介绍了化学竞赛中无机化学部分的重要知识点——硼族元素。
通过对硼族元素的概述、性质、化合物以及应用等方面的详细讲解,旨在帮助参赛者更好地掌握这一部分内容,提高化学竞赛成绩。
一、硼族元素概述硼族元素位于元素周期表的第二族,包括硼(B)、铝(Al)、镓(Ga)、铟(In)和铍(Tl)等元素。
硼族元素在自然界中分布广泛,其中硼和铝是地壳中含量较多的元素。
硼族元素在化学性质上具有一定的相似性,但在物理性质和应用方面存在较大差异。
二、硼族元素的性质1.电子结构:硼族元素的原子结构中,最外层电子数为3个,因此它们在化学反应中容易失去3个电子,形成+3价离子。
2.金属性和非金属性:从上到下,硼族元素的金属性逐渐增强,非金属性逐渐减弱。
硼和铝具有较强的非金属性,而铟和铍的金属性较强。
3.离子半径:硼族元素的离子半径随着原子序数的增加而增大,这是因为原子核对最外层电子的吸引力逐渐减弱。
4.电负性:硼族元素的电负性随着原子序数的增加而减小,这是因为原子核对最外层电子的吸引力逐渐减弱。
三、硼族元素的化合物1.氧化物:硼族元素与氧元素形成的氧化物具有多种类型,如硼酸、氧化铝、氧化镓等。
这些氧化物在工业、医药等领域具有广泛的应用。
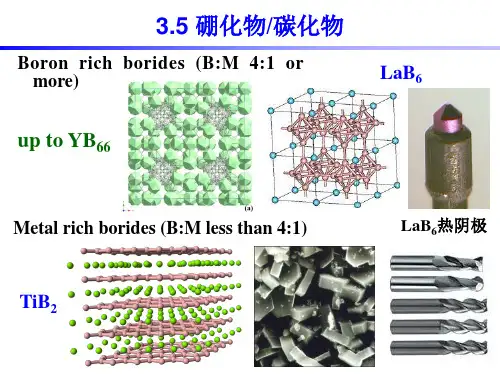
2.硼化物:硼族元素与金属元素形成的硼化物具有高熔点、高硬度和良好的导电性等特点,如碳化硼、氮化硼等。
3.氢化物:硼族元素与氢元素形成的氢化物在有机合成中具有重要应用,如硼氢化钠、硼氢化铝等。
4.硼酸盐:硼酸盐是一类重要的无机化合物,如硼砂、硼酸铝等。
它们在玻璃、陶瓷、洗涤剂等领域具有广泛应用。
四、硼族元素的应用1.金属铝:铝是硼族元素中应用最广泛的元素,广泛应用于建筑、交通、包装、电力等领域。
铝具有良好的导电性、导热性和轻质等特点,是国民经济的重要支柱产业。
2.硼化合物:硼化合物在农业、医药、化工等领域具有重要应用。



第十一章 碳族和硼族元素11. 1. 01 石墨和金刚石:石墨的硬度小,熔点极高,具有如下面左图所示的层状结构。
层中碳原子碳原子 sp 2 杂化,每个碳原子与相邻的3个碳原子成 σ 键,构成平面层。
各碳原子的 p z 轨道均垂直于上述平面层,互相平行,在层内形成大π键 。
因为有离域 π 电子,所以石墨导电。
层间的分子间作用力小,易滑动,故石墨有润滑性。
层内的共价键和层间的分子间力,使得石墨成为典型的混合晶体。
木炭和焦炭基本属于石墨类型,但是晶形不完整。
金刚石的硬度最大,熔点极高,它的结构如下面右图所示,其中碳原子 sp 3 等性杂化,每个碳原子与相邻4个碳原子成 σ 键。
由于无自由电子,故金刚石不导电。
金刚石属于典型的原子晶体。
11. 1. 02 碳簇:以 C 60 为代表的碳簇,是碳单质的第3种同素异形体,碳簇是 20 世纪 80 年代被发现的。
可以从正二十面体出发去理解 C 60 的几何构型。
如下面左图所示,正二十面体共有20个面,每个面都是正三角形;共12个顶点;每个面角都是五面角。
将每个顶角都截掉,截口处产生12个正五边形,原来的20个正三角形都变成了正六边形。
C 60 的几何构型就是这种截角正二十面体,如下面右图所示,共有 20 个正六边形,12 个正五边形。
11. 1. 03 碳在冶金工业中的用途:冶金工业上,用碳作还原剂还原金属氧化物矿物,例如下面的反应FeO + C ======= Fe + CO ↑是炼铁过程中的重要步骤。
一些金属硫化物矿经高温焙烧转化为氧化物后,也要用碳在高温下还原以得到金属。
11. 1. 04 二氧化碳的分子结构:CO 2 的分子为直线形。
CO 2分子中的C 原子sp 等性杂化,sp 杂化轨道与两个O 原子的p 轨道成两个σ键。
不参加杂化的p y 轨道有一个单电子,左边O 原子的 p y 轨道有一对电子,右边O 原子的p y 轨道有一个单电子,所以在 y 方向形成一个 。