高中化学专题五为现代农业技术添翼5.3无土栽培技术名师制作优质教案苏教版选修2
- 格式:doc
- 大小:75.50 KB
- 文档页数:1



第一单元土壤酸碱性的改良[知识回顾]1.溶液酸碱性及酸碱程度的测定方法2.土壤酸碱对作物生长有哪些影响?[知识学习]1.土壤的酸碱性测定方法:2.造成土壤酸碱性的可能的因素有哪些?3.阅读土壤酸碱性的改良,回顾并思考改良中可能遇到的问题。
4.中水灌溉农田有哪些优点和不足?第二单元化肥的生产与合理利用[知识回顾]1工业上如何合成氨?2物质分离的方法有哪些?3双水解与离子共存。
[知识学习]1化肥的分类:2按照作物对养分需求量的多少分:大量元素肥料,包括氮肥、磷肥和钾肥;中量元素肥料,包括钙、镁、硫肥;微量元素肥料,包括锌、硼、锰、钼、铁、铜肥;此外,还有一些有益元素肥料如含硅物料、稀土元素等。
主要肥料:(1) 氮肥:即以氮素营养元素为主要成分的化肥,(2) 包括尿素、碳酸氢铵(碳铵)、氯化铵、硫酸铵、硝酸铵、硝酸钙,(3) 氨水、等。
(4) 磷肥:即以磷素营养元素为主要成分的化肥,(5) 包括普通过磷酸钙(普钙)、重过磷酸钙(重钙,(6) 也称双料、三料过磷酸钙)、钙镁磷肥等。
(7) 钾肥:即以钾素营养元素为主要成分的化肥,(8) 目前施用不(9) 多,(10) 主要品种有硫酸钾、氯化钾、盐湖钾肥、窑灰钾肥和草木灰等。
(11) 复(12) 、混肥料:即肥料中含有两种肥料三要素(氮、磷、钾)的二元复(13) 、混肥料和含有氮、磷、钾三种元素的三元复(14) 、混肥料。
其中混肥在全国各地推广很快。
复(15) 混肥是同(16) 时含有氮、磷、钾中两种或两种以上成分的肥料,(17) 按照制造方法分为两类,(18) 复(19) 合肥料和混合肥料。
最常见的复(20)合肥是磷酸氢二铵(磷铵),(21) 此外还有尿素磷铵、硝酸磷铵、硫磷酸铵、硝酸磷肥、磷酸二铵、硝酸钾等。
(22) 微量元素肥料和某些中量元素肥料:前者如含有硼、锌(23) 、铁、钼、锰、铜等微量元素的肥料,(24) 后者如钙、镁、硫等肥料。
最常用的硼肥为硼砂,锌(25) 肥为硫酸锌,(26) 锰肥为硫酸锰,(27) 钼肥为钼酸铵,(28) 铜肥为硫酸铜,(29)铁肥为硫酸亚铁及一些有机态铁络合物。


苏教版选修2《化学与技术》专题5 为现代农业技术添翼第三单元无土栽培技术海门市四甲中学陆卫星一、教材分析:无土栽培技术是现代农业中非常重要的一个项目,对人们的生产生活带来很大的方便。
无土栽培集合生物、工程、化学等多个学科相关知识于一体的农业技术,学生在这方面的相关知识储备较少。
本节课主要从化学的角度来认识无土栽培技术,感受化学在农业方面的重要作用。
本节课围绕无土栽培的整个过程来设计栏目、问题和活动,引导学生进行知识重构,促进学生能力发展,提升学生的核心素养。
二、学情分析:学生在《必修一》中学习了溶液的配制,初步掌握了配制溶液的仪器的使用(如容量瓶),但学生在日常生活中很少有将书本知识与实际生产生活相结合的具体案例,本节课学习是一个提升学生社会责任核心素养的契机。
本节课希望学生在原有的基础上有新的突破和发展,形成观念、巩固概念,并促进学生的和谐发展,激发和维持学生的学习兴趣和热情。
三、教学目标:1、通过学习本部分内容,使学生了解无土栽培的常见类型和常用方法。
2、通过无土栽培活动的体验,培养学生的科学态度、创新精神。
3、了解无土栽培的优点和对农业生产的积极意义,培养学生积极的情感态度和价值观,使学生逐步树立责任心和使命感。
四、教学重点、难点教学重点:无土栽培的方法。
教学难点:无土栽培的原理、类型和方法。
五、教学方法问题引导、活动导学、自主互助、演绎归纳六、教学思路从现代农业的案例引入话题,然后从无土技术栽培需要的几个重要环节硬件—种植对象---营养液等几个角度进行展开研讨。
七、教学过程八、板书设计1、无土栽培与传统栽培的比较各自的优缺点2、无土栽培的所需硬件及对象3、营养液的配制4、学习与实践。


真诚为您提供优质参考资料,若有不当之处,请指正。
2019-2020年高中化学专题五为现代农业技术添翼5.3无土栽培技术教案苏教版选修[知识回顾]1.何为溶液呈电中性?[知识学习]1.营养液配制与无土栽培实验(1)母液的配制(2)营养液的配制(3)用营养液培养植(4)物幼苗2.营养液的酸碱度调整营养液的酸碱度直接影响营养液中养分存在的状态、转化和有效性。
如磷酸盐在碱性时易发生沉淀,影响利用;锰、铁等在大事性溶液中由于溶解度降低也会发生缺乏症。
所以营养液中酸碱度(即pH)的调整是不可忽略的。
pH值的测定可采用混合指标剂比色法,根据指示剂在不同的pH值的营养液中显示不同颜色的特性,以确定营养液的pH值。
如果水源的pH值为中性或微碱性,则配制成的营养液pH值与水源相近,如果不符要进行调整。
在调整pH值时,应先把强酸、强碱加水稀释(营养液偏碱时多用磷酸或硫酸来中和,偏酸时用氢氧化钠来中和),然后逐滴加入到营养液中,同时不断用pH试纸测定,至成中性为止。
[知识巩固]5.现有MgCl2、KCl、Na2SO4三种物质的混合液中,已知C Cl-=1.5mol/L,C K+┼C Na+ =1.5mol/L,C SO42-=0.5mol/L,则C Mg2+应是mol/L。
6.在无土栽培中,须配制一定量含50molNH4Cl、16molKCl和24molK2SO4的营养液。
若用KCl、NH4Cl和(NH4)2SO4三种固体来配制,三者的物质的量依次是(单位:mol):A、2、64、24B、64、2、24C、32、50、12D、16、50、247.硝酸钠10克、过磷酸钙70克、硫酸铵25克、硫本钾35克、硫酸镁40克。
计算以上配方中N的质量分数:- 1 - / 1。

一、选择题本题包括15小题,每小题3分,共45分1.下列说法正确的是A.纳米材料是指一种称为“纳米”的新物质制成的材料B.海洋中频发的赤潮是重金属离子的排放引起的C.无土栽培可代替土壤栽培,但不能取代土壤栽培D.回收废旧电池的主要目的在于贵重金属的回收利用解析:选C。
A项材料颗粒在1~100 nm之间,称为纳米材料,B项原因是N、o 22NO错误!的物质的量浓度为mo·L-1mo·L-1mo·L-1mo·L-1解析:选D。
设错误! L溶液中有NH42SO4的物质的量为,NH4NO3物质的量为。
则错误!解得错误!原NO错误!物质的量浓度=错误!=错误!mo·L-1。
15.取硝酸铵样品10 g,加入足量NaOH溶液,加热,用1 mo/L的硫酸80 mL吸收产生的气体,过量的硫酸用60 mL 1 mo/L的NaOH溶液恰好完全中和,则样品中氮的质量分数是A.14% B.28%C.30% D.25%解析:选B。
由NH4NO3~NH3~错误!H2SO4可求出放出的NH3为:1 mo/L× L×2-1 mo/L× L= mo。
则样品中含氮的质量分数为错误!×100%=28%。
二、非选择题本题包括5小题,共55分16.10分根据从草木灰中提取钾盐的实验,填写下列空白:1此实验操作顺序如下:①称量样品,②溶解、沉淀,③________,④________,⑤冷却结晶。
2用托盘天平指针向上的称量样品,若指针偏右边,则表示________填字母代号。
A.左盘重,样品轻B.左盘轻,砝码重C.右盘重,砝码轻D.右盘轻,样品重3在进行第③步操作时,有时可能要重复进行,这是由于________________________________________________________________________。
4在进行第④步操作时,有时要用玻璃棒不断小心地搅动液体,目的是防止________________。

第一单元土壤酸碱性的改良[知识回顾]1.溶液酸碱性及酸碱程度的测定方法2.土壤酸碱对作物生长有哪些影响?[知识学习]1.土壤的酸碱性测定方法:2.造成土壤酸碱性的可能的因素有哪些?3.阅读土壤酸碱性的改良,回顾并思考改良中可能遇到的问题。
4.中水灌溉农田有哪些优点和不足?第二单元化肥的生产与合理利用[知识回顾]1工业上如何合成氨?2物质分离的方法有哪些?3双水解与离子共存。
[知识学习]1化肥的分类:2按照作物对养分需求量的多少分:大量元素肥料,包括氮肥、磷肥和钾肥;中量元素肥料,包括钙、镁、硫肥;微量元素肥料,包括锌、硼、锰、钼、铁、铜肥;此外,还有一些有益元素肥料如含硅物料、稀土元素等。
主要肥料:(1) 氮肥:即以氮素营养元素为主要成分的化肥,(2) 包括尿素、碳酸氢铵(碳铵)、氯化铵、硫酸铵、硝酸铵、硝酸钙,(3) 氨水、等。
(4) 磷肥:即以磷素营养元素为主要成分的化肥,(5) 包括普通过磷酸钙(普钙)、重过磷酸钙(重钙,(6)也称双料、三料过磷酸钙)、钙镁磷肥等。
(7) 钾肥:即以钾素营养元素为主要成分的化肥,(8) 目前施用不(9) 多,(10) 主要品种有硫酸钾、氯化钾、盐湖钾肥、窑灰钾肥和草木灰等。
(11) 复(12) 、混肥料:即肥料中含有两种肥料三要素(氮、磷、钾)的二元复(13) 、混肥料和含有氮、磷、钾三种元素的三元复(14) 、混肥料。
其中混肥在全国各地推广很快。
复(15) 混肥是同(16) 时含有氮、磷、钾中两种或两种以上成分的肥料,(17) 按照制造方法分为两类,(18) 复(19) 合肥料和混合肥料。
最常见的复(20) 合肥是磷酸氢二铵(磷铵),(21) 此外还有尿素磷铵、硝酸磷铵、硫磷酸铵、硝酸磷肥、磷酸二铵、硝酸钾等。
(22) 微量元素肥料和某些中量元素肥料:前者如含有硼、锌(23) 、铁、钼、锰、铜等微量元素的肥料,(24)后者如钙、镁、硫等肥料。
最常用的硼肥为硼砂,锌(25) 肥为硫酸锌,(26) 锰肥为硫酸锰,(27) 钼肥为钼酸铵,(28) 铜肥为硫酸铜,(29) 铁肥为硫酸亚铁及一些有机态铁络合物。
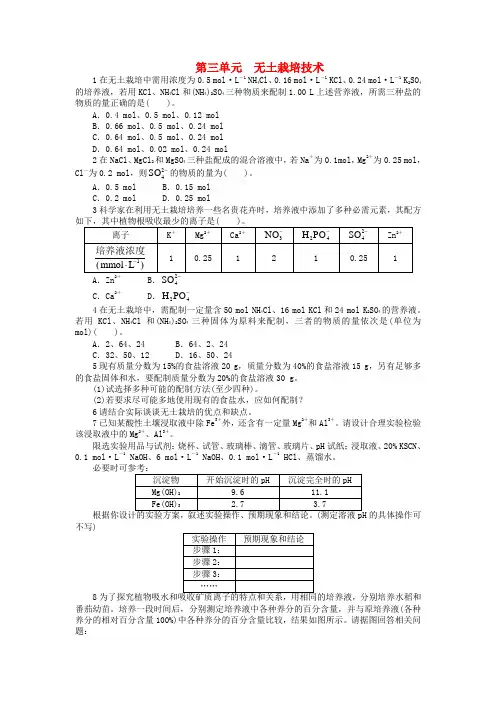
第三单元无土栽培技术1在无土栽培中需用浓度为0.5 mol·L-1NH4Cl、0.16 mol·L-1KCl、0.24 mol·L-1K2SO4的培养液,若用KCl、NH4Cl和(NH4)2SO4三种物质来配制1.00 L上述营养液,所需三种盐的物质的量正确的是( )。
A.0.4 mol、0.5 mol、0.12 molB.0.66 mol、0.5 mol、0.24 molC.0.64 mol、0.5 mol、0.24 molD.0.64 mol、0.02 mol、0.24 mol2在NaCl、MgCl2和MgSO4三种盐配成的混合溶液中,若Na+为0.1mol,Mg2+为0.25 mol,SO-的物质的量为( )。
Cl-为0.2 mol,则24A.0.5 mol B.0.15 molC.0.2 mol D.0.25 mol3科学家在利用无土栽培培养一些名贵花卉时,培养液中添加了多种必需元素,其配方SOA.Zn2+ B.4H PO-C.Ca2+ D.244在无土栽培中,需配制一定量含50 mol NH4Cl、16 mol KCl和24 mol K2SO4的营养液。
若用KCl、NH4Cl和(NH4)2SO4三种固体为原料来配制,三者的物质的量依次是(单位为mol)( )。
A.2、64、24 B.64、2、24C.32、50、12 D.16、50、245现有质量分数为15%的食盐溶液20 g,质量分数为40%的食盐溶液15 g,另有足够多的食盐固体和水,要配制质量分数为20%的食盐溶液30 g。
(1)试选择多种可能的配制方法(至少四种)。
(2)若要求尽可能多地使用现有的食盐水,应如何配制?6请结合实际谈谈无土栽培的优点和缺点。
7已知某酸性土壤浸取液中除Fe3+外,还含有一定量Mg2+和Al3+。
请设计合理实验检验该浸取液中的Mg2+、Al3+。
限选实验用品与试剂:烧杯、试管、玻璃棒、滴管、玻璃片、pH试纸;浸取液、20% KSCN、0.1 mol·L-1 NaOH、6 mol·L-1 NaOH、0.1 mol·L-1 HCl、蒸馏水。
……………………………………………………………名校名师推荐…………………………………………………
第三单元无土栽培技术
[知识回顾]
1.何为溶液呈电中性?
[知识学习]
1.营养液配制与无土栽培实验
(1)母液的配制
(2)营养液的配制
(3)用营养液培养植(4)物幼苗
2.营养液的酸碱度调整
营养液的酸碱度直接影响营养液中养分存在的状态、转化和有效性。
如磷酸盐在碱性时易发生沉淀,影响利用;锰、铁等在大事性溶液中由于溶解度降低也会发生缺乏症。
所以营养液中酸碱度(即pH)的调整是不可忽略的。
pH值的测定可采用混合指标剂比色法,根据指示剂在不同的pH值的营养液中显示不同颜色的特性,以确定营养液的pH值。
如果水源的pH值为中性或微碱性,则配制成的营养液pH值与水源相近,如果不符要进行调整。
在调整pH值时,应先把强酸、强碱加水稀释(营养液偏碱时多用磷酸或硫酸来中和,偏酸时用氢氧化钠来中和),然后逐滴加入到营养液中,同时不断用pH试纸测定,至成中性为止。
[知识巩固]
5.现有MgCl2、KCl、Na2SO4三种物质的混合液中,已知C Cl-=1.5mol/L,C K+┼C Na+ =1.5mol/L,
C SO42-=0.5mol/L,则C Mg2+应是mol/L。
6.在无土栽培中,须配制一定量含50molNH4Cl、16molKCl和24molK2SO4的营养液。
若用KCl、
NH4Cl和(NH4)2SO4三种固体来配制,三者的物质的量依次是(单位:mol):
A、2、64、24
B、64、2、24
C、32、50、12
D、16、50、24
7.硝酸钠10克、过磷酸钙70克、硫酸铵25克、硫本钾35克、硫酸镁40克。
计算以上配方中N
的质量分数:
- 1 -。