分子空间构型汇总
- 格式:ppt
- 大小:1.49 MB
- 文档页数:10

化学空间构型化学空间构型是指分子或离子在空间中所占据的特定位置和相对位置的排列方式。
化学空间构型决定了分子的物理性质和化学性质,对于理解分子的结构和反应机理至关重要。
本文将介绍几种常见的化学空间构型,包括线性、平面、立体等构型,并探讨它们在化学中的应用和影响。
线性构型是最简单的化学空间构型之一,分子中的原子或基团在一条直线上排列。
例如,氢气分子(H2)和氧气分子(O2)都具有线性构型。
线性构型的特点是分子非常稳定且具有高度对称性,这使得线性分子具有较高的解离能和较低的极性。
线性构型在有机合成中也有广泛的应用,例如线性烷烃和线性芳香烃是许多有机化合物的基础结构。
平面构型是分子中的原子或基团在同一平面上排列。
例如,苯分子(C6H6)具有平面构型,其中六个碳原子和六个氢原子都在同一平面上。
平面构型的分子通常具有较高的共轭性和极性,这使得它们在光学、电子传输和催化等领域具有重要的应用。
例如,平面构型的芳香烃是许多有机光电材料和荧光染料的基础结构。
立体构型是分子中的原子或基团在三维空间中排列的方式。
立体构型的特点是分子具有复杂的空间结构和立体异构体,这对于分子的空间相互作用和化学反应具有重要影响。
立体构型在有机化学中尤为重要,例如立体异构体可以导致不同的生物活性,这对于药物设计和合成具有重要意义。
此外,立体构型也是金属配合物和配位化合物中的重要特征,它们对于催化剂和材料的性能起着决定性的作用。
化学空间构型的研究不仅有助于理解分子的结构和性质,还可以为化学合成和材料设计提供指导。
通过对化学空间构型的探索和优化,可以合成出具有特定功能和性能的化合物和材料。
例如,通过调控分子的立体构型,可以合成出具有手性的药物,这对于提高药物的选择性和减少副作用至关重要。
此外,化学空间构型还可以影响分子之间的相互作用,例如通过分子间的空间排列可以形成氢键、范德华力等非共价相互作用,这对于理解分子的自组装和晶体结构具有重要意义。
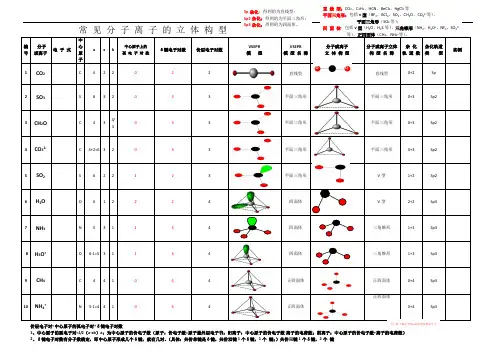
直 线 型:CO 2、C 2H 2、HCN 、BeCl 2、HgCl 2等平面三角形:包括v 型(BF 3、BCl 3、SO 3、CH 2O 、CO 32-等)、平面三角形(SO 2等);四 面 体:包括v 型(H 2O 、H 2S 等)、三角锥形(NH 3、H 3O +、NF 3、SO 32-等)、正四面体(CH 4、NH 4+等)。
常 见 分 子 离 子 的 立 体 构 型编 号分子 或离子电 子 式中心原子 axb中心原子上的 孤 电 子 对 数δ键电子对数 价层电子对数VSEPR模 型 VSEPR 模 型 名 称分子或离子 立 体 构 型 分子或离子立体 构 型 名 称 杂 化 轨 道 数 杂化轨道 类 型实例1CO 2C4 2 2 0 2 2直线型直线型0+2Sp2SO 3S 6 3 2 0 3 3平面三角形平面三角形 0+3 Sp23CH 2OC 4 34/30 3 3平面三角形平面三角形 0+3 Sp24CO 32-C 4+2=6 3 2 0 3 3平面三角形平面三角形 0+3 Sp25SO 2S 6 2 2 1 2 3平面三角形V 型1+2Sp26H 2OO 6 1 2 2 2 4四面体V 型2+2Sp37NH 3N 5 3 1 1 3 4四面体三角锥形1+3Sp38H 3O +O 6-1=5 3 1 1 3 4四面体三角锥形1+3Sp39CH 4C 4 4 1 0 4 4正四面体正四面体0+4Sp310NH 4+N 5-1=4 4 1 0 4 4正四面体正四面体0+4Sp3OO价层电子对=中心原子的孤电子对+δ键电子对数1、中心原子的孤电子对=1/2(a-xb )a :为中心原子的价电子数(原子:价电子数=原子最外层电子书;阳离子:中心原子的价电子数-离子的电荷数;阴离子:中心原子的价电子数+离子的电荷数)2、δ键电子对数有分子数确定,即中心原子形成几个δ键,就有几对。
(具体:共价单键是δ键,共价双键1个δ键,1个 键;)共价三键1个δ键,2个 键Sp 杂化:得到的为直线型; Sp2杂化:得到的为平面三角形; Sp3杂化:得到的为四面体。

杂化轨道类型及分子空间立体构型查缺补漏小专题1一、杂化轨道类型与分子构型分子结构与极性1.中心原子的杂化轨道类型与分子的空间构型杂化参与杂化的原子轨道分子构型示例轨道类型SP 一个S轨道,一个P轨道直线形CH三CHCO2BeCL2SP2一个S轨道,两个P轨道平面三角形CH2=CH2BF3\BCL3\CH2OSP3一个S轨道三个P轨道正四面体CH4\CCL4\NH4+三角锥形NH3V形H2S\H2O判断杂化轨道类型的一般方法:(1)看中心原子有没有形成双键或叁键.如果全为单键,则是SP3杂化,如果有一个双键,是SP2杂化,如果有2个双键或一个叁键,是SP杂化.(2)没有填充电子的空轨道,一般不参与杂化,1对孤电子对占据1个杂化轨道.价层电子对互斥理论几种分子或离子的立体构型:分子或离子中心原子的孤电子对数分子或离子的价层电子对数杂化轨道类型键角分子或离子的立体构型名称CO20 2 SP 180 直线形SO21 3 SP2120 V形BF3 0 3 SP2120 平面三角形CO3 2-0 3 SP2120 平面三角形CH 4 0 4 SP3109.28 正四面体形NH 4+ 0 4 SP3109.28 正四面体NH 3 1 4 SP3107 三角锥形H2O2 4 SP3105 V形另:CH3+.中心原子的价层电子对数与分子立体构型有密切的关系.对ABm型化合物,中心原子A的价层电子对数n的计算方法:n=[A的价电子数+m(8-B的价电子数)]/2;主族元素来说,价电子数等于原子的最外层电子数,计算当B为H时将式中的8改成2.高考题中考查方式:1.CO2与SO2分子的立体结构分别是和。
2.在碳酸二甲酯分子中,碳原子采用的杂化方式有,O-C-O的键角约。
3.P的氢化物的分子构型为 .其中原子采取杂化.4. 用价层电子互斥理论推断SnBr2分子中Sn-Br键的键角120°(填大于或小于或等于),石墨晶体中,每个碳原子通过杂化与周围碳原子成键.5.丙烯腈(H2C=CH-CH三N)分子中碳原子轨道杂化类型是.6.SiF4和SO32-的中心原子杂化类型是,ClO3-的空间构型为 .7.甲醛分子的空间构型是C原子的轨道杂化类型是1mol甲醛分子中§键的数目为 .Welcome To Download !!!欢迎您的下载,资料仅供参考!。



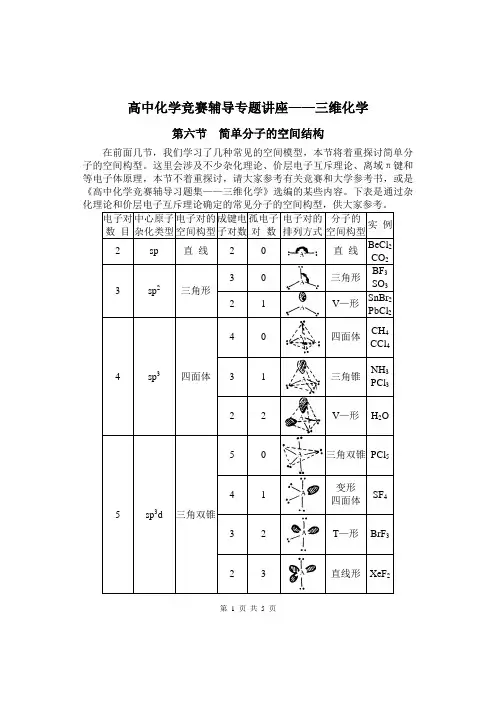
高中化学竞赛辅导专题讲座——三维化学第六节简单分子的空间结构在前面几节,我们学习了几种常见的空间模型,本节将着重探讨简单分子的空间构型。
这里会涉及不少杂化理论、价层电子互斥理论、离域π键和等电子体原理,本节不着重探讨,请大家参考有关竞赛和大学参考书,或是《高中化学竞赛辅导习题集——三维化学》选编的某些内容。
下表是通过杂第 1 页共 5 页【讨论】给出一个分子或离子,我们一般先找出中心原子,确定它的成键电子对数和孤电子对数,判断杂化类型和电子对构型,再判断分子或离子的构型。
由于等电子体具有类似的空间结构,我们也可以据此判断复杂的分子或离子的空间构型。
我们结合以下例题具体讨论。
【例题1】磷的氯化物有PCl3和PCl5,氮的氯化物只有NCl3,为什么没有NCl5?白磷在过量氯气(其分子有三种不同的相对分子质量)中燃烧时,其产物共有几种不同分子。
①【分析】PCl5中心原子P有3d轨道,能与3s、3p轨道一起参与杂化,杂化类型为sp3d,构型为三角双锥。
第二问是通过同位素来考察三角双锥的空间构型:“三角”是一个正三角形的三个顶点,等价的三个点;“双锥”是对称的两个锥顶。
P35Cl5的37Cl的一取代物可在角上和锥顶上2种情况;37Cl 的二取代物可在两个角上、两个锥顶上和一个角一个锥顶上3种情况;利用对称性,三取代物、四取代物与二取代物、一取代物是相同的。
共计有(1+2+3)×2=12种。
【解答】N原子最外层无d轨道,不能发生sp3d杂化,故无NCl5。
12种。
【练习1】PCl5是一种白色固体,加热到160℃不经过液态阶段就变成蒸气,测得180℃下的蒸气密度(折合成标准状况)为9.3g/L,极性为零,P-Cl键长为204pm和211pm两种。
继续加热到250℃时测得压力为计算值的两倍。
PCl5在加压下于148℃液化,形成一种能导电的熔体,测得P-Cl的键长为198pm和206pm两种。
(P、Cl相对原子质量为31.0、35.5)回答如下问题:①180℃下,PCl5蒸气中存在什么分子?为什么?写出分子式,画出立体结构。

一. 四种基本构型及简单变换:甲烷、乙烯、乙炔、苯1.甲烷的正四面体结构:在甲烷分子中,一个碳原子和任意两个氢原子可确定一个平面,其余两个氢原子分别位于平面的两侧,即甲烷分子中有且只有三原子共面(称为三角形规则)。
当甲烷分子中某氢原子被其他原子或原子团取代时,,可将它看作是原来氢原子位置。
CH 3CH 3左侧甲基和②C 构成“甲烷”分子,此分子中④H 、①C 、②C 构成三角形,同理①C 、②C 、③H 也构成了三角形,即乙烷分子中最多有2个碳原子(①C 、②C )和2个氢原子(③H 、④H )4个原子共面。
CH 3CH 2CH 3其结构式可写成如图2所示。
左侧甲基和②C 构成“甲烷分子”。
此分子中⑤H ,①C ,②C 构成三角形。
中间亚甲基和①C ,③C 构成“甲烷”分子。
此分子中①C ,②C ,③C 构成三角形,同理②C ,③C ,④H 构成三角形,即丙烷分子中最多三个碳原子(①C ,②C ,③C )两个氢原子(④H ,⑤H)五原子可能共面。
2.乙稀的平面结构:乙烯分子中的所有原子都在同一平面内,键角为120°。
当乙烯分子中某氢原子被其他原子或原子团取代时,则代替氢原子的原子一定在乙烯的平面内。
其结构式可写成如图4所示。
三个氢原子(①②③)和三个碳原子(④⑤⑥)六原子一定共面。
根据三角形规则[⑤C ,⑥C ,⑦H构成三角形]。
⑦H 也可能在这个平面上。
最多7原子共面。
同理可推出CH 3CH=CHCH 3至少6个原子,至多8个原子共面。
(CH 3)2C=C(CH 3)2至少6个原子(6个碳原子),至多10个原子共面(6个碳原子和4个氢原子),每个甲基可提供一个氢原子在乙烯平面.3.苯的平面结构苯分子所有原子在同一平面内, 键角为120°。
当苯分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定在苯分子所在平面内。
甲苯中的7个碳原子(苯环上的6个碳原子和甲基上的一个碳原子),5个氢原子(苯环上的5个氢原子)这12个原子一定共面。

(1)线性分子,中心原子为sp杂化,如乙炔。
(2)平面内的分子形如乙烯的,中心原子为sp2杂化。
(3)空间(正)四面体,中心原子sp3杂化,如四氯化碳。
(4)空间六面体(形如两个空间正四面体底对底拼在一起),中心原子为sp3d杂化。
(5)空间八面体(形如两个金字塔底对底拼在一起),中心原子为sp3d2杂化。
相关介绍:
分子的空间构型是指分子中各种基团或原子在空间分布的几何形状。
分子中的原子不是杂乱无章地堆积在一起,而是按照一定规律结合的整体,使分子在空间呈现出一定的几何形状(即空间构型)。
如果确定了某分子内化学键的键长和键角数据,那么这个分子的几何构型就确立了。
1940年美国的Sidgwick N.V.等人相继提出了价层电子对互斥理论,简称VSEPR法,该法适用于主族元素间形成的ABn型分子或离子。
该理论认为,一个共价分子或离子中,中心原子A周围所配置的原子B(配位原子)的几何构型,主要决定于中心原子的价电子层中各电子对间的相互排斥作用。
这些电子对在中心原子周围按尽可能互相远离的位置排布。
以使彼此间的排斥能最小。
所谓价层电子对,指的是形成σ键的电子对和孤对电子。
孤对电子的存在,增加了电子对间
的排斥力,影响了分子中的键角。
会改变分子构型的基本类型。
杂化轨道类型及分子空间立体构型查缺补漏小专题1一、杂化轨道类型与分子构型分子结构与极性1.中心原子的杂化轨道类型与分子的空间构型杂化参与杂化的原子轨道分子构型示例轨道类型SP 一个S轨道,一个P轨道直线形CH三CHCO2BeCL2SP2一个S轨道,两个P轨道平面三角形CH2=CH2BF3\BCL3\CH2OSP3一个S轨道三个P轨道正四面体CH4\CCL4\NH4+三角锥形NH3V形H2S\H2O判断杂化轨道类型的一般方法:(1)看中心原子有没有形成双键或叁键.如果全为单键,则是SP3杂化,如果有一个双键,是SP2杂化,如果有2个双键或一个叁键,是SP杂化.(2)没有填充电子的空轨道,一般不参与杂化,1对孤电子对占据1个杂化轨道.价层电子对互斥理论几种分子或离子的立体构型:分子或离子中心原子的孤电子对数分子或离子的价层电子对数杂化轨道类型键角分子或离子的立体构型名称CO20 2 SP 180 直线形SO21 3 SP2120 V形BF3 0 3 SP2120 平面三角形CO3 2-0 3 SP2120 平面三角形CH 4 0 4 SP3109.28 正四面体形NH 4+ 0 4 SP3109.28 正四面体NH 3 1 4 SP3107 三角锥形H2O2 4 SP3105 V形另:CH3+.中心原子的价层电子对数与分子立体构型有密切的关系.对ABm型化合物,中心原子A的价层电子对数n的计算方法:n=[A的价电子数+m(8-B的价电子数)]/2;主族元素来说,价电子数等于原子的最外层电子数,计算当B为H时将式中的8改成2.高考题中考查方式:1.CO2与SO2分子的立体结构分别是和。
2.在碳酸二甲酯分子中,碳原子采用的杂化方式有,O-C-O的键角约。
3.P的氢化物的分子构型为 .其中原子采取杂化.4. 用价层电子互斥理论推断SnBr2分子中Sn-Br键的键角120°(填大于或小于或等于),石墨晶体中,每个碳原子通过杂化与周围碳原子成键.5.丙烯腈(H2C=CH-CH三N)分子中碳原子轨道杂化类型是.6.SiF4和SO32-的中心原子杂化类型是,ClO3-的空间构型为 .7.甲醛分子的空间构型是C原子的轨道杂化类型是1mol甲醛分子中§键的数目为 .Welcome To Download !!!欢迎您的下载,资料仅供参考!。
第二节分子的空间构型一、等电子原理原子总数相同、价电子总数相同的分子具有相似的化学键特征,许多性质是相似的,此原理称为等电子原理。
(1)等电子体的判断方法:在微粒的组成上,微粒所含原子数目相同;在微粒的构成上,微粒所含价电子数目相同;在微粒的结构上,微粒中原子的空间排列方式相同。
(等电子的推断常用转换法,如CO2=CO+O=N2+O= N2O= N2+ N—= N3—或SO2=O+O2=O3=N—+O2= NO2—)(2)等电子原理的应用:利用等电子体的性质相似,空间构型相同,可运用来预测分子空间的构型和性质。
等电子体的判断方法具有相同价电子数和相同原子数的分子或离子具有相同的结构特征,这一原理称为等电子原理。
如果仅从概念字面出发,判断与A粒子互为等电子体的B粒子的化学式,往往感觉无从下手,或东拼西凑的试写,试写也往往只注意“价电子数”或“原子数”相同某一方面而错答。
如写CH4分子的等电子体时许多学生写成NH3(原子数不同)、CCl4(价电子数不同)等,至于再稍复杂一些的,错的更多,实际体现为问题解决方法的欠缺。
等电子体的判断一般可采取以下几种方法:1、同族元素互换法即将既定粒子中的某元素换成它的同族元素。
如:(1)CCl4的等电子体确定:换IV A族元素有SiCl4、GeCl4等;换VIIA族元素有CF4、CBr4、CI4、CFCl3、……;同时换可有SiF4、SiFCl3、……。
(2)CO2的等电子体确定:可将O原子换为S原子得COS、CS2,注意不能将C原子换为Si原子,因为CO2和SiO2的结构不同(前者为分子晶体,后者为原子晶体)。
同理,不能将BeCl2的等电子体确定为MgCl2或BeF2(后两种为离子晶体)。
(3)SO42-的等电子体确定:将一个O原子换为S原子得S2O32-;NO3-的等电子体可确定为PO3-。
(4)对于原子晶体类也可作类似推导:金刚石Cn与晶体硅Sin互为等电子体。