2017版和2002版医疗器械分类目录对比完整版
- 格式:docx
- 大小:39.65 KB
- 文档页数:2

对比分析:2002版与2017版医疗器械分类目录简介本文对比分析了2002版和2017版医疗器械分类目录之间的差异和变化。
医疗器械分类目录是中国国家药监局制定的对医疗器械进行分类管理的标准,它对医疗器械的注册、生产、销售等方面具有重要的指导作用。
主要变化1. 分类体系更新:2002版医疗器械分类目录采用的是旧版的分类标准,而2017版医疗器械分类目录进行了全面更新,采用了新的分类标准。
新的分类体系更加科学合理,更符合现代医疗器械的发展趋势。
分类体系更新:2002版医疗器械分类目录采用的是旧版的分类标准,而2017版医疗器械分类目录进行了全面更新,采用了新的分类标准。
新的分类体系更加科学合理,更符合现代医疗器械的发展趋势。
2. 分类数量增加:2017版医疗器械分类目录相对于2002版增加了大量的新的分类。
这反映了医疗器械行业的快速发展和新技术的不断涌现。
分类数量增加:2017版医疗器械分类目录相对于2002版增加了大量的新的分类。
这反映了医疗器械行业的快速发展和新技术的不断涌现。
3. 分类细化:2017版医疗器械分类目录对原有的分类进行了进一步的细化。
这使得医疗器械的管理更加精细化,有利于更好地监管和控制医疗器械的质量和安全。
分类细化:2017版医疗器械分类目录对原有的分类进行了进一步的细化。
这使得医疗器械的管理更加精细化,有利于更好地监管和控制医疗器械的质量和安全。
4. 分类名称变化:一些医疗器械的分类名称在2017版中发生了变化。
这些变化可能是为了更准确地描述医疗器械的功能和特征,或者是为了与国际标准保持一致。
分类名称变化:一些医疗器械的分类名称在2017版中发生了变化。
这些变化可能是为了更准确地描述医疗器械的功能和特征,或者是为了与国际标准保持一致。
影响与意义1. 指导医疗器械注册和审批:2017版医疗器械分类目录的更新和细化,有助于更准确地指导医疗器械的注册和审批工作。
医疗器械企业可以根据新的分类标准进行申报,提高注册成功率。
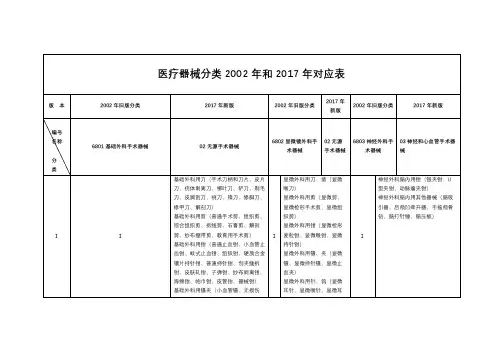

医疗器械分类目录2002与2017版本差异研究根据医疗器械监督管理条例的要求,国家药监局于2002年和2017年分别发布了医疗器械分类目录的两个版本。
本文将研究这两个版本之间的差异。
1. 变更的分类体系在2002年版本的医疗器械分类目录中,医疗器械被划分为17个类别,分别是:1. 诊断类2. 治疗类3. 手术类4. 护理类5. 检验类6. 康复类7. 体外诊断试剂类8. 体外治疗类9. 体外手术类10. 体外护理类11. 体外检验类12. 体外康复类13. 其他治疗类14. 其他手术类15. 其他护理类16. 其他检验类17. 其他康复类而在2017年版本的医疗器械分类目录中,将医疗器械划分为3个类别和16个子类别,分别是:1. 诊断类- 影像类- 检验类- 监测类- 试剂类2. 治疗类- 植入类- 植入辅助类- 介入类- 介入辅助类- 体外类- 体外辅助类3. 护理类- 康复辅助类- 康复类- 护理辅助类- 护理类可以看出,2017年版本的医疗器械分类目录对医疗器械的分类体系进行了较大的调整,将原本的17个类别简化为了3个类别和16个子类别。
2. 变动的具体条目除了分类体系的变化外,2002年版本的医疗器械分类目录和2017年版本的医疗器械分类目录之间还存在一些具体条目的变动。
具体的变动包括医疗器械的命名调整、增加新的医疗器械种类以及删除已经不再使用的医疗器械种类等。
这些变动主要是为了适应医疗器械行业的发展和技术的进步。
然而,为了确保准确性,本文不会引用任何无法被确认的内容。
如需了解具体的条目变动,请参考国家药监局发布的医疗器械分类目录的官方公告。
3. 总结医疗器械分类目录2002与2017版本之间存在较大的差异。
2017年版本的医疗器械分类目录进行了分类体系的调整,并对具体的条目进行了变动。
这些变动旨在更好地适应医疗器械行业的发展和技术的进步。
然而,为了确保准确性,请参考国家药监局发布的医疗器械分类目录的官方公告,以获取最新和可确认的信息。

2002-2017年医疗器械分类目录差异对比1. 引言医疗器械分类目录是规范医疗器械管理和使用的重要文件,对保障医疗器械安全、有效和质量可控具有重要意义。
本文档主要对比分析了2002年至2017年间我国医疗器械分类目录的差异,以期为医疗器械监管、企业和从业人员提供参考。
2. 2002年医疗器械分类目录2002年发布的《医疗器械分类目录》是我国首个医疗器械分类目录,分为四个等级:一类、二类、三类和进口医疗器械。
该目录主要依据医疗器械的风险程度和临床使用特点进行分类。
3. 2017年医疗器械分类目录2017年发布的《医疗器械分类目录》是在2002年目录基础上进行修订的,分为三个等级:一类、二类和三类。
该目录在原有基础上优化了分类原则和标准,调整了部分产品的分类等级,增加了进口医疗器械分类。
4. 差异对比4.1 分类等级调整- 从2002年到2017年,医疗器械分类等级由四个减少为三个,简化了一类和进口医疗器械的分类。
- 部分高风险产品从三类调整为二类,降低了使用门槛,提高了监管效率。
4.2 分类原则和标准优化- 2017年目录在分类原则和标准上进行了优化,更加注重医疗器械的安全性和有效性。
- 增加了对医疗器械性能、结构、作用特点等方面的考量,使分类更加科学合理。
4.3 产品分类调整- 2017年目录对部分产品的分类进行了调整,如将部分原本属于二类的产品调整为三类,提高了监管要求。
- 同时,将部分低风险产品从三类调整为二类,有助于促进医疗器械产业的发展。
4.4 进口医疗器械分类- 2017年目录增加了进口医疗器械分类,有助于加强对进口医疗器械的监管,保障患者安全。
5. 结论从2002年到2017年,我国医疗器械分类目录在分类等级、分类原则和标准、产品分类以及进口医疗器械分类等方面进行了多次调整和优化。
这些调整有助于提高医疗器械监管的科学性、合理性和有效性,促进医疗器械产业的健康发展。
企业和从业人员应密切关注目录变化,确保产品合规上市。

对比分析:2002版与2017版医疗器械分类目录1. 引言医疗器械分类目录是规范医疗器械产品管理的重要文件,对保障医疗器械安全、有效使用具有重要意义。
我国自2002年起开始实施第一版医疗器械分类目录,随着医疗器械行业的快速发展,2017年发布了新版医疗器械分类目录。
本文将对2002版与2017版医疗器械分类目录进行对比分析,以了解两者之间的差异及对行业的影响。
2. 2002版与2017版医疗器械分类目录的主要差异2.1 分类原则与方法- 2002版:主要依据产品的工作原理、结构特征和用途进行分类。
- 2017版:在2002版的基础上,增加了风险分类原则,根据产品的风险程度将其分为高风险、中风险和低风险三类。
2.2 分类体系- 2002版:分为四类,一类、二类、三类和进口医疗器械。
- 2017版:分为三类,一类、二类和三类,其中一类医疗器械分为高风险、中风险和低风险,二类和三类医疗器械根据风险程度进一步细分。
2.3 产品编码与命名规则- 2002版:采用五位数字表示,第一位数字表示产品类别,后四位数字表示具体产品。
- 2017版:采用六位数字表示,第一位数字表示产品风险类别,后五位数字表示具体产品。
2.4 产品分类举例- 2002版:心脏起搏器属于三类医疗器械。
- 2017版:心脏起搏器根据风险程度,可能被归为一类或三类医疗器械。
3. 对比分析3.1 分类细化- 2017版相较于2002版,对医疗器械的分类进行了细化,使产品分类更加精准,有助于监管和产业发展。
3.2 风险管理加强- 2017版引入了风险分类原则,有助于加强对高风险医疗器械的监管,保障患者安全。
3.3 编码与命名规则变更- 2017版的编码与命名规则更加科学合理,有助于行业内部交流和信息管理。
4. 对行业的影响- 企业:企业需要根据新版分类目录调整产品注册和备案,加强对产品风险的评估和管理。
- 监管:监管部门可依据新版分类目录更加精准地进行监管,提高监管效率。

2017版和2002版医疗器械分类目录对比近年来,随着医疗技术不断发展以及人们对健康的重视程度越来越高,医疗器械的市场需求也在不断增长。
为了方便管理和监管,国家制定了医疗器械分类目录。
本文将对比2017版和2002版医疗器械分类目录,分析其差异和改进。
一、基本介绍医疗器械分类目录是对医疗器械进行分类并编码的规范,旨在加强医疗器械的管理和监管。
在2002年发布的《医疗器械分类目录》中,医疗器械被分为17类,共计1412个品种;而在2017年发布的最新版中,医疗器械被分为22类,共计9167个品种。
可以看出,在品种和类别上,2017版比2002版有了大幅度的增长。
二、改进之处1.分门别类更清晰与2002年版相比,2017年版是在对医疗器械分类进行了更为细致的划分。
例如,在2002年版中,心血管介入类中只有一个品种,然而在2017年版中,心血管介入类被细分为28个品种。
通过这种更为详细的分类,可以更好地实现对医疗器械的管理和监管。
2.新型医疗器械覆盖更全面由于医疗技术的不断发展,医疗器械市场上也不断涌现出新型医疗器械。
比如,在2002年版中,并没有分出眼科诊疗仪器、口腔诊疗器械等新型医疗器械。
而在2017年版中,这些新型医疗器械被分别列出,覆盖面更加全面。
3.加强对注射器等特殊医疗器械的监管在2002年版中,注射器的管理及其相关规范并不明确。
而在2017年版中,针头、注射器等特殊医疗器械的管理及其相关规范得到了加强。
在这种趋势下,特殊医疗器械的安全性得到了更有效的保障。
三、总结综上所述,2017版医疗器械分类目录与2002版相比,不仅在品种、类别上发生了较大变化,而且在各方面的管理、监管方面也得到了进一步完善和加强。
相信在医疗器械的管理、监管方面,医疗器械分类目录将发挥越来越重要的作用。

对照研究:2002版与2017版医疗器械分类目录1. 引言本文对比分析了2002版与2017版医疗器械分类目录的差异。
医疗器械分类目录是对医疗器械进行分类、编码和命名的重要依据,对医疗器械管理、监督和使用具有重要意义。
2. 目录结构的变化2002版医疗器械分类目录采用了三级分类结构,分别为大类、中类和小类。
而2017版医疗器械分类目录在此基础上进行了调整,采用了四级分类结构,分别为大类、中类、小类和细目。
这一变化使得医疗器械的分类更加细致和准确。
3. 分类标准的改变在分类标准方面,2002版医疗器械分类目录主要根据医疗器械的用途和功能进行分类。
而2017版医疗器械分类目录在此基础上增加了对医疗器械的技术特征和管理要求的考虑,使得分类标准更加全面和科学。
4. 新增与调整的类别2017版医疗器械分类目录相较于2002版新增了一些类别,如计量器具类、家用器具类、植入器具类等,以适应医疗器械的发展和需求变化。
同时,对一些原有类别进行了调整和细分,使得分类更加精准。
5. 编码体系的变化2002版医疗器械分类目录采用了6位编码体系,其中前两位表示大类,中间两位表示中类,后两位表示小类。
而2017版医疗器械分类目录在此基础上增加了两位细目编码,以更好地区分不同的医疗器械。
6. 结论对比研究2002版与2017版医疗器械分类目录的差异,我们可以看到医疗器械分类的发展和完善。
2017版医疗器械分类目录相较于2002版在目录结构、分类标准、新增与调整的类别以及编码体系等方面进行了改进,使得医疗器械的分类更加准确、全面和科学。
这对于医疗器械的管理和使用具有重要意义。
以上是对照研究:2002版与2017版医疗器械分类目录的简要分析,希望对您有所帮助。
---以上所述仅为个人观点,不能作为法律依据。
如有需要,请参考相关法律法规或咨询专业人士。

医疗器械2017版与2002版器械分类目录对照表精品.doc2017版代码01有源手术器械02无源手术器械03神经和心血管手术器械04骨科手术器械05放射治疗器械06医用成像器械07医用诊察和监护器械08呼吸、麻醉和急救器械09物理治疗器械10输血、透析和体外循环器械11医疗器械消毒灭菌器械12有源植入器械13无源植入器械14注输、护理和防护器械15患者承载器械16眼科器械17口腔科器械18妇产科、辅助生殖和避孕器械19医用康复器械20中医器械21医用软件22临床检验器械23体外诊断试剂24体外诊断试剂(不需冷链运输、贮存)2017版与2002、2012版医疗器械分类目录对照表(总表)1.有源手术器械2017版代码: 012002版代码: 6821、6822、6824、6825、6854、6858、68162012版代码: 68232.无源手术器械2017版代码: 022002版代码: 6801、6802、6805、6808、6809、6816、6822、68652012版代码: 68233.神经和心血管手术器械2017版代码: 032002版代码: 6832、6833、6828、6833、6821、6822、68242012版代码: 68234.骨科手术器械2017版代码: 042002版代码: 6820、6821、6833、6854、6821、6805、6823、6826、6866、68562012版代码: 68235.放射治疗器械2017版代码: 052002版代码: 6804、6820、6822、6824、6846、68582012版代码: 6855、6806、68636.医用成像器械2017版代码: 062002版代码: 6812、6866、6822、6813、6826、6854、6846、68652012版代码: 68237.医用诊察和监护器械2017版代码: 072002版代码: 6826、68462012版代码: 68278.呼吸、麻醉和急救器械2017版代码: 082002版代码: 6870、6840(诊断试剂除外)、6822、6833、6841、6815、68582012版代码: 6840(诊断试剂需低温冷藏运输贮存)、6840(诊断试剂不需低温冷藏运输贮存)9.物理治疗器械2017版代码: 092002版代码: 68232012版代码: 682310.输血、透析和体外循环器械2017版代码: 102002版代码: 6845、68662012版代码: 682311.医疗器械消毒灭菌器械2017版代码: 112002版代码: 6830、6831、6834、6823 2012版代码: 682312.有源植入器械2017版代码: 122002版代码: 68232012版代码: 682313.无源植入器械2017版代码: 132002版代码: 68232012版代码: 682314.注输、护理和防护器械2017版代码: 142002版代码: 6815、6854、6866、6864 2012版代码: 682315.患者承载器械2017版代码: 152002版代码: 6854、68562012版代码: 682316.眼科器械2017版代码: 162002版代码: 6804、6820、6822、6824、6846、6858 2012版代码: 682317.口腔科器械2017版代码: 172002版代码: 6855、6806、68632012版代码: 682318.妇产科、辅助生殖和避孕器械2017版代码: 182002版代码: 6812、6866、6822、6813、6826、6854、6846、68652012版代码: 682319.医用康复器械2017版代码: 192002版代码: 6826、68462012版代码: 682320.中医器械2017版代码: 202002版代码: 68702012版代码: 6840(诊断试剂除外)、6822、6833、6841、6815、685821.医用软件2017版代码: 212002版代码: 无2012版代码: 无22.临床检验器械2017版代码: 222002版代码: 6840体外诊断试剂2012版代码: 6840体外诊断试剂(不需冷链运输、贮存)23.体外诊断试剂2017版代码: 232002版代码: 无2012版代码: 无24.体外诊断试剂(不需冷链运输、贮存)2017版代码: 242002版代码: 无2012版代码: 无18-37:删除无用信息,无需改写。

对照研究:2002版与2017版医疗器械分类目录1. 引言医疗器械分类目录是对医疗器械进行分类和管理的依据,对于确保医疗器械的安全、有效和质量具有重要意义。
本文将对2002版与2017版医疗器械分类目录进行对照研究,以了解和分析两版目录的主要变化和差异。
2. 2002版与2017版医疗器械分类目录的主要变化2.1 分类原则的变化2002版医疗器械分类目录主要依据产品的形态、用途和安全性进行分类,而2017版目录在原有基础上,增加了对产品技术复杂性和创新性的考量。
这意味着,2017版目录更加注重产品的技术特点和创新发展。
2.2 分类类别的调整2017版医疗器械分类目录在2002版的基础上,对部分类别的划分进行了调整。
例如,将原来的“诊断器械”和“治疗器械”合并为“诊断治疗器械”,使目录更加简洁明了。
2.3 产品编码的优化2017版医疗器械分类目录采用了更加科学、规范的产品编码体系,使产品的分类和管理更加便捷和高效。
3. 具体产品对照分析以下是对2002版与2017版医疗器械分类目录中部分具体产品的对照分析:3.1 心脏起搏器- 2002版分类目录中,心脏起搏器属于“治疗器械”类别。
- 2017版分类目录中,心脏起搏器被归类到“诊断治疗器械”类别。
3.2 人工关节- 2002版分类目录中,人工关节属于“植入性医疗器械”类别。
- 2017版分类目录中,人工关节被归类到“植入性医疗器械”的子类别“骨科植入器械”。
3.3 医疗超声设备- 2002版分类目录中,医疗超声设备属于“诊断器械”类别。
- 2017版分类目录中,医疗超声设备被归类到“诊断治疗器械”类别。
4. 结论通过对2002版与2017版医疗器械分类目录的对照研究,我们可以看到,2017版目录在分类原则、类别划分和产品编码等方面进行了优化和改进,使医疗器械的分类和管理更加科学、合理。
这些变化有助于提高医疗器械监管的有效性,促进医疗器械行业的健康发展。

医疗器械分类目录对照:2002版与2017
版
1. 引言
本文档对比了医疗器械分类目录的2002版和2017版,旨在了解两个版本之间的变化和更新内容。
2. 2002版医疗器械分类目录
2002版医疗器械分类目录是中国国家药品监督管理局于2002年颁布的标准。
该目录根据医疗器械的功能和用途对其进行分类,共分为16个类别,包括手术器械、口腔科器械、眼科器械等。
3. 2017版医疗器械分类目录
2017版医疗器械分类目录是对2002版进行修订和更新后的版本。
该目录在保留原有类别的基础上,增加了新的类别,调整了部分器械的分类。
2017版目录共分为22个类别,新增了类似生物材料器械、心血管类器械等新的分类。
4. 变化和更新内容
2017版医疗器械分类目录相对于2002版有以下几个主要变化
和更新内容:
- 类别增加:新增了类似生物材料器械、心血管类器械等新的
类别,以适应医疗器械行业的发展和创新。
- 调整分类:对部分器械进行了分类的调整,以更准确地归类
器械的功能和用途。
- 术语规范:修订了一些医疗器械的命名和术语,以提高目录
的准确性和规范性。
5. 结论
通过对比2002版和2017版医疗器械分类目录,我们可以看到
医疗器械行业的发展和创新对目录的影响。
2017版目录相对于
2002版进行了一些调整和更新,以适应新的技术和产品的出现。
了解和掌握最新的医疗器械分类目录对于相关行业人员具有重要意义,可以帮助他们更好地理解和应用医疗器械的分类和管理。
医疗器械分类目录:2002版和2017版的对比1. 引言医疗器械分类目录是规范医疗器械监管的重要文件,对保障医疗器械安全、有效和质量可控具有重要意义。
我国自2002年起开始实施第一版医疗器械分类目录,随着医疗器械行业的快速发展,2017年发布了新版医疗器械分类目录。
本文将对2002版和2017版医疗器械分类目录进行详细对比,以帮助了解新版目录的主要变化和调整。
2. 目录结构对比2.1 2002版目录结构2002版医疗器械分类目录分为四个大类,分别为:1. 第一类医疗器械2. 第二类医疗器械3. 第三类医疗器械4. 其他医疗器械每个大类下分为若干小类,共涵盖12个小类。
2.2 2017版目录结构2017版医疗器械分类目录将医疗器械分为21个大类,相较于2002版目录,新增了以下大类:1. 植入性医疗器械2. 眼耳鼻喉科医疗器械3. 口腔科医疗器械4. 康复医疗器械5. 中医医疗器械6. 体外诊断医疗器械7. 医学影像医疗器械8. 医用高值耗材同时,对原有部分大类进行了调整和细化。
3. 分类原则对比3.1 2002版分类原则2002版目录主要依据医疗器械的风险程度和作用机理进行分类,将医疗器械分为三个风险等级:1. 第一类医疗器械:低风险医疗器械,如手术器械、医用X光胶片等。
2. 第二类医疗器械:中风险医疗器械,如心脏起搏器、人工关节等。
3. 第三类医疗器械:高风险医疗器械,如人工器官、植入性支架等。
3.2 2017版分类原则2017版目录在2002版的基础上,进一步细化了分类原则,增加了以下分类依据:1. 医疗器械的功能、用途和预期效果2. 医疗器械的生物相容性3. 医疗器械的侵入程度4. 医疗器械的监测和控制能力根据这些分类依据,2017版目录将医疗器械分为低风险、中风险和高风险三个等级,并对每个等级进行了进一步细分。
4. 具体分类对比4.1 第一类医疗器械2002版目录中第一类医疗器械主要包括:1. 手术器械2. 医用X光胶片3. 医用放大镜4. 医用冷热敷包2017版目录中第一类医疗器械调整为:1. 手术器械2. 医用X光胶片3. 医用放大镜4. 医用冷热敷包5. 医用脱脂棉6. 医用脱脂纱布4.2 第二类医疗器械2002版目录中第二类医疗器械主要包括:1. 心脏起搏器2. 人工关节3. 医用缝合线4. 医用脱脂纱布2017版目录中第二类医疗器械调整为:1. 心脏起搏器2. 人工关节3. 医用缝合线4. 医用脱脂纱布5. 医用绷带6. 医用石膏4.3 第三类医疗器械2002版目录中第三类医疗器械主要包括:1. 人工器官2. 植入性支架3. 人工关节4. 心脏起搏器2017版目录中第三类医疗器械调整为:1. 人工器官2. 植入性支架3. 人工关节4. 心脏起搏器5. 医用高值耗材6. 医学影像医疗器械5. 总结综上所述,2017版医疗器械分类目录相较于2002版目录,在结构、分类原则和具体分类方面均进行了较大幅度的调整和优化。
2002与2017年度医疗器械分类目录对照本文档旨在对2002年度和2017年度的医疗器械分类目录进行详细对照,以便于了解和掌握我国医疗器械分类的发展变化。
一、概述医疗器械分类目录是依据医疗器械的风险程度、作用原理、使用形式等因素,将医疗器械分为不同的类别,以指导生产和监管。
我国自2002年开始实施第一版医疗器械分类目录,随后在2017年发布了新版医疗器械分类目录。
二、2002年度医疗器械分类目录2002年度医疗器械分类目录将医疗器械分为以下四大类:1. 第一类医疗器械:风险程度低,主要包括卫生材料、家庭医疗设备等。
2. 第二类医疗器械:风险程度中等,主要包括医用敷料、医用影像设备、医用电气设备等。
3. 第三类医疗器械:风险程度高,主要包括心脏起搏器、人工关节、植入式药物释放系统等。
4. 其他类医疗器械:主要包括实验仪器、医学模型等。
三、2017年度医疗器械分类目录2017年度医疗器械分类目录在2002年度的基础上进行了调整,将医疗器械分为以下四大类:1. 第一类医疗器械:风险程度低,主要包括卫生材料、家庭医疗设备等。
2. 第二类医疗器械:风险程度中等,主要包括医用敷料、医用影像设备、医用电气设备等。
3. 第三类医疗器械:风险程度高,主要包括心脏起搏器、人工关节、植入式药物释放系统等。
4. 其他类医疗器械:主要包括实验仪器、医学模型等。
四、对照分析对比2002年度和2017年度的医疗器械分类目录,可以发现以下几点变化:1. 分类体系基本保持一致,都分为四大类。
2. 在第二类和第三类医疗器械中,部分子类别的名称和归属发生了调整,以更准确地反映医疗器械的风险程度和特点。
3. 新版目录对部分医疗器械的分类进行了细化,例如将医用电气设备进一步细分为医用高频设备、医用磁共振设备等。
4. 新版目录新增了一些新兴领域的医疗器械,如基因检测设备、生物芯片等。
五、结论通过对照2002年度和2017年度的医疗器械分类目录,我们可以看出我国医疗器械分类体系在不断完善和发展。
新版目录共22个子目录:1.手术类器械设置4个子目录:通用手术器械分设《01有源手术器械》和《02无源手术器械》;单独设置《03神经和血管手术器械》;单独设置《04骨科手术器械》。
2.有源器械为主的器械设置8个子目录:《05放射治疗器械》《06医用成像器械》《07医用诊察和监护器械》《08呼吸、麻醉和急救器械》《09物理治疗器械》《10输血、透析和体外循环器械》《11医疗器械消毒灭菌器械》《12有源植入器械》。
3.无源器械为主的器械设置3个子目录:《13无源植入器械》《14注输、护理和防护器械》《15患者承载器械》。
4.按照临床科室划分3个子目录:《16眼科器械》《17口腔科器械》《18妇产科、生殖和避孕器械》。
5.《19医用康复器械》和《20中医器械》是根据《医疗器械监督管理条例》中对医用康复器械和中医器械两大类产品特殊管理规定而单独设置的子目录。
6.《21医用软件》是收录医用独立软件产品的子目录。
7.《22临床检验器械》子目录放置在最后,为后续体外诊断试剂修订预留空间。
医疗器械经营(零售),销售对象为消费者,原则上只能选择家用医疗器械代码。
第二类医疗器械经营备案(零售)可选经营范围:2002版代码:6801、6815、6820、6821、6822、6823、6826、6827、6840(诊断试剂除外)、6840(诊断试剂不需低温冷藏运输贮存)、6841、6846、6854、6856、6863、6864、68662017版代码:02、07、08、09、14、15、16、17、18、19、20、22、6840体外诊断试剂(不需冷链运输、贮存)第三类医疗器械经营许可(零售)可选经营范围:2002版代码:6815、6820、6822、6826、6854、68662017版代码:07、08、09、14、16。
2002与2017年度医疗器械分类目录对照本文档将对比2002年和2017年两个不同时间点的医疗器械分类目录,以便了解两个时间点之间的变化和进展。
2002年医疗器械分类目录2002年的医疗器械分类目录是指当时用于对医疗器械进行分类和管理的标准目录。
该目录包含了各种不同类型的医疗器械,并根据其用途、特征和功能将其分为不同的类别。
以下是2002年医疗器械分类目录的一些常见类别:- 诊断类器械:用于医学诊断和检测的工具和设备。
- 治疗类器械:用于医学治疗和康复的工具和设备。
- 手术类器械:用于医学手术和手术操作的工具和设备。
- 植入类器械:用于植入或植入固定的医疗器械。
- 监测类器械:用于监测和记录生理参数的工具和设备。
2017年医疗器械分类目录2017年的医疗器械分类目录是更新后的版本,用于更好地适应医疗器械的发展和需求变化。
该目录相比于2002年版本进行了一些修改和更新,以便更好地对医疗器械进行分类和管理。
以下是2017年医疗器械分类目录的一些常见类别:- 体外诊断类器械:用于体外诊断和检测的工具和设备。
- 治疗类器械:用于医学治疗和康复的工具和设备。
- 手术类器械:用于医学手术和手术操作的工具和设备。
- 植入类器械:用于植入或植入固定的医疗器械。
- 监测类器械:用于监测和记录生理参数的工具和设备。
对比分析通过对比2002年和2017年的医疗器械分类目录,可以发现一些变化和进展。
尽管两个时间点的目录都包含了类似的类别,但2017年的目录更加注重体外诊断类器械,并将其单独列为一个类别。
这种变化反映了医疗器械领域的发展趋势,即体外诊断技术的重要性日益增加。
随着医学科技的进步,体外诊断类器械在疾病诊断和治疗中起到了关键作用,因此在2017年的目录中得到了更多的关注和重视。
此外,2017年的目录可能还对其他类别进行了一些细微的修订和更新,以更好地反映医疗器械的现状和需求。
然而,本文档无法提供具体的细节,因为无法确认这些细节的准确性。
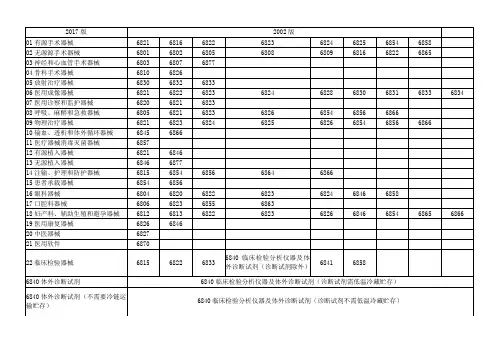
2017 版2002 版
01有源手术器械68216816682268236824682568546858
02无源源手术器械68016802680568086809681668226865
03神经和心血管手术器械680368076877
04骨科手术器械68106826
05放射治疗器械683068326833
06医用成像器械682168226823682468286830683168336834 07医用诊察和监护器械682068216823
08呼吸、麻醉和急救器械6805682168236826685468566866
09物理治疗器械68216823682468256826685468566866
10输血、透析和体外循环器械68456866
11医疗器械消毒灭菌器械6857
12有源植入器械68216846
13无源植入器械68466877
14注输、护理和防护器械68156854685668646866
15患者承载器械68546856
16眼科器械6804682068226823682468466858
17口腔科器械6806682368556863
18妇产科、辅助生殖和避孕器械681268136822682368266846685468656866 19医用康复器械68266846
20中医器械6827
21医用软件6870
22临床检验器械6815682268336840 临床检验分析仪器及体
68416858外诊断试剂(诊断试剂除外)
6840 体外诊断试剂6840 临床检验分析仪器及体外诊断试剂(诊断试剂需低温冷藏贮存)6840 体外诊断试剂(不需要冷链运
输贮存)
6840 临床检验分析仪器及体外诊断试剂(诊断试剂不需低温冷藏贮存)
2002 旧版分类2017 新版2002 旧版分类2017 新版6801 基础外科手术器械026828 医用磁共振设备06
6802 显微外科手术器械026830 医用 X 射线设备05;06 6803 神经外科手术器械036831 医用 X 射线附属设备及部件05;06 6804 眼科手术器械166832 医用高能射线设备05;08 6805 耳鼻喉科手术器械02;086833 医用核素设备05; 06;07; 22 6806 口腔科手术器械176834 医用射线防护用品、装置06
6807 胸腔心血管外科手术器械036840 临床检验分析仪器及诊断试剂
6840 体外诊断试剂(诊断试剂需低温冷藏运输贮存)
6808 腹部外科手术器械036840 临床检验分析仪器及体外诊断6840 体外诊断试剂(不需要冷链运输试剂(诊断试剂不需低温冷藏贮存)贮存)
6809 泌尿肛肠外科手术器械026840 临床检验分析仪器及体外诊断
22试剂(诊断试剂除外)
6810 矫形外科(骨科)手术器械046841 医用化验和基础设备器具22 6812 妇产科用手术器械186845 体外循环及血液处理设备10 6813 计划生育手术器械186846 植入材料和人工器官12;13;16;18;19
6815 注射穿刺器械14;226854 手术室、急救室、诊疗室设备
01;08;14;15;18及器具
6816 烧伤(整形)科手术器械01;026855 口腔科设备及器具17 6820 普通诊察器械07;166856 病房护理设备及器具08;15 6821 医用电子仪器设备1; 6;7;8;9;126857 消毒和灭菌设备及器具11
6822 医用光学器具、仪器及内窥镜设备1;6;16;18; 226858 医用冷辽、低温、冷藏设备及器
01; 09;16; 22
具
6823 医用超声仪器及有关设备1;6;7;8; 9;16;17;186863 口腔科材料17 6824 医用激光仪器设备01;06;09;166864 医用卫生材料及辅料14 6825 医用高频仪器设备01;096865 医用缝合材料及粘合剂02;18 6826 物理治疗及康复设备04; 08; 09; 18; 196866 医用高分子材料及制品08; 10;14; 18 6827 中医器械206870 软件21。