江苏省常熟中学2014_2015学年高一化学下学期期中试题(扫描版)
- 格式:doc
- 大小:793.00 KB
- 文档页数:7

2014~2015学年度第二学期期中调研测试高一化学试题本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共6页。
本试卷满分100分。
考试时间100分钟。
第Ⅰ卷(选择题共69分)注意事项:1.答题前,考生务必在答题纸姓名栏内写上自己的姓名、考试科目、准考证号等,并用2B铅笔涂写在答题纸上。
2.每小题选出正确答案后,用2B铅笔把答题纸上对应题号的答案标号涂黑Ⅰ。
如需改动,用橡皮擦干净后,再选涂其他答案。
不能答在试题卷上。
考试结束,将答题纸交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16单项选择题:在每题的4个选项中,只有1个选项是符合要求的(本部分23题,每题3分,共69分)1.绿色能源是指使用不会对环境造成污染的能源。
下列属于绿色能源的是①太阳能②风能③潮汐能④ 煤⑤天然气⑥石油A.①②③B.③④C.④D.①②⑥2.下列化学用语对应正确的是A.Cl-离子的结构示意图: B.白磷分子的比例模型:C.H2O2的结构式:H-O-O-H D.CCl4的电子式:3.下列说法正确的是A.H、D、T表示三种氢原子B.卤族元素最高化合价均为正7价,最低化合价均为负1价C.金属元素的原子最外层电子数,都少于4个D.目前人们已发现了5000多种核素,说明发现了5000多种元素4.氰酸铵(NH4CNO)与尿素[CO(NH2)2]A.互为同系物 B.互为同分异构体 C.都是共价化合物 D.都是有机化合物5.下列四组物质中互为同素异形体的是A .纯碱与苏打B .12CO 和14COC .CH 3CHO 与CH 2—CH 2D .金刚石和富勒烯(C 60)6.元素周期表是学习化学的重要工具。
下图是元素周期表中的一格,以下对该图信息的解读中,不正确的是A .该元素的原子序数为6B .该元素所有原子的质子数均为6C .该元素的相对原子质量为12.01D .该元素没有同位素,所有原子的中子数均为67.元素在周期表中的位置,能反映原子结构和元素的化学性质,下列有关说法正确的是A .由长、短周期元素共同组成的元素族称为主族 (除零族外)B .同一元素不可能既表现金属性,又表现非金属性C .短周期元素原子形成简单离子后,最外层电子都达到8电子稳定结构D .互为同位素的不同核素,物理性质和化学性质都不同8.如图所示,元素周期表中的金属和非金属元素的分界线处用虚线表示。
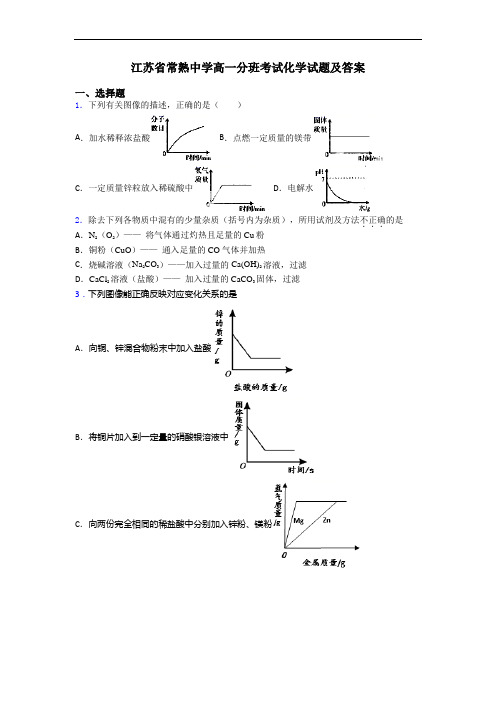
江苏省常熟中学高一分班考试化学试题及答案一、选择题1.下列有关图像的描述,正确的是()A.加水稀释浓盐酸 B.点燃一定质量的镁带C.一定质量锌粒放入稀硫酸中 D.电解水2.除去下列各物质中混有的少量杂质(括号内为杂质),所用试剂及方法不正确...的是A.N2(O2)——将气体通过灼热且足量的Cu粉B.铜粉(CuO)——通入足量的CO气体并加热C.烧碱溶液(Na2CO3)——加入过量的Ca(OH)2溶液,过滤D.CaCl2溶液(盐酸)——加入过量的CaCO3固体,过滤3.下列图像能正确反映对应变化关系的是A.向铜、锌混合物粉末中加入盐酸B.将铜片加入到一定量的硝酸银溶液中C.向两份完全相同的稀盐酸中分别加入锌粉、镁粉D.加热一定质量的氯酸钾和二氧化锰的固体混合4.下列除杂(括号内为杂质)选用的试剂或方法正确的是 ( ) A.CuO(C):隔绝空气高温加热B.N a2SO4溶液(N a OH):加适量稀盐酸C.CO2(HCl):将气体通入足量的氢氧化钠溶液D.CaCl2溶液(HCl):加入过量碳酸钙,充分反应后过滤5.等质量的镁、铝、锌分别与相同质量20%的盐酸充分反应,产生氢气的质量大小关系的猜测:①Al>Mg>Zn; ②Al=Mg=Zn; ③Al=Mg>Zn; ④Al=Zn>Mg; ⑤Al>Mg=Zn.其中错误的个数为A.5个 B.2个 C.3个 D.4个6.下列除杂方案中(括号中物质是杂质),正确的是()A.N2(O 2):通过红热的木炭 B.烧碱(纯碱):加适量稀盐酸、蒸发C.Cu(CuO):加过量的盐酸溶液并过滤 D.NaHCO3(Na2CO3):高温煅烧7.下列曲线能正确表达对应的反应或过程的是A.向一定量的盐酸中逐滴加水稀释B.某温度下将一定量接近饱和的KNO3溶液恒温蒸发水分C.金属与一定量的稀硫酸反应,由图像可知,金属N比金属M活泼D.将a、b、c三种物质的饱和溶液分别由t1℃升温至t2℃时,所得溶液中溶质质量分数大小关系是:a>b>c8.向硫酸亚铁、硫酸铜的混合溶液中加入一些锌粉,充分反应后,过滤,得到滤渣A和滤液。

江苏省苏州市常熟中学2019-2020学年高一下学期期中考试试题注意事项:1.本试卷分选择题和非选择题,共23 题,满分100 分;考试用时90 分钟。
2.答题前,考生务必将自己的姓名、考点名称、考场号、座位号用0.5 毫米黑色墨水签字笔填写在答题卡相对应的位置上,并认真核对条形码上的准考号、姓名是否与本人的相符合。
3.答选择题必须用2B 铅笔把答题卡相对应题目的答案标号涂黑,如需改动,请用橡皮擦干净后,再选涂其他答案;答非选择题必须用0.5 毫米黑色墨水签字笔写在答题卡指定的位置上,不在答题区域内的答案一律无效,不得用其他笔答题。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Zn-65选择题(共44 分)单项选择题(包括10 题,每题 2 分,共20 分,每题只有一个选项符合题意)1.化学与生活息息相关,下列关于生活中的化学,说法错误的是( )A. 近期,全球爆发了新型冠状病毒,从化学角度,可用含氯的消毒剂、75%酒精、过氧化氢进行病毒的杀灭B. 汽车的排气管上装有“催化转化器”,使有毒的CO和NO反应生成N2和CO2C. 大量燃烧化石燃料排放的废气中含大量CO2、SO2,造成大气污染,从而使雨水pH=5.6D. 积极推广太阳能、风能、地热能及水能等的使用,减少化石燃料的使用『答案』C『解析』『详解』A. 新型冠状病毒主要成分是蛋白质,含氯的消毒剂、75%酒精、过氧化氢进行病毒能够使蛋白质发生变性,因而具有杀菌消毒作用,从而可以将病毒杀灭,A正确;B. 汽车的排气管上装有“催化转化器”,可以使有毒的CO和NO发生氧化还原反应转化为空气的成分N2和CO2,从而减少空气中污染物的含量,B正确;C. 大量燃烧化石燃料排放的废气中含大量CO2溶于水产生碳酸,碳酸电离产生H+,使雨水pH=5.6,SO2溶于水产生H2SO3,H2SO3的酸性比H2CO3强,从而使雨水的pH<5.6,C错误;D. 积极推广太阳能、风能、地热能及水能等的使用,既满足了人类对能源的需要,同时也减少了对化石燃料开采及使用,D正确;故合理选项是C。

江苏省南通中学2014-2015学年度第二学期期中考试高一化学试卷本试卷总分100分,考试时间90分钟。
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Al—27 S—32 Ca—40Fe—56 Cu—64 Mg—24 Cl —35.5 K—39 Ba —137Ni—59第Ⅰ部分(选择题69分)一、单项选择题:在每题的4个选项中,只有1个选项符合要求的(本部分23题,每题3分,共69分)。
1.下列物质不计入“空气污染指数”项目的是A.二氧化硫B.二氧化碳C.二氧化氮D.可吸入颗粒2.Al2O3是刚玉的主要成分。
Al2O3属于A.酸B.盐C.单质D.氧化物3.下列气体中,既能用碱石灰干燥,又能用排水法收集的是A.CO B.NO2C.SO2D.NH34.关于元素周期表的说法正确的是A.元素周期表有8个主族B.ⅠA族的元素全部是金属元素C.元素周期表有7个周期D.短周期是指第一、二周期5.下列物质中属于含有共价键的离子化合物的是A.CaCl2 B.Na2O2C.NaCl D.H2SO46.23592U是核电站的主要燃料,下列关于23592U的说法正确的是A.质量数为235 B.中子数为92C.电子数为143 D.质子数为2357.中华语言博大精深,下列词语中,其含意是物理变化的是A.蜡炬成灰B.曾青得铁C.百炼成钢D.大浪淘沙8.下列选项描述的过程能实现化学能转化为热能的是A.光合作用B.烧炭取暖C.风力发电D.电解冶炼9.下列物质与化学式相应的是A.小苏打—Na2CO3B.钡餐—BaCO3C.漂白粉的有效成分—Ca(ClO)2D.水玻璃—H2SiO310.当其他条件不变时,下列说法正确的是A.使用催化剂一定能加快反应速率B.用粉状锌代替块状锌与稀硫酸反应一定会加快反应速率C.当反应物与生成物浓度相等时,可逆反应一定已达到化学平衡状态D.在合成氨反应中,增大N2浓度一定可以使H2的转化率达到100%11.关于化学反应中的说法错误..的是A.右图所示的反应为放热反应B.化学反应中有物质变化也有能量变化C.需要加热的化学反应不一定是吸热反应D.化学键断裂吸收能量,化学键生成放出能量12.在溶液中能大量共存的离子组是A.Fe3+、OH一、HCO3-B.Ba2+、OH一、C1—C.H+、K+、CO32-、D.NH4+、NO3—、OH—13关于短周期元素x、y、z说法错误的是A.元素x、y位于同一周期B.元素x、y、z都是非金属元素C.元素z的氢化物比x的氢化物稳定D.元素最高价氧化物的水化物酸性y<z 14.下列化学用语表示正确的是A.OH—的电子式:︰∙∙∙∙O︰H B.F—的结构示意图C.N2的结构式:︰N≡N︰D.碳酸氢钠的电离方程式:NaHCO3=Na++H++CO32-15.纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹的“脱氯剂”,Na2S2O3和C12反应的化学方程式为4C12+ Na2S2O3+5H2O=2NaCl+2H2SO4+6HCl,有关该反应的说法正确的是A.该反应中氧化剂是C12B.每有1mol C12反应转移1mole-C.反应中S元素的价态降低D.该反应中H2O被氧化16.设N A为阿伏加德罗常数,下列说法中错误的是A.在标准状况下,22.4 LSO3所含的硫原子数目为N AB.常温常压下,7.8g过氧化钠含有的离子数为0.3N AC.18 g 水所含的电子数目为10 N AD.3.2g O2、O3混合物中所含氧原子一定是0.2N A17.下列实验方法或操作能达到实验目的的是A.收集SO2 B.测量Cu与浓硝酸C.二氧化锰固体和D.吸收HCl反应产生气体的体积反应双氧水制取O218.下列反应的离子方程式正确的是A.过氧化钠和水反应:2Na2O2+2 H2O =4Na++4OH-+O2↑B.氧化铝溶于氢氧化钠溶液:Al2O3+2 OH-=2AlO2-+H2↑C.氢氧化钡溶液滴入稀硫酸中:Ba2++ OH一+H++ SO42- =BaSO4 ↓+H2 OD.二氧化碳通入足量氢氧化钠溶液:CO2+ OH-=HCO3-19.右图装置中,U形管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液(呈酸性..),各加入生铁块,放置一段时间。

江苏省响水中学2014~2015学年度第二学期高一年级期中考试化学试题注意事项:1、本试题分第Ⅰ卷和第Ⅱ卷,共4页2、满分:100分 ,考试时间:75分钟可能用到的相对原子质量:H:1 Li:3 He:4 C:12 N:14 O:16 S:32 Cl:35.5 Na:23 Al:27 Mg:24 Ca:40 Zn:65 Fe:56 Cu:64 第Ⅰ卷(选择题,共计69分)一、单项选择题:在每题的4个选项中,只有1个选项是符合要求的(本部分23题,每题3分。
共69分)。
1.“绿色化学”要求从根本上减少乃至杜绝污染。
下列对农作物收割后留下的秸秆的处理方法中,不符合“绿色化学”要求的是 A .就地焚烧 B .发酵后作农家肥 C .加工成精饲料 D .制造沼气2.下列物质中,既有离子键又有共价键的是 A .CaCl 2 B .KOH C .H 2O D .HCl3. 某元素的原子核外有三个电子层,M 层的电子数是L 层电子数的1/2,则该元素的原子是 A .LiB .AlC .SiD .K4.某元素最高价氧化物对应水化物的化学式是H 2XO 4,这种元素的气态氢化物的分子式为 A .HXB .H 2XC .XH 3D .XH 45.下列说法不正确的是 A .氧气和臭氧互为同素异形体B .CH 3-CH 2OH 和 CH 3-O-CH 3 互为同分异构体C .He 32和He 42互为同位素D .He 42的最外层电子数为2,所以He 42具有较强的金属性 6.关于元素周期表的说法正确的是A .元素周期表有8个主族B .ⅠA 族的元素全部是金属元素C .元素周期表有7个周期D .短周期是指第一、二周期 7.下列化学用语正确的是 A .氯化钠的电子式:B .氯化氢的电子式C .碳元素位于周期表中第2周期ⅥA 族D .H 2O 的结构式:H —O —H 8.对于反应中的能量变化,表述正确的是ww w .ks5 u .co m A .吸热反应中,反应物的总能量大于生成物的总能量 B .形成化学键的过程会释放能量C .加热才能发生的反应一定是吸热反应D .氧化反应均为吸热反应9.对于在密闭容器中、一定条件下进行的可逆反应2SO 2(g)+O 23(g),能说明反应已达到平衡状态的是( )A .v (O 2)∶v (SO 2) =1∶2B .各物质浓度相等C .c (SO 2)保持不变D .c (SO 2)∶c (O 2)∶c (S03)=2∶1∶210.下列过程能实现热能转化为化学能的是A .HCl 十NaOH=NaCl 十H 2OB .碳酸钙受热分解C .镁条溶于盐酸D .CaO 十H 2O=Ca(OH)2 11.下列关于化学能转化为电能的四种装置的说法正确的是稀硫酸Z nCuH222碳棒2糊4Cl 糊锌筒电池Ⅰ 电池Ⅱ 电池Ⅲ 电池Ⅳ A .电池Ⅰ中锌是正极 B .电池Ⅱ是一次电池C .电池Ⅲ工作时,氢气发生还原反应D .电池Ⅳ工作时,电子由锌通过导线流向碳棒 12.下列各组元素的原子序数中,其相应的元素原子能形成X 2Y 共价化合物的是 A .3与8 B .1与16 C .12与17 D .6与813.某元素最高正价与负价绝对值之差为4,该元素的离子与跟其核外电子排布相同的离子形成的化合物是 A .K 2SB .MgOC .MgSD .NaF14.一定条件下,在体积一定的密闭容器中加入1 mol N 2和3 mol H 2发生反应:N 2 + 3H 2(正反应是放热反应)。

江苏省苏州市常熟中学高一化学下学期期末试卷含解析一、单选题(本大题共15个小题,每小题4分。
在每小题给出的四个选项中,只有一项符合题目要求,共60分。
)1. 化学与科学、技术、社会、环境密切相关。
下列有关说法错误的是A.2010年11月广州亚运会燃放的焰火是某些金属元素焰色反应所呈现出来的色彩B.化学面对现代日益严重的环境问题显的无能为力C.化学将在能源、资源的合理开发和安全应用方面大显身手D.化学是一门以实验为基础的自然科学参考答案:B略2. 将5mL0.4mol/LAgNO3溶液与10mL 0.3mol/LBaCl2溶液混合.反应后,溶液中离子浓度最大的是()A. Ag+B. NO3﹣C. Ba2+D. Cl﹣参考答案:Dn(AgNO3)=0.4mol/L×0.005L=0.002mol,n(BaCl2)=0.3mol/L×0.01L=0.003mol,二者反应方程式为:2AgNO3 +BaCl2═Ba(NO3)2+2AgCl↓,根据方程式知,硝酸银完全反应,剩余n(BaCl2)为0.002mol,所以溶液中的溶质是硝酸钡和氯化钡,n[Ba(NO3)2]=0.001mol,氯化钡和硝酸钡都是强酸强碱盐,在水溶液里完全电离,根据物料守恒知,n(NO3﹣)=0.002mol,n(Cl﹣)=0.004mol,Ag+完全参加反应,n(Ba2+)=0.003mol,所以离子浓度大小顺序是c(Cl﹣)>c(Ba2+)>c(NO3﹣)>c (Ag+),故选D.3. 一定温度下,可逆反应3X(g)+Y(g) ?2Z(g)达到限度的标志是A. 单位时间内生成3n mol X,同时消耗n mol YB. X的生成速率与Z的生成速率相等C. X、Y、Z的浓度相等D. X、Y、Z的分子数之比为3∶1∶2参考答案:A试题分析:A项个物质的浓度保持不变,所以达到反应限度;B项X与Y的生成速率之比为3:2时达限度;C项各物质的浓度为定值时达限度;D项各物质的个数比与反应限度无关。
江苏省盐城中学2014—2015学年度第二学期期中考试高一年级化学试题(2015.5)命题人:卞 淼、仇 静 审核人: 高 炳 东试卷说明:本场考试时间100分钟,总分120分。
本卷可能用到的相对原子质量 O :16 Mg :24 S :32Zn :65一、选择题(本题包括23小题,每小题3分,共69分。
每小题只有一个....选项符合题意) 1.每年6月5日为世界环境日,今年世界环境日的主题为“资源效率、可持续消费与生产”,提倡节能减排,以下措施中不能体现这一思想的是A .开发太阳能、风能、氢能等清洁能源B .大力发展火电,缓解用电紧张C .研制出性能优良的催化剂,降低反应所需温度D .提倡绿色生活,使用公共交通 2.下列各组物质中,化学键类型完全相同的一组是A .CO 2和H 2SB .NaCl 和NH 4ClC .CCl 4和KClD .MgCl 2和SO 23.通过控制或改变反应条件可以加快、减缓甚至阻止反应的进行,使化学反应有利于人类的生存和提高生活质量。
下列各图所示的措施中,能加快化学反应速率的是A .B .C . D.AB C D 4.下列说法正确的是A .需要加热方能发生的反应一定是吸热反应B .吸热反应在常温下一定很难发生C .反应是放热还是吸热,由反应物和生成物所具有的总能量的相对大小决定D .化学反应只生成新物质,没有能量的变化5.电池是人类生产和生活中的重要能量来源,各式各样电池的发明是化学对人类的一项重大贡献。
下列有关电池的叙述错误..的是 A .锌锰干电池工作一段时间后锌片变薄 B .氢氧燃料电池工作时氢气在负极被还原 C .氢氧燃料电池可将化学能直接转变为电能 D .高纯度的硅可作为太阳能电池的主要材料6.下列说法中,正确的是A .IA 和VIIA 族元素间只能形成离子化合物B .第三周期:从左到右元素最高正价从+1到+7递增C .同主族的单核阴离子:还原性越强,离子半径越小D .同周期金属:原子失电子能力越强,最高化合价越高7.人造地球卫星用到的一种高能电池——银锌蓄电池,其电池的电极反应式为:Zn + 2OH --2e -= ZnO + H 2O ,Ag 2O + H 2O + 2e -= 2Ag + 2OH -。
江苏省常熟中学高一下学期第二次质量检测化学试题一、选择题1.二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构与双氧水分子相似。
常温下,S2Cl2是一种橙黄色液体,遇水可发生反应,并产生能使品红褪色的气体。
下列说法中不正确的是A.S2Br2与S2Cl2结构相似,沸点S2Br2 > S2Cl2B.S2Cl2的结构式为Cl—S—S—ClC.S2Cl2中S显—1价D.2S2Cl2+2H2O=SO2↑+3S↓+4HCl【答案】C【详解】A. 组成和结构相似的分子晶体,相对分子质量越大,分子间作用力越大,熔、沸点越高;S2Br2与S2Cl2结构相似,S2Br2相以分子质量较大,所以沸点S2Br2 > S2Cl2,A正确;B. 由题中信息分子结构与双氧水分子相似,双氧水的结构式为H-O-O-H,所以S2Cl2的结构式为Cl-S-S-Cl,B正确;C. 氯和硫都是第3周期元素,氯的非金属性较强,所以S2Cl2中Cl显-1价,S显+1价,C错误;D. 由题中信息S2Cl2遇水可发生反应,并产生能使品红褪色的气体,可知反应后生成二氧化硫,所以S2Cl2与水发生反应的化学方程式为2S2Cl2+2H2O=SO2↑+3S↓+4HCl,D正确;故选C。
2.工业上获得下列物质不是以海水或海洋资源为主要原料的是( )①Fe ②Mg ③Na ④NaOH ⑤I2 ⑥Cu ⑦SiA.①⑥⑦B.①②⑦C.⑤⑥⑦D.①④⑥【答案】A【详解】①Fe是用CO还原铁矿石制得;②Mg是先从海水中分离出MgCl2,然后熔融电解获得;③Na是先从海水中提取食盐,然后熔融电解获得;④NaOH是电解饱和食盐水获得;⑤I2是从海藻类植物中提取的;⑥Cu是采用高温氧化铜矿石的方法获得;⑦Si是在高温条件下,用焦炭还原二氧化硅获得;综合以上分析,①⑥⑦不是以海水或海洋资源为主要原料获得,故选A。
3.下列说法不正确...的是( )A.生铁和钢都是铁和碳的合金B.氯化钙是漂白粉的有效成分C.玻璃、水泥属传统硅酸盐产品D.氧化铝陶瓷是新型无机非金属材料【答案】B【详解】A.生铁和钢都是铁合金,含有的杂质元素主要是碳,因此二者都是铁和碳的合金,A正确;B.漂白粉的主要成分是氯化钙、次氯酸钙,有效成分是次氯化钙,B错误;C.玻璃、水泥的主要成分是硅酸盐,因此都属于传统硅酸盐产品,C正确;D.氧化铝陶瓷、高温结构陶瓷、生物陶瓷都是新型无机非金属材料,D正确;故合理选项是B。
江苏省扬州中学2014-2015学年度第二学期期中考试高一化学试卷2015.4本试卷共120分。
考试时间100分钟可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cu-64第Ⅰ卷(选择题共40分)单项选择题(本题包括10小题,每题2分,共20分。
每小题只有一个....选项符合题意)1、科学家发现两种粒子:第一种是只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”;第二种是由四个氧原子构成的分子。
下列有关这两种粒子的说法不.正确..的是A.“四中子”不显电性B.“四中子”的质量数为4,其质量比氢原子大C.“零号元素”在元素周期表中与氢元素占同一位置D.第二种粒子的化学式为O4,与O2互为同素异形体2、下列化学用语书写正确的是A.氯原子的结构示意图:B.氯化铵的电子式:C.CO2的结构式:O=C=O D.CH4的比例模型:3、一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3=2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为A.5∶3 B.5∶4 C.1∶1 D.3∶54、下列有关物质的性质、应用或制取的说法正确的是A.自来水厂可用明矾对水进行消毒杀菌B.工业上将氯气通入澄清石灰水中,制取漂白粉C.除去氯化钙溶液中少量盐酸,加入足量碳酸钙粉末,充分搅拌再过滤D.常温下浓硝酸与铝不反应,可用铝制容器存放浓硝酸5、甲、乙两种非金属①甲比乙容易与H2化合②甲原子能与乙阴离子发生置换反应③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强;④与某金属反应时,甲原子得电子数目比乙的多;⑤甲的单质熔、沸点比乙的低。
能说明甲比乙的非金属性强的是A.只有④B.只有⑤C.①②③D.①②③④6、下列装置所示的实验能达到实验目的的是7、下列各组顺序的排列错误..的是 A .半径:F —>Na +>Mg 2+>Al 3+B .沸点:H 2O< H 2S < H 2SeC .酸性:HClO 4>H 2SO 4>H 3PO 4D .熔点:SiO 2>NaCl >CO 28、A 元素的原子最外层电子数是a ,次外层电子数是b ;B 元素的原子M 层电子数是(a -b),L 层电子数是(a +b),则A 、B 两元素形成的化学式最可能表示为 A .B 3A 2 B .BA 2C .A 3B 2D .AB 29、下列离子方程式正确的是 A .向盐酸中滴加氨水:H ++ OH —=H 2OB .Na 2SiO 3溶液中通入过量的CO 2:SiO 32-+CO 2+H 2O =H 2SiO 3↓+CO 32-学科网C .FeBr 2溶液中通入足量的Cl 2:2Fe 2++4Br -+3Cl 2=2Fe 3++2Br 2+6Cl -学科网D .Na 2SO 3溶液中加入稀硝酸:SO 32-+2H +=SO 2↑+H 2O 学科网 10、对于反应2SO 2+O 2催化剂 加热2SO 3,下列判断正确的是A .2 mol SO 2和足量的O 2反应,可生成2 mol SO 3B .达到反应限度时SO 2、O 2、SO 3的分子数之比一定为2∶1∶2C .达到反应限度时SO 2的消耗速率必定等于O 2的生成速率的2倍D .若反应在恒容容器中进行,气体密度保持不变,可以判定反应到达平衡不定项选择题(本题包括5小题,每小题4分,共20分。
2019-2020学年江苏省常熟市高一下学期期中考试化学注意事项:1.本试卷分选择题和非选择题两部分,共100分。
考试时间90分钟2.请把选择题的答案用2B铅笔填涂在答题卡上或答题纸的指定位置,把非选择题的答案用黑色墨水签字笔写在答题纸的指定位置。
3.可能用到的相对原子质量:H1 C12 N14 O16 Zn65第I卷(选择题,共44分)一、单项选择题(本题共10小题,每小题2分,共20分。
每小题只有一个....选项符合题意。
)1.化学与生活息息相关,下列关于生活中的化学,说法错误的是A.近期,全球爆发了新型冠状病毒,从化学角度,可用含氯的消毒剂、75%酒精、过氧化氢进行病毒的杀灭B.汽车的排气管上装有“催化转化器”,使有毒的CO和NO反应生成N2和CO2C.大量燃烧化石燃料排放的废气中含大量CO2、SO2,造成大气污染,从而使雨水pH=D.积极推广太阳能、风能、地热能及水能等的使用,减少化石燃料的使用2.下列化学用语表示正确的是A.硫离子的结构示意图:B.甲烷分子的球棍模型:C.过氧化氢分子的电子式:2的结构式::N≡N:3.可逆反应3A(g)+B(g)2C(g)+2D(g)在不同条件下的反应速率如下,其中反应速率最快的是A.v(A)=0.6 mol·L-1·min-1B.v B.v(B)=0.3 mol·L-1·min-1C.v(C)=0.5 mol·L-1·min-1D.v D.v(D)=0.2 mol·L-1·min-14.有关元素周期表的说法中错误的是A.元素周期表有7个周期,16个族B.元素周期表中,VIII族包括第8、9、10三个纵行C.同周期元素形成的简单离子的电子层数相同D.作为半导体材料的元素大多数位于金属与非金属的分界线附近5.下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是2和SiO22和H2O 和4和NH4Cl6.下列说法正确的是A.形成离子键的阴阳离子间只存在静电吸引力B.任何分子中每个原子最外层均满足8电子结构C.冰融化时,水分子中H-O键发生断裂D.熔沸点由高到低的顺序是:金刚石>NaCl>H2O7.下列离子方程式中,正确的是A.碳酸氢铵溶液中加入足量的浓氢氧化钠溶液并加热:NH4++OH-∆==NH3↑+H2OB.铜与稀硝酸的反应:Cu+4H++2NO3-=Cu2++2NO2↑+2H2OC.向Ba(OH)2溶液中滴加稀硫酸:Ba2++OH-+H++SO42-=BaSO4↓+H2OD.过量二氧化硫与氢氧化钠溶液反应:SO2+OH-=HSO3-8.下列有关化学反应速率、化学反应限度的说法中,正确的是A.反应C(s)+H2O(g)CO(g)+H2(g),增加碳的用量可加快反应速率B.用铁片与稀硫酸反应制H2,改用98%的浓硫酸可加快生成H2的速率C.反应2SO2(g)+O2(g)2SO3(g)在密闭容器中进行,压缩容器体积,反应速率增大D.可逆反应达到化学平衡状态时,正、逆反应的速率相等且都为09.下列事实与带点物质表现出的性质(括号中)对应关系不正确的是A.SO2.能使含有酚酞的氢氧化钠溶液褪色(漂白性)B.常温下,铁遇浓硫酸...、浓硝酸...发生钝化(强氧化性)C.久置的浓硝酸...,颜色略显黄色(不稳定性)D.蔗糖与浓硫酸...反应中有黑色物质生成(脱水性)10.设N A表示阿伏加德罗常数的值,下列说法正确的是A.1 L 0.1 mol·L-1氨水中含有0.1 N A NH3分子B.46 g NO2和N2O4混合气体中含有的原子数为3N AC.1 mol Na2O2中含有的阴离子数为2N AD.常温常压下,12 g 14C所含中子数为6N A二、不定项选择题(本题包括8小题,每小题3分,共计24分。