27、何谓配合物的稳定常数
- 格式:doc
- 大小:18.50 KB
- 文档页数:1



第一章测试1.配合物结构分为内界和外界() A:错 B:对答案:B2.配位化学发展史上最早见于记录的配合物是() A:普鲁士蓝KFe[Fe(CN)6]·nH2O B:二茂铁 C:大环配合物 D:蔡氏盐答案:A3.配位化学是无机化学的一个重要分支学科,它研究的对象是配合物。
()A:错 B:对答案:B4.配位化学发展史上标志着配位化学研究的开始的配合物是() A:二茂铁B:CoCl3· 6NH3 C:蔡氏盐 D:大环配合物答案:B5.无机物同样存在着几何异构、电离异构和光学异构现象。
() A:错 B:对答案:B第二章测试1.在[Co(en)(C2O4)2]-中,Co3+的配位数是(). A:4 B:6 C:2 D:3 答案:B2.下面配合物中,关于中心原子特征描述正确的是() A:中心原子也可以是电中性的原子甚至阴离子 B:中心原子是指能提供空轨道的带正电阳离子 C:所有选项均正确 D:少数高氧化态的非金属元素也能作中心原子答案:C3.超分子配合物的概念是由下面那个化学家提出的() A:罗勤慧 B:戴安邦 C:莱恩 D:道尔顿答案:C4.分子中既存在离子键,共价键还存在配位键的有() A:AlCl3B:[Co(NH3)6]3+Cl3 C:KCN D:Na2SO4 答案:B5.超分子配合物的概念是由道尔顿提出的。
() A:对 B:错答案:B第三章测试1.价键理论可以解释配合物的() A:磁性和颜色 B:空间构型和颜色 C:颜色和氧化还原性 D:磁性和空间构型。
答案:D2.配合物的磁矩主要取决于形成体的() A:成单电子数 B:电荷数 C:原子序数D:成对电子数。
答案:A3.晶体场理论的核心是() A:M-L键由点电荷之间的作用形成 B:除了静电作用,包括轨道重叠的共价作用 C:配体的电子对转移到金属的杂化原子轨道中 D:Jahn-Teller效应答案:A4.下列配体的配位能力的强弱次序正确的为() A:X->H2O>CH->NH3>NCS-B:CN->NH3>NCS->H2O>X- C:X->CN->H2O>NH3>NCS- D:CN->NH3>NCS->H2O>X- 答案:B5.IF5所具有的对称元素是() A:一个对称面,一个对称中心 B:一个三重轴,三个二重轴,四个对称面,一个对称中心 C:一个五重轴,五个二重轴,六个对称面,一个对称中心 D:一个四重轴,四个对称面答案:D第四章测试1.下列离子中反位效应最大的是() A:Br- B:F- C:Cl- D:I-答案:D2.氧化还原方法合成配合物时,常用的氧化剂有() A:K2Cr2O4 B:空气 C:过氧化氢 D:PbO2 答案:BCD3.在水热条件下,亚氨基二乙酸作为主配体构筑稀土配合物时易原位生成()A:甲酸 B:丙酸 C:乙酸 D:草酸答案:D4.唯一能在原子级别上确定配合物结构的分析手段是() A:红外 B:元素分析C:X射线单晶衍射法 D:质谱答案:C5.下列属于配合物单晶的培养方法是() A:常规溶液法 B:水热或溶剂热法 C:金属热还原法 D:扩散法答案:ABD第五章测试1.配合物PtCl2(NH3)2为平面四边形,则它可能有的异构现象称为() A:几何异构 B:旋光异构 C:配位异构 D:离解异构答案:A2.[VO(acac)2]的几何构型是() A:四面体 B:八面体 C:三角双锥 D:四方锥答案:D3.配位数为6的配合物的空间构型有八面体和三棱柱等两种。

金属离子与氨羧配位剂的配合物稳定常数对于理解化学反应和预测化学平衡非常重要。
本文将介绍金属离子与氨羧配位剂的配合物稳定常数的定义、影响因素以及计算方法。
一、金属离子与氨羧配位剂的配合物稳定常数的定义金属离子与氨羧配位剂通过配位键形成配合物,配合物稳定常数(K)是定量描述配合物形成的程度的常数。
金属离子与氨羧配位剂形成的配合物可以用如下的化学方程式表示:Mn+ + L ⇌ MLn+其中Mn+代表金属离子,L代表氨羧配位剂,MLn+代表金属离子与氨羧配位剂形成的配合物。
配合物稳定常数K的定义如下:K = [MLn+]/([Mn+][L])其中[MLn+]、[Mn+]和[L]分别代表配合物、金属离子和氨羧配位剂的浓度。
配合物稳定常数K的值越大,表示配合物形成的程度越高;反之,K的值越小,表示配合物形成的程度越低。
二、金属离子与氨羧配位剂的配合物稳定常数的影响因素1. 金属离子的电荷:金属离子的电荷越大,与氨羧配位剂形成的配合物稳定常数K越大。
2. 氨羧配位剂的性质:不同的氨羧配位剂有不同的配位能力,影响金属离子与氨羧配位剂形成配合物稳定常数K的大小。
3. 溶剂的性质:不同溶剂对金属离子与氨羧配位剂形成的配合物稳定常数K有不同的影响。
4. 温度:温度的升高通常会使金属离子与氨羧配位剂形成的配合物稳定常数K增大。
三、金属离子与氨羧配位剂的配合物稳定常数的计算方法金属离子与氨羧配位剂的配合物稳定常数可以通过不同的实验方法来测定,如紫外-可见光谱法、电化学法、核磁共振法等。
通过实验测定得到的数据可以计算配合物稳定常数K的值。
还可以通过计算方法来估算配合物稳定常数K的值,常用的计算方法有理论计算、量子化学计算等。
金属离子与氨羧配位剂的配合物稳定常数是描述配合物形成程度的重要物理化学常数,对于理解化学反应和应用化学平衡有着重要的意义。
通过实验测定和计算方法可以得到金属离子与氨羧配位剂的配合物稳定常数的数值,进而更深入地理解金属离子与氨羧配位剂的配合物形成规律。




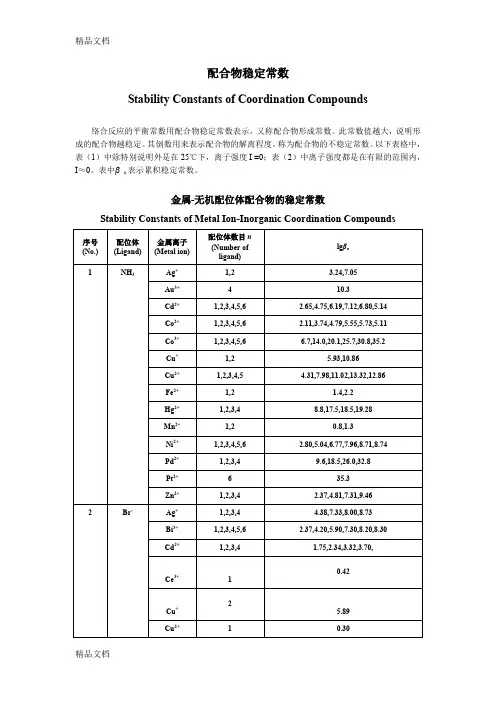
配合物稳定常数
Stability Constants of Coordination Compounds
络合反应的平衡常数用配合物稳定常数表示,又称配合物形成常数。
此常数值越大,说明形成的配合物越稳定。
其倒数用来表示配合物的解离程度,称为配合物的不稳定常数。
以下表格中,表(1)中除特别说明外是在25℃下,离子强度I =0;表(2)中离子强度都是在有限的范围内,I≈0。
表中βn表示累积稳定常数。
金属-无机配位体配合物的稳定常数
Stability Constants of Metal Ion-Inorganic Coordination Compounds
金属-有机配位体配合物的稳定常数
(表中离子强度都是在有限的范围内,I≈0。
)
Stability Constants of Metal Ion-Organic Coordination Compounds
EDTA的lgαY(H)值
lgαY(H) Values of EDTA
精品文档
精品文档。

第五章 配合物在溶液中的稳定性在配位化学的研究应用中,常提及配合物的稳定性问题,配合物的稳定性在化学上有重要意义。
对配合物而言,其稳定性可包括热力学稳定性、动力学稳定性、氧化还原稳定性以及在水溶液、非水溶液或融盐中的稳定性等。
习惯上所说配合物的稳定性并且应用最多的是在水溶液中的热力学稳定性。
本章主要讨论热力学范畴的配合物在水溶液中的稳定常数和配位平衡,以及影响稳定性的因素和氧化还原稳定性等问题。
5. 1配合物的几种稳定常数稳定常数有不同的表示方法,在水溶液中经验平衡常数与标准平衡常数是一样的,故在讨论时所用平衡常数均为经验平衡常数。
5.1.1.浓度稳定常数(生成常数)和不稳定常数(解离常数)若M 表示金属离子,L 表示配体,则配离子的生成平衡与解离平衡一般可分别以下式表示,为简明起见略去各物种电荷:由此可见, )f K K (或稳越大,表示配离子越难解离,配合物也就越稳定。
故稳定常数是衡量配合物在溶液中稳定的尺度。
5.1.2. 逐级稳定常数与积累稳定常数实际上,配离子在溶液中的生成与解离都是逐级进行的:上式中的n K K K ,.......,21称为配离子的逐级稳定常数。
对以下各反应的平衡常数称为积累稳定常数,以 n βββ,.......,21表示:][]][[)(]][[][)(n nd nn f nML L M K K L M ML K K ML nL M ==+或或不稳稳 ]][[][.......................................................................]][[][]][[][1n 122 21 L ML ML K ML LML L ML ML K ML L ML L M ML K ML LM n n n n --=+=+=+第i 级积累稳定常数与逐级稳定常数之间的关系为:f K K K ......211=β。
5.1.3.混合配体化合物的稳定常数如配合物的形成过程:则:)(,][]][[][ij ji j i ij K N n N n j i B A M B MA ββ==≤=+=稳时,当ij β为混合配体化合物的积累稳定常数,n为配位数,N 为中心原子(离子)的最高配位数.若形成过程为:若形成过程为:这些稳定常数均为多重平衡的总结果,即总的平衡常数,它反映了体系达平衡后各个浓度之间的关系。
配合物的组成和不稳定常数的测定(物理化学李俊)一、目的要求1.掌握用分光光度法测定配合物组成及稳定常数的基本原理和方法。
2.通过实验,掌握测量原理和分光光度计的使用方法,二、实验原理1,用等摩尔连续递变法测定配合物的组成“递变法”实际上是一种物理化学分析方法。
可用来研究当两个组分混合时,是否发生化合,配合,缔合等作用,以及测定两者之间的化学比。
其原理是:在保持总浓度不变的前提下,依次逐渐改变体系中两个组分的比值,并测定不同摩尔分数时的某一物理化学参量。
在本实验中就是测定不同摩尔分数时溶液的光密度值D,作光密度对摩尔分数的曲线图,如图3-1,所示。
从曲线上光密度的极大值D极大所对应的摩尔分数值,即可求出配位数n值。
为了配制溶浓时方便,通常取相同摩尔浓度的金属离子M溶液和配位体L溶液。
在维持总体积不变的条件下,按不同的体积比配成一系列混合溶液。
这样体积比亦就是摩尔分数之比。
设X L为D极大时L溶液的体积分数:M溶液的体积分数为:则配合物的配位数为:若溶液中只有配合物MLn具有颜色,则溶液的D与MLn的含量成正比。
从D-X图上曲线的极大位置即可直接求出n,但当配制成的溶液中除配合物外,尚有金属离子M及配位体L 与配合物在同一波长λ最大下也存在一定程度的吸收时,所观察到的光密度D并不完全由配合物MLn的吸收所引起,必须加以校正。
所以选择适当的波长范围,仅使配合物MLn有吸收,M和L都不吸收或极少吸收。
2.配合物平衡常数的测定假定配合物中心离子浓度不变,而渐增加配位体浓度,随着配位体浓度的改变,中心离子被配成MLn,溶液的光密度值D不断升高。
当中心离子被完全配合后,如继续增加配位体的浓度,则溶液的光密度值D趋于恒定,如图3-2。
设配合物在稀溶液中有如下解离平衡存在:最初浓度平衡浓度式中,n-配位数,已由实验确定;a-解离度:C-配合物未解离时的浓度(在本实验中亦为M完全配合时的配合物浓度)。
式中Dm 是M 完全被配合时溶液的光密度值,Dn 是L 与M 摩尔比为n 时溶液的光密度,此时虽达平衡,但M 未被完全配合。
配合物稳定常数
Stability Constants of Coordination Compounds
络合反应的平衡常数用配合物稳定常数表示,又称配合物形成常数。
此常数值越大,说明形成的配合物越稳定。
其倒数用来表示配合物的解离程度,称为配合物的不稳定常数。
以下表格中,表(1)中除特别说明外是在25℃下,离子强度I =0;表(2)中离子强度都是在有限的范围内,I≈0。
表中βn表示累积稳定常数。
金属-无机配位体配合物的稳定常数
Stability Constants of Metal Ion-Inorganic Coordination Compounds
金属-有机配位体配合物的稳定常数
(表中离子强度都是在有限的范围内,I≈0。
)
Stability Constants of Metal Ion-Organic Coordination Compounds
EDTA的lgαY(H)值lgαY(H) Values of EDTA。
何谓配合物的稳定常数
在溶液中,金属离子M n+与配位剂Y 4
的配位反应如下:
M n+ + Y 4 ⇌ M Y n-4 当配位反应达到平衡时:K My =]
][[][44-+-Y M MY n n 式中:][4-n MY ——金属离子与EDTA 形成的配合物的浓度;
[Y 4-]——未配位的EDTA 阴离子的浓度;
[M n+
]——未配位的游离的金属离子的浓度。
K My 是配合物的稳定常数,也叫形成常数。
配合物的稳定常数越大,表示形成的配合物越稳定。
由于稳定常数只考虑了溶液中金属离子(M n+)、配位剂阴离子(Y 4)和配合物(MY n-4)三者之间的平衡关系,没有考虑酸度等因素对配位平衡的影响,因此,它不能说明配合物的实际稳定程度。
配合物的稳定常数的数值通常很大,为了方便,常用其对数值表示。
例如: 69.842210]
][[][2==-+--Y Mg MgY K MgY 69.8lg 2=-MgY。