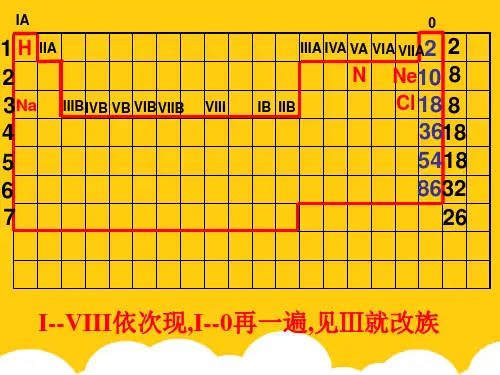
___M__g_A__l__S_i__P__S___C_l__A_r_______________
同周期元素原子结构上的相同点为
___电__子__层__数__相__同_________ 不同点为
原子结 构包括:
质__子__数__不__同__,___最__外__层__电__子__数_ 不同 质子数、
与钠同主族的元素有
Cs 泽固体
越越 来来 越越 剧剧 烈烈
实验内容
1、将少量 氯水分别加 入NaBr、KI 溶液中,后 加CCl4 2、将少量 溴水加入KI 溶液中,后 加淀粉溶液
实验现象
CCl4层分 别呈橙红 色、紫色
溶液变 蓝色
实验结论 Cl2可置换出 Br2 、 Ⅰ2, Cl2的氧化性 比Br2 、 Ⅰ2 强
正确,周期数=电子层数 Cl2可置换出Br2 、 I2 ,Br2可置换出 I2
H Li K Rb Cs Fr 5、同主族元素原子的最外层电子数一定相同
7、IA族元素称为碱金属元素,VIIA族元素称 CCl4层分别呈橙红色、紫色
钠、钾分别与水反应 钾与O2反应更剧烈,发出紫色火焰
为卤族元素 同主族元素原子结构上的相同点为_____________________ 不同点为_________________________
得电子能力__增__强______, 失电子能力
原子结构包_括减_:质_子弱数_、_电子_层_数、;最外同层电子主数 族元素从上到下,
原子半径___增_大________, 得电子能力 _____________相似的一族元素,它们在化学性质上表现
________________________
___减__弱_____,失电子能力__增__强________。 钾与O2反应更剧烈,发出紫色火焰