浙江省部分在用药用辅料参考名录xls
- 格式:xls
- 大小:84.50 KB
- 文档页数:1

浙江省人力资源和社会保障厅、浙江省物价局关于公
布第四批复合西药的通知
文章属性
•【制定机关】浙江省人力资源和社会保障厅,浙江省物价局
•【公布日期】2014.11.26
•【字号】浙人社发〔2014〕151号
•【施行日期】2015.01.01
•【效力等级】地方规范性文件
•【时效性】现行有效
•【主题分类】药政管理
正文
浙江省人力资源和社会保障厅浙江省物价局关于公布第四批
复合西药的通知
浙人社发〔2014〕151号各市、县(市、区)人力资源和社会保障局、物价局,嘉兴市社会保障事务局:
为加强基本医疗保险用药管理,合理保障参保人员的用药需求,根据《关于印发浙江省基本医疗保险、工伤保险和生育保险药品目录的通知》(浙人社发〔2010〕215号)和《关于复合西药列入基本医疗保险支付范围有关问题的通知》(浙人社发〔2010〕216号)精神,经专家认定,现将第四批复合西药名单予以公
布:
一、《第四批复合西药》(详见附件)中所列品种已经核实,列入基本医疗保险用药范围,按乙类药品支付。
二、本批公布的复合西药不再核定最高零售价,按集中采购价格执行。
三、本通知自2015年1月1日起执行。
请各地及时做好计算机信息管理系统药品数据库的更新工作,确保药品费用及时支付。
附件:第四批基本医疗保险复合西药
浙江省人力资源和社会保障厅
浙江省物价局
2014年11月26日。


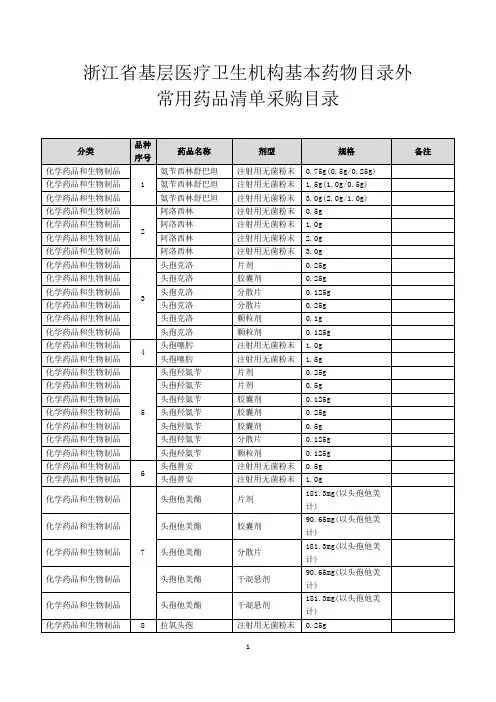
浙江省基层医疗卫生机构基本药物目录外常用药品清单采购目录
说明
一、药品的名称
化学药品和生物制品名称主要采用通用名称中表达化学成分部分,剂型单列;未标明酸根或盐基的药品,其主要化学成分相同而酸根或盐基不同的均为采购目录的药品;酯类衍生物的药品单独标明。
中成药采用药品通用名称。
二、药品的剂型
药品的剂型主要依据2010 年版《中华人民共和国药典》“制剂通则”等有关规定进行归类处理,未归类的剂型以目录中标注的为准,其中片剂(即普通片)、胶囊剂(即硬胶囊剂)、软胶囊(含胶丸)、混悬液(即口服混悬剂)、合剂(含口服液)、注射用无菌粉末(含粉针剂、冻干粉针剂、溶媒结晶粉针剂)。
三、药品的规格
药品的规格主要依据2010 年版《中华人民共和国药典》。
同一品种剂量相同但表述方式不同的暂视为同一规格;中成药片剂与胶囊剂日服用剂量一致的视为同一规格;未标注具体规格的,其剂型对应的规格暂以国家药品管理部门批准的规格为准。
四、其他
1.中成药成份中的“麝香”为人工麝香,“牛黄”为人工牛黄,有“备注”的除外;
2.目录中属于《浙江省临床供应紧张药品采购目录》的药品,本次
集中采购无需报名和网上申报,仍按我省现行供应紧张药品采购方法管理;
3.目录中属于麻醉药品、精神药品、医疗用毒性药品的,不纳入本次集中采购范围,继续按照国家和我省现行规定采购使用。
21。


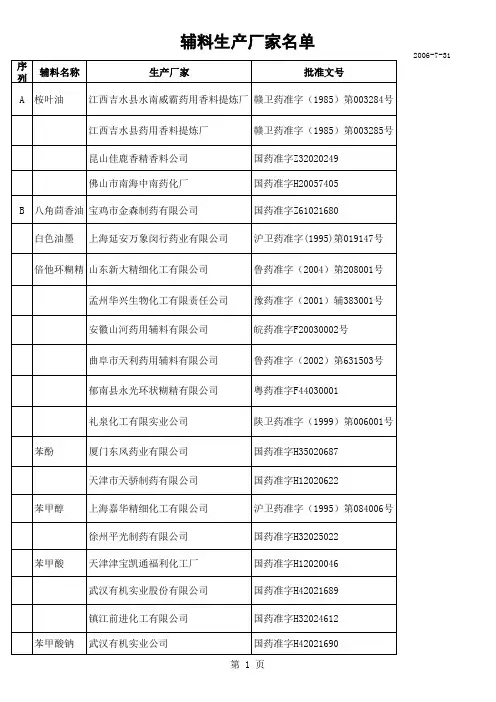
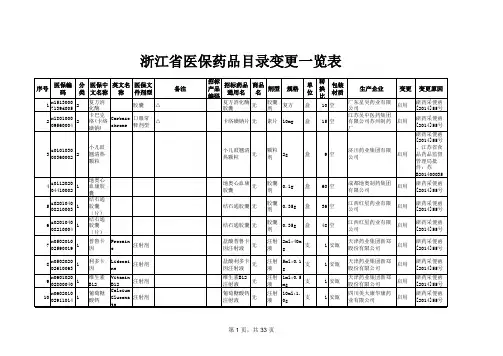

浙江省基层医疗卫四医疗卫生机构基本药物目录外常用药品清单(暂定)第一部分化学药品和生物制品一、抗微生物药二、抗寄生虫病药三、麻醉药四、镇痛、解热、抗炎、抗风湿、抗痛风药五、神经系统用药(三)其他六、治疗精神障碍药六、治疗精神障碍药(一)抗精神病药(二)抗抑郁药七、心血管系统用药(一)抗心绞痛药(二)抗高血压药(三)调脂及抗动脉粥样硬化药(四)周围血管舒张药八、呼吸系统用药(一)祛痰药(二)镇咳药九、消化系统用药(一)抗酸药及抗溃疡病药(二)助消化药(三)胃肠解痉药及胃动力药(四)泻药及止泻药(五)肝病辅助治疗药(六)微生态制剂(七)利胆药(八)肛肠科用药(九)其他十、泌尿系统用药(一)良性前列腺增生用药十一、血液系统用药(一)抗贫血药(二)抗血小板药(三)促凝血药(四)升白细胞药物十二、激素及影响内分泌药(一)肾上腺皮质激素类药(三)雌激素、孕激素及抗孕激素十三、抗变态反应药十四、免疫系统用药十五、抗肿瘤药(一)抗肿瘤抗生素十六、维生素、矿物质类药(一)维生素(二)矿物质(三)肠外营养药(四)肠内营养药十七、调节水、电解质及酸碱平衡药(一)水、电解质平衡调节药十八、皮肤科用药(二)肾上腺皮质激素类药(三)其他十九、眼科用药(二)散瞳药(三)其他二十、耳鼻喉科用药二十一、妇产科用药(一)其他暂定)。
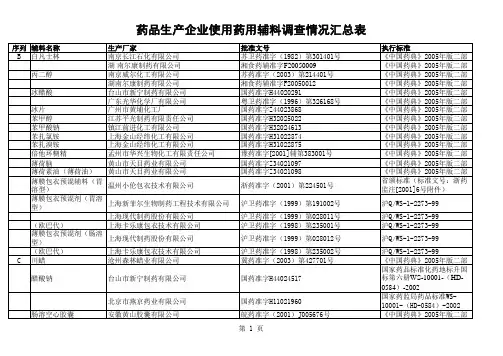
浙江省药用辅料使用管理暂行规定为加强药用辅料的管理,我局根据《药品管理法》、《药品生产质量管理规范》、以及国家食品药品监督管理局“关于药用辅料质量标准问题的复函”(食药监注函[2003]4号)等相关法律法规制定我省药用辅料使用管理暂行规定。
一、药用辅料的执行标准:1、国家药用标准2、地方药用标准3、企业标准。
本“暂行规定”所指的企业标准系指药品生产企业所用的药用辅料,无国家或地方药用标准,但有药用历史的辅料,企业依据国外药典标准、食品标准、化工标准等制定的质量标准。
药品生产企业制订药用辅料企业标准,应将该质量标准草案、标准起草依据和起草说明,连同三批样品一并报送省药检所复核。
企业标准应能全面科学的评价和控制辅料的质量符合药用要求。
其中药品注册时所附的相关辅料标准,已随药品注册经审评、批准的,可作为企业标准,直接执行。
二、药用辅料的使用要求1、药品生产企业应使用经国家或省食品药品监督管理部门批准,持有药用辅料批准文号的辅料,并对药品生产中使用的辅料质量负责。
2、已有国家或地方批准文号的药用辅料,药品生产企业必须采购有批准文号的药用辅料用于药品生产。
如有批准文号的药用辅料市场上确无供应,企业采购未取得药用辅料批准文号的辅料,首批使用前应送市级(含)以上药品检验所按国家或地方药用标准检验,检验合格后方可用于药品生产。
3、采购没有国家或地方药用标准,执行企业标准的药用辅料,首批使用前应送市级(含)以上药检所检验合格后,方可用于药品生产。
4、无批准文号、无药用标准又没有药用历史的辅料以及我国未生产过的药用辅料,按新辅料有关规定申报,待国家局注册批准后方可用于药品生产。
5、变更辅料按药品注册管理办法的有关规定,上报国家局批准后方可进行相应的变更。
三、供应商审计1、药品生产企业应制订对辅料供应商审计的管理制度、审计标准和操作程序。
由质量管理部门会同有关部门对辅料供应商进行定期审计,以确保符合要求。
不直接从生产厂家购入的辅料,应对生产厂家及供应商家分别审计。