消毒产品检验技术规范样本
- 格式:doc
- 大小:26.50 KB
- 文档页数:20

消毒技术规范20021.1 引言根据《中华人民共和国传染病防治法》、《中华人民共和国传染病防治法实施办法》和《消毒管理办法》制订本规范。
本规范含总则、消毒检验技术规范、医疗卫生机构消毒技术规范和疫源地消毒技术规范四个部分。
1.2适用范围本规范适用于在中华人民共和国境内生产、经营、使用和检验消毒产品的组织,医疗卫生机构以及传染病疫源地和其他一切需要消毒的场所。
1.3术语1.3.1 消毒 disinfection杀灭或清除传播媒介上病原微生物,使其达到无害化的处理。
1.3.2 灭菌 sterilization杀灭或清除传播媒介上一切微生物的处理。
1.3.3 化学指示物 chemical indicator利用某些化学物质对某一杀菌因子的敏感性,使其发生颜色或形态改变,以指示杀菌因子的强度(或浓度)和/或作用时间是否符合消毒或灭菌处理要求的制品。
1.3.4 生物指示物 biological indicator将适当载体染以一定量的特定微生物,用于指示消毒或灭菌效果的制品。
1.3.5 消毒剂 disinfectant用于杀灭传播媒介上的微生物使其达消毒或灭菌要求的制剂。
1.3.6 灭菌剂 sterilant可杀灭一切微生物(包括细菌芽孢)使其达到灭菌要求的制剂。
1.3.7 高效消毒剂high-efficacydisinfectant指可杀灭一切细菌繁殖体(包括分枝杆菌)、病毒、真菌及其孢子等,对细菌芽孢(致病性芽孢菌)也有一定杀灭作用,达到高水平消毒要求的制剂。
1.3.8 中效消毒剂intermediate-efficacy disinfectant指仅可杀灭分枝杆菌、真菌、病毒及细菌繁殖体等微生物,达到消毒要求的制剂。
1.3.9 低效消毒剂low-efficacy disinfectant指仅可杀灭细菌繁殖体和亲脂病毒,达到消毒要求的制剂。
1.3.10 有效氯 available chlorine有效氯是衡量含氯消毒剂氧化能力的标志,是指与含氯消毒剂氧化能力相当的氯量(非指消毒剂所含氯量),其含量用mg/L或%浓度表示。

消毒产品检验技术规范
1. 消毒产品检验方法:包括对产品成分、理化性质、杀菌效果等方面进行检测的具体方法和步骤。
2. 消毒产品化学成分分析:通过分析消毒产品的化学成分,确定产品是否符合相关要求。
3. 消毒产品理化性质检验:包括对消毒产品的外观、pH值、溶解性、稳定性等方面进行检测。
4. 消毒产品杀菌效果评价:通过实验室测试,评估消毒产品对不同细菌、的杀灭能力。
5. 消毒产品毒性评价:通过实验评估消毒产品对人体的毒性和刺激性,确保产品对人体无害。
6. 消毒产品贮存稳定性评价:评估产品在贮存期间的性能变化和稳定性。
7. 消毒产品标签标识检验:检验产品的标签上是否包含正确的使用说明、成分信息等,并确保标签和包装符合相关法规要求。
8. 消毒产品包装检验:检验产品包装的完整性、防伪性能等。
9. 消毒产品微生物检验:通过培养和检测微生物,评价产品的无菌性和抗菌效果。
10. 消毒产品残留物检验:检验产品使用后是否有残留物,确保产品不会对环境和使用者产生不良影响。
通过进行上述检验,可以确保消毒产品的质量和安全性符合相关标准和法规要求,保护公众的健康安全。
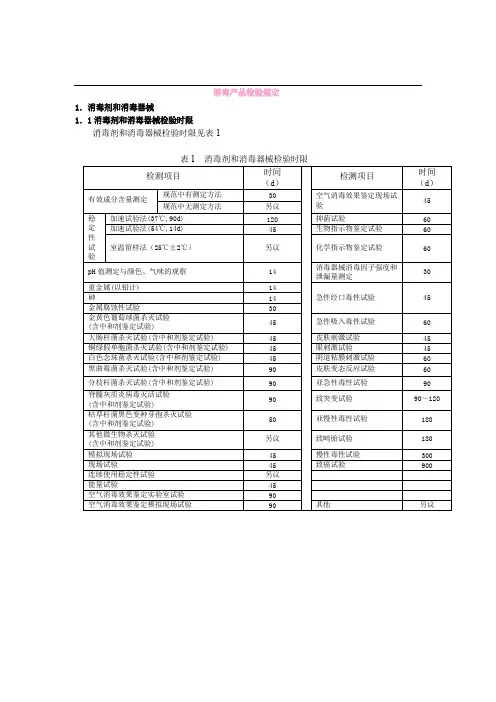
消毒产品检验规定1.消毒剂和消毒器械1.1消毒剂和消毒器械检验时限消毒剂和消毒器械检验时限见表1表1消毒剂和消毒器械检验时限1.2灭菌医用包装材料检验时限灭菌医用包装材料检验时限见表2表2灭菌医用包装材料检验时限1.3说明(1)表1、表2项目中所需时间只适用于单项检测。
(2)检验机构应有样品受理人与委托检验单位按照《规范》要求共同商定检验项目;检验时限为自受理样品之日起至出具检验报告之日,而且是指最长时限。
(3)检验机构受理样品时应出具检验受理通知单,并注明出具报告时间。
(4)表1、表2内所列检测时间在特殊情况下可另议,特殊情况是指中和剂筛选困难,实验动物来源不足,有效成分含量无标准测定方法,实验材料紧缺,特殊对象消毒等。
(5)根据产品性能所进行的理化、微生物与毒理试验检测时间应不超过5个月,单项检测时间较长者除外。
2消毒剂和消毒器械检验所需样品数量及规格2.1消毒剂检验所需样品数量及规格消毒剂检验所需样品数量及规格见表3表3消毒剂检验所需样品数量及规格注:1.特殊情况由检验机构与送检单位协商确定样品数量2.所有样品按此表数量,同时另提供同一批号复检和留存样各一套2.2消毒器械检验所需样品数量及规格(1)大型消毒器械1件,中、小型消毒器械3件。
(2)消毒指示物检验所需样品数量及规格见表4注:1.压力蒸汽灭菌生物指示物全套检测需3个包装(每个包装不少于100个)2.压力蒸汽灭菌化学指示卡全套检测需3个包装(每个包装不少于70个)3.压力蒸汽灭菌化学指示胶带全套检测需10卷4.压力蒸汽灭菌化学指示标签全套检测需3个包装(每个包装不少于50个)5.紫外线照射强度化学指示卡全套检测需3个包装(每个包装不少于70个)6.如包装中数量少于本表要求者,其总数不得少于总数规定。
2.3灭菌医用包装材料检验所需样品数量及规格灭菌医用包装材料检验所需样品数量及规格见表5表5灭菌医用包装材料检验所需样品数量及规格注:1.特殊情况由检验机构与送检单位协商确定样品数量2.所有样品按此表数量,同时另提供同一批号复检和留存样各一套3.消毒剂和消毒器械检验项目及要求3.1消毒剂检验项目及要求消毒剂检验项目及要求见表注“+”为必须做项目;“空格”为不做项目;“*”为模拟现场试验与现场试验任选其一。

消毒产品检验技术规范1. 引言消毒产品是维护公共卫生和预防疾病传播的重要手段之一。
为确保消毒产品的有效性和安全性,需要建立统一的检验技术规范。
本文档旨在规范消毒产品的检验方法和要求,以提高消毒产品的质量和可靠性。
2. 术语和定义•消毒产品:指能够杀灭病原微生物或抑制其繁殖的化学物质、材料或设备。
•检验:指对消毒产品进行实验室分析、观察和评估,以确定其是否符合特定要求或标准。
•检验方法:指用于测定、分析和评估消毒产品性能的技术和操作规程。
3. 检验项目消毒产品的检验项目应包括内容:3.1 杀菌效力消毒产品的杀菌效力是评估其消毒能力的重要指标。
检验应进行项目:•最小杀菌浓度:测定在特定条件下,能够有效杀灭细菌的最低浓度。
•杀菌速度:评估消毒产品对不同细菌的杀灭速度。
•残留效果:测定消毒产品残留在物表上的有效杀菌时间。
3.2 安全性评估消毒产品的安全性评估是保证其对人体和环境无害的重要要求。
检验应进行项目:•感觉刺激性:评估消毒产品对皮肤和眼睛的刺激程度。
•急性毒性:测定消毒产品对动物的急性毒性,以评估其对人体的潜在危害。
•慢性毒性:评估消毒产品长期使用对人体可能产生的慢性毒性风险。
3.3 物理性能消毒产品的物理性能对其使用效果和稳定性有重要影响。
检验应进行项目:•pH值:测定消毒产品的酸碱性。
•溶解性:评估消毒产品在不同温度和pH值条件下的溶解性。
•温度稳定性:测定消毒产品在不同温度条件下的稳定性,以评估其适用范围。
4. 检验方法消毒产品的检验方法应符合要求:•准确性:检验方法应具有高准确性,能够可靠地评估消毒产品的性能。
•重复性:检验方法应具有较好的重复性,不同实验室之间的结果应具有较高的一致性。
•灵敏度:检验方法应具有足够的灵敏度,能够满足不同消毒产品的检验需求。
•可操作性:检验方法应具有较好的可操作性,能够在实验室条件下进行。
5. 检验报告进行消毒产品检验后,应根据检验结果检验报告,报告中应包含内容:•检验项目和方法:说明所进行的检验项目和所采用的检验方法。



1.1 引言根据《中华人民共和国传染病防治法》、《中华人民共和国传染病防治法实施办法》和《消毒管理办法》制订本规范。
本规范含总则、消毒检验技术规范、医疗卫生机构消毒技术规范和疫源地消毒技术规范四个部分。
1.2 适用范围本规范适用于在中华人民共和国境内生产、经营、使用和检验消毒产品的组织,医疗卫生机构以及传染病疫源地和其他一切需要消毒的场所。
1.3 术语1.3.1 消毒disinfection杀灭或清除传播媒介上病原微生物,使其达到无害化的处理。
1.3.2 灭菌sterilization杀灭或清除传播媒介上一切微生物的处理。
1.3.3 化学指示物chemical indicator利用某些化学物质对某一杀菌因子的敏感性,使其发生颜色或形态改变,以指示杀菌因子的强度(或浓度)和/或作用时间是否符合消毒或灭菌处理要求的制品。
1.3.4 生物指示物biological indicator将适当载体染以一定量的特定微生物,用于指示消毒或灭菌效果的制品。
1.3.5 消毒剂disinfectant用于杀灭传播媒介上的微生物使其达消毒或灭菌要求的制剂。
1.3.6 灭菌剂sterilant可杀灭一切微生物(包括细菌芽孢)使其达到灭菌要求的制剂。
1.3.7 高效消毒剂high-efficacy disinfectant指可杀灭一切细菌繁殖体(包括分枝杆菌)、病毒、真菌及其孢子等,对细菌芽孢(致病性芽孢菌)也有一定杀灭作用,达到高水平消毒要求的制剂。
1.3.8 中效消毒剂intermediate-efficacy disinfectant指仅可杀灭分枝杆菌、真菌、病毒及细菌繁殖体等微生物,达到消毒要求的制剂。
1.3.9 低效消毒剂low-efficacy disinfectant指仅可杀灭细菌繁殖体和亲脂病毒,达到消毒要求的制剂。
1.3.10 有效氯available chlorine有效氯是衡量含氯消毒剂氧化能力的标志,是指与含氯消毒剂氧化能力相当的氯量(非指消毒剂所含氯量),其含量用mg/L 或%浓度表示。

消毒产品检验技术规范1. 引言消毒产品在维护公共卫生和预防疾病传播方面起着重要作用。
为确保消毒产品的质量和安全性,需要进行相关的检验工作。
本文档旨在制定消毒产品检验技术规范,以提供一套标准的检验方法和要求。
2. 检验项目2.1 细菌灭活率检验细菌灭活率是衡量消毒产品杀菌效果的重要指标之一。
常用的细菌灭活率检验方法包括菌落计数法和浸润法。
2.1.1 菌落计数法菌落计数法是通过菌落的形成和计数来评估消毒产品对细菌的杀灭能力。
应选择适当的细菌菌株,并按照相关标准进行培养和接种。
将预定量的细菌暴露于消毒产品中,经过一定时间后,采样并在培养基上培养菌落,计数并计算细菌灭活率。
2.1.2 浸润法浸润法是将消毒产品涂布或浸渍在细菌培养基上,然后观察细菌生长情况以评估其杀菌效果。
需要选择合适的细菌菌株和培养基,并按照规定的时间和温度进行培养。
观察细菌生长情况,包括菌落形成、颜色变化等,并计算细菌灭活率。
2.2 物理性能检验消毒产品的物理性能对其使用效果与安全性都有直接影响。
常见的物理性能检验项目包括外观检查、pH值测定、溶解性、蒸发残留物等。
2.2.1 外观检查外观检查是对消毒产品外观特征进行观察和评估。
应检查产品的颜色、透明度、杂质等,并记录外观评价结果。
2.2.2 pH值测定pH值是衡量溶液酸碱性的重要指标。
应使用合适的仪器和试剂对消毒产品的pH值进行检测,并记录测定结果。
2.2.3 溶解性溶解性是指消毒产品在特定溶剂中的溶解情况。
应选取适当的溶剂,将消毒产品加入并充分搅拌,观察其溶解情况,并记录结果。
2.2.4 蒸发残留物蒸发残留物是指消毒产品在蒸发后留下的残留物。
应将一定量的消毒产品加热至蒸发,然后测定残留物的质量,并计算蒸发残留物的百分比。
2.3 化学成分检验消毒产品中的化学成分是影响其杀菌效果和安全性的重要因素。
常见的化学成分检验项目包括活性成分含量、消毒副产物、重金属离子等。
2.3.1 活性成分含量活性成分含量是指消毒产品中主要杀菌成分的含量。

卫生质量检验指南:消毒产品1. 引言本指南旨在提供关于消毒产品的卫生质量检验方法和指导,以确保这些产品的有效性和安全性。
消毒产品用于杀灭或去除病原微生物,以防止疾病传播和维护公共卫生。
本指南将重点介绍消毒产品的质量标准和检验步骤。
2. 质量标准为了确保消毒产品的质量和效力,以下是一些常见的质量标准:- 成分含量:消毒产品应明确标注活性成分的含量,并符合相关法规要求。
- 杀灭率:消毒产品应具备足够的杀灭率,以确保对目标微生物的有效消灭。
- 安全性:消毒产品应符合国家和地区的安全标准,并不应对人体健康产生不良影响。
- 标签信息:消毒产品的标签应包含正确的使用说明、警示信息和储存条件,以确保用户正确使用产品。
3. 检验步骤以下是一些常见的消毒产品检验步骤:步骤一:成分含量检验使用合适的分析方法,检测消毒产品中活性成分的含量。
确保成分含量符合法规要求。
步骤二:杀灭率测试使用标准的微生物学方法,评估消毒产品对目标微生物的杀灭率。
确保消毒产品具备足够的杀灭能力。
步骤三:安全性评估进行安全性评估,包括对消毒产品的毒性和刺激性等方面的测试。
确保消毒产品对人体健康无不良影响。
步骤四:标签信息检查检查消毒产品的标签信息,确保标签中包含正确的使用说明、警示信息和储存条件。
4. 结论通过按照本指南提供的质量标准和检验步骤进行检验,可以确保消毒产品的质量和安全性。
这对于维护公共卫生、预防疾病传播至关重要。
建议相关机构和实验室按照本指南进行消毒产品的质量检验,并确保产品符合相关法规要求和标准。

消毒产品检查技术规范Technical Standard for Testing Disinfection Products 1 消毒产品消毒效果检查技术规范1.1 消毒剂杀微生物实验1.1.1 合用范畴重要合用于消毒剂鉴定和寻常检测,用来评价各种用途消毒剂对微生物杀灭效果。
按此办法进行实验,只是对消毒剂杀菌能力重要方面进行验证,侧重反映消毒剂实用剂量与杀菌能力。
不能反映消毒剂全面特性。
1.1.2 菌悬液与菌片制备1.1.3 活菌培养计数技术1.1.4 残留消毒剂去除办法1.1.5 中和剂鉴定实验1.1.6 物理法去除残留消毒剂实验1.1.7 细菌定量杀灭实验1.1.8 杀灭分枝杆菌实验1.1.9 真菌杀灭实验1.1.10 病毒灭活实验1.1.11 能量实验1.1.12 各种因素对消毒剂杀菌作用影响测定1.2 消毒剂模仿现场和现场消毒鉴定实验1.2.1 消毒剂对食(饮)具消毒效果模仿现场鉴定实验1.2.2 消毒剂对医疗器械消毒模仿现场实验1.2.3消毒剂对医疗器械模仿现场灭菌实验1.2.4 持续使用稳定性实验1.2.5消毒剂对手消毒模仿现场实验1.2.6消毒剂对手消毒现场实验1.2.7 消毒剂对皮肤消毒模仿现场实验1.2.8消毒剂对皮肤消毒现场实验1.2.9消毒剂对其她表面消毒模仿现场鉴定实验1.2.10消毒剂对其她表面消毒现场鉴定实验1.3 空气消毒效果鉴定实验1.3.1 目检测消毒器械或消毒剂对空气中细菌杀灭和清除作用,以验证其对空气消毒效果。
其她办法对空气消毒效果,亦可参照本实验关于原则进行。
1.3.2 实验设备和器材1.3.3 实验阶段1.3.4 实验室实验与模仿现场实验操作程序1.3.5 现场实验1.4 水消毒效果鉴定实验1.4.1生活饮用水消毒效果鉴定1.4.1.1 目检测生活饮用水消毒剂与消毒器械杀菌效果,以验证其对生活饮用水消毒能否达到卫生合格原则。
1.4.1.2 实验器材1.4.1.3 实验阶段1.4.1.4 实验菌污染水样配制1.4.1.5 实验菌污染水样中活菌培养计数1.4.1.6 实验室杀菌实验操作程序1.4.1.7 杀菌效果影响因素测定实验操作程序1.4.1.8 模仿现场实验和现场实验1.4.2 人工游泳池水消毒效果鉴定1.4.3 注意事项1.5 灭菌与消毒器械消毒功能鉴定实验1.5.1 干热灭菌柜1.5.1.1 目测定干热灭菌柜对细菌芽孢杀灭效果,以验证其灭菌性能与否符合设计规定。

消毒产品理化检验技术规范2。
2.1消毒产品原料或单方制剂的测定法2.2。
1.1 常用器材(1)移液管(1 ml、5ml、10 ml、25 ml);移液器(100μl,1000μl).(2)滴定管 (2 ml、5ml、10 ml、15 ml、25 ml、50 ml,酸式与碱式)。
(3) 毛细滴管。
(4)碘量瓶 (100ml、250 ml)。
(5) 容量瓶 (50ml、100 ml、250 ml、1000 ml).(6)锥形瓶(100ml、250 ml、500 ml)。
(7) 称量杯(瓶)。
(8) 吸球。
(9) 分液漏斗(250ml).(10)研钵。
(11) 量筒。
(12) 烧杯。
(13)垂熔玻璃滤器。
(14)酒精比重计.(15) 天平(感量 0。
1mg).(16)比色皿.(17)分光光度计.(18) 大气采样器.(19)注射器(1ml、5ml、100ml);微量注射器(10μl、25μl、100μl)。
(20) 气相色谱仪。
(21)高效液相色谱仪。
2。
2.1。
2 含量测定方法2。
2。
1。
2.1 有效氯含量的测定(1) 配制2 mol/L硫酸、100g/L 碘化钾与5g/L淀粉等溶液。
配制并标定 0。
1mol/L 硫代硫酸钠滴定液(见2。
2.。
1.3。
1).(2)精密吸取液体含氯消毒剂适量,使其相当于有效氯约0.6g,置100ml容量瓶中,加蒸馏水至刻度,混匀.对固体含氯消毒剂,精密称取适量使其相当于有效氯约0.6g,置烧杯中以蒸馏水溶解,转入100ml容量瓶中。
称量杯及烧杯需用蒸馏水洗3次,洗液全部转入容量瓶。
(3) 向 100ml 碘量瓶中加2 mol/L 硫酸 10ml,10 0g/L碘化钾溶液 10ml 和混匀的消毒剂稀释液10.0ml。
此时,溶液出现棕色。
盖上盖并振摇混匀后加蒸馏水数滴于碘量瓶盖缘,置暗处5min。
打开盖,让盖缘蒸馏水流入瓶内.用硫代硫酸钠滴定液(装于25 ml滴定管中) 滴定游离碘,边滴边摇匀。
消毒产品卫生安全评价技术要求1 范围本标准规定了消毒产品卫生安全评价的基本要求及内容。
本标准适用于中华人民共和国境内生产、经营和使用的除新消毒产品以外的第一类、第二类消毒产品(消毒剂、消毒器械、指示物、抗(抑)菌制剂)的卫生安全评价。
本标准不适用于定制消毒器械的卫生安全评价。
2 规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅所注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
生活饮用水消毒剂和消毒设备卫生安全评价规范(试行)(2005年版)卫生部(卫监督发〔2005〕336号)3 术语和定义下列术语和定义适用于本文件。
3.1消毒产品卫生安全评价 hygiene and safety evaluation of disinfectant product对消毒产品有效性和卫生安全性进行的综合评价,评价内容包括产品标签(铭牌)、说明书、检验报告、企业标准或质量标准、生产企业卫生许可证(境外允许生产销售的证明文件及报关单)、消毒剂、指示物和抗(抑)菌制剂的产品配方、消毒器械的结构图等。
3.2产品责任单位responsible entity依法承担因产品缺陷而致他人人身伤害或财产损失的赔偿责任的个人、法人及其他组织。
委托生产加工时,特指委托方,进口产品的责任单位为在华责任单位。
3.3第一类消毒产品classⅠdisinfectant product用于医疗器械的高水平消毒剂和消毒器械、灭菌剂和灭菌器械,皮肤/黏膜消毒剂,生物指示物、灭菌效果化学指示物。
3.4第二类消毒产品class Ⅱ disinfectant product除第一类产品外的消毒剂、消毒器械、化学指示物,以及带有灭菌标识的灭菌物品包装物、抗(抑)菌制剂。
3.5定制消毒器械customized disinfection instrument为单一项目设计制造,没有批量生产的非定型消毒器械。
消毒产品检验技术规范1. 引言随着疾病传播的风险增加,消毒产品的需求也越来越大。
消毒产品的效果直接关系到公众的健康和安全。
因此,为了确保消毒产品的质量和效果,制定一套科学的检验技术规范十分重要。
本文档旨在提供一套规范,以指导消毒产品的检验工作。
2.适用范围本技术规范适用于各类消毒产品的检验,包括但不限于: - 手部消毒剂 - 表面消毒剂 - 消毒液 - 消毒器械3. 检验项目3.1 化学成分•检验消毒产品的化学成分,确保符合相关法规和标准。
•检测主要成分的浓度,以确认其符合产品标签上声明的内容。
3.2 杀菌效果•使用标准菌株进行杀菌实验,评估消毒产品对不同病原菌的杀菌效果。
•根据实验结果评定消毒产品的杀菌力。
3.3 pH 值•测定消毒产品的 pH 值,以确认其符合规定的范围。
•pH 值可以影响杀菌效果,因此该项指标十分重要。
3.4 残留物•检验样品中的残留物质,例如有机化合物、重金属等。
•确保样品中残留物的含量不超过国家规定的限量。
3.5 毒性评估•对消毒产品进行毒性评估,以确认其对人体的安全性。
•毒性评估包括急性毒性和慢性毒性的测试。
4. 检验方法4.1 样品准备•按照标准要求,选取合适的样品进行测试。
•样品应保证没有污染和变质。
4.2 实验操作•针对不同的检验项目,采用相应的实验方法和操作流程。
•实验操作应严格按照标准要求进行,确保数据的准确性和可靠性。
4.3 仪器设备•使用适当的检验仪器设备进行检验。
•仪器设备应符合国家标准,并经过校准和检测。
4.4 数据处理•对实验获得的数据进行分析和处理。
•利用统计学方法,评估样品的性能和符合度。
5. 结果评定5.1 等级划分•根据检验结果,将样品的质量等级进行划分。
•制定相应的等级准则,以评定样品的质量。
5.2 报告编制•对检验结果进行详细报告的编制。
•报告应包括实验操作、数据处理和结果评定等内容。
6. 术语和定义•提供一份术语和定义的列表,以解释使用到的专业术语。
2.1消毒产品消毒效果检验技术规范2.1.1 消毒剂杀微生物试验2.1.1.1 适用范围主要适用于消毒剂鉴定和日常监测,用来评价各种用途的消毒剂对微生物的杀灭效果。
按此方法进行的试验,只是对消毒剂的杀菌能力的重要方面进行验证,侧重反映消毒剂的实用剂量与杀菌能力。
不能反映消毒剂的全面特性。
2.1.1.2 菌悬液与菌片的制备2.1.1.2.1 适用范围制备消毒剂杀菌试验用细菌悬液与菌片,以供消毒剂杀菌试验时使用。
2.1.1.2.2 试验器材(1)菌种:金黄色葡萄球菌ATCC 6538、铜绿假单胞菌ATCC 15442、大肠杆菌8099、枯草杆菌黑色变种ATCC 9372、龟分枝杆菌脓肿亚种ATCC 93326、白色葡萄球菌8032、白色念珠菌ATCC10231、黑曲霉菌ATCC16404。
在上述规定的菌株基础上,根据消毒剂特定用途或试验特殊需要,还可增选其他菌株。
(2)有机干扰物:见附录A。
(3)磷酸盐缓冲液:见附录A。
(4)无菌蒸馏水。
(5)稀释液:见附录A。
(6)细菌培养基:胰蛋白胨大豆琼脂培养基(TSA),胰蛋白胨大豆肉汤培养基(TSB)等,见附录A。
(7)革兰染色液:见附录A。
(8)芽孢染色液:见附录A。
(9)恒温水浴箱。
(10)玻璃漏斗。
(11)刻度吸管(1.0ml、5.0ml、10.0ml),毛细吸管。
(12)数字可调移液器(10μl,20μl,100μl,200μl,1000μl)及配套用一次性塑料吸头。
(13)离心机。
(14)电动混合器(15)浊度计。
2.1.1.2.3 细菌悬液制备程序(1)细菌繁殖体悬液的制备1)取冻干菌种管,在无菌操作下打开,以毛细吸管加入适量营养肉汤,轻柔吹吸数次,使菌种融化分散。
取含 5.0 ml~10.0ml 营养肉汤培养基试管,滴入少许菌种悬液,置37℃培养18h~24h。
用接种环取第1代培养的菌悬液,划线接种于营养琼脂培养基平板上,于37℃培养18h~24h。
消毒产品检验规定1.消毒剂和消毒器械1.1消毒剂和消毒器械检验时限消毒剂和消毒器械检验时限见表1表1 消毒剂和消毒器械检验时限1.2 灭菌医用包装材料检验时限灭菌医用包装材料检验时限见表21.3 说明(1)表1、表2项目中所需时间只适用于单项检测。
(2)检验机构应有样品受理人与委托检验单位按照《规范》要求共同商定检验项目;检验时限为自受理样品之日起至出具检验报告之日,而且是指最长时限。
(3)检验机构受理样品时应出具检验受理通知单,并注明出具报告时间。
(4)表1、表2内所列检测时间在特殊情况下可另议,特殊情况是指中和剂筛选困难,实验动物来源不足,有效成分含量无标准测定方法,实验材料紧缺,特殊对象消毒等。
(5)根据产品性能所进行的理化、微生物与毒理试验检测时间应不超过5个月,单项检测时间较长者除外。
2 消毒剂和消毒器械检验所需样品数量及规格2.1消毒剂检验所需样品数量及规格消毒剂检验所需样品数量及规格见表3注: 1.特殊情况由检验机构与送检单位协商确定样品数量2.所有样品按此表数量,同时另提供同一批号复检和留存样各一套2.2 消毒器械检验所需样品数量及规格(1)大型消毒器械1件,中、小型消毒器械3件。
(2)消毒指示物检验所需样品数量及规格见表4注: 1. 压力蒸汽灭菌生物指示物全套检测需3个包装(每个包装不少于100个)2. 压力蒸汽灭菌化学指示卡全套检测需3个包装(每个包装不少于70个)3. 压力蒸汽灭菌化学指示胶带全套检测需10卷4. 压力蒸汽灭菌化学指示标签全套检测需3个包装(每个包装不少于50个)5. 紫外线照射强度化学指示卡全套检测需3个包装(每个包装不少于70个)6. 如包装中数量少于本表要求者,其总数不得少于总数规定。
2.3 灭菌医用包装材料检验所需样品数量及规格灭菌医用包装材料检验所需样品数量及规格见表52.所有样品按此表数量,同时另提供同一批号复检和留存样各一套3.消毒剂和消毒器械检验项目及要求3.1 消毒剂检验项目及要求消毒剂检验项目及要求见表注“+”为必须做项目;“空格”为不做项目;“*”为模拟现场试验与现场试验任选其一。
消毒产品检验规定1.消毒剂和消毒器械1.1消毒剂和消毒器械检验时限消毒剂和消毒器械检验时限见表1表1 消毒剂和消毒器械检验时限1.2 灭菌医用包装材料检验时限灭菌医用包装材料检验时限见表2说明1表1、表2项目中所需时间只适用于单项检测.2检验机构应有样品受理人与委托检验单位按照规范要求共同商定检验项目;检验时限为自受理样品之日起至出具检验报告之日,而且是指最长时限.3检验机构受理样品时应出具检验受理通知单,并注明出具报告时间.4表1、表2内所列检测时间在特殊情况下可另议,特殊情况是指中和剂筛选困难,实验动物来源不足,有效成分含量无标准测定方法,实验材料紧缺,特殊对象消毒等.5根据产品性能所进行的理化、微生物与毒理试验检测时间应不超过5个月,单项检测时间较长者除外.2 消毒剂和消毒器械检验所需样品数量及规格2.1消毒剂检验所需样品数量及规格消毒剂检验所需样品数量及规格见表3表 3 消毒剂检验所注: 1.特殊情况由检验机构与送检单位协商确定样品数量2.所有样品按此表数量,同时另提供同一批号复检和留存样各一套2.2 消毒器械检验所需样品数量及规格1大型消毒器械1件,中、小型消毒器械3件.2消毒指示物检验所需样品数量及规格见表4注: 1. 压力蒸汽灭菌生物指示物全套检测需3个包装每个包装不少于100个2. 压力蒸汽灭菌化学指示卡全套检测需3个包装每个包装不少于70个3. 压力蒸汽灭菌化学指示胶带全套检测需10卷4. 压力蒸汽灭菌化学指示标签全套检测需3个包装每个包装不少于50个5. 紫外线照射强度化学指示卡全套检测需3个包装每个包装不少于70个6. 如包装中数量少于本表要求者,其总数不得少于总数规定.2.3 灭菌医用包装材料检验所需样品数量及规格灭菌医用包装材料检验所需样品数量及规格见表5表5 灭菌医用包装材料检验所需样品数量及规格注:1.特殊情况由检验机构与送检单位协商确定样品数量 2.所有样品按此表数量,同时另提供同一批号复检和留存样各一套3.消毒剂和消毒器械检验项目及要求3.1 消毒剂检验项目及要求消毒剂检验项目及要求见表注“+”为必须做项目;“空格”为不做项目;“”为模拟现场试验与现场试验任选其一.“±”为选做项目,具体选项按下列原则确定:①说明书中未注明不得用于金属物品消毒的消毒剂,必须进行该项试验;②说明书中注明对真菌具有杀灭作用消毒剂,必须进行该项试验;③根据特定的消毒对象、使用说明书内容和其他资料确定相应的检测项目;④使用说明书中表明对消毒对象上的某一特定微生物具有杀灭作用的消毒剂,必须进行该微生物的杀灭试验.⑤消毒剂使用过程中接触皮肤的,做该项试验;⑥皮肤、手、足消毒接触创面的,做该项试验;⑦用于皮肤、手、足的消毒剂,依其成分有致敏倾向,做该项试验;⑧根据前一阶段毒理试验结果判定,如亚急性毒性试验不通过的,需做亚慢性毒性试验.消毒器械检验项目及要求消毒器械检验项目及要求,见表7.表7 消毒器械检验项目及要求注:“+”为必须做项目;“空格”为不做项目;“”为模拟现场试验与现场试验任选其一.模拟现场试验所用指示微生物应选择所涉及使用范围按规范要求的指示微生物中抗力较强者.产生化学因子的消毒器械其毒理试验的检验项目参照表6进行.“±”为选做项目,具体选项按下列原则确定:①环氧乙烷灭菌消毒柜、等离子体、低温甲醛灭菌柜等可不测定,其他消毒器械均应进行该项试验.②需要添加化学物质生成消毒因子的消毒器械应进行该项试验.③说明书中未注明不得用于金属物品消毒的产生化学因子的消毒器械,必须进行该项试验.④根据特定的消毒对象、使用说明书内容和其他资料确定相应的检测项目.⑤使用说明书中表明对消毒对象上的某一特定微生物具有杀灭作用的消毒器械,必须进行该微生物的杀灭试验此外,紫外线灯按一般物体表面消毒要求进行选项,但不做模拟现场或现场试验.3.3 指示物检验项目及要求1压力蒸汽灭菌生物指示物1生物指示物含菌量测定2存活时间和杀灭时间的测定3D值的测定4稳定性试验2压力蒸汽灭菌化学指示物1测定饱和蒸汽条件下的指示物颜色变化情况2测定饱和蒸汽条件下的嗜热脂肪杆菌芽孢存活情况3稳定性试验3紫外线灯辐射强度指示卡1紫外线强度比较测试2稳定性试验4消毒剂浓度试纸1消毒剂浓度比较测试2稳定性试验5 消毒剂浓度试纸全套检测须10个最小包装3.4 灭菌医用包装材料检验项目及要求灭菌医用包装材料检验项目及要求见表8表8 灭菌医疗用品包装材料检验项目注:“+”为必须做项目;“空格”为不做项目;“±”为根据包装材料特性、使用说明书内容和其它有关资料而确定的项目.4. 卫生用品和一次性使用医疗用品检验规定卫生用品和一次性使用医疗用品检验时限、检验所需样品数量及规格卫生用品检验时限、检验所需样品数量及规格见表9表 9 卫生用品检验时限、检验所需样品数量及规格说明:1.本表项目所需时间只适用于单项检测.卫生用品微生物污染检测和杀抑菌效果检测以及毒理学试验的检验时限为90d,毒理学试验需做致突变试验时,总检验时限为150d.2.特殊情况由检验机构与送检单位协商确定样品数量和检验时限,但检验机构应在受理样品之前告知送检单位.一次性使用医疗用品检验时限、检验所需样品数量及规格见表10表10 一次性使用医疗用品检验时限、检验所需样品数量及规格说明:1.本表项目所需时间只适用于单项检测,全项目检测所需时间为45d.2.检测项目所需样品数均按此表数量并另外提供复检和留样各一套.3.特殊情况由检验机构与送检单位协商确定样品数量和检验时限,但检验机构应在受理样品之前告知送检单位.4.现场试验和稳定性试验仅限于对有杀菌、消毒作用医疗用品的检测.卫生用品和一次性使用医疗用品检验项目及要求1 卫生用品检验项目及要求见表11表11 卫生用品备案的检验项目一注:“+”为必须做项目;空格为不做项目;“+”按以下原则选择项目:①采用环氧乙烷消毒的,进行该项试验;②使用说明中标明对某一特定微生物有杀灭作用的,进行该项试验;③国家或行业标准中对该类产品有特殊规定的,应进行该项卫生学指标检测.表11 卫生品备案的检验项目二–隐形眼镜护理用品注:“+”为必须做项目;空格为不做项目;“+”按以下原则选择项目:①多次量使用的产品进行该项试验;②含过氧化氢的产品进行该项试验;③使用说明中标明对某一特定微生物有杀灭作用的,进行该项试验;④国家或行业标准中对该类产品有特殊规定的,进行该项卫生学指标检测表11 卫生用品备案的检验项目三–皮肤粘膜清洁卫生用品注:“+”为必须做项目;空格为不做项目;“+”按以下原则选择项目:①使用说明中标明对真菌有作用或用于外阴部的产品进行该项试验;②使用说明中标明对某一特定微生物有杀灭作用的,应进行该项试验;③国家或行业标准中对该类产品有特殊规定的,进行该项卫生学指标检测.表11 卫生用品备案的检验项目四 - 其他一次性使用卫生用品注:“+”为必须做项目;空格为不做项目;“+”按以下原则选择项目:①采用环氧乙烷消毒的产品进行该试验;②使用说明中标明对真菌有作用或用于外阴部的产品进行该项试验;③使用说明中标明对某一特定微生物有杀灭作用的,应进行该项试验;④国家或行业标准中对该类产品有特殊规定的,进行该项卫生学指标检测.表11 卫生用品备案的毒理学检验项目五注:“+”为必须做项目;空格为不做项目;“+”按以下原则选择项目:①根据产品用途选择项目;②根据产品的原材料情况选择项目.产品原料、材质、生产工艺相同,不同规格、品牌的产品,只需选择其中一种产品进行检测.2 一次性使用医疗用品检验项目及要求见表12表12 一次性使用医疗用品检验项目及要求注:“+”为必须做项目;空格为不做项目;“+”按以下原则选择项目:①使用的消毒药剂必须取得卫生部消毒剂卫生许可批件;②采用环氧乙烷消毒、灭菌的,进行该项目检测;③国家或行业标准中对该类产品有特殊规定的,进行该项卫生学指标检测.。
消毒产品检验技术规范
Technical Standard for Testing Disinfection Products 1 消毒产品消毒效果检验技术规范
1.1 消毒剂杀微生物试验
1.1.1 适用范围
主要适用于消毒剂鉴定和日常检测, 用来评价各种用途的消毒剂对微生物的杀灭效果。
按此方法进行的试验, 只是对消毒剂的杀菌能力的重要方面进行验证, 侧重反映消毒剂的实用剂量与杀菌能力。
不能反映消毒剂的全面特性。
1.1.2 菌悬液与菌片的制备
1.1.3 活菌培养计数技术
1.1.4 残留消毒剂的去除方法
1.1.5 中和剂鉴定试验
1.1.6 物理法去除残留消毒剂试验
1.1.7 细菌定量杀灭试验
1.1.8 杀灭分枝杆菌试验
1.1.9 真菌杀灭试验
1.1.10 病毒灭活试验
1.1.11 能量试验
1.1.12 各种因素对消毒剂杀菌作用影响的测定
1.2 消毒剂模拟现场和现场消毒鉴定试验
1.2.1 消毒剂对食( 饮) 具消毒效果的模拟现场鉴定试验
1.2.2 消毒剂对医疗器械的消毒模拟现场试验
1.2.3消毒剂对医疗器械的模拟现场灭菌试验
1.2.4 连续使用稳定性试验
1.2.5消毒剂对手消毒的模拟现场试验
1.2.6消毒剂对手消毒现场试验
1.2.7 消毒剂对皮肤消毒的模拟现场试验
1.2.8消毒剂对皮肤消毒现场试验
1.2.9消毒剂对其它表面消毒模拟现场鉴定试验
1.2.10消毒剂对其它表面消毒现场鉴定试验
1.3 空气消毒效果鉴定试验
1.3.1 目的
检测消毒器械或消毒剂对空气中细菌的杀灭和清除作用, 以验证其对空气的消毒效果。
其它方法对空气的消毒效果, 亦可参照本试验的有关原则进行。
1.3.2 试验设备和器材
1.3.3 试验阶段
1.3.4 实验室试验与模拟现场试验操作程序
1.3.5 现场试验
1.4 水的消毒效果鉴定试验
1.4.1生活饮用水消毒效果鉴定
1.4.1.1 目的
检测生活饮用水消毒剂与消毒器械的杀菌效果, 以验证其对生活饮用水消毒能否达到卫生合格标准。
1.4.1.2 试验器材
1.4.1.3 试验阶段
1.4.1.4 试验菌污染水样的配制
1.4.1.5 试验菌污染水样中活菌的培养计数
1.4.1.6 实验室杀菌试验操作程序
1.4.1.7 杀菌效果影响因素测定试验操作程序
1.4.1.8 模拟现场试验和现场试验
1.4.2 人工游泳池水消毒效果鉴定
1.4.3 注意事项
1.5 灭菌与消毒器械消毒功效鉴定试验
1.5.1 干热灭菌柜
1.5.1.1 目的
测定干热灭菌柜对细菌芽孢的杀灭效果, 以验证其灭菌性能是否符合设计规定。
1.5.1.2 试验器材
1.5.1.3 柜内温度测定
1.5.1.4 灭菌试验
1.5.1.5 评价规定
1.5.1.6 注意事项
1.5.2 红外线消毒碗柜
1.5.
2.1 目的
检测红外线消毒碗柜对餐饮具的消毒效果, 以验证其杀灭微生物性能是否符合实际规定。
1.5.
2.2 试验器材
1.5.
2.3 柜内温度测定
1.5.
2.4 大肠杆菌杀灭试验
1.5.
2.5 脊髓灰质炎病毒灭活试验
1.5.
2.6 评价规定
1.5.
2.7 注意事项
1.5.3 微波灭菌柜
1.5.3.1 目的
测定微波灭菌柜对微生物的杀灭效果, 以验证其消毒活灭菌性能是否符合原设计规定。
1.5.3.2 试验器材
1.5.3.3 细菌及其芽孢和真菌杀灭试验操作程序
1.5.3.4 评价规定
1.5.3.5 注意事项
1.5.4 紫外线灯
1.5.4.1 目的
测定紫外线灯( 包括双灯管组合灯具) 辐照强度及对微生物的杀灭作用, 以验证其杀菌性能是否达到合格标准。
1.5.4.2 试验器材
1.5.4.3 辐照强度测定
1.5.4.4 细菌及其芽孢和真菌杀灭效果的测定
1.5.4.5 评价规定
1.5.4.6 臭氧产生量的测定
1.5.4.7 有效使用期的测定
1.5.4.8 注意事项
1.5.5 紫外线消毒箱
1.5.5.1 目的
测定紫外线消毒箱对物体表面微生物的杀灭效果, 以验证其杀菌性能是否符合原设计规定。
1.5.5.2 试验器材
1.5.5.3 紫外线照射强度测定
1.5.5.4 对微生物杀灭效果的测定
1.5.5.5 注意事项
1.5.6 环氧乙烷灭菌器
1.5.6.1 目的
测定环氧乙烷灭菌器对细菌芽孢的杀灭能力, 以验证其杀菌性能是否符合原设计规定。
1.5.6.2 试验器材
1.5.6.3 灭菌试验操作程序
1.5.6.4 评价规定
1.5.6.5 注意事项
1.5.7 臭氧消毒柜
1.5.7.1 目的
测定臭氧消毒柜对物体表面微生物的杀灭效果, 以验证其杀菌性能是否符合原设计规定。
1.5.7.2试验器材
1.5.7.3 臭氧浓度测定
1.5.7.4 杀灭微生物试验操作程序
1.5.7.5 评价规定
1.5.7.6 注意事项
1.5.8 臭氧水消毒器
1.5.8.1 目的
检测臭氧水消毒器发生的臭氧水消毒剂对物品表面的消毒效果, 以验证臭氧水消毒剂对物品表面消毒的实用剂量。
臭氧水消毒剂指应用臭氧消毒设备制备的含臭氧的水溶液, 并以其作为消毒剂, 用于对物品表面灯的消毒。
1.5.8.2 试验器材
1.5.8.3 臭氧浓度测定
1.5.8.4 杀灭微生物试验操作程序
1.5.8.5 脊髓灰质炎病毒灭火试验
1.5.8.6 评价规定
1.5.8.7 注意事项
1.6 灭菌与消毒指示器材鉴定试验
1.6.1 压力蒸汽灭菌生物指示物鉴定试验
1.6.1.1 目的
测定压力蒸汽灭菌生物指示物所含菌量, 以及在121℃±0.5℃ 饱和蒸汽作用下的存活时间、杀灭时间于D值是否达到要求指标。
1.6.1.2 实验器材
1.6.1.3 生物指示物微生物含量与抗力标准
1.6.1.4 生物指示物含菌量的测定
1.6.1.5 存活时间和杀灭时间的测定
1.6.1.6 D值的测定
1.6.1.7 稳定性试验
1.6.1.8 注意事项
1.6.2 压力蒸汽灭菌化学指示卡鉴定试验
1.6.
2.1 目的
测定下排气式、预真空式和脉动真空式压力蒸汽灭菌化学指示卡产品在饱和蒸汽作用下所产生的颜色变化, 与拟代表的温度、杀菌作用时间的吻合情况, 以作为判断该指示卡是否合格的依据。
对其它相似类型化学指示物的鉴定, 可参照本试验的有关原则进行。