限时集训(一) 物质的分类、转化与分散系
- 格式:doc
- 大小:121.00 KB
- 文档页数:5


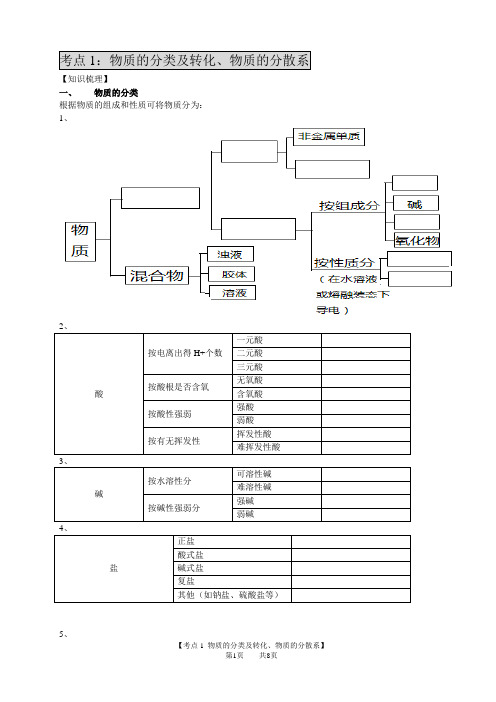
考点1:物质的分类及转化、物质的分散系【知识梳理】一、物质的分类根据物质的组成和性质可将物质分为:1、酸按电离出得H+个数一元酸二元酸三元酸按酸根是否含氧无氧酸含氧酸按酸性强弱强酸弱酸按有无挥发性挥发性酸难挥发性酸碱按水溶性分可溶性碱难溶性碱按碱性强弱分强碱弱碱盐正盐酸式盐碱式盐复盐其他(如钠盐、硫酸盐等)5、胶体的性质:①丁达尔现象②电泳③聚沉④常见的胶体⑤胶体的制备(物理分散法、化学凝聚法)如:用氯化铁溶液制取氢氧化铁胶体【例题】1、下列说法正确的是A、凡在溶液中能电离出H+的化合物都是酸B、与水反应生成酸的氧化物,不一定是酸性氧化物C、金属氧化物均为碱性氧化物D、不能与酸反应的氧化物一定能与碱反应2.下列说法正确的是()A.含氧元素的化合物就一定是氧化物B.由不同种元素组成的纯净物就是化合物C.溶于水后得到的溶液能导电的物质是电解质D.只含有一种元素的物质不可能是混合物3.关于胶体和溶液的区别,下列叙述中正确的()A.溶液呈电中性,胶体带电荷B.溶液中通过一束光线出现明显光路,胶体中通过一束光线没有特殊现象C.溶液中溶质粒子能通过滤纸,胶体中分散质粒子不能通过滤纸D.溶液与胶体的本质区别在于分散质微粒直径大小,前者小于1nm,后者介于1nm~100nm之间4、在西部大开发中,投入巨资兴建了“西气东输”工程,将西部蕴藏的丰富的资源通过管道送到东部地区。
这里所指的“西气”的主要成分是()A、CH4B、COC、H2D、NH35、“垃圾是放错了位置的资源”,应该分类回收。
生活中废弃的铁锅、铝质易拉罐、铜导线等可以归为一类加以回收,他们属于()A、有机物B、金属或合金C、氧化物D、盐【高考链接】1、某合作学习小组讨论辨析一下说法:①粗盐和酸雨都是混合物;②沼气和水煤气都是可再生能源;③冰和干冰既是纯净物又是化合物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和熟石灰都是碱。

目夺市安危阳光实验学校物质的分类与转化物质的分散系1.(2018·浙江4月学考真题)下列属于酸的是( )A.HNO3B.CaCO3C.CO2D.NaOH【解析】选A。
酸是指电离出的阳离子全部是H+的化合物,B属于盐,C属于氧化物,D属于碱。
2.(2018·浙江4月学考真题)下列属于物理变化的是( )A.煤的气化B.天然气的燃烧C.烃的裂解D.石油的分馏【解析】选D。
煤的气化是指将煤转化为可燃性气体的过程,为化学变化;天然气燃烧生成水和CO2,发生的是化学变化;烃的裂解是将大分子烃裂化为小分子烃的过程,为化学变化;石油的分馏属于物理变化。
3.古“丝绸之路”我国商人运出的货物有:①丝绸、②茶叶、③白糖、④瓷器、⑤纸张、⑥植物油、⑦明矾、⑧金银铜器等。
下列说法正确的是( )A.④、⑦、⑧都属于盐类B.①、③、⑤、⑥都属于高分子化合物C.①、②、⑤、⑥都属于蛋白质D.①、②、③、⑤、⑥的主要成分都属于有机物【解析】选D。
阳离子是金属离子或铵根离子、阴离子是酸根离子的化合物为盐,而④瓷器、⑧金银铜器均是混合物,不是盐,A错误;相对分子质量在一万以上的是高分子化合物,③白糖是蔗糖、⑥植物油是高级脂肪酸的甘油酯,均不是高分子化合物,B错误;②茶叶、⑤纸张、⑥植物油均不是蛋白质,C错误;含碳的化合物为有机物,①丝绸、②茶叶、③白糖、⑤纸张、⑥植物油均是有机物,D 正确。
4.下列有关叙述正确的是 ( )A.直径在1~100 nm的粒子称为胶体B.用过滤的方法可以将胶体和溶液分离C.利用丁达尔效应可以区别溶液和胶体D.胶体区别于其他分散系的本质特征是丁达尔效应【解析】选C。
胶体是一类分散质直径在1~100 nm的分散系,A项错误;胶体和溶液都能通过滤纸,无法将二者分离,B项错误;丁达尔效应是区别溶液和胶体的简单、便捷的方法,C项正确;胶体区别于其他分散系的本质特征是分散质粒子直径的大小,胶体分散质微粒直径在1~100 nm,D项错误。

专题一 第一单元 物质的分类与转化 物质的分散系班级: 姓名:【考试说明要求】1.了解物质的组成、结构和性质的关系。
了解化学反应的本质、基本原理以及能量变化等规律。
2.理解混合物和纯净物、单质和化合物、金属和非金属的概念。
3.了解胶体是一种常见的分散系。
【学习内容】【例题】判断下列分类标准是否合理1.根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸等;2.根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应;3.根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液;4.酸性氧化物一定是非金属氧化物,碱性氧化物一定是金属氧化物,酸酐一定是酸性氧化物;5.有同种元素组成的物质一定是纯净物,可以是单质、离子化合物、共价化合物;〖知识点一〗物质的分类依据与方法〖例题1〗物质分类的依据通常有组成和性质等,下列物质分类中,只考虑组成的是 ( )A .Na 2SO 4是钠盐、硫酸盐、正盐B .HNO 3是一元酸、强酸、挥发性酸C .Mg(OH)2是二元碱、难溶性碱、中强碱D .Al 2O 3是两性氧化物、金属氧化物、最高价氧化物 练1.下列每组物质都有一种物质与其他物质在分类上不同,试分析每组中物质的组成规律,请将这种不同于其他物质的物质找出来,并说出你挑选的依据。
(1)NaCl 、KCl 、NaClO 、BaCl 2 (2)HClO 3、KClO 3、Cl 2、NaClO 3(3)H 3PO 4、H 4SiO 4、HCl 、H 2SO 4 (4)空气、N 2、HCl 、CuSO 4.5H 2O(5)铜、金、汞、钠 (6)HClO 3、KClO 3、Cl 2、NaClO 3拓展:化学反应的分类方法与本质化学反应的分类关键也是选择分类的角度的依据,可以从反应物和生成物种类来分,也可以从是否有电子转移,是否有离子参加或生成,热量变化等多个角度进行分类。
练2.下列5个化学反应可以从几个角度进行分类?分类依据是什么?怎么分? ①H 2+CuO △==Cu+H 2O ②Zn+2H +=Zn 2++H 2↑ ③Ba 2++SO 42-=BaSO 4 ④2Na+Cl 2点燃====2NaCl ⑤CaCO 3+2H +=Ca 2++CO 2↑+H 2O〖知识点二〗物质的转化〖例题2〗(2010福建卷)下列各组物质中,满足下图物质一步转化关系的选项是( )根据化合物在水溶液或熔化状态下能否导电,可将其划分为电解质、非电解质。

02 物质的分类与转化及分散系【学习目标】1.掌握化学物质的分类方法,学会从不同角度对化学物质进行分类。
2.知道物质间相互转化的基本规律,初步认识氧化还原反应。
3.知道胶体是一种常见的分散系,了解胶体的重要性质和应用。
4.知道电解质和非电解质,初步学会电离方程式【学习重、难点】胶体的性质;电解质与非电解质【学习方法】讨论法、探究法、归纳法【教学过程】一、物质的分类1、从物质组成和性质特点分类书第3页图1-2 物质的分类2、从物质的导电性分:将物质分成___________、_________和____________。
如___________、_____________等是绝缘体;_________、_______________等是导体。
3、从物质的状态分:将物质分成__________物质、_________物质和____________物质。
4、从物质在水中的溶解性分:将物质分成________物质、________物质和_______物质。
5、从酸是否含氧分:将酸分成______酸(如________)和________酸(如_________)。
6、从碱在水中的溶解性分:将碱分成________性碱(如____________)和________性碱或_________性氢氧化物(如______________)7、从氧化物与酸或碱反应分:与酸反应生成盐和水的氧化物称为__________氧化物(如____________);与碱反应生成盐和水的氧化物称为__________氧化物(如____________)。
二、物质的转化1、四种基本类型反应:根据转化过程中物质组合方式特点,化学反应的四种基本类型:____________反应、______________反应、______________反应、_______________反应练习:写出下列反应的化学方程式,并标出化学反应类型(1)氯化钡溶液与稀硫酸的反应(2)氢气在氧气中燃烧的反应(3)高温下,碳与氧化铜的反应(4)碳酸钠与足量稀盐酸的反应(5)高温下,一氧化碳与氧化铁的反应(6)煅烧石灰石的反应结论:四种基本类型反应_______包含所有反应;我们所学的知识是在不断发展的。
[对接高考——高考命题常设误区汇总]分散系的分类标准错误[随堂强化落实]1.(2010·海口模拟)分类是学习和研究化学的一种常用的科学方法。
下列分类正确的是( )①根据一个酸分子电离产生氢离子的个数将酸分为一元酸、二元酸等②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应 ③根据电解质在熔融状态下能否完全电离将电解质分为强电解质和弱电解质 ④根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素 ⑤根据反应的热效应将化学反应分为放热反应和吸热反应 A .①②③ B .①②⑤ C .①②④D .③④⑤解析:③区别强弱电解质的依据是在水溶液中是否完全电离,④区别金属元素和非金属元素的主要依据是元素的物理性质、化学性质。
答案:B2.(2011·苏州高三模拟)下列实验装置或操作与微粒的大小无直接关系的是( )解析:胶体粒子直径大于1 nm ,小于100 nm ,胶体粒子能透过滤纸,但不能透过半透膜;溶液中的粒子直径小于1 nm ,可透过半透膜和滤纸,而浊液的分散质粒子直径大于100 nm,不能透过滤纸和半透膜;丁达尔效应是胶体粒子对光线的散射作用形成的,而溶液中的小分子或粒子对光线的散射作用非常微弱,故无此现象;萃取是利用了物质在不同溶剂中溶解性的不同,与分散质粒子大小无关。
答案:C3.美国宇航局将在2012年再次登陆火星,新火星车体积更大、功能更全,旨在探寻火星土壤中是否存在有机物。
已有资料表明:火星表面富含硅酸盐和硫酸盐;火星上的水以冰块和霜冻的形式存在于南北两极。
下列叙述不.正确的是()A.硅酸盐、硫酸盐都是含氧酸盐B.水玻璃是混合物,冰水混合物是纯净物C.Al2O3·2SiO2·2H2O属于氧化物D.硅酸钠、硫酸钡、水分别属于强电解质、强电解质、弱电解质解析:硅酸盐通常用二氧化硅和金属氧化物的组合形式表示其组成,Al2O3·2SiO2·2H2O属于硅酸盐。
课题:物质的分类及转化1考纲:掌握根据物质的组成对物质分类的方法,理解常见的不同类型物质的相互联系和转化关系。
预习检测:1.盐酸、硫酸和硝酸中 是混合物, 是纯净物。
2.硫酸是 元 挥发性的 溶性的无机含氧酸且是强酸。
氢氧化铁是 元 溶性的弱碱。
碳酸氢钠是 式盐。
3.现有下列物质:①碳酸钠②氧化钠③二氧化硅④铁⑤氧气⑥氢氧化钙⑦硫酸请将上述物质按下列要求分类,并将其序号填入空白处⑪按组成分类,属于单质的是 属于氧化物的是 属于酸的是 属于碱的是 属于盐的是⑫按溶解性分类,属于易溶物的是 属于难溶物的是 属于微溶物的是 ⑬按常温状态分类,属于固态的是 属于液态的是 属于气态的是4.①CaCO 3CaO+CO 2↑、②2KMnO 4=====△ K 2MnO 4+MnO 2+O 2↑③CaO+CO 2=CaCO 3、④Fe+S=====△FeS 、⑤Fe 2O 3+3CO2Fe+3CO 2、 ⑥Zn+H 2SO 4=ZnSO 4+H 2↑、 ⑦Ca(OH)2+2NH 4Cl=====△CaCl 2+2NH 3↑+2H 2O以上反应中 属于分解反应; 属于化合反应; 属于置换反应; 属于复分解反应; 属于氧化还原反应 知识梳理:知识点一:物质的分类1.根据物质的组成和性质特点对物质分类:思考:MgO 、Na 2O 是碱性氧化物,用化学方程式表示理由:、CO 2、SO 2是酸性氧化物,用化学方程式表示理由:、Al2O3是两性氧化物,用化学方程式表示理由:、注意:酸性氧化物不一定是非金属氧化物,如Mn2O7;碱性氧化物一定是金属氧化物。
非金属氧化物不一定是酸性氧化物,如CO、NO是不成盐氧化物;金属氧化物不一定是碱性氧化物,如Mn2O7、Al2O3。
2.根据状态、导电性和溶解性对物质分类(略)见课本P3知识点二:物质的转化反应前后物质类别和种类电子是否转移分为:氧化还原反应和非氧化还原反应热效应分为:吸热反应和放热反应反应程度分为:可逆反应和不可逆反应2.四种基本反应类型与氧化还原反应之间的关系思考:金属置换非金属的反应非金属置换金属的反应非金属置换非金属的反应典型例题:知识点一:物质的分类例1:下列物质按照纯净物、混合物、电解质和非电解质顺序排列的是 ( ) A、胆矾、漂白粉、氯化钾、四氯化碳 B、冰醋酸、福尔马林、硫酸钠、乙醇C、单甘油酯、混甘油酯、苛性钾、石灰石 D、盐酸、水煤气、醋酸、干冰知识点二:物质的转化例3.下列说法正确的是()A.有单质参加或有单质生成的化学反应一定是氧化还原反应B.生成物只有一种的化学反应一定是化合反应C.生成阳离子的反应一定是氧化反应D.酸与酸之间、碱与碱之间、盐与盐之间有可能反应例4现有四种物质:NaHCO3溶液、NaOH溶液、盐酸、铁粉。
限时集训(一)物质的分类、转化与分散系(限时:60分钟满分:100分)一、选择题(本题包括10小题,每小题5分,共50分)1.(2013·衡阳六校联考)胶体区别于溶液和浊液的本质是()A.有丁达尔效应B.分散质粒子的直径大小C.可以通过滤纸D.分散质粒子因吸附而带电荷2.(2012·山东高考)下列与化学概念有关的说法正确的是()A.化合反应均为氧化还原反应B.金属氧化物均为碱性氧化物C.催化剂能改变可逆反应达到平衡的时间D.石油是混合物,其分馏产品汽油为纯净物3.下列有关物质分类或归类正确的一组是()①液氨、液氯、干冰、碘化银均为化合物②氢氟酸、盐酸、水玻璃、氨水均为混合物③明矾、小苏打、醋酸、次氯酸均为电解质④碘酒、牛奶、豆浆、漂粉精均为胶体⑤Na2O2、Na2CO3、NaHCO3、Na2SiO3均为钠盐A.①和②B.②和③C.③和④D.②③⑤4.某化学学习小组讨论辨析:①漂白粉和酸雨都是混合物②煤和石油都是可再生能源③不锈钢和目前流通的硬币都是合金④硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物⑤蛋白质溶液、淀粉溶液和雾都是胶体。
上述说法正确的是() A.①③⑤B.①②④C.②③④D.③④⑤5.(2012·中山模拟)分类是化学学习和研究的常用手段。
下列分类依据和结论都正确的是()A.H2O、HCOOH、(NH4)2Fe(SO4)2中均含有氧元素,都是氧化物B.HCl、H2SO4、HNO3均具有氧化性,都是氧化性酸C.赤铁矿、磁铁矿、黄铁矿、孔雀石都是常见的铁矿石D.Na2CO3、Ba(OH)2、NH4Cl、Na2O2都属于离子化合物6.Fe(OH)3胶体和MgCl2溶液共同具备的性质是()A.两者均有丁达尔效应B.两者均能透过半透膜C.加入盐酸先沉淀,随后溶解D.分散质粒子可通过滤纸7.(2013·泉州模拟)生产生活中的许多现象或应用都与化学知识有关。
下列现象或应用与胶体性质无关的是()A.将盐卤或石膏加入豆浆中,制成豆腐B.一支钢笔使用两种不同型号的蓝黑墨水,易出现堵塞C.泡沫灭火器中将Al2(SO4)3与NaHCO3两溶液混合后,喷出大量泡沫,起到灭火作用D.清晨,人们经常能看到阳光穿过茂密的树木枝叶所产生的美丽景象8.下列说法不.正确的是()A.化学变化不产生新元素,产生新元素的变化不是化学变化B.根据分散质粒子直径大小可以将分散系分为溶液、浊液和胶体C.向25 mL沸水中逐滴加入2 mL FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热,可以制得Fe(OH)3胶体D.某粒子的电子数等于质子数,则该粒子可能是一种分子或一种离子9.食盐、蔗糖、醋酸、纯碱、汽油、明矾等是日常生活中经常使用的物质,下列有关说法或表示正确的是()A.食盐溶于水形成的分散系,能发生丁达尔效应B.蔗糖和醋酸都是弱电解质C.纯碱是碱D.明矾经水解可得到氢氧化铝胶体,1 L 0.2 mol·L-1的氢氧化铝胶体中含有氢氧化铝胶粒数小于0.2 N A10.奥运会会标是五环旗,假定奥运五环旗中的每一环或每种颜色表示一种物质,相连的环(物质)间在一定条件下能发生常见反应,不相连的环(物质)间不能发生反应,且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组物质是()11.(12分)下列每组物质都有一种物质与其他物质在分类上不同,试分析每组中物质的组成规律,将这种不同于其他物质的物质找出来。
(1)NaCl、KCl、NaClO、BaCl2________。
(2)HClO3、KClO3、Cl2、NaClO3________。
(3)H3PO4、H4SiO4、HCl、H2SO4________。
(4)浊液、溶液、胶体、水________。
(5)空气、N2、HCl、CuSO4·5H2O________。
(6)铜、金、汞、钠________。
12.(12分)“探险队员”——盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或者是水溶液),盐酸必须避开它们,否则就无法通过。
(1)请你帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线):_______。
(2)在能“吃掉”盐酸的化学反应中,属于酸与碱中和反应的有________个,属于氧化还原反应的有________个,其中能“吃掉”盐酸的盐是________,写出该反应的离子方程式:________________________________________________________________________。
(3)在不能与盐酸反应的物质中,属于电解质的是______(填写物质序号),属于非电解质的是__________。
(4)如果将盐酸换成氯气,它能沿着盐酸走出的路线“走出”这个迷宫吗?为什么?________________________________________________________________________。
13.(13分)在宏观—微观—符号之间建立联系,是化学学科特有的思维方式。
汽车尾气是造成大气污染的主要原因之一,在汽车排气管上安装“催化转换器”便可以使汽车的尾气转换成无毒气体。
如用●表示碳原子,用○表示氧原子,用表示氮原子,下图为气体转换的微观过程。
请你根据图示回答下列问题:(1)A、B、C三种物质可以归为一类的依据是__________________________________。
(2)将C归为化合物,将D归为单质的理由是_____________________________________________________________________________________________________________。
(3)用化学反应方程式表示为______________________________________________________________________________________________________________________。
化学变化过程中消耗的A物质和生成的C物质的质量比为________。
(4)从微观的角度去描述你获得的关于化学变化的有关信息(答出一条即可)___________________________________________________________________________________。
14.(13分)取少量Fe2O3粉末(红棕色)加入适量盐酸,反应的离子方程式为_________,反应后得到棕黄色的FeCl3溶液。
用此溶液做以下实验:(1)取少量溶液置于试管中,滴入NaOH溶液,看到有红褐色沉淀生成,反应的离子方程式为________________________________________________________________________ ________________________________________________________________________。
(2)在小烧杯中加入25 mL蒸馏水,加热至沸腾后,向沸水中加入2 mL FeCl3饱和溶液,继续煮沸至溶液呈______色,即可制得Fe(OH)3胶体。
(3)另取一小烧杯也加入25 mL蒸馏水后,向烧杯中也加入2 mL FeCl3饱和溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置暗处,分别用激光笔照射烧杯中的液体,可以看到______烧杯中会产生丁达尔效应,此实验可以区别________。
(4)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量的稀盐酸,边滴边振荡,可以看到的现象是____________,此变化过程涉及的离子方程式为___________________ ________________________________________________________________________。
(5)已知明矾能净水,理由是__________________________________________________。
答案1.B 2.C 3.B 4.A 5.D 6.D7.C8.D9.D10.选B A中无置换反应;B合适;C中无化合反应且不相连的物质:Cl2、NaOH溶液可以反应;D中不相连的物质:Mg和稀盐酸可以反应,不符合题意要求。
11.(1)NaClO(2)Cl2(3)HCl(或H4SiO4)(4)水(5)空气(6)钠(或汞)12.解析:(1)图中物质③⑥⑩⑦⑪⑫均不与盐酸反应,沿该路线可走出迷宫。
(2)盐酸与NaOH、Ca(OH)2的反应属于酸碱中和反应,与Zn的反应属于氧化还原反应,能“吃掉”盐酸的盐是Na2CO3,该反应的离子方程式为CO2-3+2H+===CO2↑+H2O。
(3)在不能与盐酸反应的物质中,属于电解质的是H2SO4、NaCl,属于非电解质的是CO2、SO2。
(4)如果将盐酸换成氯气,它沿着盐酸走出的路线不能“走出”这个迷宫,因为氯气或氯水与二氧化硫,铜都会发生氧化还原反应。
答案:(1)③→⑥→⑩→⑦→⑪→⑫(2)2 1 Na 2CO 3 CO 2-3+2H +===CO 2↑+H 2O (3)⑥⑪ ③⑩(4)不能,因为氯气或氯水有强氧化性,遇到二氧化硫、铜时都会发生氧化还原反应从而被“吃掉”13.(1)都含有氧元素(2)二氧化碳是由不同种原子构成的分子,而氮气是由同种原子构成的分子(3)2CO +2NO =====催化剂△N 2+2CO 2 15∶22(4)化学变化中原子的种类、数目、质量没有发生改变(其他合理答案也可)14.解析:Fe 2O 3作为一种典型的碱性氧化物,可溶于稀盐酸,化学方程式为Fe 2O 3+6HCl===2FeCl 3+3H 2O 。
(1)FeCl 3溶液与NaOH 溶液发生如下反应:FeCl 3+3NaOH===Fe(OH)3↓+3NaCl 。
(2)Fe(OH)3胶体呈红褐色。
(3)甲为FeCl 3溶液,乙为Fe(OH)3胶体,二者可用丁达尔效应区别,即用激光笔照射两液体,可在Fe(OH)3胶体中看到一条光亮的通路。
(4)向Fe(OH)3胶体中加入稀盐酸,首先可看到有Fe(OH)3沉淀生成,此时发生了胶体的聚沉,再加稀盐酸,可看到Fe(OH)3逐渐溶解,生成棕黄色溶液,离子方程式为Fe(OH)3+3H +===Fe 3++3H 2O 。
(5)明矾净水,是因Al 3+水解生成Al(OH)3胶体,能吸附水中的悬浮物,使之沉淀,从而达到净水的目的。