物化实验报告:饱和蒸汽压的测定
- 格式:doc
- 大小:118.50 KB
- 文档页数:5

饱和蒸气压的测量实验报告(范文)第一篇:饱和蒸气压的测量实验报告(范文)饱和蒸气压的测量09111601班1120162086 原野一、实验目的。
测量水在不同温度下的饱和蒸气压,并求出所测温度范围内的水的平均摩尔气化焓。
二、实验原理。
饱和蒸气压:在真空容器中,液体与其蒸气建立动态平衡时(蒸气分子向液面凝结和液体分子从表面逃逸的速率相等)液面上的蒸气压力为饱和蒸气压。
温度升高,分子运动加剧,单位时间内从液面逸出的分子数增多,所以蒸气压增大。
饱和蒸气压与温度的关系服从克劳休斯克拉贝农方程。
液体蒸发时要吸收热量,温度T下,1mol液体蒸发所吸收的热量为该物质的摩尔气化焓。
沸点:蒸气压等于外压的温度。
显然液体沸点随外压而变,101.325kPa下液体的沸点称正常沸点。
对包括气相的纯物质两相平衡系统,因Vm(g)≫Vm(l),故△Vm≈Vm(g)。
若气体视理想气体,则克劳休斯-克拉贝农方程式为:d[ln(p/Pa)]/dT=ΔvapH*m/RT^2。
因温度范围小时,ΔvapH*m可以近似作为常数,将上式积分得:ln(p/Pa)=ΔvapH*m/RT+C。
作图,得一直线,斜率为ΔvapH*m/R由斜率可求算液体的ΔvapH*m。
本实验采用升温差压法测量。
平衡管如图B,待测物质置于球管A 内,U型管中夜放置被测物质,将平衡管和抽气系统、压力计连接,在一定温度下,当U形管中的液面在同一水平时,记下此时的温度和压力,则压力计示值就是该液体的饱和蒸汽压和大气压的差值。
三、实验步骤:1、从气压计读取大气压,并记录。
2、装样:从加样口加无水乙醇,并在U型管内装入一定体积的无水乙醇。
打开数字压力计电源开关,预热5 min。
使饱和蒸汽压测定教学试验仪通大气,按下“清零”键。
3、检查系统是否漏气。
将进气阀、阀2打开,阀1关闭。
抽气减压至压力计显示压差为-80KPa时关闭进气阀和阀2,如压力计示数能在3-5min内维持不变,则系统不漏气。

饱和蒸汽压的测定的实验报告实验名称:饱和蒸汽压的测定实验目的:测量不同温度下的饱和蒸汽压,探究其变化规律,了解水的蒸发过程。
实验原理:饱和蒸汽压是指液体蒸发到一定程度时,与外界保持动态平衡时的蒸汽压强度。
在一定温度下,液体与蒸汽之间的这种平衡成为饱和状态,此时液体内部还有未蒸发的分子,但是已经达到了与空气中水分子蒸发相等的蒸汽压强度。
饱和温度的升高会使液体内部更多分子脱离表面蒸发,从而使蒸汽压增大。
实验器材:烧杯、温度计、热水浴、挂钩、弹簧秤、水。
实验步骤:1、将烧杯中加满水后用挂钩扣到弹簧秤上,测量其质量并记录下来。
2、在热水浴中加热烧杯,记下开始加热时的温度,并持续加热直到水沸腾,此时温度保持不变,可用温度计测量并记录下来。
3、记下水沸腾时的弹簧秤读数,用其减去起始重量,即得水的蒸发量。
4、重复实验步骤1-3并记录不同温度下水的蒸发量和弹簧秤读数。
5、利用实验得到的数据,根据公式P = PP/P计算出不同温度下的饱和蒸汽压。
实验数据记录:温度/℃质量/g 弹簧秤读数/N 蒸发量/g 饱和蒸汽压/Pa20 100.2 0.22 0 030 100.2 0.26 0.7 105440 100.2 0.30 1.3 194650 100.2 0.33 2.1 313860 100.2 0.38 3.1 4641实验结果分析:根据实验结果,可得到以下结论:1、随着温度的升高,饱和蒸汽压不断增大,增长速度逐渐加快。
2、在30-60℃范围内,每10℃饱和蒸汽压的增长约为1000 Pa。
3、实验数据与理论曲线存在小差距,可归因于实际操作中可能存在的误差差异。
实验结论:本实验通过测量不同温度下水的蒸发量和弹簧秤读数,计算出了不同温度下水的饱和蒸汽压。
实验结果表明,随着温度的升高,饱和蒸汽压呈现增长趋势,增长速度逐渐加快。
同时,实验数据还与理论曲线存在差距,可对实际误差进行进一步研究。

纯液体饱和蒸汽压的测定实验报告数据实验报告:纯液体饱和蒸汽压的测定一、实验目的与原理本次实验的主要目的是研究纯液体饱和蒸汽压的测定方法,通过实验数据的收集与分析,掌握液体饱和蒸汽压的计算方法,为后续相关研究提供理论依据。
实验原理:液体在一定温度下,当其表面存在足够多的蒸汽分子时,这些蒸汽分子产生的压力达到与大气压力相等的程度,此时液体就达到了饱和状态。
饱和蒸汽压是指在这种状态下,单位时间内逸出的蒸汽分子数与单位时间内返回到液面的蒸汽分子数相等时所形成的压力。
纯液体饱和蒸汽压的测定方法主要有皮尔逊法、亨利定律法和自拟方法等。
二、实验设备与材料1. 设备:实验室恒温水浴、气压计、U形管、滴定管、酒精灯等。
2. 材料:甲醇、乙醇、苯、汽油等有机溶剂,以及去离子水。
三、实验步骤与数据处理1. 皮尔逊法测定纯液体饱和蒸汽压(1)取一定量的有机溶剂,加入去离子水中,使其充分溶解。
(2)将U形管水平放置,一端浸入溶液中,另一端用酒精灯加热至90°C左右。
(3)关闭进气阀,打开排气阀,使U形管内的气体与外界大气相通,待气体稳定后,记录此时的压力值P1。
(4)继续加热U形管,使液体沸腾,记录此时的压力值P2。
(5)重复以上步骤3-4次,取平均值作为实验数据。
2. 亨利定律法测定纯液体饱和蒸汽压(1)取一定量的有机溶剂,加入去离子水中,使其充分溶解。
(2)将U形管水平放置,一端浸入溶液中,另一端用酒精灯加热至90°C左右。
(3)在另一容器中加入一定量的去离子水,并放入气压计测量初始压力值P0。
(4)关闭进气阀,打开排气阀,使U形管内的气体与外界大气相通,待气体稳定后,记录此时的压力值P1。
(5)继续加热U形管,使液体沸腾,记录此时的压力值P2。
(6)根据亨利定律公式:P2 = (P1 + P0) * R * T / (V L),其中R为气体常数,T为温度差,V为U形管内液体的体积,L为U形管内液体的升力。

实验四液体饱和蒸汽压的测定姓名:曹峻华学号:2010011970 班级:材03 同组实验者:李琦实验日期:2011.9.30 提交报告日期:2011.10.13 实验老师:陈双龙1引言1.1 实验目的1.运用克劳修斯-克拉贝龙方程,求出所测温度范围内的平均摩尔气化焓及正常沸点。
2.掌握测定饱和蒸汽压的方法。
1.2 实验原理在通常温度下(距离临界温度较远时),纯液体与其蒸气达平衡时的蒸气压称为该温度下液体的饱和蒸气压,简称为蒸气压。
蒸发1摩尔液体所吸收的热量称为该温度下液体的摩尔气化热。
液体的蒸气压与液体的本性及温度等因素有关。
液体的蒸气压与液体的本性及温度等因素有关。
随温度不同而变化,随温度不同而变化,随温度不同而变化,温度升高时,温度升高时,蒸气压增大;温度降低时,蒸气压降低,这主要与分子的动能有关。
当蒸气压等于外界压力时,液体便沸腾,此时的温度称为沸点,外压不同时,液体沸点将相应改变,当外压为p ø(101.325kPa )时,液体的沸点称为该液体的正常沸点。
液体的饱和蒸气压与温度的关系用克劳修斯(Clausius )-克拉贝龙(Clapeyron )方程式表示:式中,R 为摩尔气体常数;T 为热力学温度;Δvap H m 为在温度T 时纯液体的摩尔气化热。
假定Δvap H m 与温度无关,或因温度变化范围较小,Δvap H m 可以近似作为常数,积分上式,得:A ln p BT=-+或A ln p BT=-+vap m H RmD =-式中:B ——积分常数。
从上式可知:若将ln p 对1/T 作图应得一直线,斜率m=vap m -A H /R =-D 由此可得vap m H RmD =-同时从图上可求出标准压力时的正常沸点2实验操作2.1实验药品、仪器型号及测试装置示意图仪器:等压管1支,稳压瓶1个,负压瓶1个,恒温槽1套,真空泵1台,压力计1台,数显温度仪。
度仪。
药品:乙醇(分析纯):乙醇(分析纯) 装置图:2.2 实验条件:温度:23℃ 湿度:32% 大气压:102.09KPa 2.3 实验操作步骤及方法要点1. 装置与装样装置与装样按图一安装好整套装置,并把乙醇装入等压管中,使液面在等压管的三分之二处。

饱和蒸汽压的测定实验报告饱和蒸汽压的测定实验报告引言:饱和蒸汽压是指在一定温度下,液体与其蒸气相平衡时的压力。
测定饱和蒸汽压对于理解物质的相变过程以及研究气体的溶解度等具有重要意义。
本实验旨在通过实验方法测定饱和蒸汽压,并探究其与温度的关系。
实验原理:根据饱和蒸汽压与温度的关系,我们可以利用实验测得的温度值来计算饱和蒸汽压。
实验中,我们将使用饱和蒸汽压计进行测量。
饱和蒸汽压计是一种基于液体与其蒸气相平衡的原理,通过测量蒸气压力来间接测定饱和蒸汽压的仪器。
实验步骤:1. 准备工作:将饱和蒸汽压计放置在恒温水槽中,并调节水槽温度至所需实验温度。
2. 测量温度:使用温度计测量水槽中的温度,并记录下来。
3. 测量压力:打开饱和蒸汽压计的阀门,使其与实验系统连接。
等待一段时间,直到压力稳定后,读取饱和蒸汽压计上的压力值。
4. 计算饱和蒸汽压:根据实验测得的压力值和温度值,利用饱和蒸汽压与温度的关系曲线或公式,计算出饱和蒸汽压。
实验数据处理:根据实验测得的温度和压力数据,我们可以绘制饱和蒸汽压与温度的关系曲线。
通过曲线的斜率可以得到饱和蒸汽压与温度的定量关系。
同时,我们可以计算出实验测得的饱和蒸汽压与理论值之间的误差,并进行分析。
实验结果与讨论:通过实验测得的数据,我们绘制了饱和蒸汽压与温度的关系曲线。
从曲线上可以看出,饱和蒸汽压随着温度的升高而增加,符合饱和蒸汽压与温度的正相关关系。
同时,我们计算出了实验测得的饱和蒸汽压与理论值之间的误差,发现误差较小,说明实验结果较为准确。
实验结论:通过本实验,我们成功测定了饱和蒸汽压,并探究了饱和蒸汽压与温度的关系。
实验结果表明,饱和蒸汽压与温度呈正相关关系。
实验的数据处理和分析结果也验证了实验的可靠性和准确性。
实验中的不确定性:在实验过程中,由于仪器的精度限制以及实验操作的误差,可能会导致实验结果的不确定性。
为了减小不确定性,我们可以增加测量次数,提高仪器的精度,以及严格控制实验条件等。
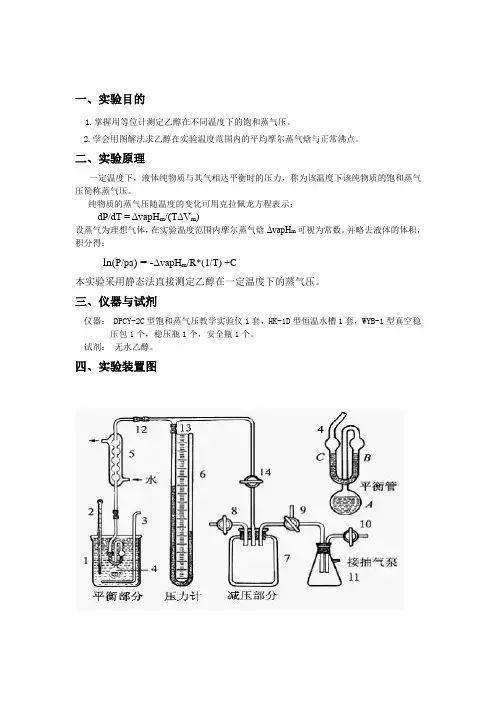
一、实验目的1.掌握用等位计测定乙醇在不同温度下的饱和蒸气压。
2.学会用图解法求乙醇在实验温度范围内的平均摩尔蒸气焓与正常沸点。
二、实验原理一定温度下,液体纯物质与其气相达平衡时的压力,称为该温度下该纯物质的饱和蒸气压简称蒸气压。
纯物质的蒸气压随温度的变化可用克拉佩龙方程表示:dP/dT = ΔvapH m/(TΔV m)设蒸气为理想气体,在实验温度范围内摩尔蒸气焓ΔvapH m可视为常数。
并略去液体的体积,积分得:ln(P/pa) = -ΔvapH m/R*(1/T) +C本实验采用静态法直接测定乙醇在一定温度下的蒸气压。
三、仪器与试剂仪器: DPCY-2C型饱和蒸气压教学实验仪1套,HK-1D型恒温水槽1套,WYB-1型真空稳压包1个,稳压瓶1个,安全瓶1个。
试剂:无水乙醇。
四、实验装置图五、实验步骤1.读取室温及大气压。
2.装样。
将等位计内装入适量待测液体乙醇,A球管约2/3体积,U形管两边各1/2体积,然后按图装好各部分。
3.教学实验仪置零。
打开教学实验仪装置,预热5分钟,选择开关打到KPa,按下面板上的置零键,显示值为00.00数值(大气压视为0看待)。
4.系统气密性检查除了真空泵前的安全瓶活塞通大气外,其余活塞都关上,接通真空泵电源关闭与真空连接的安全瓶活塞,开始抽真空。
抽气减压至压力显示-40~-53KPa时,关闭三通活塞,使系统与真空泵,大气都不相通,观察压力示数。
5.排除球管上方空间内的空气。
打开HK-1D型恒温电源,设定温度为25℃,接通冷凝水,同时调节搅拌器匀速搅拌,其目的是使等位计内外温度平衡,用WYB-1型真空稳压包控制抽气速度,抽气减压气泡逸出的速度以一个一个地逸出为宜至液体轻微沸腾,此时AB弯管内的空气不断随蒸气径C管逸出,如此沸腾3-5min可认为空气被排出、除干净(压力显示约-94KPa)。
抽气结束后,先关闭真空稳压包上与稳压瓶相连的阀门,再关闭另一侧门,打开与真空泵连接的安全瓶活塞,使其通大气,最后关电源。

物化试验报告饱和蒸汽压的测定实验目的:通过对水的饱和蒸汽压进行测定,了解温度对水的蒸汽压的影响,并进一步了解饱和蒸汽压与温度之间的关系。
实验原理:根据热力学第二定律,当液体与其蒸气在相平衡时,液体的饱和蒸汽压与温度有确定关系。
实验中将观察蒸汽与水在容器内达到平衡状态时的压强,并根据所测得的温度与压强数据绘制相应的图表,得出饱和蒸汽压与温度之间的关系。
实验仪器和药品:1.温度计:精确到0.1°C;2.水:作为实验物质;3.压力表:用于测定压力。
实验步骤:1.先将压力表校零。
2.将水加热至沸腾状态,待水温稳定后,读取温度并记录。
3.将压力表连接到容器内,等待一段时间,压力表读数稳定后记录读数。
4.将加热器温度适当提高,重复步骤3,进行多组实验,以得到不同温度下的压力读数。
5.根据实验数据绘制饱和蒸汽压与温度之间的图像。
实验数据记录:温度(℃),压力(kPa)-----,-------10,1.0220,2.3330,4.2440,7.4550,12.4360,19.7270,30.8280,47.5390,73.34100,101.32实验结果和讨论:根据实验数据,可以绘制出饱和蒸汽压与温度之间的图像。
可以明显观察到,随着温度的升高,饱和蒸汽压也随之增加。
这符合热力学第二定律的预期,也验证了饱和蒸汽压与温度之间的正相关关系。
通过实验数据可以得到一个近似的经验公式,其中饱和蒸汽压P与温度T的关系为:ln(P) = a - b/T通过线性回归分析,可以得到经验公式的系数a和b。
经过计算,得到的系数为a=11.54,b=3051.93、将系数代入公式中,可以得到一个近似的经验公式:ln(P) = 11.54 - 3051.93/T通过该公式,可以根据温度推算饱和蒸汽压。
同时,我们也可以通过已知的饱和蒸汽压值,反推出相应的温度。
实验结论:通过实验测定得到的数据和经验公式,验证了饱和蒸汽压与温度之间的正相关关系。

姓名: 班级: 学号: 实验日期:课程名称: 物理化学实验实验题目: 液体饱和蒸汽压的测定一、实验目的①了解用静态法测定异丙醇在不同温度下蒸气压的原理。
②学会用图解法求解其所在测温度范围内的平均摩尔蒸发热。
③了解真空泵、恒温槽及气压计的构造并掌握其使用方法。
二、实验原理一定温度下, 在一真空的密闭容器中, 液体很快与其蒸气建立动态平衡, 即蒸汽分子向液面凝结和液体分子从表面上逃逸的速度相等, 此时液面上的蒸汽压力就是液体在此温度是的饱和蒸汽压液体与其蒸气达到平衡时蒸气的压力, 称为这种液体在该温度时的饱和蒸气压。
饱和蒸汽压与温度的关系可用克劳修斯—克拉贝龙方程式来表示。
2ln RT H dTpd m vap ∆=式中ΔvapHm 是该液体的摩尔蒸发热, 在温度变化范围不大时, 它可以作为常数。
积分上式得:1.C 为积分常数。
如果以为纵坐标, 1/T 为横坐标作图可得一直线, 此直线的斜率即为 ,, 直接测量液体的饱和蒸气压。
测量方法是调节外压与液体蒸汽压相等, 此法一般用于蒸汽压比较大的液体。
动态法是在不同外界压力下, 测定液体的沸点。
本实验采用静态法测定乙醇的饱和蒸汽压与温度的关系, 实验装置见图 3.1.通常一套真空体系装置由四部分构成:一是机械泵、缓冲储气罐部分, 用以生产真空;二是正空的测量部分, 包括DP-A 精密数字压力计;三是蒸馏瓶部分;四是温度测量部分, 包括SWQ 智能数字恒温控制器、SYP 玻璃恒温水浴。
三、仪器与试剂1.仪器DP-A 型精密数字压力计一台;SWQ 型智能数字恒温控制器一台;缓冲储气罐一台;SYP 型玻璃恒温水浴一台;U 型等压计一个、球形冷凝管一支。
实验装置如图3.1所示。
2.试剂无水乙醇。
四、实验步骤(一)缓冲储气罐的气密性检查及使用方法1.缓冲储气罐的气密性检查2.缓冲储气罐的使用方法(二)精密数字压力计的气密性检查及使用方法1.预压及气密性的检查2.采零3.测试4.关机(三)实验仪器的链接(四)静态法测乙醇的饱和蒸汽压1.装样2.检漏3.测定五、注意事项1.先开启冷却水, 然后才能抽气。

实验四纯液体饱和蒸气压的测定一、目的要求1.明确液体饱和蒸气压的概念,了解纯液体饱和蒸气压与温度的关系——克劳修斯-克拉佩龙方程式。
2.掌握用平衡管法测定不同温度下乙醇饱和蒸气压的方法,并利用图解法求其平均摩尔蒸发焓和正常沸点。
二、基本原理在一定温度下,气液平衡时的蒸气压叫做饱和蒸气压,简称蒸气压。
纯液体的饱和蒸气压只是温度的函数,温度升高,其饱和蒸气压会增大。
当饱和蒸气压等于外压时,该液体开始沸腾。
本实验测定一系列不同温度下乙醇的饱和蒸气压。
在某一温度下,1摩尔液体转化为蒸汽的焓变为该液体在该温度下的摩尔蒸发焓Δv H m ,Δv H m 随温度而变化。
蒸气压随温度的变化率服从克拉佩龙方程:v m m,g m,L d d ()H p T T V V ∆=- (3-1) 式中:Δv H m 为摩尔蒸发焓,V m,g 为气体的摩尔体积,V m,L 为液体的摩尔体积。
和气体的体积相比较,液体的体积可以忽略,若再把气体看作理想气体,则(3-1)式可变换为:()v m2d ln Pa d p H T RT ∆= (3-2)上式称为克劳修斯-克拉佩龙方程式。
若在不大的温度间隔内,摩尔蒸发焓可以近似地看作常数,则上式积分可得:v m 212111ln()H p p R T T ∆=-- (3-3) 或()v mln Pa H p B RT∆=-+ (3-4) ()ln Pa Ap B T=-+ (3-5)式中R 为摩尔气体常数,B 为积分常数,A =Δv H m /R ,由(3-5)式可知,()ln Pa p 与1/T 是直线关系,直线的斜率为-A 。
若能得到直线的斜率,则由A =Δv H m /R 可求出平均摩尔蒸发焓Δv H m 。
本实验采用静态法测定乙醇的饱和蒸气压,即在不同温度下直接测量乙醇的蒸气压或在不同外压下测定乙醇的沸点。
具体的实验方法为平衡管法,装置如图1所示。
平衡管A 球内装待测液体,当A 球的液面上纯粹是待测液体的蒸气,且B 管与C 管的液面处于同一水平面时,则表示C 管液面上的蒸气压(即A 球液面上的蒸气压)与加在B 管液面上的外压相等。

饱和蒸汽压的测定实验报告实验报告:饱和蒸汽压的测定一、实验目的1.学习和掌握饱和蒸汽压的基本概念和原理。
2.掌握饱和蒸汽压的测定方法和实验操作流程。
3.了解并分析实验过程中可能出现的误差及其消除方法。
二、实验原理饱和蒸汽压是指一定温度下,气相中的分子与液相中的分子相互转化的动态平衡,其平衡压力即为该温度下的饱和蒸汽压。
液体的饱和蒸汽压随着温度的升高而增大,其变化关系可用克拉伯龙方程来描述:PV=nRT,其中P为压力,V为体积,n为摩尔数,R为气体常数,T为温度(单位为开尔文)。
三、实验步骤1.准备实验器材:饱和蒸汽压测定仪、温度计、压力计、水、烘箱等。
2.将饱和蒸汽压测定仪放置在烘箱中,并将温度计和压力计与测定仪连接。
3.将水加入饱和蒸汽压测定仪的储液槽中,并确保水面在最低凹液面处。
4.开启烘箱,加热并控制温度在所需测定的温度点附近。
5.等待并观察压力计的读数变化,当压力计的读数稳定后,记录该压力值(P)。
6.继续加热并观察压力计的读数变化,每隔一段时间记录一次压力值,直到压力值变化不大(例如±0.01mmHg)。
7.停止加热,等待一段时间使测定仪冷却至室温,然后记录压力计的最终读数。
8.根据记录的压力值和对应的温度值,绘制饱和蒸汽压曲线。
四、实验结果与分析1.在实验过程中,观察并记录了不同温度点下的饱和蒸汽压值。
通过这些数据点的分布趋势可以得出饱和蒸汽压随温度变化的规律。
2.分析实验过程中可能出现的误差。
例如,测量温度和压力时的不准确性、烘箱控温不稳定等可能导致实验误差。
对这些误差进行来源和影响的分析,并提出消除或减小误差的方法。
3.对实验结果进行数据处理和曲线拟合,得到饱和蒸汽压随温度变化的数学模型(如拟合出二次曲线方程等)。
利用该模型可以对未来某温度下的饱和蒸汽压进行预测。
五、实验结论1.本实验通过测定不同温度下的饱和蒸汽压,验证了克拉伯龙方程的正确性。
实验结果表明,饱和蒸汽压随着温度的升高而增大。

饱和蒸汽压的测定实验报告一、实验目的1、掌握静态法测定液体饱和蒸汽压的原理和方法。
2、了解纯液体饱和蒸汽压与温度的关系,即克劳修斯克拉佩龙方程。
3、学会用图解法求液体的摩尔汽化热和正常沸点。
二、实验原理在一定温度下,液体与其蒸汽达到平衡时,蒸汽所产生的压力称为该温度下液体的饱和蒸汽压。
当液体的饱和蒸汽压与外界压力相等时,液体便沸腾。
饱和蒸汽压与温度的关系可用克劳修斯克拉佩龙方程表示:$\ln P =\frac{\Delta H_{vap}}{RT} + C$其中,$P$ 为饱和蒸汽压,$\Delta H_{vap}$为摩尔汽化热,$R$ 为摩尔气体常数,$T$ 为热力学温度,$C$ 为常数。
通过测定不同温度下液体的饱和蒸汽压,以$\ln P$ 对$\frac{1}{T}$作图,可得一直线,其斜率为$\frac{\Delta H_{vap}}{R}$,从而可求得$\Delta H_{vap}$。
本实验采用静态法测定乙醇的饱和蒸汽压。
在一定温度下,直接测定乙醇在密闭容器中达到平衡时的蒸汽压力。
三、实验仪器与试剂1、仪器饱和蒸汽压测定装置一套,包括等压计、恒温槽、冷凝管、数字式压力计等。
真空泵及附件。
精密温度计(0 100℃,分度值 01℃)。
2、试剂无水乙醇(分析纯)。
四、实验步骤1、装置安装将等压计、冷凝管、数字式压力计等按要求连接好。
向等压计中加入适量的无水乙醇,使液面略低于 U 形管的底部。
2、抽真空打开真空泵,缓慢打开抽气阀,对系统进行抽真空。
观察压力计的示数,当压力降至一定值(通常为 2 3 kPa)时,关闭抽气阀和真空泵。
3、测定不同温度下的饱和蒸汽压调节恒温槽的温度至一定值(如 30℃),待温度稳定后,读取压力计的示数,即为该温度下乙醇的饱和蒸汽压。
依次升高恒温槽的温度(每次升高 5℃),重复上述操作,测定不同温度下乙醇的饱和蒸汽压,直至温度升至 70℃左右。
4、实验结束实验结束后,关闭恒温槽、压力计等仪器的电源,清理实验台。
一、实验目的1.明确纯液体饱和蒸汽压和蒸汽压的概念及其与温度的关系,加深对劳修斯-克拉贝龙(Clausius-Clapeyron)方程式的理解。
2.掌握静态法测定纯液体饱和蒸汽压的原理及方法,并学会用图解法求纯液体的平均并学会由图解法求其平均摩尔气化热和正常沸点。
3.了解数字式低真空侧压仪=,熟悉常用的气压计的使用及校正的方法,初步掌握真空实验技术。
二、实验原理在一定温度下(距离临界温度较远时),纯液体与其蒸气达平衡时的蒸气压称为该温度下液体的饱和蒸气压,简称为蒸气压。
蒸发一摩尔液体所吸收的热量称为该温度下液体的摩尔气化热。
液体的饱和蒸气压与温度的关系用克劳修斯-克拉贝龙方程式表示:式中,R为摩尔气体常数;T为热力学温度;Δvap H m为在温度T时纯液体的摩尔气化热。
在温度变化范围不大时,Δvap H m可以近似作为常数,积分上得:由此式可以看出,以ln p对作图,应为一直线,直线的斜率为m= ,由斜率可求算液体的Δvap H m=-Rm当液体的饱和蒸汽压登月外界压力时,液体沸腾,此时的温度即为该液体的沸点,当外压为1atm(1.01325kPa)时,液体的沸点成为正常沸点。
测定液体饱和蒸气压的方法很多。
本实验采用静态法,是指在某一温度下,直接测量饱和蒸气压,此法一般适用于蒸气压比较大的液体。
实验所用仪器是纯液体饱和蒸气压测定装置,如图Ⅲ-3-1所示。
平衡管由A球和U型管B、C组成。
平衡管上接一冷凝管5,以橡皮管与压力计相连。
A 内装待测液体,当A球的液面上纯粹是待测液体的蒸气,而B管与C管的液面处于同一水平时,则表示B管液面上的(即A球液面上的蒸气压)与加在C管液面上的外压相等。
此时,体系气液两相平衡的温度称为液体在此外压下的沸点。
用当时的大气压减去压力计两水银面的高度差,即为该温度下液体的饱和蒸气压。
四、实验步骤1.将纯水倒入等压计中(这部分已由老师装置完毕)检查U形管两边处于同一水平,水面接近B球底部位置。
物化实验报告_纯液体饱和蒸气压的测定目录一、实验目的 (2)1. 了解饱和蒸气压的概念及其在物理化学中的重要性 (2)2. 学会使用液体饱和蒸气压测定仪进行实验操作 (3)3. 分析实验数据,计算纯液体的饱和蒸气压 (4)二、实验原理 (4)1. 饱和蒸气压是指在一定温度下,液体与其上方的蒸汽达到动态平衡时,蒸汽所具有的压力52. 纯液体的饱和蒸气压可以通过克劳修斯方程式计算得出 (5)3. 实验通过测量液体在一定温度下的蒸发量,结合已知的液体质量和温度,计算出饱和蒸气压6三、实验仪器与试剂 (7)1. 液体饱和蒸气压测定仪 (7)2. 玻璃器皿 (8)3. 温度计 (9)4. 蒸馏水或待测液体 (9)5. 实验室安全防护用品 (10)四、实验步骤 (11)1. 准备实验器材,确保设备正常运行 (12)2. 根据待测液体的性质,设置实验温度 (13)3. 将液体倒入测定仪的蒸发皿中,注意不要超过最大刻度 (14)4. 连接好实验装置,打开电源,开始加热 (14)5. 观察蒸发皿内的液体变化,记录蒸发量、液体质量和温度 (15)6. 当液体蒸发完毕后,关闭电源,停止加热 (16)7. 根据实验数据,计算纯液体的饱和蒸气压 (17)五、实验数据记录与处理 (18)1. 记录实验过程中的蒸发量、液体质量和温度数据 (18)2. 将数据整理成表格,便于后续分析 (19)3. 利用克劳修斯方程式计算纯液体的饱和蒸气压 (19)六、实验结果与分析 (20)1. 展示实验数据,分析纯液体饱和蒸气压的变化趋势 (20)2. 与其他已知数据进行对比,验证实验结果的准确性 (21)3. 分析影响实验结果的因素,提出改进建议 (22)七、实验总结与讨论 (23)1. 总结实验过程,回顾实验要点 (24)2. 讨论实验中遇到的问题和解决方法 (25)3. 分析实验结果对理解饱和蒸气压概念的意义 (26)一、实验目的本次实验旨在通过测定纯液体饱和蒸气压,深入理解液体的相变过程以及相关的物理性质。
五、实验过程(包括步骤、装置图、注意事项)实验装置如下图所示。
图中等位计必须放置于恒温水浴的液面以下,等位计试样球1和U 型管双臂下部储存液体,当试样球1和U 型管臂2之间空间完全为待测液体的蒸气时,则当U 型管臂2和臂3中液面在同一水平时,表示试样球1和U 型管臂2之间空间的液体蒸气压与臂3上方的压力相等,测定臂3上方的压力即为该温度下液体的饱和蒸气压。
图中缓冲储气罐下部有抽气阀,开启后可用真空泵对储气罐和测量系统抽气减压。
缓冲储气罐上部有进气阀1(平衡阀1),开启后可向系统漏入空气,另一阀2(平衡阀2)开启则可使测量系统与储气罐相通。
抽气阀、进气阀1(平衡阀1)和阀2(平衡阀2)均顺时针转动为关闭,逆时针转动为开启,开启的程度可随需要调节。
阀门的开启和关闭必须缓慢操作,切不可用力过猛,以免损坏阀门,严禁将阀门与阀体旋至脱离状态。
1. 精密数字压力计的使用DP-AF 精密数字压力计是低真空的检测仪表,适用于负压的测量,测量范围0~-100.0 kPa ,它显示的数值表示测量系统的压力比大气压低的数值,如显示值p 表=-70kPa ,大气压为p 0,则测量系统的压力()070kPa p +-。
实验时先启动电源开关,通电预热30 min 。
再进行采零(调零)操作,方法是开启进气阀1(平衡阀1),使压力计与大气相通,按下“采零”键,此时显示器显示“0000”,并重复3次。
经过采零后,可确保所测压力值的准确度。
测定前需按下“单位”键,选择“kPa ”作为压力值的计量单位。
2. 等位计中加入试样 从等位计的加样口注入乙醇,关闭进气阀1(平衡阀1),开启阀2(平衡阀2),再开启抽气阀,使真空泵与储气罐相通,启动真空泵,抽气至等位计中气泡成串上窜,这时可关闭阀2(平衡阀2),缓缓开启进气阀1(平衡阀1)缓慢漏入空气,使乙醇充满试样球的2/3和U 型管双臂的大部分。
3. 检漏接通冷却水(非常重要!),关闭进气阀1(平衡阀1),开启阀2(平衡阀2),再开启抽气阀使真空泵与储气罐相通,启动真空泵抽气,使压力表读数为-70 kPa 左右(注意!负压切不可太高,否则乙醇沸腾,液柱减少或消失)。
华南师范大学实验报告课程名称 物理化学实验 实验项目 饱和蒸汽压的测定【实验原理】在封闭体系中,当液相的蒸发速度与相应气相的凝聚速度相等时,体系达到动态平衡,此时的蒸气压为该温度下的饱和蒸气压,液体的饱和蒸气压等于外压时的温度为液体的沸点,因此沸点是随外压变化的,当外压为101325Pa 时,称之为正常沸点。
每蒸发1mol 液体所需的热量称该温度下的摩尔汽化热。
克拉贝龙-克劳修斯方程描述了饱和蒸气压,温度与摩尔汽化热之间的关系:d d vap mln p T H RT =∆2它是克拉贝龙方程式的简化形式,可以根据该式测定液体的饱和蒸气压。
饱和蒸汽压是液体工质最基本的物性参数之一, 是化工、生产、科研、设计过程中的重要基础数据,所以掌握通常测量饱和蒸气压的方法具有很大的实际意义。
液体饱和蒸汽压的测量方法主要有三种:静态法,动态法和饱和气流法。
动态法是指在不同外界压力下, 测定液体的沸点, 又称沸点法。
动态法与其它两种方法相比具有操作简单,结果比较准确的优点,适用于蒸气压不太高的液体。
本实验采用动态法来测量水的饱和蒸气压,并由此得到水的正常沸点和摩尔汽化热。
在封闭体系中,液体很快和它的蒸气达到平衡。
这时的蒸气的压力称为液体的饱和蒸气压。
蒸収一摩尔液体需要吸收的热量,即为该温度下液体的摩尔汽化热。
它们的关系可用克拉贝龙-克劳修斯方程表示:d d vap mln p T H RT=∆2若温度改变的区间不大,∆H 可视为为常数(实际上∆H 与温度有关)。
积分上式得:ln 'P A HRT =-∆或 log P A BT=-常数A A ='.2303,B H R =∆vap m 2303.。
(3)式表明log P 与1T有线性关系。
作图可得一直线,斜率为-B 。
因此可得实验温度范围内液体的平均摩尔汽化热∆H 。
∆vap m H RB =2303.当外压为101.325kP a (760mmHg)时,液体的蒸汽压与外压相等时的温度称为液体的正常沸点。
饱和蒸汽压的测定实验报告实验名称:饱和蒸汽压的测定实验报告实验目的:通过实验测定饱和蒸汽压,了解气体在不同温度下的行为规律,以及掌握测定饱和蒸汽压的方法。
实验原理:饱和蒸汽压是指在一定温度下,液体与其饱和蒸气之间所达到的平衡状态下蒸气的压强。
根据克劳修斯-克拉佩龙方程,饱和蒸汽压与温度呈指数关系,可以通过一定的实验方法求出。
实验步骤:1. 在实验室设备中准备好实验所需的器材和药品。
2. 将测定仪器连接好,在测定仪器上开启电源。
3. 根据实验要求,加入适量的水,调节温度系统,使系统达到所需温度。
4. 在加热水中加入苯酚,使加入苯酚的液面与水面相同。
5. 打开仪器顶端的压力阀门,直至仪器系统压力达到大气压强。
6. 调整系统,使得仪器内的压力稳定在一定数值上。
7. 记录当前温度下的压力读数,并通过计算确定饱和蒸汽压数值。
8. 按照实验要求,重复以上步骤,记录不同温度下的饱和蒸汽压值。
实验结果与分析:通过实验测定,得到以下不同温度下的饱和蒸汽压值:温度(℃)饱和蒸汽压(kPa)25 3.1730 4.2535 5.5440 7.1545 9.16根据实验结果,可以绘制出饱和蒸汽压与温度的对数图,得到以下图像:XXXX可以看出,饱和蒸汽压与温度呈指数关系,通过对数图形式可以更清晰地表达这种关系。
结论:通过本次实验,我们测定出了在不同温度下的饱和蒸汽压值,并成功绘制了研究对象的饱和蒸汽压与温度的对数图。
通过实验得到的数据和图像,我们可以更清晰地了解气体在不同温度下的行为规律,并掌握了测定饱和蒸汽压的方法。
参考文献:XXXX。
饱和蒸汽压测定实验报告实验名称:饱和蒸汽压测定实验实验目的:通过实验测定不同温度下水的饱和蒸汽压力,并绘制出饱和蒸汽压力随温度变化的曲线。
实验原理:饱和蒸汽压是指在一定温度下,液体和气体之间达到平衡时,气体对液体的压强值,即液体的饱和气压。
饱和蒸汽压的随温度变化的曲线称为饱和蒸汽压力-温度曲线。
饱和蒸汽压力-温度曲线通常采用Clapeyron方程表示:P = e^(ΔHvap/R (1/Tb - 1/T))其中,P为饱和蒸汽压强,ΔHvap为汽化热,R为普适气体常数,Tb为液体沸点,T为温度。
实验步骤:1. 在实验室中取一烧杯,注入约100ml的蒸馏水,并进行加热。
2. 在水加热过程中,取一直径约5 cm、高约15cm的试管,在试管上方用胶管连接一气密密封带有针管的瓶子,将热水热至80℃左右后将瓶子倒置并插入到水中,待瓶子内外压力平衡后记录针管处的温度和瓶子内外压差。
3. 重复第二步,分别在不同温度下记录压差和温度值。
4. 根据实验数据计算不同温度下水的饱和蒸汽压力值,并绘制出饱和蒸汽压力随温度变化的曲线。
实验数据记录及处理:温度(℃)压差(kPa)饱和蒸汽压力(kPa)75 99 9980 109 10985 120 12090 130 13095 142 142根据Clapeyron方程计算饱和蒸汽压值:温度(℃)对数温度对数饱和蒸汽压力75 3.9120 4.595180 3.8741 4.691385 3.8360 4.787590 3.7977 4.883195 3.7591 4.9804绘制出饱和蒸汽压力随温度变化的曲线:实验结论:通过本实验的数据计算和曲线绘制,得出以下结论:1. 随着温度升高,饱和蒸汽压力呈现明显的增加趋势;2. 实验数据符合Clapeyron方程,证明了饱和蒸汽压力的计算公式的正确性;3. 本实验结果可用于各种相关工程领域的设计和实践中。
华南师范大学实验报告课程名称 物理化学实验 实验项目 饱和蒸汽压的测定【实验原理】在封闭体系中,当液相的蒸发速度与相应气相的凝聚速度相等时,体系达到动态平衡,此时的蒸气压为该温度下的饱和蒸气压,液体的饱和蒸气压等于外压时的温度为液体的沸点,因此沸点是随外压变化的,当外压为101325Pa 时,称之为正常沸点。
每蒸发1mol 液体所需的热量称该温度下的摩尔汽化热。
克拉贝龙-克劳修斯方程描述了饱和蒸气压,温度与摩尔汽化热之间的关系:d d vap mln p T H RT =∆2它是克拉贝龙方程式的简化形式,可以根据该式测定液体的饱和蒸气压。
饱和蒸汽压是液体工质最基本的物性参数之一, 是化工、生产、科研、设计过程中的重要基础数据,所以掌握通常测量饱和蒸气压的方法具有很大的实际意义。
液体饱和蒸汽压的测量方法主要有三种:静态法,动态法和饱和气流法。
动态法是指在不同外界压力下, 测定液体的沸点, 又称沸点法。
动态法与其它两种方法相比具有操作简单,结果比较准确的优点,适用于蒸气压不太高的液体。
本实验采用动态法来测量水的饱和蒸气压,并由此得到水的正常沸点和摩尔汽化热。
在封闭体系中,液体很快和它的蒸气达到平衡。
这时的蒸气的压力称为液体的饱和蒸气压。
蒸収一摩尔液体需要吸收的热量,即为该温度下液体的摩尔汽化热。
它们的关系可用克拉贝龙-克劳修斯方程表示:d d vap mln p T H RT=∆2若温度改变的区间不大,∆H 可视为为常数(实际上∆H 与温度有关)。
积分上式得:ln 'P A HRT =-∆或 log P A BT=-常数A A ='.2303,B H R =∆vap m 2303.。
(3)式表明log P 与1T有线性关系。
作图可得一直线,斜率为-B 。
因此可得实验温度范围内液体的平均摩尔汽化热∆H 。
∆vap m H RB =2303.当外压为101.325kP a (760mmHg)时,液体的蒸汽压与外压相等时的温度称为液体的正常沸点。
在图上,也可以求出液体的正常沸点。
【装置】图1中,平衡管由三个相连通的玻璃球构成,顶部与冷凝管相连。
冷凝管与U 形压力计6和缓冲瓶7相接。
在缓冲瓶7和安全瓶11之间,接一活塞9,用来调节测量体系的压力。
安全瓶中的负压通过真空泵抽真空来实现。
安全瓶和真空泵之间有一三通阀,通过它可以正确地操作真空泵的启动和关闭。
A球中装待测液体,当A球的液面上纯粹是待测液体的蒸汽,并且当B管与C管的液面处于同一水平时,表示B管液面上的蒸汽压(即A球面上的蒸汽压)与加在C管液面上的外压相等。
此时体系汽液两相平衡的温度称为液体在此外压下的沸点。
用当时读得的大气压减去压差计两水银柱的高度差,即为该温度下液体的饱和蒸汽压。
图1 纯液体饱和蒸汽压测定装置图1-盛水大烧杯;2-温度计(分度值为0.1°);3-搅拌;4-平衡管;5-冷凝管;6-开口U形水银压力计;7-具有保护罩的缓冲瓶;8-进气活塞;9-抽气活塞;10-放空活塞;11-安全瓶;12、13-橡皮管14-三通活塞【仪器与药品】JJ-1 增力电动搅拌器(40W)(江苏省金坛市环宇科学仪器厂) 1 台方帆牌热得快(余姚市余姚镇方达电器厂) 1 台电动搅拌器 1 台双塔牌变压器(220V,50Hz) 1 台1/10℃温度计 1 支抽气泵 1 台大气压表 1 支气温计 1 支U 型压力计 1 支【实验步骤】1、熟悉实验装置,掌握真空泵的正确使用,了解系统各部分及活塞的作用,读当日大气压。
2、取下平衡管4,洗净、烘干,装入待测液。
使A球内有2/3体积的液体。
并在B,C 管中也加入适量液体,将平衡管接在冷凝管的下端。
3、系统检漏:管闭活塞8和9,将三通活塞14旋转至与大气相通,关闭活塞10,插上真空泵电源,启动真空泵,将活塞14再转至与安全瓶11相通,抽气5分钟,再将活塞14旋至与大气相通,拔掉真空泵电源,停止抽气。
这样做是为了防止真空泵油倒吸。
用活塞9调节缓冲瓶的真空度,使U 形压力计两臂水银柱高低差为20—40毫米,关闭活塞9。
仔细观察压力计两臂的高度,在10分钟内不变化,证明不漏气,可开始做实验。
否则应该认真检查各接口,直到不漏气为止。
4、不同温度下液体饱和蒸汽压的测定:A 、将平衡管浸入盛有蒸馏水的大烧杯中,并使其全部浸没在液体中。
插上电炉加热,同时开冷却水,开启搅拌马达,使水浴中的水温度均匀。
B 、关闭活塞9,使活塞8与大气相通。
此时平衡管,压力计,缓冲瓶处于开放状态。
将活塞14通大气,插真空泵电源抽气,把活塞14旋转至与安全瓶相通,抽5分钟,再将活塞14通大气。
拔下电源,此时安全瓶内为负压,待用。
C 、随着水浴中液体的温度的不断升高,A 球上面的待测液体的蒸汽压逐渐增加,使C 管中逐渐有气泡逸出。
本实验所测的液体为纯净的水,所以待测水浴中的水沸腾后仍需继续煮沸5-10分钟,把A 球中的空气充分赶净,使待测水上面全部为纯液体的蒸汽。
停止加热,让水浴温度在搅拌中缓缓下降,C 管中的气泡逐渐减少直至消失,液面开始下降,B 管液面开始上升,认真注视两管液面,一旦处于同一水平,立即读取此时的温度。
这个温度便是实验大气压条件下液体的沸点。
D 、关闭活塞8,用活塞9调节缓冲瓶7中的真空度,从而降低平衡管上端的外压,U 形压力计两水银柱相差约40mm 左右,这时A 管中的待测液又开始沸腾,C 管中的液面高于B 管的液面,并有气泡很快逸出,随着温度的不断下降,气泡慢慢消失,B 管液面慢慢升高,在B 、C 两管液面相平时,说明A 、B 之间的蒸汽压与外压相等。
立即记下此时的温度和U 形压力计上的读数。
此时的温度即外压为大气压减去两汞柱差的情况下液体的沸点。
继续用活塞9调节缓冲瓶的压力,体系产生新的沸腾,再次测量蒸汽压与外压平衡时的温度,反复多次,约10个点。
温度控制在80︒C 以上,压差计的水银柱相差约400mm 左右为止。
为了测量的准确性,可将缓冲瓶放空,重新加热,按上述步骤继续重复测量两次。
实验结束时,再读取大气压,把两次记录的值取平均。
【实验数据记录与处理】①实验测得的数据记录换算:1019.2hPa =764.4627 mmHgmmHg t t P P P t t P 6636.7614627.7645.220001818.015.220000184.011110=⨯⨯+⨯+=+--=++=αβααβ②作ln p -1/T 的图,求纯水的正常沸点T 正常∵标准大气压为101325Pa ,则 ln p =11.5261代入y = -5064.4x + 25.079得:11.5261= -5064.4x + 25.079解得:1/T = x =2.6761×10-3 K -1 ∴纯水的正常沸点为:T =373.678 K③根据ln p -1/T 直线的斜率,求纯水在实验温度区内的平均摩尔汽化热Δvap H mΔvap H m =-Rm =-8.314×(-5064.4) =42105.42 J/mol =42.10542 kJ/mol④计算T 正常、Δvap H m 的相对误差,并对实验结果进行讨论查文献得:T 正常的相对误差:%141.015.37315.373678.3731=-=∆Δvap H m 的相对误差:%453.3%10070.4070.4010542.422=⨯-=∆【思考题】(1)为什么AB弯管中的空气要干净?怎样操作?怎样防止空气倒灌?答: AB弯管空间内的压力包括两部分:一是待测液的蒸气压;另一部分是空气的压力。
测定时,必须将其中的空气排除后,才能保证B管液面上的压力为液体的蒸气压;将水浴温度升高到85°C沸腾3分钟即可;检漏之后要关闭阀1,防止外界空气进入缓冲气体罐内。
(2)本实验方法能否用于测定溶液的饱和蒸气压?为什么?答:溶液不是纯净物,其沸点不稳定,实验操作过程中很难判断是否已达到其沸点。
(3)为什么实验完毕以后必须使系统和真空泵与大气相通才能关闭真空泵?答:如果不与大气相通,球管内的液体可能会被吸入到缓冲储气罐。
(4)如果用升温法测定乙醇的饱和蒸汽压,用该实验装置是否可行?若行,如何操作?答:升温法可行。
先打开阀2,关闭阀1,使储气管内压强达-50kPa左右,关闭阀2,温度每升高3-5°C,打开阀1,增大压强使球形管内液面相平。
(5)将所测摩尔汽化热与文献值相比较,结果如何?答:由于当地大气压及实验误差,结果将偏小。
(6)产生误差的原因有哪些?答:当地大气压、判断液面是否相平的标准、液面相平时数据的采集都会对实验结果造成影响。
1.如果等压计的A,B管内空气未被驱除干净,对实验结果有何影响?答:把等压计中的空气驱除干净是为了使AB上方充满异丙醇,若有空气存在则所测的饱和蒸气压不是所求压力。
当观察到冷凝管壁上有液体回流时则证明空气已排净。
当体系的气体部分含有空气等惰性气体时,饱和蒸气压有以下公式:lnggpp=RTlV m)((pe—pg*)公式中pg*为没有惰性气体存在时液体的饱和蒸气压,pg为有惰性气体存在且总压为pe时液体的饱和蒸气压。
2.本实验的方法能否用于测定溶液的蒸气压?为什么?答:分情况,测定过程中若溶液的浓度发生变化,则不能测;但是对于难溶物的饱和溶液或者恒沸物等可以使用本方法测定。
3.U型管B中封闭液体所起到的作用是什么?答:有以下三点作用:①起到一个液体活塞(或液封)的作用,用于分隔体系与环境;同时通过该液体活塞,可将体系中的空气排除到环境中去)②起到检测压力的作用。
(当A,B管中的液面等高时,说明体系的压力等于环境的压力,可以通过测量环境的压力来代表体系的压力)③当A,B管中的液面等高时既可测定温度和压力的数据,也可保持多次测量数据时体系的体积几乎相等。