物质的分类
- 格式:docx
- 大小:35.99 KB
- 文档页数:2

物质的分类并举例
1、元素:元素是由原子组成的化学物质,是构成物质的基本成分,没有可分解的小分子,元素可以组合形成化合物。
常见的元素有氢、氦、锂、铁、钙、铜等。
2、化合物:化合物是由两种或更多元素组成,以特定比例在原子键中化合而成的物质。
它是拥有固定化学式,具有固定物理性质的组分。
常见的化合物有醋酸、氢氧化钠、氯化钾等。
3、复合物:复合物由两种或更多种不同物质通过晶体结构或分子互相结合形成的物质,每一种物质在晶体结构或分子中都有独立的存在特性。
常见的复合物有水、石油和陶瓷等。
4、混合物:混合物是由不同物质混合而成的物质,每一种混入物质在整体结构中都能够独立被辨识,并可以经过收缩或聚焦等物理化学处理程序可以使混合物分离出来。
混合物有有机混合物、无机混合物等,其中常见的有水溶液、铁锈和冰淇淋等。
5、聚合物:聚合物是由一定数量的同类单体构成的大分子物质,它们关系密切,组成大分子结构。
它们有很多特性,例如熔点、气味、折光率等。
常见的聚合物有塑料、纤维素、橡胶等。

物质的分类与性质一、引言物质是构成世界万物的基本要素,它们以不同的形态和性质存在于我们周围。
对于人类来说,了解物质的分类和性质对于我们认识和利用自然世界具有重要意义。
本文将探讨物质的分类和性质,帮助读者更好地理解和应用这些知识。
二、物质的分类物质可以按照不同的标准进行分类。
最常见的分类方式是按照物质的组成和结构进行划分,主要分为纯物质和混合物两大类。
1. 纯物质纯物质是由同种元素或化合物组成的物质。
元素是由相同类型的原子组成的,例如氧气、金属铁等。
化合物是由不同元素以一定比例结合而成的,例如水、二氧化碳等。
纯物质具有固定的化学组成和一致的性质,可以通过物理或化学方法进行分离。
2. 混合物混合物是由两种或更多种不同物质混合而成的物质。
混合物可以是均匀混合物(溶液)或非均匀混合物(悬浮液、乳浊液等)。
混合物的组成和性质可以随着混合物中各组分的比例变化而发生改变,可以通过物理方法进行分离。
三、物质的性质物质的性质是指物质所具有的特征和行为,可以分为物理性质和化学性质两大类。
1. 物理性质物理性质是物质在不改变其化学组成的情况下所表现出的性质。
常见的物理性质包括颜色、形状、密度、熔点、沸点等。
物理性质可以通过观察和测量来确定,可以帮助我们区分和识别不同的物质。
2. 化学性质化学性质是物质在与其他物质发生化学反应时所表现出的性质。
化学性质包括物质的燃烧性、氧化性、还原性等。
通过观察物质与其他物质之间的反应,我们可以了解物质的化学性质,这对于研究物质的组成和性质具有重要意义。
四、物质的分类与性质的关系物质的分类和性质之间存在着密切的关系。
不同类别的物质具有不同的性质,这种差异主要是由于它们的组成和结构不同所致。
1. 纯物质的性质纯物质具有固定的化学组成和一致的性质,这使得我们可以通过观察和测量来确定它们的性质。
例如,金属铁具有良好的导电性和导热性,这使得它在工业生产和电子设备中得到广泛应用。
另外,纯物质的性质也可以通过化学反应来改变,例如,氧气可以与其他物质反应生成氧化物。
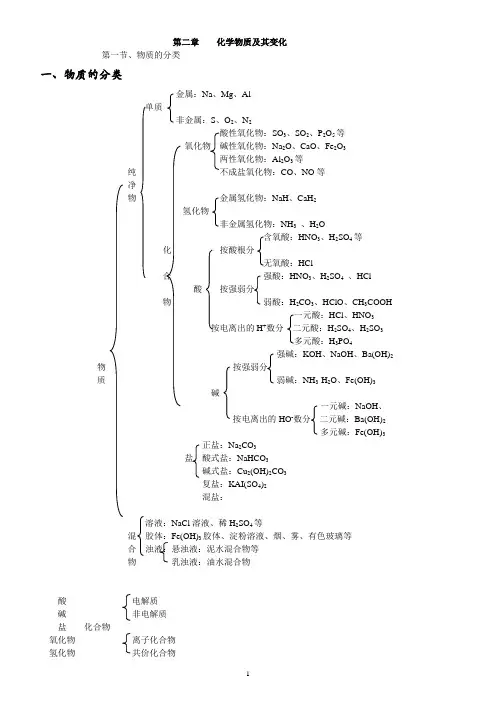
第二章化学物质及其变化第一节、物质的分类一、物质的分类金属:Na、Mg、Al单质非金属:S、O2、N2酸性氧化物:SO3、SO2、P2O5等氧化物碱性氧化物:Na2O、CaO、Fe2O3两性氧化物:Al2O3等纯不成盐氧化物:CO、NO等净物金属氢化物:NaH、CaH2氢化物非金属氢化物:NH3、H2OHNO3、H2SO4等化按酸根分HCl合强酸:HNO3、H2SO4、HCl酸按强弱分物弱酸:H2CO3、HClO、CH3COOH一元酸:HCl、HNO3按电离出的H+数分二元酸:H2SO4、H2SO3多元酸:H3PO4强碱:KOH、NaOH、Ba(OH)2物按强弱分质弱碱:NH3·H2O、Fe(OH)3碱一元碱:NaOH、按电离出的HO-数分二元碱:Ba(OH)2多元碱:Fe(OH)3正盐:Na2CO3盐酸式盐:NaHCO3碱式盐:Cu2(OH)2CO3复盐:KAI(SO4)2混盐:溶液:NaCl溶液、稀H2SO4等混胶体:Fe(OH)3胶体、淀粉溶液、烟、雾、有色玻璃等合浊液:悬浊液:泥水混合物等物乳浊液:油水混合物酸电解质碱非电解质盐化合物氧化物离子化合物氢化物共价化合物二、分散系相关概念1. 分散系:一种物质(或几种物质)以粒子形式分散到另一种物质里所形成的混合物,统称为分散系。
2. 分散质:分散系中分散成粒子的物质。
3. 分散剂:分散质分散在其中的物质。
4、分散系的分类:按照分散质粒子的大小可以把分散系分为:溶液、胶体和浊液。
(1nm==10-9m )分散质粒子直径小于1nm 的分散系叫溶液,在1nm -100nm 之间的为胶体,大于100nm 的叫做浊液。
⎢⎢⎢⎢⎢⎢⎢⎢⎣⎡⎩⎨⎧→→⎩⎨⎧→→→→⎥⎦⎤乳浊液悬浊液浊液胶气溶胶;液溶胶;固溶粒子胶体:分子胶体胶体溶液分散系分散剂分散质三、胶体:分散质粒子直径大小在10-9~10-7m 之间的分散系。
1、分类:⑴. 根据分散质微粒组成:如:3)(OH Fe 胶体胶粒是由许多3)(OH Fe 等小分子聚集一起形成的微粒,其直径在1nm ~100nm 之间,这样的胶体叫粒子胶体。

物质的分类标准物质的分类是指根据物质的不同特征将其划分为不同的类别。
这些特征可以包括化学类型、晶体结构、溶解性、电化学性质、组成方式、物理状态和元素组成等。
准确地了解这些分类标准有助于我们更好地理解物质的性质和行为。
1.物质的化学类型化学类型是指物质分子中原子之间通过共享电子而形成的键的类型。
根据原子间共享电子的方式,可以将物质分为共价化合物、离子化合物和金属化合物。
共价化合物是指原子间通过共享电子对形成键的物质,如氧气、二氧化碳等;离子化合物是指原子间通过得失电子形成离子键的物质,如食盐、氢氧化钠等;金属化合物是指由金属原子间通过共享电子形成的金属键的物质,如金属氧化物、金属硫化物等。
2.物质的晶体结构晶体结构是指物质分子或离子在空间中排列的规律性。
根据晶体中原子或离子的排列方式,可以将物质分为晶体和非晶体。
晶体是指具有高度规律性的原子或离子排列的物质,如石英、金属等;非晶体是指没有明显规律性的原子或离子排列的物质,如玻璃、橡胶等。
此外,还可以根据晶体中原子的种类和结合方式将晶体分为离子晶体、共价晶体、金属晶体和分子晶体等。
3.物质的溶解性溶解性是指物质在溶剂中溶解的程度。
不同物质在不同溶剂中的溶解度不同,因此可以根据溶解性对物质进行分类。
常见的溶解性分类标准包括水溶性和有机溶性。
水溶性是指物质在水中的溶解度,可以将物质分为可溶、微溶和不溶等;有机溶性是指物质在有机溶剂中的溶解度,可以将物质分为易溶、可溶和难溶等。
此外,也可以根据溶解过程中的热效应等特征对物质进行分类。
4.物质的电化学性质电化学性质是指物质在电场作用下的行为和反应。
根据物质在电场作用下的行为,可以将物质分为导体、半导体和绝缘体。
导体是指能够自由导电的物质,如金属;半导体是指导电性能介于导体和绝缘体之间的物质,如硅、锗等元素;绝缘体是指几乎不导电的物质,如橡胶、玻璃等。
此外,还可以根据物质在电场作用下的氧化还原性质等方面对物质进行分类。

物质的分类标准物质是构成世界万物的基本要素,我们所熟知的各种物质都可以按照不同的标准进行分类。
物质的分类标准可以从不同的角度进行划分,包括化学性质、物理性质、组成成分等多个方面。
本文将从不同的角度介绍物质的分类标准,以便更好地理解和认识物质。
一、按化学性质分类。
根据物质的化学性质,可以将物质分为元素和化合物两大类。
元素是由同一种原子组成的纯净物质,例如氧气、金属铜等;而化合物是由两种或两种以上不同元素化合而成的物质,例如水、二氧化碳等。
元素和化合物是根据它们的化学性质来进行分类的,这种分类方法主要是依据物质的化学成分来划分。
二、按物理性质分类。
按照物质的物理性质,可以将物质分为固体、液体和气体三大类。
固体是指具有一定形状和体积的物质,其分子间距较小,分子排列紧密;液体是指没有一定形状,但有一定体积的物质,其分子间距比固体大,分子间排列较为紧密;气体是指既没有一定形状也没有一定体积的物质,其分子间距最大,分子间排列最为稀疏。
这种分类方法是根据物质的物理状态和分子间距离来进行划分的。
三、按组成成分分类。
根据物质的组成成分,可以将物质分为单质和混合物两大类。
单质是由同一种原子或同一种分子组成的物质,例如金属铜、氧气等;混合物是由两种或两种以上不同物质混合而成的物质,例如空气、海水等。
这种分类方法是根据物质的组成成分来进行划分的,可以更好地区分物质的组成结构。
四、按来源分类。
按照物质的来源,可以将物质分为天然物质和人工合成物质两大类。
天然物质是指自然界中存在的物质,例如水、空气、石头等;人工合成物质是指人类通过化学合成或其他方法制造的物质,例如塑料、合成纤维等。
这种分类方法是根据物质的来源和制备方式来进行划分的,可以更好地了解物质的产生过程。
五、按用途分类。
根据物质的用途,可以将物质分为生活用品、工业原料、医药用品等多个类别。
生活用品是指日常生活中使用的物质,例如食品、衣物、家具等;工业原料是指工业生产中所需的物质,例如煤炭、石油、铁矿石等;医药用品是指医疗保健中所需的物质,例如药品、医疗器械等。

物质分类的方法一、按物质的组成分类根据物质的组成成分,可以将物质分为单质和化合物两大类。
1. 单质单质是由同一种元素组成的纯物质,它们具有相同的化学性质。
常见的单质有金属、非金属和惰性气体等。
金属是指一类具有金属光泽、导电性和延展性的物质。
常见的金属有铁、铜、铝等。
金属可以进一步分为贵金属和常金属。
非金属是指那些不具备金属特性的物质,如碳、氧、硫等。
非金属物质通常呈现出不同的颜色和形态。
惰性气体是指具有稳定的电子层结构的气体,如氦、氖等。
它们具有极低的反应性,不易与其他物质发生化学反应。
2. 化合物化合物是由两种或两种以上不同元素按照一定的比例结合而成的物质,具有新的物理和化学性质。
化合物可以分为无机化合物和有机化合物两大类。
无机化合物是由无机元素组成的化合物,如氧化物、酸、碱等。
无机化合物在自然界中广泛存在,具有多种用途。
有机化合物是由碳元素与其他元素结合而成的化合物,如糖类、脂肪类、蛋白质等。
有机化合物是生命体系中重要的组成部分。
二、按物质的状态分类根据物质的状态,可以将物质分为固体、液体和气体三大类。
1. 固体固体是物质的一种状态,具有固定的形状和体积。
常见的固体有金属、矿石、岩石等。
固体可以进一步分为晶体和非晶体。
晶体是由具有规则排列的晶格结构的固体,如钻石、盐等。
晶体具有明确的几何形状和独特的物理性质。
非晶体是由无规则排列的分子或原子组成的固体,如玻璃、橡胶等。
非晶体的物理性质与晶体有所不同。
2. 液体液体是物质的一种状态,具有流动性和固定的体积。
常见的液体有水、酒精、石油等。
液体可以进一步分为溶液和悬浊液。
溶液是由溶质和溶剂按一定比例混合而成的液体,如盐水、糖水等。
溶液是一种均匀透明的液体。
悬浊液是由悬浮物和溶液按一定比例混合而成的液体,如牛奶、果汁等。
悬浊液中的悬浮物可以通过过滤等方法分离出来。
3. 气体气体是物质的一种状态,具有可压缩性和无固定形状的特点。
常见的气体有氧气、氢气、二氧化碳等。

物质的分类与性质1. 物质分类物质是指占据空间并具有质量的物体。
根据不同的特征和性质,物质可以分为以下几类:1.1 元素元素是由同种原子组成的纯物质。
元素不能再通过化学反应分解成其他物质。
目前已知的元素有118种,如氧、金、铁等。
1.2 化合物化合物是由不同元素以固定的比例和方式结合而成的物质。
化合物可以通过化学反应分解成更简单的物质。
例如水(H2O)就是由氢元素和氧元素组成的化合物。
1.3 混合物混合物是由两种或更多种不同物质混合在一起形成的物质。
混合物的组成可以随意改变,并且可以通过物理方法分离其组分。
例如,蔬菜沙拉就是由多种蔬菜混合而成的混合物。
2. 物质性质物质的性质是指物质所具有的特点和表现。
根据物质性质的不同,我们可以将其分为以下几类:2.1 物理性质物理性质是指物质在不改变其组成的情况下所表现出的性质。
包括颜色、形状、密度、熔点、沸点等。
通过观察和测量,我们可以得到物质的物理性质。
2.2 化学性质化学性质是指物质与其他物质发生化学反应时所表现出的性质。
它涉及到物质的组成和结构的改变。
例如,金属与酸反应会产生氢气,这是金属的一种化学性质。
2.3 生物学性质生物学性质是指物质在生物体内发生的变化和作用。
这种性质涉及到物质对生物体的影响和相互作用。
例如,维生素是一种具有促进生物体生长和发育的生物学性质的物质。
2.4 环境性质环境性质是指物质与环境之间的相互作用和影响。
物质在不同的环境条件下可能表现出不同的性质。
例如,在高温下,物质的熔点和沸点可能会发生变化。
结论物质的分类和性质对我们了解和研究物质的基本特性非常重要。
通过对物质分类和性质的研究,我们可以更好地理解物质的组成和行为,为科学发展和技术创新提供基础。

物质的分类与性质物质是构成宇宙万物的基本单位,它们根据其化学组成和性质的不同,可以被分类为不同的类型。
本文将探讨物质的分类和性质,并对其进行详细描述。
一、物质的分类1. 无机物质无机物质是由非生物过程形成的物质,其主要成分是无机元素。
无机物质可以进一步分为以下几类:(1) 金属:具有导电性、延展性和可塑性的物质,如铁、铜和铝等。
(2) 非金属:不具有导电性和延展性的物质,如氧气、氮气和碳等。
(3) 水合物:由水分子结合而成的物质,如硫酸铜和硝酸铵等。
(4) 矿物质:存在于地壳中的天然无机物质,如石英、方解石和石膏等。
2. 有机物质有机物质是由生物过程形成的物质,其主要成分是有机元素(碳、氢、氧、氮、磷和硫等)。
有机物质可以进一步分为以下几类:(1) 生物体内的有机物质:包括蛋白质、脂肪和碳水化合物等。
(2) 人工合成的有机物质:如合成聚合物、染料和药物等。
3. 混合物混合物是由两种或两种以上不同物质按一定比例混合形成的物质,其组成和性质可以发生改变,但各组分保持其原有的性质。
混合物可以根据其形态和物理性质进一步分为以下几类:(1) 溶液:由溶质和溶剂混合而成的透明均匀体,如盐水和糖水等。
(2) 悬浮液:由颗粒状溶质悬浮于溶剂中而形成的不透明体,如沙水和液体草莓奶等。
(3) 凝胶:由固体颗粒分散于液体中而形成的半固体体,如果冻和胶原蛋白凝胶等。
二、物质的性质1. 物理性质物质的物理性质是指可以通过物理方法观察和测量得到的性质,而不改变物质的组成。
物质的物理性质包括:(1) 密度:物质单位体积的质量。
(2) 溶解度:物质在溶剂中能溶解的程度。
(3) 熔点:物质从固态转变为液态的温度。
(4) 沸点:物质从液态转变为气态的温度。
2. 化学性质物质的化学性质是指物质与其他物质发生化学反应时所表现出的性质。
物质的化学性质包括:(1) 可燃性:物质能被点燃并产生火焰。
(2) 氧化性:物质能与氧气反应并产生氧化物。

物质的分类及转换一、物质的分类物质是构成宇宙的基本单位,根据其性质和组成不同,可以将物质分为三类:元素、化合物和混合物。
1. 元素元素是由相同类型的原子组成的纯物质。
目前已知的元素有118种,包括氢、氧、铁等。
元素具有固定的化学性质,无法通过常规的物理或化学方法分解成其他物质。
2. 化合物化合物是由不同类型的原子通过化学键结合而成的物质。
化合物具有独特的化学性质,可以通过化学反应分解成更简单的物质。
例如,水是由氢和氧元素组成的化合物,可以通过电解或加热分解为氢气和氧气。
3. 混合物混合物是由两种或更多种不同物质混合而成的物质。
混合物的组成和性质可以不均匀,可以通过物理方法如过滤、蒸馏等分离成各个组成部分。
例如,空气是由氮气、氧气、水蒸气等气体组成的混合物,可以通过液化或净化过程分离出其中的组分。
二、物质的转换物质在自然界中不断发生着各种转换过程,包括物质的相变、化学反应等。
1. 相变相变是物质由一种相态转变为另一种相态的过程。
常见的相变有固态到液态的熔化、液态到气态的蒸发、气态到液态的凝结以及液态到固态的凝固等。
相变过程中,物质的化学组成不发生改变,只是其分子或原子的排列方式发生改变。
2. 化学反应化学反应是指物质之间发生化学变化的过程。
在化学反应中,原有物质的化学键被打破,新的化学键形成,导致物质的性质发生明显的变化。
化学反应可以分为合成反应、分解反应、置换反应、氧化还原反应等多种类型。
例如,燃烧是一种常见的氧化反应,燃料与氧气反应产生二氧化碳和水。
3. 核反应核反应是指原子核发生变化的过程,通常涉及到原子核的裂变或聚变。
核反应具有巨大的能量释放,是核能利用的基础。
例如,核裂变反应是指重核裂变成轻核的过程,核聚变反应是指轻核聚变成重核的过程。
4. 生物转化生物转化是指生物体内发生的各种化学反应和代谢过程。
生物转化是生命活动的基础,包括有机物的合成、分解、氧化还原等过程。
例如,光合作用是一种生物转化过程,植物利用光能将二氧化碳和水合成为有机物,释放出氧气。

化学中的物质分类方法
化学中的物质可以根据不同的属性和特征进行分类。
以下是几种常见的物质分类方法:
1. 根据组成元素:物质可以根据其组成元素的类型和数量进行分类。
例如,元素是由同一种原子组成的物质,而化合物是由不同种类的原子以一定比例结合而成的物质。
2. 根据物态:物质可以分为固态、液态和气态。
固态物质具有固定的形状和容积,分子间距离密集;液态物质具有固定的容积,但可以流动;气态物质没有固定的形状和容积,分子间距离较大。
3. 根据溶解性:物质可以分为溶质和溶剂。
溶质是可以溶解在溶剂中的物质,而溶剂是能够溶解其他物质的物质。
根据物质在溶剂中的溶解度可以将物质分为可溶性和不可溶性物质等。
4. 根据化学性质:物质可以根据其化学性质进行分类。
例如,物质可以被分为无机物和有机物。
无机物主要由无机元素组成,而有机物则包含碳元素,并且通常由碳与氢、氧、氮、硫等其他元素组成。
5. 根据反应类型:物质可以根据其发生的化学反应类型进行分类。
例如,物质可以是酸、碱或盐。
酸是产生氢离子的物质,碱是产生氢氧根离子的物质,而盐
是由酸和碱中的阳离子和阴离子结合而成的物质。
这些分类方法仅仅是化学中物质分类的一部分,还有其他多种方式可以根据不同的观察角度来对物质进行分类。

第1节物质的分类知识回顾在化学学习过程中,对于数以千万计的化学物质和为数更多的化学反应,常常要用到分类法,利用分类法学习化学,可以起到事半功倍的效果。
人们常按物质的组成、结构、性质等知识将物质进行分类。
分类标准可以从物质的组成、结构和性质去确定。
1.物质简单分类如下:2材料又可分为天然高分子材料和合成高分子材料,塑料、纤维和橡胶都属于合成高分子材料。
例1 物质的分类标准有多种,标准可以是物质的组成、性质、用途……请根据所学知识,依据物质所具有的某种性质,自拟两种分类标准,对以下物质进行分类,每类至少包括三种物质(填化学式)氢气、氧气、一氧化碳、二氧化硫、二氧化氮(红棕色、有毒)、水、碳。
分类标准一,包括物质分类标准二,包括物质例2请你仔细研读下列表格中的例子:现其他的规律:(1)(2)例3 生活中的下列物质,属于合成纤维的是()A.棉花B.涤纶C.羊毛D.蚕丝入门衔接一、按物质种类分类分类方法:树状分类法:如化合物分为氧化物、酸、碱、盐。
1.氧化物根据氧化物对酸碱反应的不同,可以将氧化物分为酸性氧化物、碱性氧化物、两性氧化物不成盐氧化物四类。
(1)酸性氧化物(又称酸酐):能与碱反应生成盐和水的氧化物,如2CO 、2SO 、3SO ,其对应的酸分别是32CO H 、32SO H 、42SO H 。
(2)碱性氧化物:能与酸反应生成盐和水的氧化物,如O Na 2、MgO 、CaO ,其对应的碱分别为NaOH 、2)(OH Mg 、2)(OH Ca(3)两性氧化物:既能与酸又能与碱反应生成盐和水的氧化物,如32O Al 、2)(OH ZnO H AlCl HCl OH Al 23333)(+=+ 23)(N a A l O N a O H OH Al =+(偏铝酸钠)+ O H 22(4)不成盐氧化物:既不能与酸、又不能与碱反应生成盐和水的氧化物,如CO 、NO 。
说明:不是所有的非金属氧化物都是酸性氧化物,如CO 、NO 等;也不是所有的酸性氧化物都是非金属氧化物,如72O Mn 是酸性氧化物,但所有的碱性氧化物都是金属氧化物。
物质的分类元素化合物与混合物的区别物质的分类:元素、化合物与混合物的区别在我们日常生活中,物质无处不在。
根据其组成与性质的不同,物质可以被分为元素、化合物和混合物三种类型。
本文将从不同的角度探讨这三种物质的区别。
一、组成方式1. 元素:元素是构成物质世界的基本单位,具有独特的原子结构和化学性质。
元素由相同类型的原子组成,并以特定的化学符号表示,如氧气(O₂)、铁(Fe)和金(Au)等。
元素是一种纯净的物质,不能通过常规的化学方法进行分解。
2. 化合物:化合物是由两种或两种以上的元素以固定比例结合而成的物质。
化合物的组成是通过化学反应形成的,各个元素以化学键相连,形成新的化合物。
例如,水(H₂O)是由氢(H)和氧(O)两种元素以2:1的比例组成的。
3. 混合物:混合物是由两种或两种以上的物质混合而成,其组成比例可以不固定。
混合物的组成物质之间没有化学反应,仅仅是物理上的混合。
例如,沙子和水的混合物、空气以及各种溶液都属于混合物。
二、性质与特点1. 元素:元素具有独特的物理和化学性质。
每种元素都有特定的原子序数和原子量,特定的电子结构和元素周期表中的位置。
元素的性质主要由其原子结构和电子云的分布决定,如金属的导电性能和半导体元素的电子能带结构等。
2. 化合物:化合物具有比组成元素更复杂的性质。
各个元素以特定的比例结合在一起,形成了新的化学物质。
化合物的性质取决于其组成元素和它们之间的结合方式。
例如,氧化铁(Fe₂O₃)是一种红色的固体,具有磁性,而铁(Fe)和氧(O₂)元素则没有这些性质。
3. 混合物:混合物的物理性质是可以进行分离的,每个组成物质保留着其原有的性质。
混合物的性质可以通过物理手段进行分离,如蒸馏、过滤等。
例如,如果将沙子和水的混合物加热,水会蒸发而沙子不会发生任何变化。
三、分离方式1. 元素:元素通常可以通过物理或化学方法进行分离。
有些元素在特定温度和压力下可转化为气态,如氧气。
而其他元素则需要进行特定的化学反应才能分离出来。
一、物质的分类:二、单质:1、金属:钠 Na 、镁Mg 、铝Al 、钾K 、钙Ca 、钛Ti 、锰Mn 、铁Fe 、铜Cu 、锌Zn 、银Ag 、钡Ba 、汞Hg 、铅Pb2、非金属:固态非金属单质:碳C 、硅Si 、磷P 、硫S 、碘I 2液态非金属单质:溴Br 2气态非金属单质:氢气H 2、氮气N 2、氧气O 2、氟气F 2、氯气Cl 2、臭氧O 33、稀有气体:氦气He 、氖气Ne 、氩气Ar混合物 物质纯净物单质 化合物 无机化合物有机化合物 氧化物 酸 碱 盐 金属 非金属 稀有气体三、化合物:1、氧化物:金属氧化物:氧化钠Na2O、过氧化钠Na2O2、氧化镁MgO、三氧化二铝Al2O3、氧化钙CaO、二氧化钛TiO2、二氧化锰MnO2黑色、氧化亚铁FeO、三氧化二铁Fe2O3红棕色、四氧化三铁Fe3O4黑色、氧化铜CuO黑色、氧化锌ZnO、氧化汞HgO红色非金属氧化物:水H2O液体、过氧化氢H2O2液体、一氧化碳CO、二氧化碳CO2、一氧化氮NO、二氧化氮NO2红棕色、二氧化硫SO2、三氧化硫SO3固体、二氧化硅SiO2固体、五氧化二磷P2O5固体2、酸:盐酸HCl、硫酸H2SO4、硝酸HNO3、碳酸H2CO3、磷酸H3PO43、碱:氨水NH3•H2O、氢氧化钠NaOH、氢氧化钾KOH、氢氧化钡Ba(OH)2、氢氧化钙Ca(OH)2、氢氧化铜Cu(OH)2蓝色、氢氧化铝Al(OH)3白色、氢氧化铁Fe(OH)3红褐色4、盐:氯化物:氯化钠NaCl、氯化钾KCl、氯化铵NH4Cl、氯化银AgCl、氯化镁MgCl2、氯化钙CaCl2、氯化锰MnCl2、氯化铜CuCl2、氯化锌ZnCl2、氯化钡BaCl2、氯化亚铁FeCl2、氯化铁FeCl3、氯化铝AlCl3硫酸盐:硫酸钠Na2SO4、硫酸钾K2SO4、硫酸铵(NH4)2SO4、硫酸镁MgSO4、硫酸钙CaSO4、硫酸铜CuSO4、硫酸锌ZnSO4、硫酸钡BaSO4、硫酸亚铁FeSO4、硫酸铁Fe2(SO4)3、硫酸铝Al2(SO4)3碳酸盐:碳酸钠Na2CO3、碳酸钾K2CO3、碳酸铵(NH4)2CO3、碳酸氢铵NH4HCO3、碳酸钙CaCO3、碳酸铜CuCO3、碳酸钡BaCO3其它盐:氯酸钾KClO3、高锰酸钾KMnO4、锰酸钾K2MnO4、碱式碳酸铜Cu2(OH)2CO35、几种有机物:甲烷CH4 (俗名:沼气、瓦斯、坑道气)、乙醇C2H5OH (俗名:酒精)、乙酸CH3COOH。
专题一 物质的分类【复习目标】1.认识物质的多样性,认识物质的三态及其转化。
2. 能从组成上识别氧化物。
3.区分纯净物、混合物、单质和化合物、有机物和无机物。
4.知道无机化合物可以分为氧化物、酸、碱、盐。
【知识要点梳理】 1.物质的分类2.根据所含物质种类是否单一将物质分为纯净物和混合物。
3.根据组成纯净物的元素种类是否单一将纯净物分为单质和化合物。
【注解】:①辨别纯净物和混合物可以从物质种类入手,也可以从有没有固定的化学式入手,当给出的是某物质的化学式,则该物质是纯净物,当给出的是某物质的主要成分的化学式,则该物质是混合物。
②单质(由同种元素组成的纯净物)与化合物(由不同种元素组成的纯净物)均属于纯净物(纯净物由一种物质组成); ③由同种元素组成的物质不一定是单质,如金刚石和石墨组成混合物、O 2和O 3组成的混合物;由不同种元素组成的物质也不一定是化合物,也还有可能是混合物,如CO 和CO 2; 4.根据组成和性质的不同可将化合物分为氧化物和酸、碱、盐。
(1)氧化物是指由两种元素组成,且其中一种为氧元素的化合物叫做氧化物。
5.有机物与无机物:一般把含碳元素的化合物称为有机化合物,简称有机物,如甲烷、乙醇、葡萄糖、蛋白质等。
【注解】CO 、CO 2、H 2CO 3及碳酸盐等,虽也含有碳元素,但因它们的组成和性质跟无机物相似,因此它们是无机物。
【应用示例】例1.某物质不含碳元素和氢元素,它不可能是①酸;②碱;③盐;④有机物中的( ) A .①②④ B .②③④ C .①②③ D .①③④【解析】该题从物质的组成角度考查物质分类。
酸是指在溶液中电离时阳离子完全是氢离子的化合物,一定含有氢元素;碱在溶液中电离时阴离子完全是氢氧根离子的化合物,所以一定含有氧元素;有机物指的是含碳化合物,所以一定含有碳元素;盐是指一类金属离子或铵根离子(NH 4+)与酸根离子结合的化合物,可以不含碳和氢元素。
物质的分类及转化一、物质的分类1.物质的分类方法(分类标准或依据)依物质的属性,物质一般可以有如下分类方法:(1)根据存在状态分为:气态、液态和固态物质; (2)根据导电性分为:导体、半导体和绝缘体;(3)根据物质的溶解性分为:易溶、可溶、微溶和难溶; (4)根据物质的组成分为:混合物和纯净物。
【注】物质的分类标准不同,分类结果也不同。
2.物质的分类纯净物物质混合物【思考】“在水中能电离产生H +的物质都是酸,产生OH —的物质都是碱”,这种说法对吗?化合物 非金属单质有机化合物 酸碱酸 酸根中是否有氧元素无氧酸含氧酸 一个酸分子中最多 电离的H +数 一元酸 二元酸多元酸沸点高低易挥发性酸 难挥发性酸 酸在水中溶解性不同 可溶性酸难溶性酸碱碱在水中溶解性不同可溶性碱 难溶性碱碱在水中最多能电离出OH —数一元碱 二元碱 多元碱 非均匀混合物【辨析】酸性氧化物都是非金属氧化物,碱性氧化物都是金属氧化物。
【易错提醒】金属氢化物中H 显-1价【例1】下列物质属于纯净物的是( )A.洁净的空气B.食盐水C.浮有冰块的水D.纯净的盐酸E.含氮35%的硝酸铵化肥F.生石灰【例2】今有下列三组物质,每组中都有一种物质跟其他三种属于不同的种类。
将此种物质(写化学式)和分类依据(选出的物质与其他物质不同之处)写在下面相应的表格内。
三组物质分别为:(1)O 2、F 2、S 、N 2;(2)Fe 、Na 、Al 、Si ;(3)NO 2、CO 2、CaO 、SO 2。
【例3】关于氧化物的下列说法中正确的是 ( )A.金属氧化物一定是碱性氧化物B.碱性氧化物一定是金属氧化物C.非金属氧化物一定是酸性氧化物D.酸性氧化物一定是非金属氧化物 【例4】经分析,某种物质只含有一种元素,则此物质( )A.一定是一种单质B.一定是纯净物C.一定是混合物D.可能是纯净物,也可能是混合物盐 酸根中是否有氧元素 无氧酸盐含氧酸盐 盐在水中溶解性不同 可溶性盐微溶性盐 难溶性盐 组成盐的阴、阳离子不同 正盐 酸式盐 碱式盐氧化物组成元素化学性质 金属氧化物 非金属氧化物 酸性氧化物碱性氧化物两性氧化物不成盐氧化物氢化物 金属氢化物非金属氢化物【变式】下列物质不可能由一种元素组成的是()A.单质B.氧化物C.化合物D.混合物【例5】有下列几种物质:⑴空气、⑵液态氧、⑶硝酸钾溶液、⑷硫酸铜晶体(CuSO4·5H2O)、⑸二氧化碳、⑹氧化铜、⑺锌、⑻金刚石、⑼氢氧化铜、⑽纯碱、⑾甲烷、⑿硝酸、⒀盐酸、⒁液态硫酸钾。
物质的分类
一、常见的分类方法
1.交叉分类法:对物质依据____________进行分类。
例:
2.树状分类法:对_______按照某种属性进行分类。
如:
【思维拓展】冰水混合物为混合物这句话对吗?金刚石和石墨均是由碳元素组成的单质,因此金刚石和石墨混合在一起为混合物,这句话对吗?
例1.将下列各组物质按单质、氧化物、酸、碱、盐分类顺序排列,其中正确的是( ) A.银、干冰、硫酸、烧碱、食盐 B.碘酒、冰、盐酸、烧碱、食盐 C.氢气、二氧化硫、硝酸、烧碱、硝酸钾 D.铜、氧化铜、醋酸、石灰水、氯化铜
例2.如图表示的是纯净物、单质、化合物、含氧化合物、氧化物、碱之间的包含、不包含关系,若整个大圆圈代表纯净物,则下列选项中,能正确指出①、②、③、④、⑤所属物质类别的是( ) A .①单质、③化合物
B .②碱、⑤氧化物
C .②化合物、⑤含氧化合物
D .④含氧化合物、③氧化物
【易错警示】物质分类中的易错点小结 (1)概念间的关系——“并列”与“包含”
①并列关系:纯净物与混合物,单质与化合物,酸、碱、盐与氧化物。
②包含关系:纯净物>化合物>氧化物。
(2)酸性氧化物和碱性氧化物的概念
①酸性氧化物是与碱反应生成盐和水的氧化物; ②碱性氧化物是与酸反应生成盐和水的氧化物。
(3)酸的元数是酸电离出H +的个数,而不是分子中氢原子的个数,如醋酸是一元酸而不是四元酸。
二、分类法的应用——物质间的转化 金属→碱性氧化物→碱→盐 非金属→酸性氧化物→酸→盐 如:钙→氧化钙→氢氧化钙→碳酸钙 碳→二氧化碳→碳酸→碳酸钙 写出以上各步的化学方程式:
【思维拓展】碱和盐反应时符合什么条件才能发生?试举例说明。
例3.图中,“——”表示相连的物质间在一定条件下可以反应,“→”表示丁在一定条件下通过置换反应可以转化为乙。
下面四组选项中,符合图示要求的是( )
【当堂自测】 1.判断正误
(1)①酸、②碱、③盐、④氧化物四类物质的组成一定含有氧元素的是②④。
( ) (2)硫酸铜是铜盐,也是硫酸盐。
( ) (3)水是氧化物、化合物、纯净物。
( ) (4)纯碱是碱。
( )
(5)非金属氧化物不一定是酸性氧化物。
( ) (6)氢氧化钠、乙醇、氢氧化钙都属于碱。
( ) (7)CuSO 4·5H 2O 属于混合物。
( )
(8)硫酸既属于含氧酸又属于二元酸,这种分类方法是树状分类法。
( )
3.下列物质分类中,前者包含后者的是( ) A.酸性氧化物 非金属氧化物 B.溶液 石灰乳 C.化合物 酸 D.混合物 氮气
4.下列化合物依次属于氧化物、碱、盐的一组是( ) A.碳酸钠、氢氧化钾、氧化钙
B.一氧化碳、氢氧化钠、氯化钾
C.水、硫酸、氯化钠
D.氧化铜、碱式碳酸铜、碳酸钙 【课时习题】
1.《神农本草经》说:“水银……镕化(加热)还复为丹。
”这里的“丹”是指() A .氯化物B .合金C .硫化物D .氧化物
2.下列各组物质中,第一种是酸,第二种是混合物,第三种是碱的是( ) A .硫酸、五水硫酸铜、苛性钾 B .硫酸、空气、纯碱 C .氧化铁、胆矾、熟石灰 D .硝酸、食盐水、烧碱
3.实验室里有4个药品橱,已经存放下表所示药品:
实验室新购进一些碘,应该将这些碘放在( ) A .甲橱 B .乙橱 C .丙橱 D .丁橱
4.下列各物质的分类、名称(或俗名)、化学式都正确的是( ) A.金属氧化物 氧化铁 FeO B.非金属氧化物 二氧化硫 SO 2 C.含氧酸 硫酸 H 2SO 3 D.碱 纯碱 Na 2CO 3。