高考化学复习 物质结构与性质课件
- 格式:ppt
- 大小:790.00 KB
- 文档页数:11







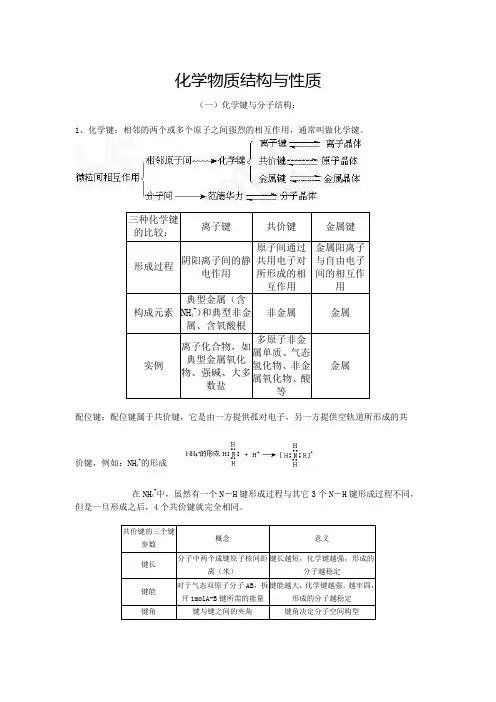
化学物质结构与性质(一)化学键与分子结构:1、化学键:相邻的两个或多个原子之间强烈的相互作用,通常叫做化学键。
配位键:配位键属于共价键,它是由一方提供孤对电子,另一方提供空轨道所形成的共价键,例如:NH 4+的形成在NH 4+中,虽然有一个N -H 键形成过程与其它3个N -H 键形成过程不同,但是一旦形成之后,4个共价键就完全相同。
键长、键能决定共价键的强弱和分子的稳定性:原子半径越小,键长越短,键能越大,分子越稳定。
共价键按成键形式可分为σ键和π键两种,σ键主要存在于单键中,π键主要存在于双键、叁键以及环状化合物中。
σ键较稳定,而π键一般较不稳定。
共价键具有饱和性和方向性两大特征。
2、分子结构:价层电子对互斥理论:把分子分成两大类:一类是中心原子上的价电子都用于形成共价键。
如CO2、CH2O、CH4等分子中的C原子。
它们的立体结构可用中心原子周围的原子数来预测,概括如下:另一类是中心原子上有孤对电子(未用于形成共价键的电子对)的分子。
如H2O和NH3中心原子上的孤对电子也要占据中心原子周围的空间,并参与互相排斥。
因而H2O分子呈V型,NH3分子呈三角锥型。
杂化轨道理论:在形成多原子分子的过程中,中心原子的若干能量相近的原子轨道重新组合,形成一组新的轨道,这个过程叫做轨道的杂化,产生的新轨道叫杂化轨道。
据参与杂化的s轨道与p轨道的数目,存在sp3、sp2、sp三种杂化。
杂化轨道理论分析多原子分子(离子)的立体结构价层电子对互斥模型判断简单分子或离子的空间构型说明:(1)等电子原理是指原子总数相同,价电子总数相同的分子或离子,对于主族元素而言,价电子就是其最外层电子数,即为最外层电子总数相等。
这一类分子或离子具有相似的化学键特征、分子结构以及部分物理性质相似,但一般情况下,化学性质并不相似。
同样,化学键相似,并不是指键角等一定相同。
利用等电子原理可判断一些简单分子或离子的主体构型,如:CO2、CNS-、NO2+、N3-的原子总数均为3,价电子总数均为16,因此,它们的空间构型均为直线型。