亲核取代反应
- 格式:ppt
- 大小:3.24 MB
- 文档页数:101

亲核取代反应讲解
亲核取代反应是有机化学常见的一种反应。
在这种反应中,一个亲核试剂汇合一个有机反应物,并且代替了原有的基团。
在这个反应中,亲核试剂成为了新的基团。
这种反应是在有机化学中广泛运用的,非常有用。
它可以用于构建长链分子,连接分子,以及进行化学变换,制造新化合物。
现在,让我们跟着下面的步骤学习一下如何进行亲核取代反应。
1. 首先,你需要准备好亲核试剂。
亲核试剂可以是任何一种有活性的物质,其分子中含有一个亲核中心,例如氨基、羟基、硫代锰酸根、氰根、卤素根等。
在这个过程中,亲核试剂将代替原有的基团。
2. 准备好需要反应的有机化合物。
选定有机化合物,将其与亲核试剂混合,具体反应条件需要根据不同化合物的特性进行调整。
3. 进行反应。
在进行反应时,通常需要一定的触发条件。
例如,需要加热、催化、加压等。
这些条件可以影响反应速率和产率。
4. 产物的分离与纯化。
完成反应后,需要对产物进行分离和纯化。
这可以通过各种方法进行,例如渗透色谱、薄层色谱、皮尔斯等方法。
通过以上步骤,亲核取代反应就完成了。
这个反应可以进行多次,生成不同的产物,依据不同的具体反应条件,可以得到不同的产物类型。
总之,亲核取代反应是有机化学中非常常见的一种反应。
通过学会这个反应,可以制造许多新型材料和化合物。
即使在化学实验室或制造工厂等工作中,软硬件机器人也可以准确地掌握这个技术,帮助实验者进行研究和开发不同的产物。
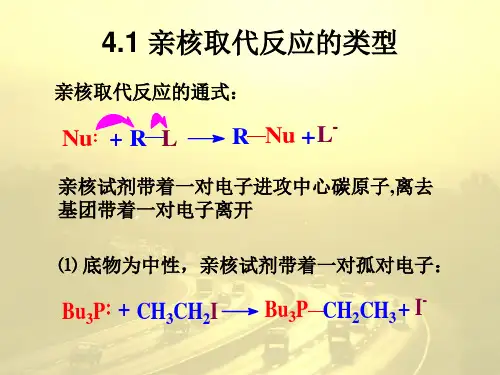


苯环的亲核取代反应(Nucleophilic Substitution Reactions of Benzene)引言:苯环是有机化学中最基本也是最重要的一个结构单元,在有机合成反应中起着举足轻重的作用。
它的亲核取代反应是有机合成中最常见的反应之一,它可以通过苯环中的芳香性π电子亲电位和亲核试剂中的亲核反应位互相作用,从而发生取代反应。
本文将介绍的基本概念、机理和应用。
一、亲核取代反应的基本概念亲核取代反应是指亲核试剂取代苯环上的一个离子后,生成一个新的化合物的过程。
在这类反应中,亲核试剂攻击苯环上的一个C-H键,形成一个中间态,然后中间态再失去一个离子,最终生成新的化合物。
亲核试剂通常是带有一个富电子密度的原子,如氢离子、卤素离子等。
二、亲核取代反应的机理亲核取代反应的机理主要包括三个步骤:攻击、失去离子和生成新化合物。
1. 攻击:亲核试剂攻击苯环上的一个C-H键,这个步骤通常是一个准平面型的过渡态。
由于苯环上的σ键和π键之间存在共轭关系,减小了C-H键的键长,导致苯环对亲核试剂的攻击具有一定的难度。
2. 失去离子:在攻击过程中,苯环上的C-H键被亲核试剂取代,形成一个中间态。
这个中间态常常是一个带有正电荷的离子,称为亲核试剂与苯环的加合物。
3. 生成新化合物:中间态经过失去离子,生成一个新的化合物。
这个过程通常是一个反应活化能相对较高的步骤。
三、苯环亲核取代反应的应用苯环亲核取代反应在有机合成中具有广泛的应用,以下列举几个常见的例子:1. 氯代反应:苯环可以与氯原子发生亲核取代反应,生成氯代苯。
氯代苯在有机合成中经常用作重要的化学试剂,如制备苯甲酸、苯酚等。
2. 溴代反应:苯环也可以与溴原子发生亲核取代反应,生成溴代苯。
溴代苯在有机合成中常用作重要的中间体,如制备苯甲醛、苯甲酸等。
3. 羟基取代反应:苯环可以与羟基(OH)发生亲核取代反应,生成苯酚。
苯酚是一种重要的有机化合物,广泛应用于化学工业和医药领域。






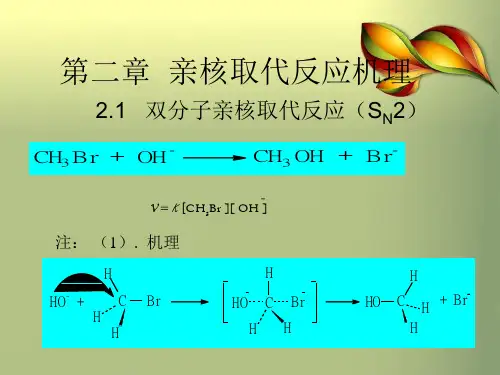
亲核取代反应一.亲核取代反应机理。
亲核取代反应是指有机分子中的与碳相连的原子或原子团被作为亲核试剂的某原子或原子团取代的反应。
反应分为SN1型(单分子取代反应),与SN2型双分子取代反应。
1.SN1型(单分子取代反应)第一步是碳原子上正电荷增加,离去基团负点性增加,经过过渡态(1)并最终解离,生成活性中间体碳正离子与离去基团负离子。
由于这一步反应的活化能较高,速率较慢,所以这一步是反应的决速步。
第二步是活性中间体的碳正离子与亲和试剂作用,生成反应产物。
这一步仅需少量能量,速率很快。
反应特点:(1)SN1反应的决速步是中心碳原子与离去基团之间化学键的异裂。
反应速率只取决于一种分子的浓度,因此,它在动力学上是一级反应。
(2)一般是一个两步反应。
第一步生成的碳正离子采取SP2杂化,是平面构型。
故若反应物的中心碳原子是手性碳,反应产物一般是一对等量的对映异构体的混合物——外消旋体。
(3)反应中间体生成的碳正离子导致反应有重排的趋势。
2.SN2型(双分子取代反应)反应中,离去基团离开中心碳原子的同时,亲核试剂与中心碳原子发生部分键合,无中间体生成。
有机反应中,将两种分子参与决速步的亲核取代反应陈伟双分子亲核取代反应。
反应特点:(1)SN2反应是一步反应,只有一个过渡态。
(2)在SN2反应中,亲核试剂进攻中心碳原子是总是从离去基团溴原子的背面沿着碳原子和离去基团连接的中心线方向进攻。
这个过程会使得碳原子与三个未参与反映的键发生翻转,这种翻转称为瓦尔登翻转,又称构型翻转。
二.影响亲核取代反应的因素1.烃基结构的影响。
对SN1反应,主要考虑碳正离子的稳定性。
对SN2反应,主要取决于过渡态形成的难易,也就是空间效应的影响。
2.离去基团的影响。
离去基团的性质对SN1和SN2将产生相似的影响:离去基团的离去能力越强,亲核取代反应越易进行。
对于离去基团:键能越弱,离去基团的稳定性越好,该离去基团的离去能力就越强。
3.亲核试剂的影响仅对SN2有影响。
亲核反应的五种反应名称亲核反应是有机化学中常见的一种反应类型,它涉及到亲电子的攻击和亲核试剂的参与。
根据亲核试剂的性质和反应机理的不同,亲核反应可以分为以下五种反应。
1. 亲核取代反应(Nucleophilic Substitution Reaction)亲核取代反应是最常见的亲核反应类型之一。
在亲核取代反应中,亲核试剂攻击一个含有亲电子的基团,将其替换掉。
常见的亲核取代反应包括SN1和SN2反应机理。
2. 亲核加成反应(Nucleophilic Addition Reaction)亲核加成反应中,亲核试剂与含有多键(通常是双键或三键)的官能团发生反应,形成一个新的化合物。
亲核试剂通常通过给予亲电子中心以亲电子形式进行反应。
3. 亲核消除反应(Nucleophilic Elimination Reaction)亲核消除反应涉及到亲核试剂与含有一对相邻碳原子之间的键的官能团发生反应。
在这种反应中,亲核试剂不仅与官能团发生反应,还通过攻击相邻的碳原子断裂化学键,从而使得官能团消失。
4. 亲核加合反应(Nucleophilic Addition-Elimination Reaction)亲核加合反应结合了亲核加成和亲核消除两种反应类型。
在亲核加合反应中,亲核试剂首先与含有多键的官能团发生加成反应,然后通过消除反应使得官能团发生重新排列。
5. 亲核环化反应(Nucleophilic Cyclization Reaction)亲核环化反应是一种特殊的亲核反应,发生在含有适当官能团的分子中。
在这种反应中,亲核试剂与官能团内的一个亲电子中心发生反应,形成一个新的环状结构。
这五种亲核反应在有机合成中起着非常重要的作用,能够构建复杂的有机分子结构,并提供了合成有机化合物的有效途径。
在实际应用中,化学家们常常根据反应条件和所需产物的特性选择适当的亲核反应类型进行研究和应用。
亲核取代反应总结1、反应定义:亲核取代反应(Nucleophilic Substitution Reaction)是指有机分子中与碳相连的某原子或基团被作为亲核试剂的某原子或基团取代的反应。
在反应过程中,取代基团提供形成新键的一对电子,而被取代的基团则带着旧键的一对电子离去.2、反应意义:这类反应是有机化学中非常重要的一类反应,不论在理论研究中还是在有机合成实际中都是极其有用的一类反应.3、反应分类:亲核取代反应的主要类型为脂肪族饱和碳上的亲核取代反应,即饱和卤代烃与亲核试剂的取代反应,较特殊结构的有苄基卤代物、烯丙基卤代物亲核反应。
其他类型还包括与酰氯、磺酸酯、磺酰卤、卤代苯等的取代反应.从电荷类型来分,亲核取代反应只能有四种类型:(1)中性底物和负离子亲核试剂反应(2)中性底物和中性亲核试剂反应(3)正离子底物和负离子亲核试剂反(4)正离子底物和中性亲核试剂反应亲核试剂包括有机和无机两类分子或离子:无机类亲核试剂:OH—、CN-、X—、H2O、NH3等有机类亲核试剂:ROH、RO—、PhO-、RS—、RMgX、RCOO-等4、反应机理类型分类:(1)双分子亲核取代反应(S N2)有两种分子参与了决定反应速率关键步骤的亲核取代反应称为双分子亲核取代反应。
反应过程中,亲核试剂从反应物离去基团的背面向与它连接的碳原子进攻,先与碳原子形成比较弱的键,同时离去基团与碳原子的键有一定程度的减弱,两者与碳原子成一条直线,碳原子上另外三个键逐渐由伞形转变成平面,这需要消耗能量,即活化能,当反应进行和达到能量最高状态即过渡态后,亲核试剂与碳原子之间的键开始形成,碳原子与离去基团之间的键断裂,碳原子上三个键由平面向另一边偏转,整个过程犹如大风将雨伞由里向外反转一样,这时就要释放能量,形成产物,S N2反应机理一般式表示为:Nu-+R X[Nuδ-···R···Xδ- ] NuR+X—例如,溴甲烷与OH—的水解反应:(2)单分子亲核取代反应(S N1)只有一种分子参与了决定反应速率关键步骤的亲核取代反应称为单分子亲核取代反应,反应中,反应物首先解离成碳正离子与带负电荷的离去基团,这个过程需要能量,是控制反应速率的一步,即慢的一部.当分子解离后,碳正离子马上与亲核试剂结合,速率极快,是快的一步。
亲核取代反应总结1、反应定义:亲核取代反应(Nucleophilic Substitution Reaction)是指有机分子中与碳相连的某原子或基团被作为亲核试剂的某原子或基团取代的反应。
在反应过程中,取代基团提供形成新键的一对电子,而被取代的基团则带着旧键的一对电子离去。
2、反应意义:这类反应是有机化学中非常重要的一类反应,不论在理论研究中还是在有机合成实际中都是极其有用的一类反应。
3、反应分类:亲核取代反应的主要类型为脂肪族饱和碳上的亲核取代反应,即饱和卤代烃与亲核试剂的取代反应,较特殊结构的有苄基卤代物、烯丙基卤代物亲核反应。
其他类型还包括与酰氯、磺酸酯、磺酰卤、卤代苯等的取代反应。
从电荷类型来分,亲核取代反应只能有四种类型:(1)中性底物和负离子亲核试剂反应(2)中性底物和中性亲核试剂反应(3)正离子底物和负离子亲核试剂反(4) 正离子底物和中性亲核试剂反应亲核试剂包括有机和无机两类分子或离子:无机类亲核试剂:OH -、CN -、X -、H 2O 、NH 3等有机类亲核试剂:ROH 、RO -、PhO -、RS -、RMgX 、RCOO -等4、反应机理类型分类:(1)双分子亲核取代反应(S N 2)有两种分子参与了决定反应速率关键步骤的亲核取代反应称为双分子亲核取代反应。
反应过程中,亲核试剂从反应物离去基团的背面向与它连接的碳原子进攻,先与碳原子形成比较弱的键,同时离去基团与碳原子的键有一定程度的减弱,两者与碳原子成一条直线,碳原子上另外三个键逐渐由伞形转变成平面,这需要消耗能量,即活化能,当反应进行和达到能量最高状态即过渡态后,亲核试剂与碳原子之间的键开始形成,碳原子与离去基团之间的键断裂,碳原子上三个键由平面向另一边偏转,整个过程犹如大风将雨伞由里向外反转一样,这时就要释放能量,形成产物,S N 2反应机理一般式表示为:Nu -+ R X [Nuδ-···R···X δ- ] NuR + X -例如,溴甲烷与OH -的水解反应:(2)单分子亲核取代反应(S N 1)只有一种分子参与了决定反应速率关键步骤的亲核取代反应称为单分子亲核取代反应,反应中,反应物首先解离成碳正离子与带负电荷的离去基团,这个过程需要能量,是控制反应速率的一步,即慢的一部。