初中化学常用物质化学式俗称及默写练习
- 格式:docx
- 大小:14.59 KB
- 文档页数:6

初中化学常用物质化学式俗称及默写练习集团档案编码:[YTTR-YTPT28-YTNTL98-UYTYNN08]初中化学常用物质化学式、俗称1.Al(OH)3氢氧化铝:胃舒平的主要成分2.BaSO4硫酸钡:钡餐、重晶石3.C碳:金刚石、石墨、木炭、活性炭、焦炭、煤的主要成分4.Ca(ClO)2和CaCl2次氯酸钙和氯化钙混合物:漂白粉(次氯酸钙)5.CaO氧化钙:生石灰6.CaO、NaOH氧化钙和氢氧化钠混合物:碱石灰7.Ca(OH)2氢氧化钙:熟石灰、石灰水8.CaCO3碳酸钙:石灰石、大理石9.CaSO4.2H2O硫酸钙晶体:(生)石膏10.(CaSO4)2.H2O硫酸钙晶体:熟石膏11.CH4:甲烷、天然气、瓦斯、沼气12.C2H5OH:乙醇、酒精13.CH3COOH:乙酸、醋酸14.C6H12O6:葡萄糖15.CO2二氧化碳:干冰、碳酸气16.CO和H2混合气:水煤气,CO:煤气17.CO(NH2)2:尿素18.CuSO4?5H2O硫酸铜晶体:蓝矾、胆矾19.Cu2(OH)2CO3碱式碳酸铜:铜绿、铜锈、孔雀石20.CuSO4和Ca(OH)2:波尔多液21.FeSO4?7H2O硫酸亚铁晶体:绿矾22.Fe2O3氧化铁:铁锈和赤铁矿主要成分23.Fe3O4四氧化三铁:磁铁矿、烤蓝、烤黑24.Hg汞:水银25.HCl氯化氢:氢氯酸、盐酸、胃酸的主要成分26.H2O2过氧化氢:双氧水27.H2和O2混合气:爆鸣气28.KAl(SO4)2.12H2O十二水硫酸铝钾:明矾29.K2CO3碳酸钾:草木灰主要成分30.KOH氢氧化钾:苛性钾31.NaOH氢氧化钠:苛性钠、烧碱,火碱32.Na2CO3碳酸钠:纯碱、苏打33.NaHCO3碳酸氢钠:小苏打34.Na2CO3.10H2O:纯碱晶体、石碱、口碱35.Na2SiO3硅酸钠:水玻璃36.NaCl氯化钠:食盐37.Na2S2O3硫代硫酸钠:大苏打、海波38.NH4HCO3碳酸氢铵:碳铵39.(NH4)2SO4硫酸铵:硫铵40.NH4NO3硝酸铵:硝铵41.NH3?H2O:一水合氨、氨水42.P磷:白磷、红磷、黄磷43.S硫:硫磺44.SiO2二氧化硅:石英、石英砂、水晶45.Fe:生铁、钢、不锈钢的主要成分初中化学常用物质化学式、俗称(默写练习一)1.Al(OH)3氢氧化铝:2.BaSO4硫酸钡:3.C碳:4.Ca(ClO)2和CaCl2次氯酸钙和氯化钙混合物:5.CaO氧化钙:6.CaO、NaOH氧化钙和氢氧化钠混合物:7.Ca(OH)2氢氧化钙:8.CaCO3碳酸钙:9.CaSO4.2H2O硫酸钙晶体:10.(CaSO4)2.H2O硫酸钙晶体:11.CH4:12.C2H5OH:13.CH3COOH:14.C6H12O6:15.CO2二氧化碳:16.CO和H2混合气:,CO:17.CO(NH2)2:18.CuSO4?5H2O硫酸铜晶体:19.Cu2(OH)2CO3碱式碳酸铜:20.CuSO4和Ca(OH)2:21.FeSO4?7H2O硫酸亚铁晶体:22.Fe2O3氧化铁:23.Fe3O4四氧化三铁:24.Hg汞:25.HCl氯化氢:26.H2O2过氧化氢:27.H2和O2混合气:28.KAl(SO4)2.12H2O十二水硫酸铝钾:29.K2CO3碳酸钾:30.KOH氢氧化钾:31.NaOH氢氧化钠:32.Na2CO3碳酸钠:33.NaHCO3碳酸氢钠:34.Na2CO3.10H2O:35.Na2SiO3硅酸钠:36.NaCl氯化钠:37.Na2S2O3硫代硫酸钠:38.NH4HCO3碳酸氢铵:39.(NH4)2SO4硫酸铵:40.NH4NO3硝酸铵:41.NH3?H2O:42.P磷:43.S硫:44.SiO2二氧化硅:45.Fe:初中化学常用物质化学式、俗称(默写练习二)1.:胃舒平的主要成分2.:钡餐、重晶石3.:金刚石、石墨、木炭、活性炭、焦炭、煤的主要成分4.:漂白粉(次氯酸钙)5.:生石灰6.:碱石灰7.:熟石灰、石灰水8.:石灰石、大理石9.:(生)石膏10.:熟石膏11.:甲烷、天然气、瓦斯、沼气12.:乙醇、酒精13.:乙酸、醋酸14.:葡萄糖15.:干冰、碳酸气16.:水煤气,CO:煤气17.:尿素18.:蓝矾、胆矾19.:铜绿、铜锈、孔雀石20.:波尔多液21.:绿矾22.:铁锈和赤铁矿主要成分23.:磁铁矿、烤蓝、烤黑24.:水银25.:氢氯酸、盐酸、胃酸的主要成分26.:双氧水27.:爆鸣气28.:明矾29.:草木灰主要成分30.:苛性钾31.:苛性钠、烧碱,火碱32.:纯碱、苏打33.:小苏打34.:纯碱晶体、石碱、口碱35.:水玻璃36.:食盐37.:大苏打、海波38.:碳铵39.:硫铵40.:硝铵41.:一水合氨、氨水42.:白磷、红磷、黄磷43.:硫磺44.:石英、石英砂、水晶45.:生铁、钢、不锈钢的主要成分。
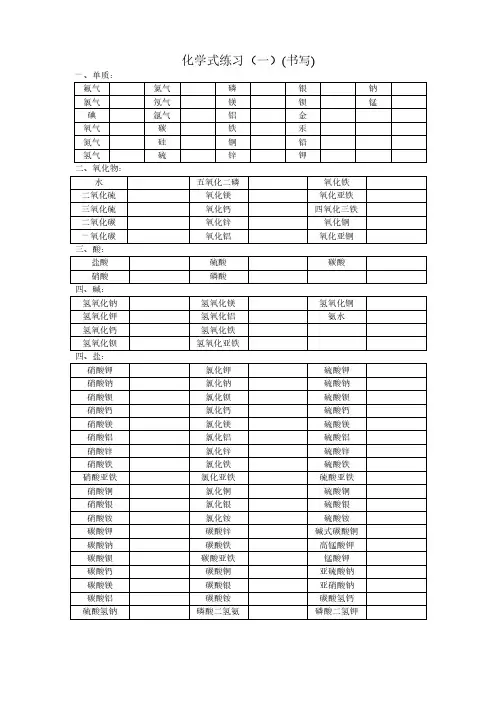
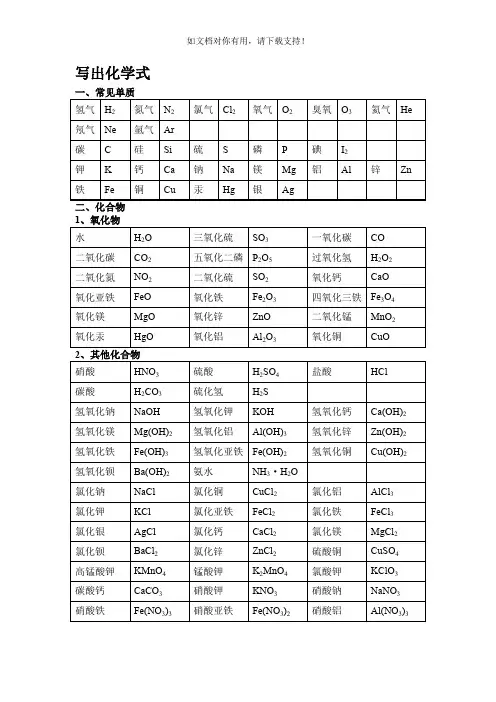
写出化学式写出物质的学名、俗名写出物质的颜色和状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;2、绿色固体:碱式碳酸铜Cu2(OH)2CO33、蓝色固体:氢氧化铜硫酸铜晶体4、紫黑色固体:高锰酸钾5、淡黄色固体:硫6、无色固体:冰干冰金刚石7、银白色固体:银铁镁铝汞等金属9、红褐色固体:氢氧化铁10、铁、镁为银白色(汞为银白色液态)11、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O43、红色固体:Cu、Fe2O3、HgO、红磷溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
(高锰酸钾溶液为紫红色)11、无色液体:水,双氧水12、蓝色溶液:硫酸铜溶液,氯化铜溶液,硝酸铜溶液13、浅绿色溶液:硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液14、黄色溶液:硫酸铁溶液,氯化铁溶液,硝酸铁溶液15、紫红色溶液:高锰酸钾溶液16、紫色溶液:石蕊溶液沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸)AgCl、(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2红褐色↓:Fe(OH)3白色↓:BaSO4其余碱。
6、(1)具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)▲注意:具有刺激性气味的液体:盐酸、硝酸、醋酸。
酒精为有特殊气体的液体。
7、有毒的,气体:CO 液体:CH3OH 固体:NaNO2 CuSO4(可作杀菌剂,与熟石灰混合配成天蓝色的粘稠状物质——波尔多液)(三)、气体的颜色17、红棕色气体:二氧化氮18、黄绿色气体:氯气19、无色气体:氧气氮气氢气二氧化碳一氧化碳二氧化硫氯化氢气体等大多数气体。
写出化学方程式一、化合反应1、镁在空气中燃烧:2Mg+ O2点燃2MgO2、铁在氧气中燃烧:3Fe +2O2点燃Fe3O43、铝在空气中燃烧:4Al+ 3O2点燃2Al2O34、氢气在空气中燃烧:2H2 +O2点燃2H2O5、红磷在空气中燃烧:4P +5O2点燃2P2O56、硫粉在空气中燃烧:S+ O2点燃27、碳在氧气中充分燃烧:C +O点燃CO28、碳在氧气中不充分燃烧:2点燃2CO9、二氧化碳通过灼热碳层:2高温2CO10、一氧化碳在氧气中燃烧:2CO +O点燃2CO211:CO2 +H2O === H2CO312、生石灰溶于水:CaO+ H2O === Ca(OH)213、无水硫酸铜作干燥剂:CuSO4 +5H2O ==== CuSO4·5H2O14、钠在氯气中燃烧:2Na+ Cl点燃2NaCl二、分解反应15、实验室用双氧水制氧气:2H2O2 MnO2 2H2O +O2↑16、加热高锰酸钾:2KMnO加热K2MnO4 + MnO2+O2↑172O 通电2H2↑+O2↑1823 === H2O +CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3高温CaO+ CO2↑三、置换反应20、铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4 +Cu21、锌和稀硫酸反应(实验室制氢气):Zn+ H2SO4 == ZnSO4+H2↑22、镁和稀盐酸反应:Mg +2HCl === MgCl2 +H2↑23、氢气还原氧化铜:H2 +CuO 加热Cu +H2O24、木炭还原氧化铜:高温2Cu +CO2↑25、甲烷在空气中燃烧:CH4点燃CO2+2H2O26、水蒸气通过灼热碳层:H2高温H2 +CO27、焦炭还原氧化铁:3C +2Fe2O3高温4Fe +3CO2↑其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+ CuSO4 == Cu(OH)2↓+ Na2SO429、甲烷在空气中燃烧:CH4 +2O2点燃CO2 +2H2O30、酒精在空气中燃烧:C2H52点燃2CO2 +3H2O31、一氧化碳还原氧化铜:CO +CuO 加热Cu+ CO232、一氧化碳还原氧化铁:3CO+ Fe23高温2Fe+ 3CO233:Ca(OH)2+ CO2 ==== CaCO3 ↓+ H2O34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+ CO2 ==== Na2CO3 +H2O35、石灰石(或小学音乐教案大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3 +2HCl === CaCl2 +H2O +CO2↑36、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO3+ 2HCl === 2NaCl +H2O +CO2↑一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg+ O2点燃2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃Fe3O43. 铜在空气中受热:2Cu+ O2加热4. 铝在空气中燃烧:4Al +3O2 点燃2Al2O35. 氢气中空气中燃烧:2H22点燃2H2O6. 红磷在空气中燃烧:4P+ 5O2点燃2P2O57. 硫粉在空气中燃烧:S +O点燃 28. 碳在氧气中充分燃烧:2点燃CO29. 碳在氧气中不充分燃烧:2点燃2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+ O2点燃2CO211. 甲烷在空气中燃烧:CH4 +2O2点燃2 2H2O12. 酒精在空气中燃烧:C2H52点燃2CO2+3H2O二.几个分解反应:13. 水在直流电的作用下分新概念英语第一册解:2H2O 通电2H2↑+ O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO3加热2CuO +H22↑15. 3 ==== 2KCl+ 3O2↑16. 加热高锰酸钾:2KMnO4 加热K2MnO4 +MnO2 +O2↑17. 碳酸不稳定而分解:H232O +CO2↑18. 高温煅烧石灰石:CaCO高温CaO +CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2+ CuO 加热Cu+ H2O20. 木炭还原氧化铜:高温2Cu +CO2↑2 初三化学方程式大合集21. 焦炭还原氧化铁:3C+ 2Fe2O高温4Fe+ 3CO2↑22. 焦炭还原四氧化三铁:2C +Fe34高温3Fe+ 2CO2↑23. 一氧化碳还原氧化铜:CO +CuO 加热Cu+ CO224. 一氧化碳还原氧化铁:3CO+ Fe23高温2Fe +3CO225. 一氧化碳还原四氧化三铁:34高温3Fe+ 4CO2(1)金属单质+酸-------- 盐+氢气(置换反应)26. 锌和稀硫酸Zn+ H2SO4 = ZnSO4+ H2↑27. 铁和稀硫酸Fe +H2SO4 = FeSO4+ H2↑28. 镁和稀硫酸Mg +H2SO4 = MgSO4 +H2↑29. 铝和稀硫酸2Al+ 3H2SO4 = Al2(SO4)3 +3H2↑30. 锌和稀盐酸Zn +2HCl === ZnCl2+ H2↑31. 铁和稀盐酸Fe+ 2HCl === FeCl2+ H2↑32. 镁和语文教案格式稀盐酸Mg 2HCl === MgCl2+ H2↑33. 铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑(2)金属单质+盐(溶液)------- 另一种金属+另一种盐34. 铁和硫酸铜溶液反应:Fe+ CuSO4 === FeSO4+ Cu35. 锌和硫酸铜溶液反应:Zn+ CuSO4 === ZnSO4+ Cu36. 铜和硝酸汞溶液反应:Cu +Hg(NO3)2 === Cu(NO3)2 +Hg(3)碱性氧化物+酸-------- 盐+水37. 氧化铁和稀盐酸反应:Fe2O3+ 6HCl === 2FeCl3+ 3H2O38. 氧化铁和稀硫酸反应:Fe2O3 +3H2SO4 === Fe2(SO4)3+ 3H2O39. 氧化铜和稀盐酸反应:CuO +2HCl ==== CuCl2 +H2O40. 氧化铜和稀硫酸反应:CuO +H2SO4 ==== CuSO4+ H2O41. 氧化镁和稀硫酸反应:MgO+ H2SO4 ==== MgSO4+ H2O42. 氧化钙和稀盐酸反应:CaO +2HCl ==== CaCl2 +H2O(4)酸性氧化物+碱-------- 盐+水43.苛性钠暴露在空气中变质:2NaOH +CO2 ==== Na2CO3+H2O44.苛性钠吸收二氧化硫气体:2NaOH +SO2 ==== Na2SO3 +H2O45.苛性钠吸收三氧化硫气体:2NaOH+ SO3 ==== Na2SO4+ H2O46.消石灰放在空气中变质:Ca(OH)2+ CO2 ==== CaCO3 ↓+ H2O47. 消石灰吸收二氧化硫:Ca(OH)2 +SO2 ==== CaSO3↓+H2O(5)酸+碱-------- 盐+水48.盐酸和烧碱起反应:HCl+ NaOH ==== NaCl+ H2O49. 盐酸和氢氧化钾反应:HCl+ KOH ==== KCl+H2O50.盐酸和氢氧化初中家长会课件铜反应:2HCl+ Cu(OH)2 ==== CuCl2 +2H2O51. 盐酸和氢氧化钙反应:2HCl+ Ca(OH)2 ==== CaCl2 +2H2O52. 盐酸和氢氧化铁反应:3HCl+ Fe(OH)3 ==== FeCl3 +3H2O53.氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 ==== AlCl3 +3H2O54.硫酸和烧碱反应:H2SO4 +2NaOH ==== Na2SO4 +2H2O55.硫酸和氢氧化钾反应:H2SO4 +2KOH ==== K2SO4 +2H2O56.硫酸和氢氧化铜反应:H2SO4 +Cu(OH)2 ==== CuSO4 +2H2O57. 硫酸和氢氧化铁反应:3H2SO4 +2Fe(OH)3==== Fe2(SO4)3+ 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O(6)酸+盐-------- 另一种酸+另一种盐59.大理石与稀盐酸反应:CaCO3 +2HCl === CaCl2 H2O +CO2↑60.碳酸钠与稀盐酸反应: Na2CO3 +2HCl === 2NaCl +H2O+ CO2↑61.碳酸镁与稀盐酸反应: MgCO3 +2HCl === MgCl2 +H2O+CO2↑62.盐酸和硝酸银溶液反应:HCl+ AgNO3=== AgCl↓+ HNO363.硫酸和碳酸钠反应:Na2CO3 +H2SO4 === Na2SO4 +H2O +CO2↑64.硫酸和氯化钡溶液反应:H2S O4 +BaCl2 ==== BaSO4↓+ 2HCl(7)碱+盐-------- 另一种碱+另一种盐65.氢氧化钠与硫酸铜:2NaOH CuSO4 ==== Cu(OH)2↓ Na2SO466.氢氧化钠与氯化铁:3NaOH FeCl3 ==== Fe(OH)3↓ 3NaCl67.氢氧化钠与氯化镁:2NaOH MgCl2 ==== Mg(OH)2↓ 2NaCl68. 氢氧化钠与氯化铜:2NaOH CuCl2 ==== Cu(OH)2↓ 2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2 Na2CO3 === CaCO3↓ 2NaOH(8)盐+盐----- 两种新盐70.氯化钠溶液新概念英语第二册和硝酸银溶液:NaCl +AgNO3==== AgCl↓+ NaNO371.硫酸钠和氯化钡:Na2SO4+ BaCl2 ==== BaSO4↓+ 2NaCl五.其它反应:72.二氧化碳溶解于水:CO2+ H2O === H2CO373.生石灰溶于水:CaO+ H2O === Ca(OH)274.氧化钠溶于水:Na2O +H2O ==== 2NaOH75.三氧化硫溶于水:SO3 +H2O ==== H2SO476.硫酸铜晶体受热分解:CuSO4·5H2O 加热CuSO4 5H2O77.无水硫酸铜作干燥剂:CuSO4+ 5H24·5H2。

初中化学式大全-空白默写版(已排版w o r d版)+答案初中化学式大全写出化学式一、常见单质二、化合物1、氧化物2、其他化合物3、常见有机化合物写出物质的学名、俗名写出物质的颜色和状态1、白色固体:2、绿色固体:3、蓝色固体:4、紫黑色固体:5、淡黄色固体:6、无色固体:7、银白色固体:9、红褐色固体:10、银白色:,(为银白色液态)11、黑色固体:溶液的颜色:凡含的溶液呈蓝色;凡含的溶液呈浅绿色;凡含的溶液呈棕黄色,其余溶液一般不无色。
(溶液为紫红色)11、无色液体:12、蓝色溶液:13、浅绿色溶液:14、黄色溶液:15、紫红色溶液:16、紫色溶液:沉淀(即不溶于水的盐和碱):①盐:白色↓:②碱:蓝色↓:红褐色↓:白色↓:6、(1)具有刺激性气体的气体:(2)无色无味的气体:▲注意:具有刺激性气味的液体:盐酸、硝酸、醋酸。
酒精为有特殊气体的液体。
7、有毒的,气体:CO 液体:CH3OH 固体:NaNO2 CuSO4(可作杀菌剂 ,与熟石灰混合配成天蓝色的粘稠状物质——波尔多液)(三)、气体的颜色17、红棕色气体:18、黄绿色气体:19、无色气体:写出化学方程式一、化合反应1、镁在空气中燃烧:2、铁在氧气中燃烧:3、铝在空气中燃烧:4、氢气在空气中燃烧:5、红磷在空气中燃烧:6、硫粉在空气中燃烧:7、碳在氧气中充分燃烧:8、8、碳在氧气中不充分燃烧:9、9、二氧化碳通过灼热碳层:10、10、一氧化碳在氧气中燃烧:11、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):12、生石灰溶于水:13、无水硫酸铜作干燥剂:14、钠在氯气中燃烧:二、分解反应15、实验室用双氧水制氧气:16、加热高锰酸钾:17、水在直流电的作用下分解:18、碳酸化学物理学报不稳定而分解:19、高温煅烧石灰石(二氧化碳工业制法):三、置换反应20、铁和硫酸铜溶液反应:21、锌和稀硫酸反应(实验室制氢气):22、镁和稀盐酸反应:23、氢气还原氧化铜:24、木炭还原氧化铜:25、甲烷在空气中燃烧:26、水蒸气通过灼热碳层:27、焦炭还原氧化铁:其他28、氢氧化钠溶液与硫酸铜溶液反应:29、甲烷在空气中燃烧:30、酒精在空气中燃烧:31、一氧化碳还原氧化铜:32、一氧化碳还原氧化铁:33、二氧化碳通过澄清石灰水(检验二氧化碳):34、氢氧化钠和二氧化碳反应(除去二氧化碳):35、35、石灰石(或小学音乐教案大理石)与稀盐酸反应(二氧化碳的实验室制法):36、碳酸钠与浓盐酸反应(泡沫灭火器的原理):一.物质与氧气的反应:二.(1)单质与氧气的反应:三.1. 镁在空气中燃烧:四.2. 铁在氧气中燃烧:五.3. 铜在空气中受热:六.4. 铝在空气中燃烧:七.5. 氢气中空气中燃烧:八.6. 红磷在空气中燃烧:九.7. 硫粉在空气中燃烧:十.8. 碳在氧气中充分燃烧:十一.9. 碳在氧气中不充分燃烧:十二.(2)化合物与氧气的反应:十三.10. 一氧化碳在氧气中燃烧:11.甲烷在空气中燃烧:12.12. 酒精在空气中燃烧:13.二.几个分解反应:14.13. 水在直流电的作用下分新概念英语第一册解:15.14. 加热碱式碳酸铜:16.15. 加热氯酸钾(有少量的二氧化锰):17.16. 加热高锰酸钾:18.17. 碳酸不稳定而分解:19.18. 高温煅烧石灰石:20.三.几个氧化还原反应:21.19. 氢气还原氧化铜:22.20. 木炭还原氧化铜:23.2 初三化学方程式大合集24.21. 焦炭还原氧化铁:25.22. 焦炭还原四氧化三铁:26.23. 一氧化碳还原氧化铜:27.24. 一氧化碳还原氧化铁:28.25. 一氧化碳还原四氧化三铁:29.四.单质、氧化物、酸、碱、盐的相互关系30.(1)金属单质+酸 -------- 盐+氢气(置换反应)31.26. 锌和稀硫酸32.27. 铁和稀硫酸33.28. 镁和稀硫酸34.29. 铝和稀硫酸35.30. 锌和稀盐酸36.31. 铁和稀盐酸37.32. 镁和语文教案格式稀盐酸38.33. 铝和稀盐酸39.(2)金属单质+盐(溶液) ------- 另一种金属+另一种盐40.34. 铁和硫酸铜溶液反应:41.35. 锌和硫酸铜溶液反应:42.36. 铜和硝酸汞溶液反应:43.(3)碱性氧化物+酸 -------- 盐+水44.37. 氧化铁和稀盐酸反应:45.38. 氧化铁和稀硫酸反应:46.39. 氧化铜和稀盐酸反应:47.40. 氧化铜和稀硫酸反应:48.41. 氧化镁和稀硫酸反应:49.42. 氧化钙和稀盐酸反应:50.(4)酸性氧化物+碱 -------- 盐+水51.43.苛性钠暴露在空气中变质:52.44.苛性钠吸收二氧化硫气体:53.45.苛性钠吸收三氧化硫气体:54.46.消石灰放在空气中变质:55.47. 消石灰吸收二氧化硫:56.(5)酸+碱 -------- 盐+水57.48.盐酸和烧碱起反应:58.49. 盐酸和氢氧化钾反应:59.50.盐酸和氢氧化铜反应:60.51. 盐酸和氢氧化钙反应:61.52. 盐酸和氢氧化铁反应:62.53.氢氧化铝药物治疗胃酸过多:63.54.硫酸和烧碱反应:64.55.硫酸和氢氧化钾反应:65.56.硫酸和氢氧化铜反应:66.57. 硫酸和氢氧化铁反应:67.58. 硝酸和烧碱反应:68.(6)酸+盐 -------- 另一种酸+另一种盐69.59.大理石与稀盐酸反应:70.60.碳酸钠与稀盐酸反应:71.61.碳酸镁与稀盐酸反应:72.62.盐酸和硝酸银溶液反应:73.63.硫酸和碳酸钠反应:74.64.硫酸和氯化钡溶液反应:75.(7)碱+盐 -------- 另一种碱+另一种盐76.65.氢氧化钠与硫酸铜:77.66.氢氧化钠与氯化铁:78.67.氢氧化钠与氯化镁:79.68. 氢氧化钠与氯化铜:80.69. 氢氧化钙与碳酸钠:81.(8)盐+盐 ----- 两种新盐82.70.氯化钠溶液和硝酸银溶液:71.硫酸钠和氯化钡:五.其它反应:72.二氧化碳溶解于水:73.生石灰溶于水:74.氧化钠溶于水:75.三氧化硫溶于水:76.硫酸铜晶体受热分解:77.无水硫酸铜作干燥剂:初中化学式大全答案写出化学式一、常见单质二、化合物1、氧化物2、其他化合物3、常见有机化合物写出物质的学名、俗名写出物质的颜色和状态3、白色固体:MgO、P2O5、CaO、 NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;2、绿色固体:碱式碳酸铜 Cu2(OH)2CO33、蓝色固体:氢氧化铜硫酸铜晶体4、紫黑色固体:高锰酸钾5、淡黄色固体:硫6、无色固体:冰干冰金刚石7、银白色固体:银铁镁铝汞等金属9、红褐色固体:氢氧化铁10、铁、镁为银白色(汞为银白色液态)11、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O43、红色固体:Cu、Fe2O3、HgO、红磷溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。

九年级化学必背知识(默写格式)1.碳酸氢铵,又称为小苏打,化学式为NH4HCO3,是一种白色固体,但稳定性较差,易受热分解。
2.中国古代的化学工艺包括造纸、火药、瓷器、青铜器的制造以及铁的冶炼。
3.空气的成分(体积分数)为:氮气(N2)78%、氧气(O2)21%、稀有气体(Ar、He、Ne、Kr、Xe)1%、二氧化碳(CO2)0.04%以及其他微量气体。
4.探究空气中氧气含量的实验可以使用磷(P)而不是镁(因为镁会产生明亮的白光)、铁(因为铁会生成铁氧化物)或者碳或蜡烛(因为它们会产生大量的烟雾)。
5.葡萄糖、面粉和蔗糖都含有碳元素,因此它们可以燃烧,但是燃烧时会产生黑色物质(炭黑)。
6.金刚石和石墨都由碳元素构成,但是它们的晶体结构不同,因此它们的物理性质也不同。
7.“铜绿”的主要成分是碱式铜盐和水合氧化铜,它是铜生锈(铜、氧气、水和二氧化碳共同作用)的产物,但是受热容易分解,生成黑色氧化铜。
8.氧气(O2)的密度比空气大,因此可以用密度法收集,它不溶于水,因此可以用水法收集,液态和固态的氧气都存在。
9.在进行蜡烛燃烧实验时,需要用干燥的氧气,因此可以用干燥法收集,如果需要纯净的氧气,则可以用分离法收集。
10.在进行铁丝燃烧实验时,需要在氧气瓶里放入干燥剂,以防止氧气中含有水分。
11.氧化反应包括燃烧和缓慢氧化,它们都能释放出能量,常见的缓慢氧化包括食物的腐烂、油漆的干燥和有机肥料的分解等。
12.纯氧可以用火柴点燃,非纯氧可以用还原剂(如磷)进行检验。
13.工业制氧气可以使用分馏法,利用氮气和氧气的沸点不同,先蒸发出氮气,留下氧气。
14.在固体加热制气体时,试管口需要倾斜放置,以防止产生的气体倒流和溢出。
15.在高锰酸钾制氧气时,管口需要放置棉花,以防止产生的气体中含有高锰酸钾颗粒。
2除臭(用臭氧)16.氧气验满:使用向上排空气法时,在氧气收集瓶中放置带火星的木条,若木条再次燃烧,则说明氧气已经满了;使用排水法收集时,若氧气收集瓶中的水已经全部被排出,则氧气已经满了。

一、常见物质的化学名俗称化学式:①氧化钙(生石灰)——C a O②氢氧化钙(熟石灰消石灰石灰乳澄清石灰水)——Ca(OH)2③碳酸钙(石灰石、大理石的主要成分)—— CaCO3④氯化钠(食盐)——NaCl⑤氢氧化钠(火碱、烧碱、苛性钠)—— NaOH⑥碳酸钠(纯碱、苏打)——Na2CO3⑦碳酸氢钠(小苏打)—— NaHCO3⑧氧化铁(铁锈、赤铁矿的主要成分)——Fe2O3⑨四氧化三铁(磁铁矿的主要成分)—— Fe3O4⑩碳(金刚石、石墨)—— C⑾二氧化碳(固态干冰)——CO2⑿水(固态冰)—— H2O⒀甲烷(天然气)——CH4⒁乙醇(酒精)—— C2H5OH⒂乙酸(醋酸)——CH3COOH二、常见物质的颜色:红色的固体——Cu、Fe2O3、P(红磷)黑色的固体——C、CuO、Fe3O4、FeO、MnO2、铁粉白色的固体——MgO、P2O5、P(白磷)、CuSO4(无水硫酸铜)、KCl、NaCl等黄色的固体—— S 蓝色的固体——CuSO4·5H2O蓝色絮状沉淀——Cu(OH)2红褐色絮状沉淀——Fe(OH)3常见不溶于酸的白色沉淀——BaSO4、AgCl溶于酸并产生二氧化碳气体的白色沉淀——BaCO3、CaCO3等不溶性碳酸盐的沉淀溶于酸但不产生气体的白色沉淀——Mg(OH)2、Al(OH)3等不溶性碱的沉淀蓝色的溶液—— CuSO4、CuCl2、Cu(NO3)2等含Cu2+溶液浅绿色的溶液——FeSO4、FeCl2、Fe(NO3)2等含Fe2+溶液黄色的溶液——FeCl3、Fe2(SO4)3、Fe(NO3)3等含Fe3+溶液三、常见气体(1)具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)◎干燥剂的选择:1、浓硫酸可干燥:酸性气体(如:CO2、SO2、SO3、NO2、HCl、)中性气体(如:H2、O2、N2、CO)※不能干燥碱性气体(如:NH3)2、氢氧化钠固体、生石灰、碱石灰可干燥:碱性气体(如:NH3)中性气体(如:H2、O2、N2、CO)※不能干燥酸性气体(如:CO2、SO2、SO3、NO2、HCl、)3、无水硫酸铜固体遇水由白色变蓝色,可检验水的存在,并吸收水蒸气。
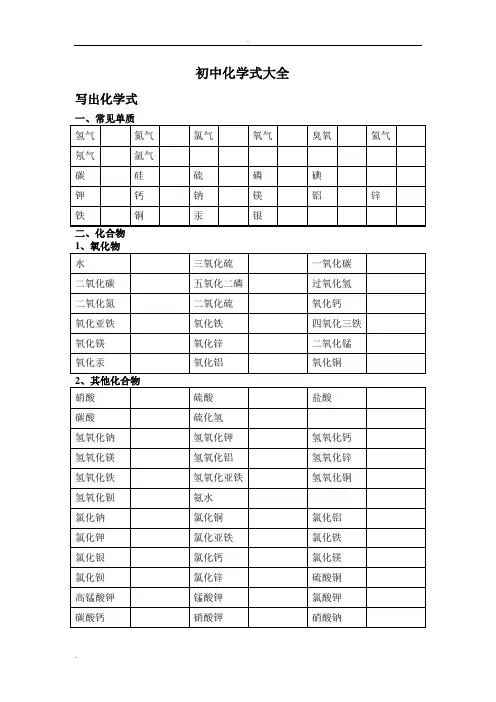
初中化学式大全写出化学式写出物质的学名、俗名写出物质的颜色和状态1、白色固体:2、绿色固体:3、蓝色固体:4、紫黑色固体:6、无色固体:7、银白色固体:9、红褐色固体:10、银白色:,(为银白色液态)11、黑色固体:溶液的颜色:凡含的溶液呈蓝色;凡含的溶液呈浅绿色;凡含的溶液呈棕黄色,其余溶液一般不无色。
(溶液为紫红色)11、无色液体:12、蓝色溶液:13、浅绿色溶液:14、黄色溶液:15、紫红色溶液:16、紫色溶液:沉淀(即不溶于水的盐和碱):①盐:白色↓:等②碱:蓝色↓:红褐色↓:白色↓:6、(1)具有刺激性气体的气体:(2)无色无味的气体:▲注意:具有刺激性气味的液体:盐酸、硝酸、醋酸。
酒精为有特殊气体的液体。
7、有毒的,气体:CO 液体:CH3OH 固体:NaNO2 CuSO4(可作杀菌剂,与熟石灰混合配成天蓝色的粘稠状物质——波尔多液)(三)、气体的颜色18、黄绿色气体:19、无色气体:写出化学方程式一、化合反应1、镁在空气中燃烧:2、铁在氧气中燃烧:3、铝在空气中燃烧:4、氢气在空气中燃烧:5、红磷在空气中燃烧:6、硫粉在空气中燃烧:7、碳在氧气中充分燃烧:8、碳在氧气中不充分燃烧:9、二氧化碳通过灼热碳层:10、一氧化碳在氧气中燃烧:11、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):12、生石灰溶于水:13、无水硫酸铜作干燥剂:14、钠在氯气中燃烧:二、分解反应15、实验室用双氧水制氧气:16、加热高锰酸钾:17、水在直流电的作用下分解:18、碳酸化学物理学报不稳定而分解:19、高温煅烧石灰石(二氧化碳工业制法):三、置换反应20、铁和硫酸铜溶液反应:21、锌和稀硫酸反应(实验室制氢气):22、镁和稀盐酸反应:23、氢气还原氧化铜:24、木炭还原氧化铜:25、甲烷在空气中燃烧:26、水蒸气通过灼热碳层:27、焦炭还原氧化铁:其他28、氢氧化钠溶液与硫酸铜溶液反应:29、甲烷在空气中燃烧:30、酒精在空气中燃烧:31、一氧化碳还原氧化铜:32、一氧化碳还原氧化铁:33、二氧化碳通过澄清石灰水(检验二氧化碳):34、氢氧化钠和二氧化碳反应(除去二氧化碳):35、石灰石(或小学音乐教案大理石)与稀盐酸反应(二氧化碳的实验室制法):36、碳酸钠与浓盐酸反应(泡沫灭火器的原理):一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2. 铁在氧气中燃烧:3. 铜在空气中受热:4. 铝在空气中燃烧:5. 氢气中空气中燃烧:6. 红磷在空气中燃烧:7. 硫粉在空气中燃烧:8. 碳在氧气中充分燃烧:9. 碳在氧气中不充分燃烧:(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:11.甲烷在空气中燃烧:12. 酒精在空气中燃烧:二.几个分解反应:13. 水在直流电的作用下分新概念英语第一册解:14. 加热碱式碳酸铜:15. 加热氯酸钾(有少量的二氧化锰):16. 加热高锰酸钾:17. 碳酸不稳定而分解:18. 高温煅烧石灰石:三.几个氧化还原反应:19. 氢气还原氧化铜:20. 木炭还原氧化铜:2 初三化学方程式大合集21. 焦炭还原氧化铁:22. 焦炭还原四氧化三铁:23. 一氧化碳还原氧化铜:24. 一氧化碳还原氧化铁:25. 一氧化碳还原四氧化三铁:四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质+酸-------- 盐+氢气(置换反应)26. 锌和稀硫酸27. 铁和稀硫酸28. 镁和稀硫酸29. 铝和稀硫酸30. 锌和稀盐酸31. 铁和稀盐酸32. 镁和语文教案格式稀盐酸33. 铝和稀盐酸(2)金属单质+盐(溶液)------- 另一种金属+另一种盐34. 铁和硫酸铜溶液反应:35. 锌和硫酸铜溶液反应:36. 铜和硝酸汞溶液反应:(3)碱性氧化物+酸-------- 盐+水37. 氧化铁和稀盐酸反应:38. 氧化铁和稀硫酸反应:39. 氧化铜和稀盐酸反应:40. 氧化铜和稀硫酸反应:41. 氧化镁和稀硫酸反应:42. 氧化钙和稀盐酸反应:(4)酸性氧化物+碱-------- 盐+水43.苛性钠暴露在空气中变质:44.苛性钠吸收二氧化硫气体:45.苛性钠吸收三氧化硫气体:46.消石灰放在空气中变质:47. 消石灰吸收二氧化硫:(5)酸+碱-------- 盐+水48.盐酸和烧碱起反应:49. 盐酸和氢氧化钾反应:50.盐酸和氢氧化铜反应:51. 盐酸和氢氧化钙反应:52. 盐酸和氢氧化铁反应:53.氢氧化铝药物治疗胃酸过多:54.硫酸和烧碱反应:55.硫酸和氢氧化钾反应:56.硫酸和氢氧化铜反应:57. 硫酸和氢氧化铁反应:58. 硝酸和烧碱反应:(6)酸+盐-------- 另一种酸+另一种盐59.大理石与稀盐酸反应:60.碳酸钠与稀盐酸反应:61.碳酸镁与稀盐酸反应:62.盐酸和硝酸银溶液反应:63.硫酸和碳酸钠反应:64.硫酸和氯化钡溶液反应:(7)碱+盐-------- 另一种碱+另一种盐65.氢氧化钠与硫酸铜:66.氢氧化钠与氯化铁:67.氢氧化钠与氯化镁:68. 氢氧化钠与氯化铜:69. 氢氧化钙与碳酸钠:(8)盐+盐----- 两种新盐70.氯化钠溶液和硝酸银溶液:71.硫酸钠和氯化钡:五.其它反应:72.二氧化碳溶解于水:73.生石灰溶于水:74.氧化钠溶于水:75.三氧化硫溶于水:76.硫酸铜晶体受热分解:77.无水硫酸铜作干燥剂:初中化学式大全答案写出化学式写出物质的学名、俗名写出物质的颜色和状态3、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;2、绿色固体:碱式碳酸铜Cu2(OH)2CO33、蓝色固体:氢氧化铜硫酸铜晶体4、紫黑色固体:高锰酸钾5、淡黄色固体:硫6、无色固体:冰干冰金刚石7、银白色固体:银铁镁铝汞等金属9、红褐色固体:氢氧化铁10、铁、镁为银白色(汞为银白色液态)11、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O43、红色固体:Cu、Fe2O3、HgO、红磷溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
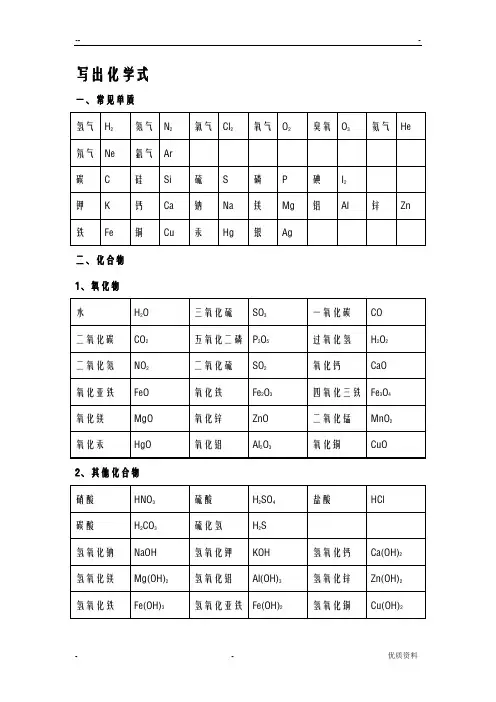
写出化学式一、常见单质二、化合物1、氧化物2、其他化合物3、常见有机化合物写出物质的学名、俗名写出物质的颜色和状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;2、绿色固体:碱式碳酸铜Cu2(OH)2CO33、蓝色固体:氢氧化铜硫酸铜晶体4、紫黑色固体:高锰酸钾5、淡黄色固体:硫6、无色固体:冰干冰金刚石7、银白色固体:银铁镁铝汞等金属9、红褐色固体:氢氧化铁10、铁、镁为银白色(汞为银白色液态)11、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O43、红色固体:Cu、Fe2O3、HgO、红磷溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
(高锰酸钾溶液为紫红色)11、无色液体:水,双氧水12、蓝色溶液:硫酸铜溶液,氯化铜溶液,硝酸铜溶液13、浅绿色溶液:硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液14、黄色溶液:硫酸铁溶液,氯化铁溶液,硝酸铁溶液15、紫红色溶液:高锰酸钾溶液16、紫色溶液:石蕊溶液沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸)AgCl、BaSO4(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2红褐色↓:Fe(OH)3白色↓:其余碱。
6、(1)具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)▲注意:具有刺激性气味的液体:盐酸、硝酸、醋酸。
酒精为有特殊气体的液体。
7、有毒的,气体:CO 液体:CH3OH 固体:NaNO2CuSO4(可作杀菌剂,与熟石灰混合配成天蓝色的粘稠状物质——波尔多液)(三)、气体的颜色17、红棕色气体:二氧化氮18、黄绿色气体:氯气19、无色气体:氧气氮气氢气二氧化碳一氧化碳二氧化硫氯化氢气体等大多数气体。

化学式大全默写答案一、常见单质氢气:H2氖气:Ne碳:C钾:K铁:Fe氮气:N2氩气:Ar硅:Si钙:Ca铜:Cu氯气:Cl2硫:S钠:Na汞:Hg氧气:O2磷:P镁:Mg银:Ag臭氧:O3碘:I2铝:Al氦气:He锌:Zn二、化合物1、氧化物水:H2O二氧化碳:CO2二氧化氮:NO2氧化亚铁:FeO氧化镁:MgO氧化汞:HgO三氧化硫:SO3一氧化碳:CO过氧化氢:H2O2 氧化钙:CaO五氧化二磷:P2O5二氧化硫:SO2氧化铁:Fe2O3氧化锌:ZnO氧化铝:Al2O3硫酸:H2SO4硫化氢:H2S氢氧化钾:___氢氧化铝:Al(OH)3 氢氧化亚铁:Fe(OH)2 氨水:NH3·H2O氯化铜:CuCl2氯化亚铁:FeCl2氯化钙:CaCl2氯化锌:ZnCl2锰酸钾:KMnO4硝酸钾:KNO3硝酸亚铁:Fe(NO3)2 硫酸铜:CuSO4氯酸钾:KClO3硝酸钠:NaNO3硝酸铝:Al(NO3)3碳酸钠:Na2CO3碳酸氢钠:NaHCO3硝酸银:AgNO3硫酸钡:BaSO4甲烷:CH4乙醇:C2H5OH碳酸铵:(NH4)2CO3硫酸___:FeSO4硝酸铵:NH4NO3葡萄糖:C6H12O6三、常见有机化合物金刚石、石墨:C干冰(固体二氧化碳):CO2水银、汞Hg、苛性钠、火碱NaOH、生石灰CaO、碳酸钠晶体Na2CO3·10H2O、钙酒精、乙醇C2H5OH、氨气NH3、盐酸、氢氯酸HCl、胆矾、蓝矾、硫酸铜晶体CuSO4·5H2O、亚硫酸H2SO3、碳酸氢钠、小苏打NaHCO3、氢硫酸H2S、甲醇CH3OH、熟石灰、消石Ca(OH)2、醋酸、乙酸CH3COOH、灰、纯碱Na2CO3、亚硝酸钠NaNO2、氨水、一水合NH3·H2O、铜绿、孔雀石Cu2(OH)2CO3.以下是一些化学物质的名称和性质:1、白色固体:氧化镁(MgO)、五氧化二磷(P2O5)、氧化钙(CaO)、氢氧化钠(NaOH)、氢氧化钙(Ca(OH)2)、高氯酸钾(KClO3)、氯化钾(KCl)、碳酸钠(Na2CO3)、氯化钠(NaCl)、无水硫酸铜(CuSO4);2、绿色固体:碱式碳酸铜(Cu2(OH)2CO3);3、蓝色固体:氢氧化铜、硫酸铜晶体;4、紫黑色固体:高锰酸钾;5、淡黄色固体:硫;6、无色固体:干冰、金刚石;7、银白色固体:银、铁、镁、铝、汞等金属;8、红褐色固体:氢氧化铁;9、铁、镁为银白色(汞为银白色液态);10、黑色固体:石墨、炭粉、铁粉、氧化铜、二氧化锰、三氧化二铁;11、红色固体:铜、三氧化二铁、氧化汞、红磷。

写出化学式写出物质的学名、俗名写出物质的颜色和状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;2、绿色固体:碱式碳酸铜Cu2(OH)2CO33、蓝色固体:氢氧化铜硫酸铜晶体4、紫黑色固体:高锰酸钾5、淡黄色固体:硫6、无色固体:冰干冰金刚石7、银白色固体:银铁镁铝汞等金属9、红褐色固体:氢氧化铁10、铁、镁为银白色(汞为银白色液态)11、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O43、红色固体:Cu、Fe2O3、HgO、红磷溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
(高锰酸钾溶液为紫红色)11、无色液体:水,双氧水12、蓝色溶液:硫酸铜溶液,氯化铜溶液,硝酸铜溶液13、浅绿色溶液:硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液14、黄色溶液:硫酸铁溶液,氯化铁溶液,硝酸铁溶液15、紫红色溶液:高锰酸钾溶液16、紫色溶液:石蕊溶液沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸)AgCl、(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2红褐色↓:Fe(OH)3白色↓:BaSO4其余碱。
6、(1)具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)▲留意:具有刺激性气味的液体:盐酸、硝酸、醋酸。
酒精为有特别气体的液体。
7、有毒的,气体:CO 液体:CH3OH 固体:NaNO2 CuSO4(可作杀菌剂,及熟石灰混合配成天蓝色的粘稠状物质——波尔多液)(三)、气体的颜色17、红棕色气体:二氧化氮18、黄绿色气体:氯气19、无色气体:氧气氮气氢气二氧化碳一氧化碳二氧化硫氯化氢气体等大多数气体。
写出化学方程式一、化合反响1、镁在空气中燃烧:2Mg+ O2点燃2MgO2、铁在氧气中燃烧:3Fe +2O2点燃Fe3O43、铝在空气中燃烧:4Al+ 3O2点燃2Al2O34、氢气在空气中燃烧:2H2 +O2点燃2H2O5、红磷在空气中燃烧:4P +5O2点燃2P2O56、硫粉在空气中燃烧:S+ O2点燃27、碳在氧气中充分燃烧:C +O点燃CO28、碳在氧气中不充分燃烧:2点燃2CO9、二氧化碳通过灼热碳层:2高温2CO10、一氧化碳在氧气中燃烧:2CO +O点燃2CO211:CO2 +H2O === H2CO312、生石灰溶于水:CaO+ H2O === Ca(OH)213、无水硫酸铜作枯燥剂:CuSO4 +5H2O ==== CuSO4·5H2O14、钠在氯气中燃烧:2Na+ Cl点燃2NaCl二、分解反响15、试验室用双氧水制氧气:2H2O2 MnO2 2H2O +O2↑16、加热高锰酸钾:2KMnO加热K2MnO4 + MnO2+O2↑172O 通电2H2↑+O2↑18、碳酸化学物理学报不稳定而分解:H2CO3 === H2O +CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3高温CaO+ CO2↑三、置换反响20、铁和硫酸铜溶液反响:Fe+ CuSO4 == FeSO4 +Cu21、锌和稀硫酸反响(试验室制氢气):Zn+ H2SO4 == ZnSO4+H2↑22、镁和稀盐酸反响:Mg +2HCl === MgCl2 +H2↑23、氢气复原氧化铜:H2 +CuO 加热Cu +H2O24、木炭复原氧化铜:高温2Cu +CO2↑25、甲烷在空气中燃烧:CH4点燃CO2+2H2O26、水蒸气通过灼热碳层:H2高温H2 +CO27、焦炭复原氧化铁:3C +2Fe2O3高温4Fe +3CO2↑其他28、氢氧化钠溶液及硫酸铜溶液反响:2NaOH+ CuSO4 == Cu(OH)2↓+ Na2SO429、甲烷在空气中燃烧:CH4 +2O2点燃CO2 +2H2O30、酒精在空气中燃烧:C2H52点燃2CO2 +3H2O31、一氧化碳复原氧化铜:CO +CuO 加热Cu+ CO232、一氧化碳复原氧化铁:3CO+ Fe23高温2Fe+ 3CO233:Ca(OH)2+ CO2 ==== CaCO3 ↓+ H2O34、氢氧化钠和二氧化碳反响(除去二氧化碳):2NaOH+ CO2 ==== Na2CO3 +H2O35、石灰石(或小学音乐教案大理石)及稀盐酸反响(二氧化碳的试验室制法):CaCO3 +2HCl === CaCl2 +H2O +CO2↑36、碳酸钠及浓盐酸反响(泡沫灭火器的原理): Na2CO3+ 2HCl === 2NaCl +H2O +CO2↑一.物质及氧气的反响:(1)单质及氧气的反响:1. 镁在空气中燃烧:2Mg+ O2点燃2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃Fe3O43. 铜在空气中受热:2Cu+ O2加热4. 铝在空气中燃烧:4Al +3O2 点燃2Al2O35. 氢气中空气中燃烧:2H22点燃2H2O6. 红磷在空气中燃烧:4P+ 5O2点燃2P2O57. 硫粉在空气中燃烧:S +O点燃 28. 碳在氧气中充分燃烧:2点燃CO29. 碳在氧气中不充分燃烧:2点燃2CO(2)化合物及氧气的反响:10. 一氧化碳在氧气中燃烧:2CO+ O2点燃2CO211. 甲烷在空气中燃烧:CH4 +2O2点燃CO2 2H2O12. 酒精在空气中燃烧:C2H52点燃2CO2+3H2O二.几个分解反响:13. 水在直流电的作用下分新概念英语第一册解:2H2O 通电2H2↑+ O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO3加热2CuO +H22↑15. 3 ==== 2KCl+ 3O2↑16. 加热高锰酸钾:2KMnO4 加热K2MnO4 +MnO2 +O2↑17. 碳酸不稳定而分解:H2CO3 === H2O +CO2↑18. 高温煅烧石灰石:CaCO高温CaO +CO2↑三.几个氧化复原反响:19. 氢气复原氧化铜:H2+ CuO 加热Cu+ H2O20. 木炭复原氧化铜:高温2Cu +CO2↑2 初三化学方程式大合集21. 焦炭复原氧化铁:3C+ 2Fe2O高温4Fe+ 3CO2↑22. 焦炭复原四氧化三铁:2C +Fe34高温3Fe+ 2CO2↑23. 一氧化碳复原氧化铜:CO +CuO 加热Cu+ CO224. 一氧化碳复原氧化铁:3CO+ Fe23高温2Fe +3CO225. 一氧化碳复原四氧化三铁:34高温3Fe+ 4CO2(1)金属单质+酸-------- 盐+氢气(置换反响)26. 锌和稀硫酸Zn+ H2SO4 = ZnSO4+ H2↑27. 铁和稀硫酸Fe +H2SO4 = FeSO4+ H2↑28. 镁和稀硫酸Mg +H2SO4 = MgSO4 +H2↑29. 铝和稀硫酸2Al+ 3H2SO4 = Al2(SO4)3 +3H2↑30. 锌和稀盐酸Zn +2HCl === ZnCl2+ H2↑31. 铁和稀盐酸Fe+ 2HCl === FeCl2+ H2↑32. 镁和语文教案格式稀盐酸Mg 2HCl === MgCl2+ H2↑33. 铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑(2)金属单质+盐(溶液)------- 另一种金属+另一种盐34. 铁和硫酸铜溶液反响:Fe+ CuSO4 === FeSO4+ Cu35. 锌和硫酸铜溶液反响:Zn+ CuSO4 === ZnSO4+ Cu36. 铜和硝酸汞溶液反响:Cu +Hg(NO3)2 === Cu(NO3)2 +Hg(3)碱性氧化物+酸-------- 盐+水37. 氧化铁和稀盐酸反响:Fe2O3+ 6HCl === 2FeCl3+ 3H2O38. 氧化铁和稀硫酸反响:Fe2O3 +3H2SO4 === Fe2(SO4)3+ 3H2O39. 氧化铜和稀盐酸反响:CuO +2HCl ==== CuCl2 +H2O40. 氧化铜和稀硫酸反响:CuO +H2SO4 ==== CuSO4+ H2O41. 氧化镁和稀硫酸反响:MgO+ H2SO4 ==== MgSO4+ H2O42. 氧化钙和稀盐酸反响:CaO +2HCl ==== CaCl2 +H2O(4)酸性氧化物+碱-------- 盐+水43.苛性钠暴露在空气中变质:2NaOH +CO2 ==== Na2CO3+H2O44.苛性钠汲取二氧化硫气体:2NaOH +SO2 ==== Na2SO3 +H2O45.苛性钠汲取三氧化硫气体:2NaOH+ SO3 ==== Na2SO4+ H2O46.消石灰放在空气中变质:Ca(OH)2+ CO2 ==== CaCO3 ↓+ H2O47. 消石灰汲取二氧化硫:Ca(OH)2 +SO2 ==== CaSO3↓+H2O(5)酸+碱-------- 盐+水48.盐酸和烧碱起反响:HCl+ NaOH ==== NaCl+ H2O49. 盐酸和氢氧化钾反响:HCl+ KOH ==== KCl+H2O50.盐酸和氢氧化初中家长会课件铜反响:2HCl+ Cu(OH)2 ==== CuCl2 +2H2O51. 盐酸和氢氧化钙反响:2HCl+ Ca(OH)2 ==== CaCl2 +2H2O52. 盐酸和氢氧化铁反响:3HCl+ Fe(OH)3 ==== FeCl3 +3H2O53.氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 ==== AlCl3 +3H2O54.硫酸和烧碱反响:H2SO4 +2NaOH ==== Na2SO4 +2H2O55.硫酸和氢氧化钾反响:H2SO4 +2KOH ==== K2SO4 +2H2O56.硫酸和氢氧化铜反响:H2SO4 +Cu(OH)2 ==== CuSO4 +2H2O57. 硫酸和氢氧化铁反响:3H2SO4 +2Fe(OH)3==== Fe2(SO4)3+ 6H2O58. 硝酸和烧碱反响:HNO3+ NaOH ==== NaNO3 +H2O(6)酸+盐-------- 另一种酸+另一种盐59.大理石及稀盐酸反响:CaCO3 +2HCl === CaCl2 H2O +CO2↑60.碳酸钠及稀盐酸反响: Na2CO3 +2HCl === 2NaCl +H2O+ CO2↑61.碳酸镁及稀盐酸反响: MgCO3 +2HCl === MgCl2 +H2O+CO2↑62.盐酸和硝酸银溶液反响:HCl+ AgNO3=== AgCl↓+ HNO363.硫酸和碳酸钠反响:Na2CO3 +H2SO4 === Na2SO4 +H2O +CO2↑64.硫酸和氯化钡溶液反响:H2S O4 +BaCl2 ==== BaSO4↓+ 2HCl(7)碱+盐-------- 另一种碱+另一种盐65.氢氧化钠及硫酸铜:2NaOH CuSO4 ==== Cu(OH)2↓ Na2SO466.氢氧化钠及氯化铁:3NaOH FeCl3 ==== Fe(OH)3↓ 3NaCl67.氢氧化钠及氯化镁:2NaOH MgCl2 ==== Mg(OH)2↓ 2NaCl68. 氢氧化钠及氯化铜:2NaOH CuCl2 ==== Cu(OH)2↓ 2NaCl69. 氢氧化钙及碳酸钠:Ca(OH)2 Na2CO3 === CaCO3↓ 2NaOH(8)盐+盐----- 两种新盐70.氯化钠溶液新概念英语第二册和硝酸银溶液:NaCl +AgNO3==== AgCl↓+ NaNO371.硫酸钠和氯化钡:Na2SO4+ BaCl2 ==== BaSO4↓+ 2NaCl五.其它反响:72.二氧化碳溶解于水:CO2+ H2O === H2CO373.生石灰溶于水:CaO+ H2O === Ca(OH)274.氧化钠溶于水:Na2O +H2O ==== 2NaOH75.三氧化硫溶于水:SO3 +H2O ==== H2SO476.硫酸铜晶体受热分解:CuSO4·5H2O 加热CuSO4 5H2O77.无水硫酸铜作枯燥剂:CuSO4+ 5H24·5H2。
初中化学常见物质的俗称和化学式(常考部分)①生石灰—— CaO②熟石灰——Ca(OH)2③石灰石、大理石—— CaCO3④食盐——NaCl⑤火碱、烧碱、苛性钠—— NaOH⑥纯碱、苏打——Na2CO3⑦小苏打—— NaHCO3⑧铁锈、赤铁矿——Fe2O 3⑨磁铁矿—— Fe3O4⑩金刚石、石墨、木炭—— C⑾干冰——CO2⑿冰—— H2O⒀天然气(甲烷)——CH4⒁酒精(乙醇)—— C2H5 OH⒂醋酸(乙酸)——CH3COOH(16)双氧水(过氧化氢)—— H2O 2(17)水银(汞)—— Hg (18)尿素(碳酰胺)—— CO(NH2)2(材料题拓展部分)①铜绿、铜锈、孔雀石(碱式碳酸铜)—— Cu2(OH)2CO3:②碱石灰(氢氧化钠、氧化钙混合)—— NaOH 与CaO③明矾(十二水硫酸铝钾)—— KAl(SO4)2.12H2O④胆矾、蓝矾(五水硫酸铜)—— CuSO4.5H2O⑤草木灰(碳酸钾)—— K2CO3⑥硝石(硝酸钾)—— KNO3⑦漂白粉(次氯酸钙)—— Ca(ClO)2⑧漂白液(次氯酸钠)—— NaClO⑨石英、石英、水晶、玛瑙、砂子(二氧化硅)——SiO2⑩辉铜矿(硫化亚铜)——Cu2S⑾赤铜矿(氧化亚铜)—— Cu2O⑿菱铁矿(碳酸亚铁)—— FeCO3。
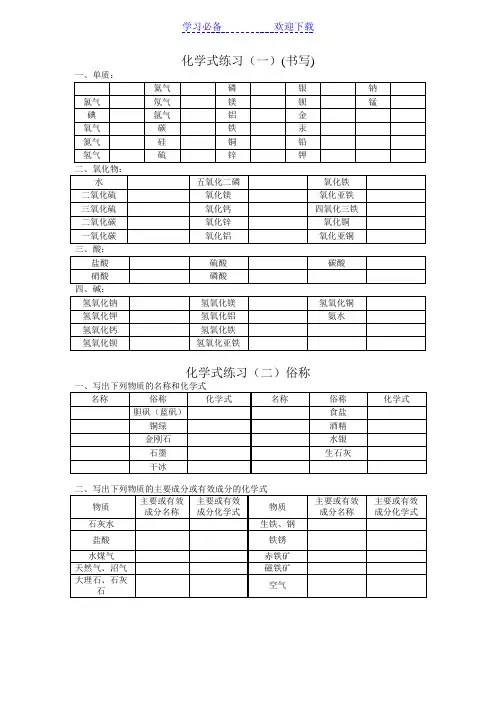
初中化学常用物质化学式、俗称(OH)3氢氧化铝:胃舒平的主要成分硫酸钡:钡餐、重晶石碳:金刚石、石墨、木炭、活性炭、焦炭、煤的主要成分(ClO)2和CaCl2次氯酸钙和氯化钙混合物:漂白粉(次氯酸钙)5.CaO氧化钙:生石灰6.CaO、NaOH氧化钙和氢氧化钠混合物:碱石灰7.Ca(OH)2氢氧化钙:熟石灰、石灰水8.CaCO3碳酸钙:石灰石、大理石9.硫酸钙晶体:(生)石膏10.(CaSO4)硫酸钙晶体:熟石膏11.CH4:甲烷、天然气、瓦斯、沼气12.C2H5OH:乙醇、酒精13.CH3COOH:乙酸、醋酸14.C6H12O6:葡萄糖15.CO2二氧化碳:干冰、碳酸气16.CO和H2混合气:水煤气,CO:煤气17. CO(NH2)2:尿素18.CuSO45H2O硫酸铜晶体:蓝矾、胆矾19.Cu2(OH)2CO3碱式碳酸铜:铜绿、铜锈、孔雀石20.Cu SO4和Ca(OH)2:波尔多液21.FeSO47H2O硫酸亚铁晶体:绿矾22.Fe2O3氧化铁:铁锈和赤铁矿主要成分23.Fe3O4四氧化三铁:磁铁矿、烤蓝、烤黑24.Hg汞:水银25.HCl氯化氢:氢氯酸、盐酸、胃酸的主要成分26.H2O2过氧化氢:双氧水27.H2和O2混合气:爆鸣气28.KAl(SO4)十二水硫酸铝钾:明矾29.K2CO3碳酸钾:草木灰主要成分30.KOH氢氧化钾:苛性钾31.NaOH氢氧化钠:苛性钠、烧碱,火碱32.Na2CO3碳酸钠:纯碱、苏打33.NaHCO3碳酸氢钠:小苏打34.:纯碱晶体、石碱、口碱35.Na2SiO3硅酸钠:水玻璃36.NaCl氯化钠:食盐37.Na2S2O3硫代硫酸钠:大苏打、海波38.NH4HCO3碳酸氢铵:碳铵39.(NH4)2SO4硫酸铵:硫铵40.NH4NO3硝酸铵:硝铵41.NH3H2O:一水合氨、氨水42.P磷:白磷、红磷、黄磷43.S硫:硫磺44.SiO2二氧化硅:石英、石英砂、水晶45.Fe:生铁、钢、不锈钢的主要成分初中化学常用物质化学式、俗称(默写练习一)(OH)3氢氧化铝:硫酸钡:碳:(ClO)2和CaCl2次氯酸钙和氯化钙混合物:5.CaO氧化钙:6.CaO、NaOH氧化钙和氢氧化钠混合物:7.Ca(OH)2氢氧化钙:8.CaCO3碳酸钙:9.硫酸钙晶体:10.(CaSO4)硫酸钙晶体:11.CH4:12.C2H5OH:13.CH3COOH:14.C6H12O6:15.CO2二氧化碳:16.CO和H2混合气: ,CO:17. CO(NH2)2:18.CuSO45H2O硫酸铜晶体:19.Cu2(OH)2CO3碱式碳酸铜:20.Cu SO4和Ca(OH)2:21.FeSO47H2O硫酸亚铁晶体:22.Fe2O3氧化铁:23.Fe3O4四氧化三铁:24.Hg汞:25.HCl氯化氢:26.H2O2过氧化氢:27.H2和O2混合气:28.KAl(SO4)十二水硫酸铝钾:29.K2CO3碳酸钾:30.KOH氢氧化钾:31.NaOH氢氧化钠:32.Na2CO3碳酸钠:33.NaHCO3碳酸氢钠:34.:35.Na2SiO3硅酸钠:36.NaCl氯化钠:37.Na2S2O3硫代硫酸钠:38.NH4HCO3碳酸氢铵:39.(NH4)2SO4硫酸铵:40.NH4NO3硝酸铵:41.NH3H2O:42.P磷:43.S硫:44.SiO2二氧化硅:45.Fe:初中化学常用物质化学式、俗称(默写练习二)1. :胃舒平的主要成分2. :钡餐、重晶石3. :金刚石、石墨、木炭、活性炭、焦炭、煤的主要成分4. :漂白粉(次氯酸钙)5.:生石灰6.:碱石灰7.:熟石灰、石灰水8.:石灰石、大理石9.:(生)石膏10.:熟石膏11.:甲烷、天然气、瓦斯、沼气12.:乙醇、酒精13.:乙酸、醋酸14.:葡萄糖15.:干冰、碳酸气16.:水煤气,CO:煤气17. :尿素18.:蓝矾、胆矾19.:铜绿、铜锈、孔雀石20.:波尔多液21.:绿矾22.:铁锈和赤铁矿主要成分23.:磁铁矿、烤蓝、烤黑24.:水银25.:氢氯酸、盐酸、胃酸的主要成分26.:双氧水27.:爆鸣气28. :明矾29.:草木灰主要成分30.:苛性钾31.:苛性钠、烧碱,火碱32.:纯碱、苏打33.:小苏打34.:纯碱晶体、石碱、口碱35. :水玻璃36.:食盐37.:大苏打、海波38.:碳铵39.:硫铵40.:硝铵41.:一水合氨、氨水42. :白磷、红磷、黄磷43.:硫磺44.:石英、石英砂、水晶45.:生铁、钢、不锈钢的主要成分。
写出化学式写出物质的学名、俗名写出物质的颜色和状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;2、绿色固体:碱式碳酸铜Cu2(OH)2CO33、蓝色固体:氢氧化铜硫酸铜晶体4、紫黑色固体:高锰酸钾5、淡黄色固体:硫6、无色固体:冰干冰金刚石7、银白色固体:银铁镁铝汞等金属9、红褐色固体:氢氧化铁10、铁、镁为银白色(汞为银白色液态)11、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O43、红色固体:Cu、Fe2O3、HgO、红磷溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
(高锰酸钾溶液为紫红色)11、无色液体:水,双氧水12、蓝色溶液:硫酸铜溶液,氯化铜溶液,硝酸铜溶液13、浅绿色溶液:硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液14、黄色溶液:硫酸铁溶液,氯化铁溶液,硝酸铁溶液15、紫红色溶液:高锰酸钾溶液16、紫色溶液:石蕊溶液沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸)AgCl、(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2红褐色↓:Fe(OH)3白色↓:BaSO4其余碱。
6、(1)具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)▲注意:具有刺激性气味的液体:盐酸、硝酸、醋酸。
酒精为有特殊气体的液体。
7、有毒的,气体:CO 液体:CH3OH 固体:NaNO2 CuSO4(可作杀菌剂,与熟石灰混合配成天蓝色的粘稠状物质——波尔多液)(三)、气体的颜色17、红棕色气体:二氧化氮18、黄绿色气体:氯气19、无色气体:氧气氮气氢气二氧化碳一氧化碳二氧化硫氯化氢气体等大多数气体。
写出化学方程式一、化合反应1、镁在空气中燃烧:2Mg+ O2点燃2MgO2、铁在氧气中燃烧:3Fe +2O2点燃Fe3O43、铝在空气中燃烧:4Al+ 3O2点燃2Al2O34、氢气在空气中燃烧:2H2 +O2点燃2H2O5、红磷在空气中燃烧:4P +5O2点燃2P2O56、硫粉在空气中燃烧:S+ O2点燃27、碳在氧气中充分燃烧:C +O点燃CO28、碳在氧气中不充分燃烧:2点燃2CO9、二氧化碳通过灼热碳层:2高温2CO10、一氧化碳在氧气中燃烧:2CO +O点燃2CO211:CO2 +H2O === H2CO312、生石灰溶于水:CaO+ H2O === Ca(OH)213、无水硫酸铜作干燥剂:CuSO4 +5H2O ==== CuSO4·5H2O14、钠在氯气中燃烧:2Na+ Cl点燃2NaCl二、分解反应15、实验室用双氧水制氧气:2H2O2 MnO2 2H2O +O2↑16、加热高锰酸钾:2KMnO加热K2MnO4 + MnO2+O2↑172O 通电2H2↑+O2↑18、碳酸化学物理学报不稳定而分解:H2CO3 === H2O +CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3高温CaO+ CO2↑三、置换反应20、铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4 +Cu21、锌和稀硫酸反应(实验室制氢气):Zn+ H2SO4 == ZnSO4+H2↑22、镁和稀盐酸反应:Mg +2HCl === MgCl2 +H2↑23、氢气还原氧化铜:H2 +CuO 加热Cu +H2O24、木炭还原氧化铜:高温2Cu +CO2↑25、甲烷在空气中燃烧:CH4点燃CO2+2H2O26、水蒸气通过灼热碳层:H2高温H2 +CO27、焦炭还原氧化铁:3C +2Fe2O3高温4Fe +3CO2↑其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+ CuSO4 == Cu(OH)2↓+ Na2SO429、甲烷在空气中燃烧:CH4 +2O2点燃CO2 +2H2O30、酒精在空气中燃烧:C2H52点燃2CO2 +3H2O31、一氧化碳还原氧化铜:CO +CuO 加热Cu+ CO232、一氧化碳还原氧化铁:3CO+ Fe23高温2Fe+ 3CO233:Ca(OH)2+ CO2 ==== CaCO3 ↓+ H2O34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+ CO2 ==== Na2CO3 +H2O35、石灰石(或小学音乐教案大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3 +2HCl === CaCl2 +H2O +CO2↑36、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO3+ 2HCl === 2NaCl +H2O +CO2↑一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg+ O2点燃2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃Fe3O43. 铜在空气中受热:2Cu+ O2加热4. 铝在空气中燃烧:4Al +3O2 点燃2Al2O35. 氢气中空气中燃烧:2H22点燃2H2O6. 红磷在空气中燃烧:4P+ 5O2点燃2P2O57. 硫粉在空气中燃烧:S +O点燃 28. 碳在氧气中充分燃烧:2点燃CO29. 碳在氧气中不充分燃烧:2点燃2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+ O2点燃2CO211. 甲烷在空气中燃烧:CH4 +2O2点燃CO2 2H2O12. 酒精在空气中燃烧:C2H52点燃2CO2+3H2O二.几个分解反应:13. 水在直流电的作用下分新概念英语第一册解:2H2O 通电2H2↑+ O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO3加热2CuO +H22↑15. 3 ==== 2KCl+ 3O2↑16. 加热高锰酸钾:2KMnO4 加热K2MnO4 +MnO2 +O2↑17. 碳酸不稳定而分解:H2CO3 === H2O +CO2↑18. 高温煅烧石灰石:CaCO高温CaO +CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2+ CuO 加热Cu+ H2O20. 木炭还原氧化铜:高温2Cu +CO2↑2 初三化学方程式大合集21. 焦炭还原氧化铁:3C+ 2Fe2O高温4Fe+ 3CO2↑22. 焦炭还原四氧化三铁:2C +Fe34高温3Fe+ 2CO2↑23. 一氧化碳还原氧化铜:CO +CuO 加热Cu+ CO224. 一氧化碳还原氧化铁:3CO+ Fe23高温2Fe +3CO225. 一氧化碳还原四氧化三铁:34高温3Fe+ 4CO2(1)金属单质+酸-------- 盐+氢气(置换反应)26. 锌和稀硫酸Zn+ H2SO4 = ZnSO4+ H2↑27. 铁和稀硫酸Fe +H2SO4 = FeSO4+ H2↑28. 镁和稀硫酸Mg +H2SO4 = MgSO4 +H2↑29. 铝和稀硫酸2Al+ 3H2SO4 = Al2(SO4)3 +3H2↑30. 锌和稀盐酸Zn +2HCl === ZnCl2+ H2↑31. 铁和稀盐酸Fe+ 2HCl === FeCl2+ H2↑32. 镁和语文教案格式稀盐酸Mg 2HCl === MgCl2+ H2↑33. 铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑(2)金属单质+盐(溶液)------- 另一种金属+另一种盐34. 铁和硫酸铜溶液反应:Fe+ CuSO4 === FeSO4+ Cu35. 锌和硫酸铜溶液反应:Zn+ CuSO4 === ZnSO4+ Cu36. 铜和硝酸汞溶液反应:Cu +Hg(NO3)2 === Cu(NO3)2 +Hg(3)碱性氧化物+酸-------- 盐+水37. 氧化铁和稀盐酸反应:Fe2O3+ 6HCl === 2FeCl3+ 3H2O38. 氧化铁和稀硫酸反应:Fe2O3 +3H2SO4 === Fe2(SO4)3+ 3H2O39. 氧化铜和稀盐酸反应:CuO +2HCl ==== CuCl2 +H2O40. 氧化铜和稀硫酸反应:CuO +H2SO4 ==== CuSO4+ H2O41. 氧化镁和稀硫酸反应:MgO+ H2SO4 ==== MgSO4+ H2O42. 氧化钙和稀盐酸反应:CaO +2HCl ==== CaCl2 +H2O(4)酸性氧化物+碱-------- 盐+水43.苛性钠暴露在空气中变质:2NaOH +CO2 ==== Na2CO3+H2O44.苛性钠吸收二氧化硫气体:2NaOH +SO2 ==== Na2SO3 +H2O45.苛性钠吸收三氧化硫气体:2NaOH+ SO3 ==== Na2SO4+ H2O46.消石灰放在空气中变质:Ca(OH)2+ CO2 ==== CaCO3 ↓+ H2O47. 消石灰吸收二氧化硫:Ca(OH)2 +SO2 ==== CaSO3↓+H2O(5)酸+碱-------- 盐+水48.盐酸和烧碱起反应:HCl+ NaOH ==== NaCl+ H2O49. 盐酸和氢氧化钾反应:HCl+ KOH ==== KCl+H2O50.盐酸和氢氧化初中家长会课件铜反应:2HCl+ Cu(OH)2 ==== CuCl2 +2H2O51. 盐酸和氢氧化钙反应:2HCl+ Ca(OH)2 ==== CaCl2 +2H2O52. 盐酸和氢氧化铁反应:3HCl+ Fe(OH)3 ==== FeCl3 +3H2O53.氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 ==== AlCl3 +3H2O54.硫酸和烧碱反应:H2SO4 +2NaOH ==== Na2SO4 +2H2O55.硫酸和氢氧化钾反应:H2SO4 +2KOH ==== K2SO4 +2H2O56.硫酸和氢氧化铜反应:H2SO4 +Cu(OH)2 ==== CuSO4 +2H2O57. 硫酸和氢氧化铁反应:3H2SO4 +2Fe(OH)3==== Fe2(SO4)3+ 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O(6)酸+盐-------- 另一种酸+另一种盐59.大理石与稀盐酸反应:CaCO3 +2HCl === CaCl2 H2O +CO2↑60.碳酸钠与稀盐酸反应: Na2CO3 +2HCl === 2NaCl +H2O+ CO2↑61.碳酸镁与稀盐酸反应: MgCO3 +2HCl === MgCl2 +H2O+CO2↑62.盐酸和硝酸银溶液反应:HCl+ AgNO3=== AgCl↓+ HNO363.硫酸和碳酸钠反应:Na2CO3 +H2SO4 === Na2SO4 +H2O +CO2↑64.硫酸和氯化钡溶液反应:H2S O4 +BaCl2 ==== BaSO4↓+ 2HCl(7)碱+盐-------- 另一种碱+另一种盐65.氢氧化钠与硫酸铜:2NaOH CuSO4 ==== Cu(OH)2↓ Na2SO466.氢氧化钠与氯化铁:3NaOH FeCl3 ==== Fe(OH)3↓ 3NaCl67.氢氧化钠与氯化镁:2NaOH MgCl2 ==== Mg(OH)2↓ 2NaCl68. 氢氧化钠与氯化铜:2NaOH CuCl2 ==== Cu(OH)2↓ 2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2 Na2CO3 === CaCO3↓ 2NaOH(8)盐+盐----- 两种新盐70.氯化钠溶液新概念英语第二册和硝酸银溶液:NaCl +AgNO3==== AgCl↓+ NaNO371.硫酸钠和氯化钡:Na2SO4+ BaCl2 ==== BaSO4↓+ 2NaCl五.其它反应:72.二氧化碳溶解于水:CO2+ H2O === H2CO373.生石灰溶于水:CaO+ H2O === Ca(OH)274.氧化钠溶于水:Na2O +H2O ==== 2NaOH75.三氧化硫溶于水:SO3 +H2O ==== H2SO476.硫酸铜晶体受热分解:CuSO4·5H2O 加热CuSO4 5H2O77.无水硫酸铜作干燥剂:CuSO4+ 5H24·5H2。
初中常用的化学式-、俗名答案work Information Technology Company.2020YEAR初中常见化学式和化学方程式一、常见单质初中常见化学式和俗名1、食盐:主要成分:氯化钠,化学式NaCl2、二氧化碳固体:化学式CO2,俗称干冰3、氧化钙:化学式CaO,俗称生石灰4、氢氧化钙:化学式Ca(OH)2,俗称熟石灰、消石灰、石灰浆氢氧化钙溶液:俗称石灰水,主要成分Ca(OH)25、甲烷:化学式CH4,俗称天然气,瓦斯、沼气的主要成分6、乙醇:化学式C2H5OH ,俗称酒精7、汞:化学式Hg,俗称水银8、过氧化氢:化学式H2O2,俗称双氧水9、硫酸铜晶体:化学式CuSO4·5H2O,俗称胆矾、蓝矾10、氢氧化钠:化学式NaOH,俗称火碱、烧碱、苛性钠11、大理石、石灰石、水垢、锅垢的主要成分: CaCO312、氢氯酸(HCl):盐酸(氯化氢气体溶于水所得的溶液),学名:氢氯酸14、碳酸钠:化学式:Na2CO3,俗称纯碱、苏打15、碳酸氢钠:化学式:NaHCO3,俗称小苏打16、铁锈主要成分:氧化铁;化学式:Fe2O3一、化合反应1. 镁在空气中燃烧:2Mg + O2点燃 2MgO2. 铁在氧气中燃烧:3Fe + 2O2点燃 Fe3O43. 铜在空气中受热:2Cu + O2加热 2CuO4. 铝在空气中燃烧:4Al + 3O2点燃 2Al2O35. 氢气中空气中燃烧:2H2 + O2点燃 2H2O6. 红磷在空气中燃烧:4P + 5O2点燃 2P2O57. 硫粉在空气中燃烧: S + O2点燃 SO28. 碳在氧气中充分燃烧:C + O2点燃 CO29. 碳在氧气中不充分燃烧:2C + O2点燃 2CO10. 一氧化碳在氧气中燃烧:2CO + O 2 点燃 2CO 211、二氧化碳和水反应生成碳酸:CO 2 + H 2O == H 2CO 312、二氧化碳通过灼热的炭层:CO 2 + C 2CO 13.二氧化碳溶解于水:CO 2 + H 2O === H 2CO 3 14.生石灰溶于水:CaO + H 2O === Ca(OH)2 15.三氧化硫溶于水:SO 3 + H 2O ==== H 2SO 416.无水硫酸铜作干燥剂:CuSO 4 + 5H 2O ==== CuSO 4·5H 2O 二.几个分解反应:17. 水在直流电的作用下分解:2H 2O 通电 2H 2↑+ O 2 ↑18. 加热碱式碳酸铜:Cu 2(OH)2CO 3 加热 2O + CO 2↑19. 3 ==== 2KCl + 3O 2 ↑ 20. 加热高锰酸钾:2KMnO 4 加热 K 2MnO 4 + MnO 2 + O 2↑ 21. 碳酸不稳定而分解:H 2CO 3 === H 2O + CO 2↑ 22. 高温煅烧石灰石:CaCO 3 高温 CaO + CO 2↑23.硫酸铜晶体受热分解:CuSO 4·5H 2O 加热 CuSO 4 + 5H 2O 三、置换反应24. 氢气还原氧化铜:H 2 + CuO 加热 Cu + H 2O 25. 木炭还原氧化铜:C+ 2CuO 高温 2Cu + CO 2↑ 26. 焦炭还原氧化铁:3C+ 2Fe 2O 3 高温 4Fe + 3CO 2↑ 27. 焦炭还原四氧化三铁:2C+ Fe 3O 4 高温 3Fe + 2CO 2↑ 金属单质 + 酸 -------- 盐 + 氢气28. 锌和稀硫酸Zn + H 2SO 4 = ZnSO 4 + H 2↑ 29. 铁和稀硫酸Fe + H 2SO 4 = FeSO 4 + H 2↑ 30. 镁和稀硫酸Mg + H 2SO 4 = MgSO 4 + H 2↑ 31. 铝和稀硫酸2Al +3H 2SO 4 = Al 2(SO 4)3 +3H 2↑ 32. 锌和稀盐酸Zn + 2HCl === ZnCl 2 + H 2↑ 33. 铁和稀盐酸Fe + 2HCl === FeCl 2 + H 2↑ 34. 镁和稀盐酸Mg+ 2HCl === MgCl 2 + H 2↑ 35. 铝和稀盐酸2Al + 6HCl == 2AlCl 3 + 3H 2↑(2)金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐 36. 铁和硫酸铜溶液反应:Fe + CuSO 4 === FeSO 4 + Cu 37. 锌和硫酸铜溶液反应:Zn + CuSO 4 === ZnSO 4 + Cu38. 铜和硝酸汞溶液反应:Cu + Hg(NO 3)2 === Cu(NO 3)2 + Hg 四、复分解反应(1)碱性氧化物 +酸 -------- 盐 + 水39. 氧化铁和稀盐酸反应:Fe 2O 3 + 6HCl === 2FeCl 3 + 3H 2O高温40. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 === Fe2(SO4)3 + 3H2O41. 氧化铜和稀盐酸反应:CuO + 2HCl ==== CuCl2 + H2O42. 氧化铜和稀硫酸反应:CuO + H2SO4 ==== CuSO4 + H2O43. 氧化镁和稀硫酸反应:MgO + H2SO4 ==== MgSO4 + H2O44. 氧化钙和稀盐酸反应:CaO + 2HCl ==== CaCl2 + H2O(2)酸 + 碱 -------- 盐 + 水45.硫酸和烧碱反应:H2SO4 + 2NaOH ==== Na2SO4 + 2H2O46.硫酸和氢氧化钾反应:H2SO4 + 2KOH ==== K2SO4 + 2H2O47.硫酸和氢氧化铜反应:H2SO4 + Cu(OH)2 ==== CuSO4 + 2H2O48. 硫酸和氢氧化铁反应:3H2SO4 + 2Fe(OH)3==== Fe2(SO4)3 + 6H2O49. 盐酸和氢氧化钾反应:HCl + KOH ==== KCl +H2O50.盐酸和氢氧化铜反应:2HCl + Cu(OH)2 ==== CuCl2 + 2H2O51. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 ==== CaCl2 + 2H2O52. 盐酸和氢氧化铁反应:3HCl + Fe(OH)3 ==== FeCl3 + 3H2O53.氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 ==== AlCl3 + 3H2O 54.盐酸和烧碱起反应:HCl + NaOH ==== NaCl +H2O55. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O(3)酸 + 盐 -------- 另一种酸 + 另一种盐56.大理石与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑57.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑58.碳酸镁与稀盐酸反应: MgCO3 + 2HCl === MgCl2 + H2O + CO2↑59.盐酸和硝酸银溶液反应:HCl + AgNO3 === AgCl↓ + HNO360.硫酸和碳酸钠反应:Na2CO3 + H2SO4 === Na2SO4 + H2O + CO2↑61.硫酸和氯化钡溶液反应:H2SO4 + BaCl2 ==== BaSO4↓+ 2HCl (4)碱 + 盐 -------- 另一种碱 + 另一种盐62.氢氧化钠与硫酸铜:2NaOH + CuSO4 ==== Cu(OH)2↓ + Na2SO4 63.氢氧化钠与氯化铁:3NaOH + FeCl3 ==== Fe(OH)3↓ + 3NaCl 64.氢氧化钠与氯化镁:2NaOH + MgCl2 ==== Mg(OH)2↓ + 2NaCl65. 氢氧化钠与氯化铜:2NaOH + CuCl2 ==== Cu(OH)2↓ + 2NaCl66. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 === CaCO3↓+ 2NaOH (5)盐 + 盐 ----- 两种新盐67.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 ==== AgCl↓ + NaNO3 68.硫酸钠和氯化钡:Na2SO4 + BaCl2 ==== BaSO4↓ + 2NaCl五、其他反应类型69、二氧化碳通入澄清石灰水中:CO2 + Ca(OH)2 == CaCO3↓+ H2O70. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 ==== CaSO3↓+ H2O71、氢氧化钠溶液吸收二氧化硫:SO 2 + 2NaOH ==Na 2SO 3+ H 2O 72、氢氧化钠在空气中变质:CO 2+ 2NaOH = Na 2CO 3 + H 2O73.苛性钠吸收三氧化硫气体:2NaOH + SO 3 ==== Na 2SO 4 + H 2O74、一氧化碳还原氧化铜:CO + CuO Cu + CO 2 75、酒精燃烧:C 2H 5OH + 3O 2 2CO 2 + 3H 2O76、甲烷燃烧:CH 4 + 2O 2 CO 2 + 2H 2O△点燃点燃7。
初中化学常用物质化学式、俗称(OH)3氢氧化铝:胃舒平的主要成分
硫酸钡:钡餐、重晶石
碳:金刚石、石墨、木炭、活性炭、焦炭、煤的主要成分(ClO)2和CaCl2次氯酸钙和氯化钙混合物:漂白粉(次氯酸钙)
5.CaO氧化钙:生石灰
6.CaO、NaOH氧化钙和氢氧化钠混合物:碱石灰
7.Ca(OH)2氢氧化钙:熟石灰、石灰水
8.CaCO3碳酸钙:石灰石、大理石
9.硫酸钙晶体:(生)石膏
10.(CaSO4)硫酸钙晶体:熟石膏
11.CH4:甲烷、天然气、瓦斯、沼气
12.C2H5OH:乙醇、酒精
13.CH3COOH:乙酸、醋酸
14.C6H12O6:葡萄糖
15.CO2二氧化碳:干冰、碳酸气
16.CO和H2混合气:水煤气,CO:煤气
17. CO(NH2)2:尿素
18.CuSO4?5H2O硫酸铜晶体:蓝矾、胆矾
19.Cu2(OH)2CO3碱式碳酸铜:铜绿、铜锈、孔雀石
20.Cu SO4和Ca(OH)2:波尔多液
21.FeSO4?7H2O硫酸亚铁晶体:绿矾
22.Fe2O3氧化铁:铁锈和赤铁矿主要成分
23.Fe3O4四氧化三铁:磁铁矿、烤蓝、烤黑
24.Hg汞:水银
25.HCl氯化氢:氢氯酸、盐酸、胃酸的主要成分
26.H2O2过氧化氢:双氧水
27.H2和O2混合气:爆鸣气
28.KAl(SO4)十二水硫酸铝钾:明矾
29.K2CO3碳酸钾:草木灰主要成分
30.KOH氢氧化钾:苛性钾
31.NaOH氢氧化钠:苛性钠、烧碱,火碱
32.Na2CO3碳酸钠:纯碱、苏打
33.NaHCO3碳酸氢钠:小苏打
34.:纯碱晶体、石碱、口碱
35.Na2SiO3硅酸钠:水玻璃
36.NaCl氯化钠:食盐
37.Na2S2O3硫代硫酸钠:大苏打、海波
38.NH4HCO3碳酸氢铵:碳铵
39.(NH4)2SO4硫酸铵:硫铵
40.NH4NO3硝酸铵:硝铵
41.NH3?H2O:一水合氨、氨水
42.P磷:白磷、红磷、黄磷
43.S硫:硫磺
44.SiO2二氧化硅:石英、石英砂、水晶
45.Fe:生铁、钢、不锈钢的主要成分
初中化学常用物质化学式、俗称(默写练习一)(OH)3氢氧化铝:
硫酸钡:
碳:
(ClO)2和CaCl2次氯酸钙和氯化钙混合物:
5.CaO氧化钙:
6.CaO、NaOH氧化钙和氢氧化钠混合物:
7.Ca(OH)2氢氧化钙:
8.CaCO3碳酸钙:
9.硫酸钙晶体:
10.(CaSO4)硫酸钙晶体:
11.CH4:
12.C2H5OH:
13.CH3COOH:
14.C6H12O6:
15.CO2二氧化碳:
16.CO和H2混合气:,CO:
17. CO(NH2)2:
18.CuSO4?5H2O硫酸铜晶体:
19.Cu2(OH)2CO3碱式碳酸铜:
20.Cu SO4和Ca(OH)2:
21.FeSO4?7H2O硫酸亚铁晶体:
22.Fe2O3氧化铁:
23.Fe3O4四氧化三铁:
24.Hg汞:
25.HCl氯化氢:
26.H2O2过氧化氢:
27.H2和O2混合气:
28.KAl(SO4)十二水硫酸铝钾:
29.K2CO3碳酸钾:
30.KOH氢氧化钾:
31.NaOH氢氧化钠:
32.Na2CO3碳酸钠:
33.NaHCO3碳酸氢钠:
34.:
35.Na2SiO3硅酸钠:
36.NaCl氯化钠:
37.Na2S2O3硫代硫酸钠:
38.NH4HCO3碳酸氢铵:
39.(NH4)2SO4硫酸铵:
40.NH4NO3硝酸铵:
41.NH3?H2O:
42.P磷:
43.S硫:
44.SiO2二氧化硅:
45.Fe:
初中化学常用物质化学式、俗称(默写练习二)
1. :胃舒平的主要成分
2. :钡餐、重晶石
3. :金刚石、石墨、木炭、活性炭、焦炭、煤的主要成分
4. :漂白粉(次氯酸钙)
5.:生石灰
6.:碱石灰
7.:熟石灰、石灰水
8.:石灰石、大理石
9.:(生)石膏
10.:熟石膏
11.:甲烷、天然气、瓦斯、沼气
12.:乙醇、酒精
13.:乙酸、醋酸
14.:葡萄糖
15.:干冰、碳酸气
16.:水煤气,CO:煤气
17. :尿素
18.:蓝矾、胆矾
19.:铜绿、铜锈、孔雀石
20.:波尔多液
21.:绿矾
22.:铁锈和赤铁矿主要成分
23.:磁铁矿、烤蓝、烤黑
24.:水银
25.:氢氯酸、盐酸、胃酸的主要成分
26.:双氧水
27.:爆鸣气
28. :明矾
29.:草木灰主要成分
30.:苛性钾
31.:苛性钠、烧碱,火碱
32.:纯碱、苏打
33.:小苏打
34.:纯碱晶体、石碱、口碱
35. :水玻璃
36.:食盐
37.:大苏打、海波
38.:碳铵
39.:硫铵
40.:硝铵
41.:一水合氨、氨水
42. :白磷、红磷、黄磷
43.:硫磺
44.:石英、石英砂、水晶
45.:生铁、钢、不锈钢的主要成分。