第八章分光光度法
- 格式:ppt
- 大小:1.38 MB
- 文档页数:109

分光度光度法分光光度法学习资料一、分光光度法的基本概念1. 定义- 分光光度法是通过测定被测物质在特定波长处或一定波长范围内光的吸收度,对该物质进行定性和定量分析的方法。
它利用物质对光的选择性吸收特性,不同的物质由于其分子结构不同,对不同波长的光有不同程度的吸收。
2. 原理基础- 朗伯 - 比尔定律(Lambert - Beer law)是分光光度法的基本定律。
- 朗伯定律指出:当一束平行单色光垂直通过某一均匀非散射的吸光物质时,其吸光度与光通过的路径长度成正比,即A = k_1b(其中A为吸光度,b为光程长度,k_1为比例常数)。
- 比尔定律指出:当一束平行单色光垂直通过某一均匀非散射的吸光物质时,其吸光度与吸光物质的浓度成正比,即A = k_2c(其中c为吸光物质的浓度,k_2为比例常数)。
- 合并朗伯定律和比尔定律得到朗伯 - 比尔定律:A=varepsilon bc,其中varepsilon为摩尔吸光系数,单位为L/(mol· cm),它表示物质对某一特定波长光的吸收能力,varepsilon越大,表明该物质对该波长光的吸收能力越强。
二、分光光度计的结构与组成1. 光源- 提供足够强度和稳定的连续光谱。
在可见光区常用钨灯或卤钨灯,其发射光的波长范围为320 - 2500nm;在紫外光区常用氢灯或氘灯,发射光的波长范围为180 - 375nm。
2. 单色器- 它的作用是将光源发出的复合光分解为单色光。
主要部件包括狭缝、准直镜和色散元件(如棱镜或光栅)。
通过调节狭缝宽度可以控制出射光的带宽和光强。
3. 样品池- 用于盛放被测溶液。
在可见光区可以使用玻璃样品池,而在紫外光区则需使用石英样品池,因为玻璃对紫外光有吸收。
4. 检测器- 检测透过样品池后的光强,并将光信号转换为电信号。
常见的检测器有光电管和光电倍增管等。
光电倍增管具有更高的灵敏度,可检测微弱的光信号。
5. 信号显示与处理系统- 将检测器输出的电信号进行放大、处理,并以吸光度或透光率等形式显示出来。




分光光度原理
分光光度法是一种利用物质对光的吸收、透射或散射特性来测定物质浓度、纯度或其他性质的分析方法。
它是利用物质对特定波长的光的吸收特性来定量分析物质的方法。
分光光度法广泛应用于化学、生物、环境、食品等领域,是一种非常重要的分析方法。
分光光度法的原理基于比尔定律,即溶液中物质的吸光度与物质的浓度成正比。
根据比尔定律,溶液中物质的吸光度A与物质的浓度C之间存在以下关系,A=εlc,其中ε为摩尔吸光系数,l为光程,c为物质的浓度。
根据比尔定律,当光束通过溶液时,溶液中的物质会吸收特定波长的光,吸收的光强与物质的浓度成正比。
因此,可以通过测定光束通过溶液前后的光强差来确定溶液中物质的浓度。
在分光光度法中,常用的光源有白炽灯、钨丝灯、氘灯、钠灯等,常用的检测器有光电管、光电二极管、光电倍增管等。
光源发出的光经过进样器进入样品,样品吸收部分光线后,剩余的光线进入检测器进行检测。
检测器将检测到的光信号转化为电信号,经过放大和处理后,最终转化为浓度或吸光度的显示值。
分光光度法的应用非常广泛,例如在环境监测中,可以利用分光光度法来测定水中重金属、有机物等的浓度;在生物领域,可以利用分光光度法来测定蛋白质、核酸等的浓度;在食品领域,可以利用分光光度法来测定食品中添加剂、污染物等的含量。
分光光度法还可以用于药物分析、化工生产、医学诊断等领域。
总之,分光光度法作为一种快速、准确、灵敏的分析方法,在化学、生物、环境、食品等领域都有着重要的应用价值。
通过合理选择光源、进样器、检测器等仪器设备,结合适当的实验条件和数据处理方法,可以实现对不同物质的快速、准确测定,为各个领域的科研工作和生产实践提供有力支持。



分析化学分光光度法一、分光光度原理1、分光光度法分光光度法是通过测定被测物质在特定波长处或一定波长范围内光的吸收度,对该物质进行定性和定量分析的方法。
在分光光度计中,将不同波长的光连续地照射到一定浓度的样品溶液时,便可得到与众不同波长相对应的吸收强度。
如以波长(λ)为横坐标,吸收强度(A)为纵坐标,就可绘出该物质的吸收光谱曲线。
利用该曲线进行物质定性、定量的分析方法,称为分光光度法,也称为吸收光谱法。
用紫外光源测定无色物质的方法,称为紫外分光光度法;用可见光光源测定有色物质的方法,称为可见光光度法。
它们与比色法一样,都以Beer-Lambert定律为基础。
上述的紫外光区与可见光区是常用的。
但分光光度法的应用光区包括紫外光区,可见光区,红外光区。
2、基本原理当一束强度为I0的单色光垂直照射某物质的溶液后,由于一部分光被体系吸收,因此透射光的强度降至I,则溶液的透光率T为: I/ I0根据朗伯(Lambert)-比尔(Beer)定律:A=abc式中A为吸光度,b为溶液层厚度(cm),c为溶液的浓度(g/dm^3),a为吸光系数。
其中吸光系数与溶液的本性、温度以及波长等因素有关。
溶液中其他组分(如溶剂等)对光的吸收可用空白液扣除。
由上式可知,当固定溶液层厚度L和吸光系数时,吸光度A与溶液的浓度成线性关系。
在定量分析时,首先需要测定溶液对不同波长光的吸收情况(吸收光谱),从中确定最大吸收波长,然后以此波长的光为光源,测定一系列已知浓度c溶液的吸光度A,作出A-c工作曲线。
在分析未知溶液时,根据测量的吸光度A,查工作曲线即可确定出相应的浓度。
这便是分光光度法测量浓度的基本原理。
上述方法是依据标准曲线法来求出未知浓度值,在满足要求(准确度和精密度)的条件下,可以应用比较法求出未知浓度值。
二、仪器原理依据分光光度法测量原理,把比较法应用到仪器之中——浓度直读功能。
用标准溶液将仪器调整好,再测定样品时,直接显示样品浓度值。
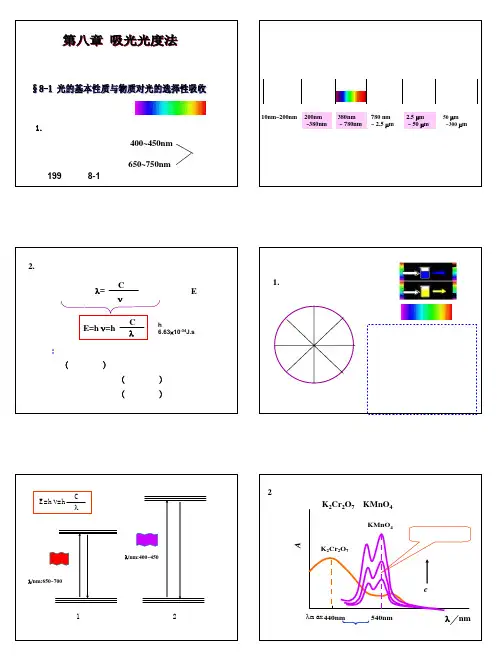
1.电磁波谱紫光波长:400~450nm红光650~750nm一、光的基本性质吸光光度法(分光光度法):根据物质对光的选择性吸收来进行测定的一种方法可见光教材:199页,表8-1光学光谱区(真空紫外)远红外中红外近红外可见近紫外远紫外10nm~200nm200nm ~380nm 380nm ~780nm 780 nm ~2.5 µm 2.5 µm ~50 µm 50 µm ~300 µm2. 光的波粒二象性波动性:λ=νC 粒子性:E波粒二象性:λC E=h ν=h结论:一定波长的光具有一定的能量,波长越长(频率越低),光量子的能量越低。
单色光:具有相同能量(相同波长)的光。
混合光:具有不同能量(不同波长)的光复合在一起,例如白光。
h 为普朗克常数:6.63×10-34J.s二、物质对光的选择性吸收1.物质对光的选择性吸收青(蓝绿)红橙黄绿绿蓝蓝紫物质的分子具有一系列不连续的特征能级,通常分子处于能量最低的基态,吸收了一定入射光的能量后产生能级跃迁,进入能量较高的激发态,当入射光的能量与物质分子的某一能级差恰好相等时,才有可能发生能级跃迁(1)(2)基态第一激发态第一激发态λC E=h ν=hλ/nm:650~700λ/nm:400~450λmax 440nm540nmAλnmK 2Cr 2O 7KMnO 4K 2Cr 2O 7和KMnO 4的吸收曲线定量分析基础定性分析基础c增大2.吸收曲线三、吸光光度法的特点1.灵敏度高(0.01克黄金/吨矿石)2.操作简便,测定速度快3.应用广泛,几乎可测所有无机离子,广泛应用于冶金,环境,生物,医学等领域吸收光谱峰的位置(λmax )定性峰的高矮(吸收程度的大小)定量I a =I 0 -I一、朗伯-比尔定律I oIbSdx I a当一束平行单色光垂直照到某均匀溶液时,假设:液层厚度b ,截面积为s ,溶液浓度为c ,入射光强度为I 0,该溶液吸收光的强度为I a ,透过光的强度为I将b 切割为dx ,薄层中所含吸光质点数为dN ,入射光强度为I b ,穿过薄层后光的强度减弱了dI b-dI b = K 1I b dN dN = 6.02×1023cSdx -dI b = K 16.02×1023S cI b dx 令:K 2= 6.02×1023K 1S ∴-dI b = K 2I b cdx ,cdx K I dI 2b b =−∫∫=−bI I b b cdx K I dI20cb K I I20ln=−Kcb I I=−∴0lg303.22K K =令:液层厚度b ,截面积S ,吸光物质浓度c ,薄层中所含吸光质点数为dNI 0dx bII bI t根据光的量子理论:透光率或透射比T (0~1, 0~100%)定义透光率:I I T =定义吸光度:有意义的取值范围为∞-0KbcI I T A =−=−=0lglg 透过光强度入射光的强度朗伯-比尔定律的数学表达式Kcb I I=−0lgI II I A 00lg lg =−=朗伯-比尔定律朗伯-比耳定律是吸光光度法的理论基础,是用光度法进行定量测定的依据朗伯-比耳定律的物理意义:当一束平行单色光垂直通过某均匀溶液时,溶液的吸光度A 与液层厚度b 及吸光物质的浓度c 成正比:A= Kbc单色平行光均匀溶液注意:A=-lg= KcbI I 0吸光度与光程的关系A = K b c0.10b0.202b0.00光源检测器显示器参比吸光度与浓度的关系A = Kb c0.10c0.202c0.00光源检测器显示器参比二、光度法的灵敏度1.吸光系数a (吸收系数)当液层厚度b 以cm ,吸光物质的浓度c 以g/L 为单位时,朗伯-比尔定律表示为A = abca 称为吸光系数,单位为L/(g ⋅cm)在朗伯-比尔定律A = Kbc 中,系数K 在一定条件下是常数,表明用光度法进行测定的灵敏度KλT吸光物质性质K=cbA 2.摩尔吸光系数εc mol/L b cm εL/(mol.cm)A= bcεε吸光物质的灵敏度吸光物质对光的吸收能力ε=cbA 当液层厚度b 以cm ,吸光物质浓度c 以mol/L 为单位时,朗伯-比尔定律表示为二乙基胺二硫代甲酸钠(铜试剂,DDTC )双硫腙ε436=12800 L/(mol.cm)CuCuε495=158000 L/(mol.cm)<ελT吸光物质性质λmaxεmaxA= -lgT = -lg0.603 = 0.220c=140×10-6112.4=1.25 ×10-6mol/Lε=bcA =2 ×1.25 ×10-60.220= 8.8×104 L/(mol.cm)例1 (203页,8-1),利用双硫腙光度法测Cd 2+,已知Cd 2+的质量浓度为140µg/L,比色皿厚度为2cm,在520nm 处测得透光率为0.603,求吸光度A 及摩尔吸光系数ε(M cd =112.4g/mol)解:A= εbcε=bc A A= εbc c mol/Lbcmmol/1000cm 3bc/1000mol/cm 2bcM ×1061000S(µg/cm 2)∴S=bcM ×103将代入得bc=εAS=εAM ×103µg/cm 23.桑德尔灵敏度SA=0.001时(检测极限),单位截面积光程内所能检出吸光物质的最低含量µg/cm 2bc →单位截面积光程所能检出吸光物质的最低含量因为:A=0.001,代入上式:S 灵敏度ε灵敏度S=εM ∴例2(205页,8-2)、已知双硫腙光度法测定Cd 2+时ε520nm =8.8×104L/(mol ·cm),求桑德尔灵敏度S.A=0.001时,单位截面积光程内所能检出吸光物质的最低含量µg/cm 2解,S=εM cd =8.8×104112.4=1.3 ×10-3µg/cm 2A= εbcS=εAM ×103例3,Fe 2+用邻二氮菲显色,当c=0.76 µg/ml,于波长λ510nm,吸收池厚度b=2.0cm 时,测得T%=50.2,求摩尔吸光系数和桑德尔灵敏度各为多少?(M Fe =55.85 g/mol)c= 0.76 µg/ml=7.6 ×10-4g/L=1.36 ×10-5mol/L由A=εbc 得:解:A=-lgT=-lg0.502=0.299ε=A bc =0.2992.0×1.36 ×10-5=1.1 ×104L/(cm.mol)S=εM Fe =1.1×10455.85= 5.1 ×10-3µg/cm 2三、利用朗伯-比尔定律进行定量分析A= εbc b 一定, λmax 一定,同一种物质,ε一定配制一系列标准溶液,由标准溶液:c 1, c 2, c 3……测得吸光度:A 1, A 2, A 3…...A 对c 作图工作曲线1.工作曲线法(标准曲线法)c (mg/ml)c 1c 2c 3c 4c 5A.....A xc x 工作曲线(标准曲线)A 1A 2A 3A 4A 5A 标A x=ε标b c 标εx b c x2.比较法:四、对朗伯-比尔定律偏离.工作曲线(标准曲线)A= εbccc 1c 2c 3c 4c 5A..原因:仪器或溶液的实际条件与朗伯-比尔定律所要求的前提条件不一致..A 总=-lg I t1+I t2I o1+I o2=-lgI o110-ε1bc +I o210-ε2bc I o1+I o2(一)、由于非单色光引起的偏移∴I t =I o 10-εbcA= εbc =-lgII o假设:入射光I oλ2I o2I t2A 2λ1I o1I t1A 1A 总=-lg10-εbc (I o1+I o2)I o1+I o2= εbc 造成偏离A 总= εbc若λ1与λ2相差很大,ε1= ε2=ε如果λ1和λ2相差不大,即∆λ= |λ1-λ2|很小,可以近似认为ε1= ε2= εA 总=-lg I t1+I t2I o1+I o2=-lgI o110-ε1bc +I o210-ε2bcI o1+I o2克服由非单色光所造成的偏离¾选择单色器(单色性能较好)¾选择入射光波长(λmax )¾选择适当的浓度范围(不应过高)浓度及非单色光的影响λ1λ2abA 5A 1A 4A 2λ3λ/nmA浓度: b>a波长: λ3>λ2>λ1A 3A 6(二)、由于溶液本身的化学和物理性质所引起的偏离1.由于介质不均匀所引起的偏离bI oI I a 发生散射:T 实I o -I a -I r=I o=II o2.由于溶液的化学反应所引起的偏离分析浓度或总浓度C 总吸光质点浓度C 质C工作曲线A=Kcb I r因为:T 实<T 理∴A 实>A 理T 理I o -I a =I o =I I o 吸光物质因解离、络合、缔合等化学变化而改变浓度如:Cr 2O 72-+H 2O 2CrO 42-+2H +λ=375nmλ=350nm单体:SNH +(CH 3)2NN(CH 3)22SNH +(CH 3)2NN(CH 3)22λmax = 660 nm 二聚体:λmax = 610 nmAcλmax = 660 nmAλ660 nm 610 nm亚甲基蓝阳离子(MB )方便、较灵敏,准确度差(半定量)一、光度分析的几种方法1.目视比色法观察方向空白c 1c 2c 3c 4c x1).可以任意选择某种波长的单色光2).扩大入射光波长的范围3)灵敏度、准确度高2.光电比色法和吸光光度法:共同点:以朗伯-比尔定律为基础的仪器分析方法主要区别:获得单色光的手段不同光电比色法以滤光片为单色器,谱带宽度约有几十纳米吸光光度法以棱镜或光栅为单色器,谱带宽度约有几纳米光源单色器狭缝样品室检测器二、紫外-可见分光光度计氙灯氢灯钨灯1.光源卤钨灯。
