片剂质量检查
- 格式:docx
- 大小:123.01 KB
- 文档页数:5

片剂的质量检查、处方设计及举例一、片剂的质量检查〔一〕外观性状片剂外观应完整光洁,色泽均匀,有适宜的硬度和耐磨性,除另有规定外,对于非包衣片,应符合片剂脆碎度检查法的要求,防止包装、贮运过程中发生磨损或破碎。
〔二〕重量差异片重差异过大,意味着每片中主药含量不一,对治疗可能产生不利影响。
糖衣片的片芯应检查重量差异并符合规定,包糖衣后不再检查重量差异。
薄膜衣片应在包薄膜衣后检查重量差异并符合规定。
检查法:取供试品2021精密称定总重量,求得平均片重后,再分别精密称定每片的重量,每片重量与平均片重相比拟〔凡无含量测定的片剂,每片重量应与标示片重比拟〕,超出重量差异限度的不得多于2片,并不得有1片超出限度1倍。
凡规定检查含量均匀度的片剂,一般不再进行重量差异检查。
〔三〕脆碎度仪器装置:内径约为286mm,深度为39mm,内壁抛光,一边可翻开的透明耐磨塑料圆筒〔见图〕,筒内有一自中心向外壁延伸的弧形隔片〔内径为80mm±1mm,内弧外表与轴套外壁相切〕,使圆筒转动时,片剂产生滚动。
圆筒固定于水平转轴上,转轴与电动机相连,转速为每分钟25转±1转。
每转动一圈,片剂滚动或滑动至筒壁或其他片剂上。
检查法:片重为或以下者取假设干片,使其总重约为;片重大于者取10片。
用吹风机吹去脱落的粉末,精密称重,置圆筒中,转动100次。
取出,同法除去粉末,精密称重,减失重量不得过1%,且不得检出断裂、龟裂及粉碎的片。
【经典】最正确选择题在进行脆碎度检查时,片剂的减失重量不得超过%%『正确答案』C〔四〕崩解时限崩解系指口服固体制剂在规定条件下全部崩解溶散或成碎粒,除不溶性包衣材料或破碎的胶囊壳外,应全部通过筛网,但已软化或轻质上漂且无硬心者,可作符合规定论。
凡规定检查溶出度、释放度或融变时限的制剂,不再进行崩解时限检查。
1咀嚼片、缓、控释片,不需要作崩解时限检查。
2标准:〔五〕溶出度或释放度检查根据?药典?的有关规定,溶出度检查用于一般的片剂,而释放度检查适用于缓释控释制剂,其主要原因在于:崩解度检查并不能完全正确地反映主药的溶出速度和溶出程度以及机体的吸收情况。
实验二 水杨酸片的制备及质量检查一、实验目的1. 通过片剂制备,掌握湿法制粒压片的工艺过程。
2. 掌握单冲压片机的使用方法及片剂质量的检查方法。
3. 掌握片剂的质量检查方法,并了解压片力对片剂硬度或崩解的影响。
二、实验指导片剂是应用最为广泛的药物剂型之一。
片剂的制备方法有制颗粒压片(分为湿法制粒和干法制粒),粉末直接压片和结晶直接压片。
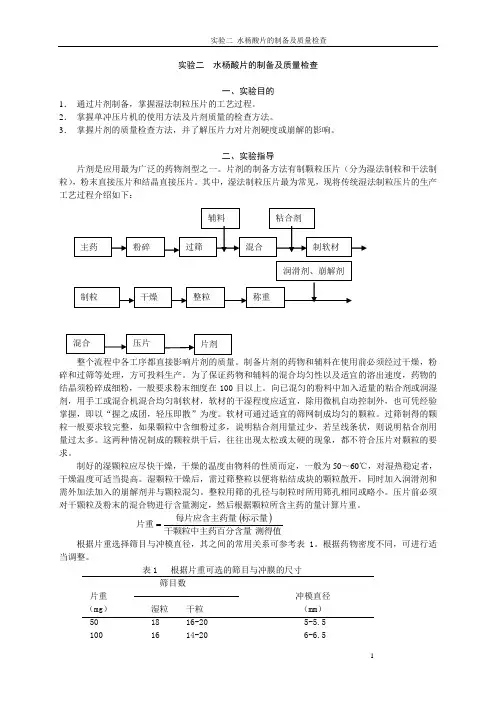
其中,湿法制粒压片最为常见,现将传统湿法制粒压片的生产工艺过程介绍如下:整个流程中各工序都直接影响片剂的质量。
制备片剂的药物和辅料在使用前必须经过干燥,粉碎和过筛等处理,方可投料生产。
为了保证药物和辅料的混合均匀性以及适宜的溶出速度,药物的结晶须粉碎成细粉,一般要求粉末细度在100目以上。
向已混匀的粉料中加入适量的粘合剂或润湿剂,用手工或混合机混合均匀制软材,软材的干湿程度应适宜,除用微机自动控制外,也可凭经验掌握,即以“握之成团,轻压即散”为度。
软材可通过适宜的筛网制成均匀的颗粒。
过筛制得的颗粒一般要求较完整,如果颗粒中含细粉过多,说明粘合剂用量过少,若呈线条状,则说明粘合剂用量过太多。
这两种情况制成的颗粒烘干后,往往出现太松或太硬的现象,都不符合压片对颗粒的要求。
制好的湿颗粒应尽快干燥,干燥的温度由物料的性质而定,一般为50~60℃,对湿热稳定者,干燥温度可适当提高。
湿颗粒干燥后,需过筛整粒以便将粘结成块的颗粒散开,同时加入润滑剂和需外加法加入的崩解剂并与颗粒混匀。
整粒用筛的孔径与制粒时所用筛孔相同或略小。
压片前必须对干颗粒及粉末的混合物进行含量测定,然后根据颗粒所含主药的量计算片重。
()测得值干颗粒中主药百分含量标示量每片应含主药量片重=根据片重选择筛目与冲模直径,其之间的常用关系可参考表1。
根据药物密度不同,可进行适当调整。
表1 根据片重可选的筛目与冲膜的尺寸筛目数片重 冲模直径(mg ) 湿粒 干粒 (mm )50 18 16-20 5-5.5100 16 14-20 6-6.5150 16 14-20 7-8200 14 12-16 8-8.5300 12 10-16 9-10.5500 10 10-12 12制成的片剂需按照《中国药典》规定的片剂的质量检查项目进行检查。



片剂的质量检测任务】片剂的质量检查学习情境三片剂的质量检测任务一阿司匹林片的质量检测一、片剂的质量检测制剂和原料药不同,除含主药外,往往还含有附加剂,附加剂有时会影响主药的测定。
当附加剂对主药的测定有干扰时,对样品需进行一些预处理,如过滤、萃取、色谱分别等,以消除其影响;或者选择一些专属性更强的方法进行测定。
1.片剂的检测步骤片剂系药物与适合辅料混匀压制而成的圆片状或异形片状的固体制剂。
片剂的分析步骤包括:外观及性状(如色泽、臭味等)检查,鉴别,常规检查及杂质检查,含量测定。
片剂中附加剂对测定产生干扰,需选择适当方法排除。
2.片剂的常规检查片剂的常规检查包括:重量差异,崩解时限,溶出度检查,含量匀称度及微生物限度检查。
〔1〕重量差异检查表6-1 片剂重量差异限度要求平均片重或标示片重重量差异限度/% 0.30g以下±7.5 0.30g及0.30g以上±5 重量差异是指按规定称量方法测得片剂每片的重量与平均片重之间的差异程度。
片剂片重的差异可引起各片间主药含量的差异,重量差异可反映片剂匀称性。
检查法取供试品20片,周密称定总重量,求得平均片重后,再分别周密称定每片的重量,每片重量与平均片重相比较(凡无含量测定的片剂,每片重量应与标示片重比较),按表6-1中的规定,超出重量差异限度的不得多于2片,并不得有1片超出限度1倍。
糖衣片的片心应检查重量差异并符合规定,包糖衣后不再检查重量差异。
薄膜衣片应在包薄膜衣后检查重量差异并符合规定。
〔2〕崩解时限检查崩解时限是指口服固体制剂在规定条件下全部崩解溶散或成碎粒,除不溶性的包衣材料或破裂的胶囊壳除外,应全部通过筛XX所需时间的限度。
片剂经口服后在胃肠道中首先要经过崩解,药物才能被释放、汲取。
片剂、胶囊剂需进行崩解时限检查,丸剂需检查溶散时限。
仪器装置接受升降式崩解仪,主要结构为一能升降的金属支架与下端镶有筛XX的吊篮,并附有挡板。
检查法将吊篮通过上端的不锈钢轴悬挂于金属支架上,浸入1000mL烧杯中,并调整吊篮的位置使其下降时筛XX距烧杯底部25mm,烧杯内盛有温度为37℃±1℃的水,调整水位高度使吊篮上升时筛XX在水面下15mm处。


片剂的质量检查实验报告1. 引言片剂是一种常见的口服药物剂型,其质量的稳定性对于药物的治疗效果具有重要影响。
本实验旨在通过一系列质量检查实验来评估片剂的质量特性,并提供科学依据以确保片剂的质量稳定性和安全性。
2. 实验目的本实验的主要目的是通过以下几个方面来评估片剂的质量:- 片剂的物理特性:包括外观、尺寸、形状等方面的评估。
- 片剂的质量一致性:包括质量分析、均匀度测试等方面的评估。
- 片剂的溶解性:通过溶解度测试来评估片剂在不同介质中的溶解性。
3. 实验步骤步骤1:外观检查首先,对片剂的外观进行检查。
观察片剂的颜色、形状、表面光滑度等特征,并记录下来。
步骤2:尺寸测定使用显微镜和卡尺等工具,测量片剂的尺寸。
包括直径、厚度等参数,并记录下来。
步骤3:质量分析将一定数量的片剂称重,并记录下来。
然后将这些片剂粉碎,并再次称重。
通过计算前后两次称重的差值来评估片剂的质量。
步骤4:均匀度测试从不同部位随机选取若干片剂进行药物含量的测定。
使用适当的分析方法,如高效液相色谱法等,测定片剂中活性成分的含量,并计算其相对标准偏差以评估片剂的均匀度。
步骤5:溶解度测试根据药物的特性选择合适的介质,如磷酸盐缓冲液、模拟胃肠液等。
将片剂置入溶液中,在一定时间内进行搅拌,并测定溶解液中活性成分的浓度。
通过计算溶出度和溶出速度等指标来评估片剂的溶解性。
4. 结果分析根据实验数据,对片剂的质量进行综合评估和分析。
比较不同样品之间的差异,并与药典中的标准进行对比。
根据评估结果,对片剂的质量稳定性和合格性进行判断。
5. 结论根据本次实验的结果,我们得出以下结论: - 片剂在外观、尺寸、形状等方面符合要求。
- 片剂的质量一致性较好,药物含量均匀分布。
- 片剂在不同介质中具有良好的溶解性。
6. 建议基于本次实验的结果和分析,我们提出以下建议: - 继续进行长期稳定性试验以评估片剂的长期质量稳定性。
- 加强对片剂质量控制的监督和追踪,确保生产过程中质量的一致性和稳定性。

片剂的质量检查项目
片剂是一种常见的药物剂型,其质量直接影响到药物的治疗效果
和安全性。
因此,片剂的质量检查非常重要。
本文将介绍片剂的质量
检查项目,以帮助读者更好地了解和辨别片剂的质量。
1. 外观检查:片剂应该外观整洁、色泽均匀,表面无裂纹、破损、粉末等。
2. 尺寸检查:片剂应该符合其规格尺寸,长度、宽度、厚度应该
一致。
3. 均匀度检查:片剂必须保证每一颗片剂的药物含量相等,否则
会影响剂量的准确度。
可采用荧光分析法或HPLC分析法进行检查。
4. 溶解度检查:片剂在口腔中溶解后,药物必须能够充分溶解并
迅速吸收。
可以采用体外溶解率试验进行检查。
5. 分散性检查:若片剂为悬浮片,则需要检查悬浮液的稳定性和
均匀性。
6. 含量测定:片剂药品的含量应该符合产品说明书标示的内容,
可采用滴定法、重量差分析法等进行检查。
7. 超微量物质检测:片剂中是否存在超微量物质,如重金属、农
药残留等,可以使用质谱法、原子吸收光谱法等进行检测。
总之,片剂的质量检查需要全面、细致、科学的检测手段和方法。
只有通过检查合格,才能保证片剂的质量,确保患者的用药安全。


片剂质量检查的主要内容
片剂质量检查是指对制备好的片剂进行质量评估和控制的过程。
它是药企保证片剂产品符合药典要求以及满足临床应用需要的重要
环节。
主要内容包括以下几个方面:
1. 外观检查:外观是片剂的首要指标之一,也是患者接受药品的第一印象。
外观检查包括片剂的形状、颜色、气味、质地等方面。
通过仔细观察片剂的外观特征,可以初步判断片剂是否符合质量要求。
2. 尺寸和重量检查:片剂的尺寸和重量对于患者的服用体验和剂量控制非常重要。
质量检查中需要测量片剂的长度、厚度和直径,并比较与规定要求是否相符。
同时还需要测量片剂的重量,确保每片剂的剂量准确。
3. 含量测定:片剂的含量测定是评估片剂质量的重要指标。
含量测定一般通过药物分析方法,如高效液相色谱法、紫外分光光度法等进行。
通过测定片剂中有效成分的含量,可以确保每片剂的药物剂量在规定范围内。
4. 溶出度测定:溶出度是评价片剂释放药物速度和程度的重要指标。
溶出度测定可以通过体外溶出度试验来进行,通过测定片剂中药物在一定时间内溶出的百分比,评估片剂的药物释放性能。
5. 片剂硬度测定:片剂的硬度直接影响其在包装和患者服用过程中的耐受性。
硬度测定可以通过药物硬度计来进行,按一定压力测试片剂的硬度值。
合格的片剂应具有足够的硬度以保持其完整性,并能够方便地分割成均匀的剂量。
总之,片剂质量检查的主要内容涵盖了外观、尺寸和重量、含量、溶出度以及硬度等方面的评估。
这些检查内容的合格与否直接关系到片剂的质量和疗效,对于确保片剂的安全性和有效性具有重要意义。

片剂的质量检查第五节片剂的质量检查、处方设计及举例1.片剂的质量检查⑴外观性状应完整光洁、色泽均匀、无杂斑、无异物⑵片重差异应符合药典规定。
具体检查方法:取20片,精密称定每片的片重并求得平均片重,然后以每片片重与平均片重比较,超出差异限度的药片不得多于2片,并不得有一片超出限度1倍。
平均片重0.30克以下,重量差异限度+-7.5%;平均片重0.30克及以上,重量差异限度+-5%⑶脆碎度用Roche脆碎度测定仪,通常脆碎度<1%为合格。
⑷崩解时限凡规定检查溶出度、释放度或融变时限的制剂,不再进行崩解时限检查。
方法:中国药典采用升降式崩解仪。
除另有规定外,取6片,启动崩解仪进行检查,各片均应在15分钟内全部崩解,如有一片不完全,应另取6片重复,均应符合规定。
普通压制片:应在15min内全部崩解薄膜衣片:应在30min内全部崩解糖衣片:应在60min内全部崩解肠衣片:先在盐酸溶液(9→100)中检查2h,每片不得有裂缝崩解或软化现象,于pH为6.8的磷酸盐缓冲液中1h内应全部崩解。
含片:应在30min内全部崩解或溶化。
舌下片:应在5min内全部崩解或溶化。
可溶片:水温15℃~25℃,应在3min内全部崩解或溶化。
结肠定位肠溶片:pH为7.8~8.0的磷酸盐缓冲液中60min内全部释放或崩解。
⑸溶出度或释放度溶出度检查用于一般的片剂,而释放度检查用于缓控释制剂溶出度:是指药物从片剂或胶囊等固体制剂在规定的介质中溶出的速度和程度。
凡检查溶出度或释放度的制剂,不在进行崩解时限的检查。
药物的溶出度可以反应药物在体内吸收的情况,药物体外溶出与体内吸收具有相关性。
溶出度的判断标准:6片中,每片的溶出量按标示量计算,均不低于规定限度6片中,如有1~2片低于规定限度,但不低于规定限度-10%,且其平均溶出量不低于规定限度,仍可判断符合规定6片中,如有1~2片低于规定限度,其中仅有1片低于规定限度-10%,但不低于规定限度-20%,且其平均溶出量不低于规定限度时,应另取6片复试;初、复试的12片中有1~3片低于规定限度,其中仅有1片低于规定限度-10%,但不低于规定限度-20%,且其平均溶出量不低于规定限度,也可判断符合规定⑹含量均匀度含量均匀度:是指小剂量或单剂量固体制剂、半固体制剂和液体制剂的每片(个)含量符合标示量的程度。
简述片剂质量检查的主要内容。
片剂质量检查的主要内容可分为以下几个方面:
一、定性检查:
1、外观检查:包括外形、规格、颜色、品牌等,需要查看与标准药品样品的一致性;
2、包装完整性检查:查看包装完整性,需要检查是否有破损等异常情况;
3、检查标签:查看标签内容是否准确,需要根据标签信息判断正确性;
4、仪器检查:当检查时,需要检查生产日期、质量保证期和有效期等,以确保产品质量可控。
二、定量检查:
定量检查是片剂质量检查的重要环节,主要包括:
1、药品含量测定:对药品的有效成分进行测定,以确保药品的安全和有效性;
2、特性检查:检查片剂的苗度、透光度等特性,以确保片剂质量;
3、类别检查:确定片剂的剂型,类别,以确保其符合标准要求;
4、存储条件检查:确保片剂在一定条件下的质量,需要检查存储环境和温度等参数是否满足要求。
片剂的质量检查项目 Revised at 2 pm on December 25, 2020.
片剂的质量检查项目:外观性状、片重差异、硬度和脆碎度、崩解度(压制片崩解时限为15m i n,浸膏片、糖衣片、薄膜衣片为60m i n)、溶出度或释放度、含量均匀度。
1.外观性状:完整光洁,色泽均匀,无异物,无杂斑,有效期内保持不变。
2.片重差异:取20片称重,将每片片重与平均片重比较,超出差异限度的药片不得多于2片,并不得有1片超出限度1倍。
糖衣片、薄膜衣片应在包衣前查片芯的重量差异,包衣后不再
检测。
查均匀度的片剂,不必查片重。
3.硬度和脆碎度:应用孟山都硬度计法和罗许脆碎仪法。
4.崩解度(崩解时限):吊篮法检查。
其中压制片(素片)为15min。
包衣片(浸膏片、糖衣片、薄膜衣片)为60min(素片的4倍)。
而肠溶衣片在人工胃液中2小时内不得有裂缝、崩解或软化等,医学教|育网收集整理在人工肠液中1小时内需全部溶散或崩解并通过筛网。
5.溶出度或释放度:如口含片、咀嚼片(不查崩解度)。
6.含量均匀度:取10片分别测定每片的相对含量,按《中国药典》法检查判断是否合格。
片剂四用测定仪:用于药片的硬度、脆碎度、崩解时限、溶出度的测试。
一、崩解时限1、崩解时限:是指片剂在规定的液体介质和条件下破碎成小粒子并通过规定筛网所需的时间。
崩解度是片剂的重要质量指标之一。
制剂崩解的快慢及崩解后颗粒的大小,均有可能影响药物疗效。
影响片剂崩解的因素:如主药的理化性质、崩解剂及其用量、粘合剂的粘性和用量、润滑剂的疏水性、颗粒大小等等。
依据《中国药典》202X年版崩解时限检查法检查,应符合规定:口含片、咀嚼片、溶液片、缓控释片,不需要作崩解时限检查。
〔1〕压制片应在15min内全部崩解。
〔2〕浸膏片、薄膜衣片应在1h内全部崩解。
〔3〕肠衣片先在盐酸溶液〔9→1000〕中检查2h,每片不得有裂缝崩解或软化现象,于ph为6.8的磷酸盐缓冲液中1h内应全部崩解。
2、崩解时限检查应用片剂四用测定仪进行测定。
采纳吊篮法,方法如下:取药片6片,分别置于吊篮的玻璃管中,每管各加一片,开动仪器使吊篮浸入37±1.0℃的水中,按肯定的频率〔30-32次/min〕和幅度〔55±2mm〕往复运动。
从片剂置于玻璃管开始计时,至片剂破碎并全部固体粒子都通过玻璃管底部的筛网〔Φ2mm〕为止,该时间即为该片剂的崩解时间,应符合规定崩解时限〔一般压制片为15min〕。
如有1片不符合要求,应另取6片复试,均应符合规定。
不同种类的片剂崩解时限:一般片剂在15min内全部崩解;薄膜衣片应在30min内全部崩解;糖衣片应在1小时内全部崩解;含片应在30min内全部崩解;舌下片应在5min内全部崩解。
二、硬度和脆碎度它们是反映药物的压缩成形性,对片剂的生产、运输和贮存带来直接影响,对片剂的崩解,溶出度都有直接影响。
用于测定片剂硬度和脆碎度的仪器有:孟山都硬度计、Roche脆碎仪等。
硬度一般指外表硬度,可用片剂硬度测定仪测定,《中国药典》未规定硬度的大小,但生产企业为了保证药片在包衣、包装、运转过程中片子的完整都对其做了具体的规定;脆碎度的测定《中国药典》已有规定。
实用文档之"片剂的质量检查项目:外观性状、片重差异、硬度和脆碎度、崩解度(压制片崩解时限为15min,浸膏片、糖衣片、薄膜衣片为60min)、
溶出度或释放度、含量均匀度。
"
1.外观性状:完整光洁,色泽均匀,无异物,无杂斑,有效期内保持不
变。
2.片重差异:取20片称重,将每片片重与平均片重比较,超出差异限度的药片不得多于2片,并不得有1片超出限度1倍。
糖衣片、薄膜衣片应在包衣前查片芯的重量差异,包衣后不再检测。
查均匀度的片剂,不必查片重。
3.硬度和脆碎度:应用孟山都硬度计法和罗许脆碎仪法。
4.崩解度(崩解时限):吊篮法检查。
其中压制片(素片)为15min。
包衣片(浸膏片、糖衣片、薄膜衣片)为60min(素片的4倍)。
而肠溶衣片在人工胃液中2小时内不得有裂缝、崩解或软化等,医学教|育网收集整理在人工肠液中1小时内需全部溶散或崩解并通过筛网。
5.溶出度或释放度:如口含片、咀嚼片(不查崩解度)。
6.含量均匀度:取10片分别测定每片的相对含量,按《中国药典》法检
查判断是否合格。
执业药师西药药剂学知识点辅导:片剂的质量检查一、片剂的质量要求《中国药典》2005年版要求片剂在生产与贮藏期间应符合下列规定:(1)原料药与辅料混合均匀。
含药量小或含毒、剧药物的片剂,应采用适宜方法使药物分散均匀。
(2)凡属挥发性或对光、热不稳定的药物,在制片过程中应遮光、避热,以避免成分损失或失效。
(3)压片前的物料或颗粒应控制水分,以适应制片工艺的需要,防止片剂在贮存期间发霉、变质。
(4)含片、口腔贴片、咀嚼片、分散片、泡腾片等根据需要可加入矫味剂、芳香剂和着色剂等附加剂。
(5)为增加稳定性、掩盖药物不良臭味、改善片剂外观等,可对片剂进行包衣。
(6)片剂外观应完整光洁,色泽均匀,有适宜的硬度和耐磨性,除另有规定外,对于非包衣片,应符合片剂脆碎度检查法的要求,防止包装、运输过程中发生磨损或破碎。
(7)片剂的溶出度、释放度、含量均匀度、微生物限度等应符合要求。
必要时,薄膜包衣片剂应检查残留溶剂。
(8)除另有规定外,片剂应密封贮存。
二、质量检查除另有规定外,片剂应进行以下相应检查。
(一)重量差异取供试品20片,精密称总重量,求得平均片重后,再分别精密称定每片的重量,每片重量与平均片重相比较(凡无含量测定的片剂,每片重量应与标示片重比较),按表中的规定,超出重量差异限度的不得多于2片,并不得有1片超出限度1倍。
糖衣片的片芯应检查重量差异并符合规定,包糖衣后不再检查重量差异。
薄膜衣片应在包薄膜衣后检查重量差异并符合规定。
凡规定检查含量均匀度的片剂,一般不再进行重量差异检查。
(二)崩解时限照《中国药典》2005年版崩解时限检查法检查,应符合规定:口含片、咀嚼片、溶液片、缓控释片,不需要作崩解时限检查。
崩解时限标准:(1)压制片应在15min内全部崩解。
(2)浸膏片、薄膜衣片应在1h内全部崩解。
(3)肠衣片先在盐酸溶液(9→1000)中检查2h,每片不得有裂缝崩解或软化现象,于ph为6.8的磷酸盐缓冲液中1h内应全部崩解。
片剂质量检查
Document serial number【UU89WT-UU98YT-UU8CB-UUUT-UUT108】
实验二片剂的质量检查
I.实验目的
掌握片剂的外观形状描述、硬度、脆碎度、崩解与溶出度的测定方法和测定原理。
II.实验原理
1.外观:
应当完整光洁,色泽均匀,无异物,无杂斑
2.崩解时限:
是指片剂在规定的液体介质和条件下破碎成小粒子并通过规定筛网所需的时间。
崩解度是片剂的重要质量指标之一制剂崩解的快慢及崩解后颗粒的大小,均有可能影响药物疗效。
影响片剂崩解的因素:如主药的理化性质、崩解剂及其用量、粘合剂的粘性和用量、润滑剂的疏水性、颗粒大小等等。
通过使用不同类型的辅料制备阿司匹林片,比较它们的崩解时限,可以了解这些辅料的性质。
根据《中国药典》2005年版崩解时限检查法检查,应符合规定:口含片、咀嚼片、溶液片、缓控释片,不需要作崩解时限检查。
(1)压制片应在15min内全部崩解。
(2)浸膏片、薄膜衣片应在1h内全部崩解。
(3)肠衣片先在盐酸溶液(9→1000)中检查2h,每片不得有裂缝崩解或软化现象,于ph为的磷酸盐缓冲液中1h内应全部崩解。
3.硬度和脆碎度
它们是反映药物的压缩成形性,对片剂的生产、运输和贮存带来直接影响,对片剂的崩解,溶出度都有直接影响。
用于测定片剂硬度和脆碎度的仪器有:孟山都硬度计、Roche脆碎仪等。
4.溶出度
指在规定条件下,药物从片剂、胶囊剂或颗粒剂等固体制剂溶出的速率和程度。
III.实验步骤
1、检查外观
2、崩解时限的测定:
崩解仪的调试:
将吊篮通过上端的不锈钠轴悬挂于金属支架上,浸入盛有37℃的水的1000ml烧杯中,打开开关,吊篮做升降运动,每分钟约30-32次。
调节吊篮的位置,使其下降时筛网距离烧杯底部约25mm,吊篮上升时筛网在水面下25mm处。
支架上下运动的距离约55mm;
测定崩解时限:
取普通片剂药片(如阿司匹林片)6片,分别置上述吊篮的6个玻璃管中(如药片漂浮可投入塑料挡板),立即启动崩解仪进行检查,记录崩解完全的时间,各片均应在15min内全部崩解,如有1片不能崩解,应另取6片按上述方法复试,均应符合规定。
不同种类的片剂崩解时限:
普通片剂在15min内全部崩解、薄膜衣片应在30min内全部崩解、糖衣片应在1小时内全部崩解、含片应在30min内全部崩解、舌下片应在5min内全部崩解。
3、硬度检查
将片剂立面放置于孟山都硬度仪上,归零后逐步、缓慢增加压力,直至片剂被压碎,读取表盘读数,即为片剂硬度。
4、度检查
片重为或以下者取若干片,使其总重约为;片重大于者取10片。
用吹风机吹去脱落的粉末,精密称重,置圆筒中,转动100次。
取出,同法除去粉末,精密称重,减失重量不得过1%,且不得检出断裂、龟裂及粉碎的片。
本试验一般仅作1次。
如减失重量超过1%时,可复检2次,3次的平均减失重量不得过1%,并不得检出断裂、龟裂及粉碎的片。
5、溶出度的测定
量取经脱气处理的溶出介质(L的HCL)900ml,倒入每个操作容器内,加热使溶剂温度保持在37度左右。
取供试品(阿司匹林片)6片,分别投入6个的转篮内,将转篮降入容器中,立即计时,在规定取样点吸取溶液适量,立即经微孔滤膜滤过(自取样至滤过应在30s内完成),测量不同取样点溶液的吸光度。
IV.实验结果
1、外观性状:
可见完整光洁,色泽均匀,无异物,无杂斑,故检验合格
2、实验中阿司匹林6片均在3min之内全部崩解,按药典规定,压制片应在15min内崩解完全,故检验合格
3、硬度:
此处共计6片,是按照班级所有同学测量的,应当全班分成三组,每组取两片的数据
片剂标准硬度为3-5kg,故检验合格。
4、脆碎度
检查前总片重m1=
检查后总片重m2=
(m1-m2)/ m1*100%=%<1%
故检验合格。