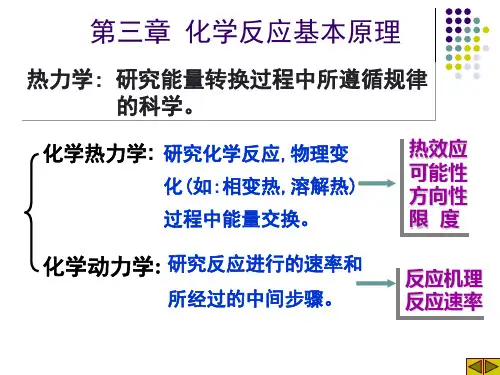
第三章 化学反应基本原理
- 格式:ppt
- 大小:242.50 KB
- 文档页数:19






初中化学反应基本原理教案教学目标:1. 了解化学反应的概念和特点;2. 掌握化学反应的基本原理,包括反应物、生成物、反应条件等;3. 能够运用化学反应的基本原理分析和解释一些常见的化学现象。
教学重点:1. 化学反应的概念和特点;2. 化学反应的基本原理。
教学难点:1. 化学反应的判断和分析;2. 化学反应条件的理解。
教学准备:1. 实验室用具:烧杯、试管、试剂等;2. 教学课件或黑板。
教学过程:一、导入(5分钟)1. 通过一些日常生活中的化学现象,如烧水、铁生锈等,引导学生思考化学反应的概念和特点;2. 学生分享对化学反应的理解,教师总结并板书化学反应的定义和特点。
二、化学反应的基本原理(15分钟)1. 介绍化学反应的基本原理,包括反应物、生成物、反应条件等;2. 通过实验室演示或视频资料,展示一些常见的化学反应,如酸碱中和、氧化还原等;3. 引导学生观察和分析化学反应中的反应物、生成物和反应条件;4. 学生分组讨论,总结化学反应的基本原理。
三、案例分析(15分钟)1. 给学生发放一些化学反应的案例,要求学生根据化学反应的基本原理进行分析和判断;2. 学生独立完成案例分析,教师巡回指导;3. 学生汇报分析结果,教师点评并讲解。
四、课堂小结(5分钟)1. 教师引导学生回顾本节课所学内容,总结化学反应的基本原理;2. 学生分享学习收获,教师给予鼓励和评价。
五、作业布置(5分钟)1. 让学生结合课堂所学,选取一些生活中的化学现象,运用化学反应的基本原理进行分析和解释;2. 完成课后练习,巩固所学知识。
教学反思:本节课通过生活中的化学现象导入,激发学生的学习兴趣,引导学生思考化学反应的概念和特点。
通过实验室演示和视频资料,让学生直观地感受化学反应的基本原理,并通过分组讨论和案例分析,培养学生运用化学反应的基本原理分析和解决问题的能力。
整个教学过程中,教师注重启发引导,学生积极参与,课堂氛围活跃。
作业布置结合生活实际,让学生能够将所学知识运用到生活中,提高学生的实践能力。


化学反应原理课本
化学反应原理是化学科学中的重要内容之一。
化学反应是指原子、离子或分子之间发生一系列的转化过程,形成新的物质。
化学反应的原理是基于分子能量和键的断裂和形成。
化学反应的原理可以归结为以下几个方面:
1. 反应物的相互作用:在化学反应中,反应物会发生相互作用,通过传递电子、质子或自由基等方式,原子、离子或分子之间发生物质和能量的转移。
2. 化学键的形成与断裂:在化学反应中,化学键会发生形成和断裂。
当化学键断裂时,反应物分子中的原子重新组合,形成新的化学键,从而生成新的物质。
3. 反应速率与反应动力学:不同的化学反应具有不同的反应速率。
反应速率受到反应物浓度、温度、压力等因素的影响。
反应速率可以通过动力学研究来确定。
4. 反应平衡与化学平衡常数:化学反应可能达到平衡状态,即反应物和生成物浓度达到一定比例。
反应平衡可以通过化学平衡常数来描述,该常数与反应物浓度之比有关。
5. 反应热力学与热效应:化学反应在发生时会伴随着能量的转化,有些反应会释放热量,称为放热反应;有些反应会吸收热量,称为吸热反应。
反应热力学可以研究反应的热效应。
化学反应原理的研究不仅对于了解化学反应过程和性质有重要意义,也对于实际应用具有重要价值。
通过对化学反应原理的深入研究,可以指导新化合物的合成、催化剂的设计和反应条件的优化等工作。


第三章 理想流动反应器概述按照操作方式,可以分为间歇过程和连续过程,相应的反应器为间歇反应器和流动反应器。
对于间歇反应器,物料一次性加入,反应一定时间后把产物一次性取出,反应是分批进行的。
物料在反应器内的流动状况是相同的,经历的反应时间也是相同的。
对于流动反应器,物料不断地加入反应器,又不断地离开反应器。
考察物料在反应器内的流动状况。
有的物料正常的通过反应器,有的物料进入反应器的死角,有的物料短路(即近路)通过反应器,有的物料在反应器内回流。
在流动反应器中物料的流动状况不相同,造成物料浓度不均匀,经历的反应时间不相同,直接影响反应结果。
物料在反应器内的流动状况看不见摸不着。
人们采用流动模型来描述物料在反应器内的流动状况。
流动模型分类如下:理想流动模型 流动模型非理想流动模型特别强调的是,对于流动反应器,必须考虑物料在反应器内的流动状况;流动模型是专指反应器而言的。
第一节 流动模型概述3-1 反应器中流体的流动模型平推流模型全混流模型一、物料质点、年龄、奉命及其返混1.物料质点物料质点是指代表物料特性的微元或微团。
物料由无数个质点组成。
2.物料质点的年龄和寿命年龄是对反应器内质点而言,指从进入反应器开始到某一时刻,称为年龄。
寿命是对离开反应器的质点而言,指从进入反应器开始到离开反应器的时间。
3.返混(1)返混指流动反应器内不同年龄质点间的混合。
在间歇反应器中,物料同时进入反应器,质点的年龄都相同,所以没有返混。
在流动反应器中,存在死角、短路和回流等工程因素,不同年具的质点混合在一起,所以有返混。
(2)返混的原因a.机械搅拌引起物料质点的运动方向和主体流动方向相反,不同年龄的质点混合在一起;b.反应器结构造成物料流速不均匀,例如死角、分布器等。
造成返混的各种因素统称为工程因素。
在流动反应器中,不可避免的存在工程因素,而且带有随机性,所以在流动反应器中都存在着返混,只是返混程度有所不同而已。
二、理想流动模型1.平推流模型(活塞流模型、理想置换模型、理想排挤模型)平推流模型认为物料进入反应器后沿着流动方向象气缸里的活塞一样向前移动,彼此不相混合。
化学反应原理第三章第三节沉淀溶解平衡化学反应原理第三章第三节沉淀溶解平衡教学案⽂登⼀中⾼⼆化学组新授教学案引、导学、测议、教查、练出⽰⽬标学习指导⾃主学习⾃我检测合作探究讲解提⾼⾃查反馈拓展训练〖教学流程〗〖学习过程〗【温故知新】1.根据溶解度的不同可将物质分为难溶、微溶、可溶、易溶。
2. CaCO3、FeS、Mg(OH)2等难溶电解质在⽔溶液中以何种形式存在?学习内容⼀:沉淀溶解平衡与溶度积【学习⽬标】1. 知道难溶电解质在⽔中存在沉淀溶解平衡,并能结合实例进⾏描述。
2. 了解沉淀溶解平衡的概念及其影响因素。
3. 了解溶度积的含义、表达式的书写及其计算。
4. 知道溶度积是沉淀溶解平衡的平衡常数,溶度积可以反映难溶电解质在⽔中的溶解能⼒。
【学习指导】沉淀溶解平衡建⽴的描述总结沉淀溶解平衡的概念;1.根据PbI3.通过阅读表3-3-1⼏种难溶电解质的Ksp,总结常见沉淀AgCl、AgBr、AgI 溶解能⼒的⼤⼩;【⾃主学习】阅读教材P页【观察·思考】90—91实验现象:在上层清液中滴加KI溶液后,有______________产⽣。
结论解释:说明上层清液中有_______当加⼊KI后,I-浓度增⼤,从⽽有___⾊的____⽣成。
⼀、沉淀溶解平衡1、定义:⼀定温度下,难溶电解质在⽔中_________的速率和_________的速率相等时,形成电解质的________ 溶液,达到平衡状态,我们把这种平衡称为沉淀溶解平衡。
2、沉淀溶解平衡的特征:(1)_________(2)________(3)_______(4)______ (5)____3、影响沉淀溶解平衡的因素:(1)内因:(2)外因:⼆、沉淀溶解平衡常数-----溶度积常数或溶度积Ksp1、定义:在⼀定条件下,难溶电解质在溶液中达到时,其称为溶度积常数简称为溶度积,⽤______表⽰,有单位。
例如: Mg(OH)2(s) ≒ Mg2 + (aq) +2OH- (aq)25℃ Ksp = [Mg2 + ][OH-]2= 5.6×10-12mol3·L-32、表达式:(见P96页)对于 AmBn (s)3、溶度积的影响因素:溶度积(Ksp )的⼤⼩与_____________和______________有关,与⽆关。