尿素的标准化学知识点归纳
- 格式:docx
- 大小:12.69 KB
- 文档页数:3


尿素
尿素是一种有机化合物,其化学式为(NH₂)₂CO。
在不同应用领域,尿素的标准可能涉及不同的参数和规范。
以下是一些可能的尿素标准:
1.化学纯度:尿素的化学纯度是一个关键参
数。
标准可能规定尿素中其他杂质的最大允
许含量,确保产品符合特定纯度要求。
2.氮含量:尿素中的氮含量通常是一个关注
的指标,因为氮是尿素中的主要元素。
标准
可能规定产品中氮的最低或最高含量。
3.水含量:尿素中的水分含量也是一个重要
的质量参数。
标准可能规定产品中的最大允
许水分含量。
4.颗粒度和晶体形态:尿素的颗粒度和晶体
形态对其在不同应用中的溶解性和反应性
可能产生影响。
标准可能包括对颗粒度和晶
体形态的要求。
5.重金属和其他杂质:尿素中的重金属和其
他杂质的含量可能受到限制。
标准可能规定
这些杂质的最大允许含量。
6.pH值:尿素溶液的pH值可能是另一个需
要监控的参数,特别是在一些农业和生物化
学应用中。
7.安全和环保标准:尤其是用于农业或食品
生产的尿素,可能受到有关安全和环保方面
的标准的限制。
请注意,具体的尿素标准可能会根据产品的用途、生产国家/地区以及行业要求而有所不同。

化学中考知识点总结尿素一、尿素的基本概念尿素是一种无机化合物,化学式为(NH2)2CO,又称做碳酰胺。
它是一种含有两个氨基(NH2)和一个羰基(CO)的有机胺,是氨和二氧化碳发生缩合反应制得的。
二、尿素的性质1. 物理性质(1)纯尿素为无色、无味且易溶于水的结晶固体,呈白色结晶粉末状。
(2)它具有很强的吸湿性,能与水形成氢键,使其在水溶液中电离产生尿酰离子。
2. 化学性质(1)尿素可以和酚酞溶液产生显色反应,可以用来定量分析。
(2)当尿素受热分解时,会生成氨气和氰酸盐。
三、尿素的用途1. 化肥生产尿素是一种重要的化肥原料,可以直接用于农作物的施肥,也可以用于生产其他复合肥料。
2. 化学工业尿素也被用于生产其他化学品,如有机总成分合成、合成树脂、合成塑料等。
3. 医药领域尿素在医药领域也有广泛的应用,可以用作皮肤保湿剂、止痒剂、解毒剂等。
四、尿素的制备1. 由氨与二氧化碳的直接合成NH3 + CO2 → (NH2)2CO这种方法是最常用的工业生产方法,通常在高温和高压下进行。
2. 尿素是由尿液蒸发和结晶而成的这是古老的尿素获取方法,在很早的时候就被人们采用,但效率较低且工艺复杂。
五、尿素的分解反应尿素在高温下可以分解为氨气和二氧化碳。
这个反应在实验室中经常使用,直接用作检验氨气的方法。
6. 尿素的性质变化尿素在高温下会发生热分解至多肽,氨、氰酸和二氧化碳。
虽然尿素是固体,但它容易与水结合,也是稳定在湿环境中。
在较高温度下,尿素还会与酚酞产生显色反应,常用于化学定量分析的试剂。
7. 尿素的特性尿素具有无色、易溶于水的特性,呈弱碱性,成为细胞外液中的主要氮源。
此外,它还可以用来合成无酰胺,并成为有机综合中间体。
八、尿素的反应尿素是一种弱碱,其碱性能够和酸类发生中和反应。
此外它还可以和一些重金属离子发生络合反应。
九、尿素在医药领域的应用1. 作为外用药制剂尿素是一种优良的皮肤软化剂,可以用于治疗由于干燥引起的皮肤瘙痒、糜烂和角质硬化等情况。

尿素高中化学那部分
《尿素:高中化学的重要知识点》
尿素是一种常见的有机化合物,化学式为(NH₂)₂CO。
它是由两个氨基和一个羰基(碳氧
双键)组成的有机分子。
尿素在高中化学中是一个重要的知识点,因为它在生物、医药和工业领域都有广泛的应用。
在生物领域,尿素是人体代谢的产物之一。
当蛋白质和氨基酸代谢产生过多的氨基基团时,肝脏会将其转化为尿素,然后通过肾脏排泄出体外。
这个过程被称为尿素氮的代谢。
因此,尿素是人体排泄氨的主要途径,维持了体内氮平衡。
此外,尿素还被用作肥料,通过提供植物所需的氮元素来促进植物生长。
在医药领域,尿素有着广泛的用途。
它可以作为一种皮肤保湿剂,被添加到化妆品和护肤品中以帮助皮肤保持水分和柔软度。
此外,尿素还可以用于治疗一些皮肤病,例如湿疹和银屑病。
它还可以作为一种脱毛剂,通过溶解角质层来去除多余的毛发。
在工业领域,尿素被用作化肥和生产其他化学品的原料。
尿素是一种常见的氮肥,可溶于水,提供植物所需的氮元素。
此外,尿素还可以用于生产尿素树脂、尿素甲醛树脂和尿素硝化甲醇等化工产品,广泛应用于木材、造纸、医药、农药和塑料等行业。
总的来说,高中化学学习中的尿素知识不仅能帮助学生理解生物、医药和工业领域的应用,还能为他们打下进一步学习有机化学和化学工程的基础。
因此,学生们应该认真学习尿素的性质、制备和应用,将其作为化学学习中的重要知识点。


尿素CO(NH2)2,亦称脲。
相当于碳酸的二酰氨。
在人的蛋白质分解最终产物中占有相当大的比例。
在普通膳食的情况下,每日尿中可排出25—30克,接近尿中总氮量的87%。
一般来说,两栖类的成体、软骨鱼类和哺乳类具有相同的倾向。
因在这些生物体中,尿素是在鸟氨酸循环中形成的,所以排出尿素的动物具有所必需的整个酶系统,在动物中欠缺其中任何一种酶便排出尿酸(鸟类)或氨(硬骨鱼类)。
刀豆和大豆植物的种子中存在很多的脲酶,它可使尿素水解为二氧化碳和氨。
尿素也是很重要的肥料。
尿素外观为白色晶体或粉末。
是动物蛋白质代谢后的产物,通常用作植物的氮肥。
尿素是哺乳类动物排出体内含氮代谢物的形式。
它在肝合成,其过程被称为尿素循环。
别名:碳酰二胺、碳酰胺、脲分子式:CO(NH2)2,因为在人尿中含有这种物质,所以取名尿素。
尿素含氮(N)46%,是固体氮肥中含氮量最高的。
生产方法:工业上用液氨和二氧化碳为原料,在高温高压条件下直接合成尿素,化学反应如下。
2NH3+CO2→NH2COONH4→CO(NH2)2+N2O尿素易溶于水,在20℃时100毫升水中可溶解105克,水溶液呈中性反应。
尿素产品有两种。
结晶尿素呈白色针状或棱柱状晶形,吸湿性强。
粒状尿素为粒径1~2毫米的半透明粒子,外观光洁,吸湿性有明显改善。
20℃时临界吸湿点为相对湿度80%,但30℃时,临界吸湿点降至72.5%,故尿素要避免在盛夏潮湿气候下敞开存放。
目前在尿素生产中加入石蜡等疏水物质,其吸湿性大大下降。
尿素是生理中性肥料,在土壤中不残留任何有害物质,长期施用没有不良影响。
但在造粒中温度过高会产生少量缩二脲,又称双缩脲,对作物有抑制作用。
我国规定肥料用尿素缩二脲含量应小于0.5%。
缩二脲含量超过1%时,不能做种肥,苗肥和叶面肥,其他施用期的尿素含量也不宜过多或过于集中。
尿素是有机态氮肥,经过土壤中的脲酶作用,水解成碳酸铵或碳酸氢铵后,才能被作物吸收利用。
因此,尿素要在作物的需肥期前4~8天施用。

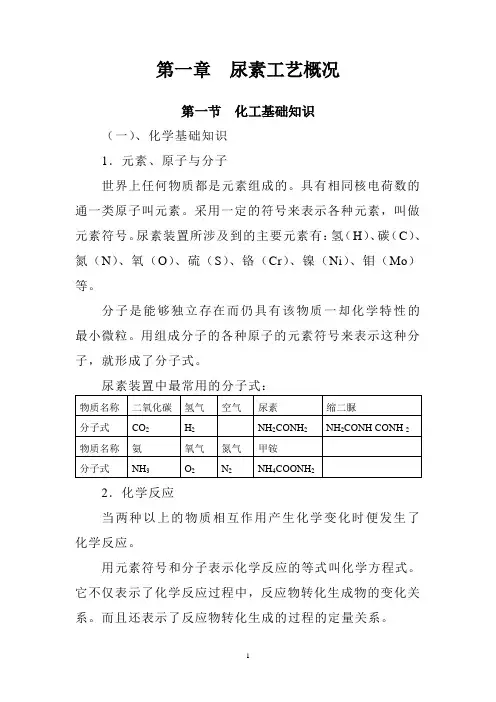
第一章尿素工艺概况第一节化工基础知识(一)、化学基础知识1.元素、原子与分子世界上任何物质都是元素组成的。
具有相同核电荷数的通一类原子叫元素。
采用一定的符号来表示各种元素,叫做元素符号。
尿素装置所涉及到的主要元素有:氢(H)、碳(C)、氮(N)、氧(O)、硫(S)、铬(Cr)、镍(Ni)、钼(Mo)等。
分子是能够独立存在而仍具有该物质一却化学特性的最小微粒。
用组成分子的各种原子的元素符号来表示这种分子,就形成了分子式。
尿素装置中最常用的分子式:2.化学反应当两种以上的物质相互作用产生化学变化时便发生了化学反应。
用元素符号和分子表示化学反应的等式叫化学方程式。
它不仅表示了化学反应过程中,反应物转化生成物的变化关系。
而且还表示了反应物转化生成的过程的定量关系。
(二)、化工基础知识化工生产是以煤、石油、天然气、水、空气等天然资源或农副产品为原料,经过一系列化学变化或化学处理为主要手段,改变物质原来的性质,状态和组成,制成所需的产品。
1.化工单元操作化学工业的种类很多,涉及酸、碱、化肥、医药以及石油化工等,它们所采用的生产方法、工艺流程、设备大小也往往千差万别,各有不同。
它们之所以统归化学工业范筹,首先是因为这些工业过程中所用的原料最终变为产品,不仅在物质上发生了变化,而且一般地都伴随化学性质的变化,而这些不同的生产过程都是一些基本操作组成,如流体的流动与输送、压缩、分离、传热、蒸发、精馏、解吸、吸收、冷却、破碎等操作,我们把这些操作称为化学基本单元操作。
若干单元操作串联起来就构成了一个化工产品的生产过程。
在尿素的生产工艺中几乎包括了所有的化工单元操作。
2.化工单元操作分类按照单元操作所遵循的基本规律不同可归纳为几个基本过程:(1)、动量传递过程:包括遵循流体动力学规律的一些单元操作,如流体的流动与输送、沉降、离心泵以及固态流态化、空气压缩等。
(2)、热量传递过程:简称传热过程,包括主要遵循热交换基本规律的一些单元操作,如传热、蒸发、冷凝等。


尿素的主要化学性质及生理作用尿素别名碳酰二胺、碳酰胺、脲。
是由碳、氮、氧和氢组成的有机化合物,又称脲(与尿同音)。
其化学公式为CON2H4、(NH2)2CO或CN2H4O,国际非专利药品名称为Carbamide。
外观是白色晶体或粉末。
它是动物蛋白质代谢后的产物,通常用作植物的氮肥。
尿素在肝合成,是哺乳类动物排出的体内含氮代谢物。
这代谢过程称为尿素循环。
尿素是第一种以人工合成无机物质而得到的有机化合物。
活力论从此被推翻。
可与酸作用生成盐。
有水解作用。
化肥在高温下可进行缩合反应,生成缩二脲、缩三脲和三聚氰酸。
加热至尿素分子模型160℃分解,产生氨气同时变为氰酸。
因为在人尿中含有这种物质,所以取名尿素。
尿素含氮(N)46%,是固体氮肥中含氮量最高的。
生产方法:工业上用液氨和二氧化碳为原料,在高温高压条件下直接合成尿素,化学反应如下:2NH3+CO2→NH2COONH4→CO(NH2)2+H2O尿素在酸、碱、酶作用下(酸、碱需加热)能水解生成氨和二氧化碳。
对热不稳定,加热至150~160℃将脱氨成缩二脲。
若迅速加热将脱氨而三聚成六元环化合物三聚氰酸。
(机理:先脱氨生成异氰酸(HN=C=O),再三聚。
)与乙酰氯或乙酸酐作用可生成乙酰脲与二乙酰脲。
在乙醇钠作用下与丙二酸二乙酯反应生成丙二酰脲(又称巴比妥酸,因其有一定酸性)。
在氨水等碱性催化剂作用下能与甲醛反应,缩聚成脲醛树脂。
与水合肼作用生成氨基脲。
尿素易溶于水,在20℃时100毫升水中可溶解105克,水溶液呈中性反应。
尿素产品有两种。
结晶尿素呈白色针状或棱柱状晶形,吸湿性强。
粒状尿素为粒径1~2毫米的半透明粒子,外观光洁,吸湿性有明显改善。
20℃时临界吸湿点为相对湿度80%,但30℃时,临界吸湿点降至72.5中心以化工行业技术需求和科技进步为导向,以资源整合、技术共享为基础,分析测试、技术咨询为载体,致力于搭建产研结合的桥梁。
以“专心、专业、专注“为宗旨,致力于实现研究和应用的对接,从而推动化工行业的发展。

尿素生产方法:工业上用液氨和二氧化碳为原料,在高温高压条件下直接合成尿素,化学反应如下:2NH3+CO2→NH2COONH4→CO(NH2)2+H2O尿素在酸、碱、酶作用下(酸、碱需加热)能水解生成氨和二氧化碳。
对热不稳定,加热至150~160℃将脱氨成缩二脲。
若迅速加热将脱氨而三聚成六元环化合物三聚氰酸。
(机理:先脱氨生成异氰酸(HN=C=O),再三聚。
)尿素是一种高浓度氮肥,属中性速效肥料,也可用于生产多种复合肥料。
在土壤中不残留任何有害物质,长期施用没有不良影响。
尿素是有机态氮肥,经过土壤中的脲酶作用,水解成碳酸铵或碳酸氢铵后,才能被作物吸收利用。
因此,尿素要在作物的需肥期前4~8天施用。
我国尿素颗粒度占95%以上是0.8-2.5mm小颗粒,有强度低、易结块和破碎粉化等弊病。
若要知道大颗粒尿素,势必要大幅度增加造粒塔高度和塔径,很不现实。
同时小颗粒尿素无法进行进一步加工成掺混肥、包覆肥、缓效或长效肥等提高肥料利用率。
肥料的改性产品:大颗粒尿素改性:大颗粒尿素加工成缓效肥料,肥效可以提高60-70%,而普通尿素的尿素氮肥利用率仅为30%。
涂层尿素:在尿素颗粒表面涂上不渗透或半渗透物质的膜层。
蜡聚合物硫磺包膜尿素:利用水渗透性不同的包膜材料包裹在水溶性肥料表面,使肥料养分持续缓慢释放,提高肥效。
涂硫尿素生产技术:据统计亚洲地区2006年缺硫大6000kt/a,而我国百分之三十的耕地缺硫。
采用转鼓帘涂布技术在尿素颗粒上涂以硫磺,是实施涂硫尿素生产较为理想的方法。
涂硫尿素能达到养分缓慢释放的效果。
工业小颗粒尿素单位体积比表面积大,涂布相同厚度的硫磺比大颗粒尿素需要的质量百分数高,而且大部分小颗粒尿素都有一个孔或表面凹陷,致使难以获得满意的涂层。
因此涂硫所用的尿素应选用大而圆的尿素颗粒。
汉枫缓释肥料有限公司从加拿大引进了年产11万吨涂硫尿素生产线。
国内主要尿素生产企业汇总华东山东鲁西化工股份;山东寿光联盟化工;山东华鲁恒升;山东明水大化;山东中化平原化工(中化化肥);山东鲁南化肥;山东兖矿峄山;山东瑞星化工;山东阿斯得化工;山东恒通化工;山东滕州瑞达;山东中农润田化工;山东永兴化工;山东烟台巨力(莱阳);山东瀚海化工;山东东明县化肥厂;山东济宁恒力化工;山东章丘日月化工;山东青岛金浪化工集团(莱西);山东青岛碱业天柱(化肥);山东宁阳飞达化工;山东诸城良丰化学;山东鲁洲集团化工;山东齐鲁一化;山东金乡德华化工(济宁市金乡县)(现已停产);山东海化集团;江苏灵谷化工股份(宜兴);江苏新沂恒盛化工;江苏金陵石化(中石化);江苏灵谷化工(姜堰分厂);江苏华昌化工股份;江苏大丰劲力化肥;江苏双多化工(阜宁县);安徽昊源化工;安徽临泉化工股份(晋煤集团);安庆石化(中石化);安徽三星化工;安徽淮化化工;安徽金禾化工;安徽红四方化工股份;安徽六安建来化工;安徽定远县化肥(临泉);浙江镇海石化(中石化);浙江巨化;浙江新化华北内蒙鄂尔多斯联合化工;内蒙古天野(中海油);内蒙古乌拉山化肥;山西天泽煤化工;山西晋丰煤化工;山西天脊煤化工集团;山西丰喜肥业;山西兰花科创;山西天脊中化化肥;山西霍州化学工业(宜化);山西永济中农化工;山西五台山化工;山西原平昊华;山西焦化集团;河北沧州大化;河北正元化肥集团;河北景化化工(宜化);河北东光县化肥厂;河北迁安化工;河北冀州银海化肥;河北金石化肥;河北藁城化肥厂;河北张家口双环化肥;河北张家口宣化化工;河北元氏县化肥厂;河北曲阳县化肥厂;河北唐山邦力大银;河北晶龙丰利;河北邯郸冀南;天津吉华化工;天津腾飞化工华中河南心连心化肥;河南中原大化;河南安阳化学;河南延化化工;河南平顶山飞行;河南骏马化工集团;河南大江化工(宜化);河南昊利达化工;河南兴华宜化(灵化);河南息县化肥厂;河南丰秋县化肥厂;河南庆阳县化肥厂;河南漯河宜化;河南洛阳偃师(宜化);河南太康县化肥厂;河南临颍县化肥厂河南西平县化肥厂;河南绿宇化电;河南三门峡金茂化工;河南大通化工;河南罗山金鼎;河南开封晋开;湖北宜化集团;湖北当阳华强;湖北大化(中石化);湖北三宁化工;湖北枣阳化学;湖北宜化浠水;湖北东圣化工;湖北武汉福源;湖北潜江华润;湖北大田化工股份;湖北省嘉渔县风华化工;湖南巴陵石化(中石化);湖南宜化化工;湖南天润化工;湖南株洲海达;湖南郴州桥氮;湖南临湘化工;江西九江大化(中石化);江西江氨化学工业;江西新余金叶西北陕西渭河煤化工;陕西华山化工;陕西城化股份;甘肃兰州石化(中石油);甘肃刘化集团;甘肃张掖农友;甘肃兰州远东化肥(美丰);宁夏石化(中石油);宁夏丰友化工;新疆阿克苏华锦化工(库车);新疆新化化肥;新疆乌鲁木齐石化(中石油);新疆塔里木油田(中石油泽普石化);新疆塔里木油田(中石油库尔勒)东北辽宁华锦;辽宁盘锦中润;本溪北方煤化工;吉林长山化肥(中化);吉林通化化工;中石油大庆石化化肥厂;黑龙江黑化;黑龙江浩良河(北大荒农垦集团);黑龙江农垦勃兴化工西南四川泸天化;四川川化集团;四川美丰;重庆建峰化工;四川齐鲁二化(达州);四川玉龙化工;四川金象;重庆和邦碱胺实业;重庆江北化肥;四川成都玖源;重庆禾丰化工;贵州赤天化;贵州兴义化工(宜化);贵州美丰;贵州毕节煤海化工;云天化集团;云南云维集团;云南解化集团;云南红河锦东化工华南福建三明石化;福建永安智胜;福建顺昌富宝;广西河池化工股份;广西临川化工;广西柳州化肥;海南富岛(中海油)。
尿素小知识一、尿素定义尿素是一种有机化合物,化学式为CO(NH2)2,是由碳、氮、氧和氢组成的有机阳离子,是哺乳动物和某些鱼类体内蛋白质代谢分解的主要含氮终产物。
作为一种中性肥料,尿素适用于各种土壤和植物。
在土壤中,尿素经过土壤微生物的作用,转化为铵态氮,容易被作物吸收利用。
二、尿素用途1. 尿素是化学肥料中含氮量最高的肥料,适用于各种土壤和作物,可促进作物的生长和发育。
2. 尿素可以作为基肥和追肥使用,能促进作物根系发达,提高光合作用效率,使叶片颜色加深,提高产量。
3. 尿素适用于旱地和水田,也可用于工业和医药等领域。
三、尿素生产方法1. 氨气和二氧化碳在高温高压下反应生成尿素,这是工业化生产尿素的主要方法。
2. 尿素的生产过程中需要消耗大量的能量,因此生产成本较高。
四、尿素肥效期尿素的肥效期取决于多种因素,如土壤类型、气候条件、施肥方法和作物种类等。
一般来说,尿素的肥效期在40-60天左右。
五、尿素使用注意事项1. 尿素易溶于水,在土壤中转化较慢,因此在施用时要注意控制用量,避免过量使用对作物造成伤害。
2. 尿素施用后不能立即浇水,否则会导致养分流失和降低肥效。
3. 尿素不能与碱性肥料混用,因为尿素与碱性肥料混合容易产生氨气,导致肥效降低。
4. 尿素应该存放在干燥、阴凉、通风良好的地方,避免与潮湿的地面接触,以免吸湿结块。
六、尿素真假辨别1. 观察包装:正规的尿素肥料包装袋上都有明确的商标、生产厂家、肥料登记证号等信息。
同时,要注意包装袋是否牢固,是否有破损或变形的情况。
2. 观察颜色:尿素的颜色应为白色或微黄色晶体状,如果颜色发暗或者明显有杂质,可能是劣质尿素或者假冒伪劣产品。
3. 闻气味:尿素有刺激性气味,如果闻不到或者气味不明显,可能是假冒伪劣产品。
4. 观察溶解性:取少量尿素放在水中搅拌溶解,如果溶解速度快且溶液清澈透明,说明是真品;如果溶解速度慢或者溶液浑浊不清,可能是假冒伪劣产品。
1、尿素性质:物理无色无味,无臭的针状晶体,熔点:132.7℃含氮量46.65% 结构式: CO(NH2)2化学缩合、水解、加成缩合:H2N-CO-NH2+H-NH-CO-NH2=H2N-CO-NH-CO-NH2+NH3水解:NH2CONH2+H2O=NH4COONH2NH4COONH2+H2O=(NH4)2CO3(NH4)2CO3=2NH3+CO2+H2O加成:CO(NH2)2+HNO3=CO(NH2)2HNO3CO(NH2)2+H3PO4=CO(NH2)2H3PO4CO(NH2)2+2NaOH=Na2CO3+2NH32、尿素原料:NH3、CO2氨的物理性质:无色有刺激性气味的气体;密度比空气小;ρ氨气:ρ空气=17:29;易液化;极易溶于水(体积比1:700)无色气体,有刺激性恶臭味。
分子式NH3。
分子量17.03。
相对密度0.7714g/l。
熔点-77.7℃。
沸点-33.35℃。
自燃点651.11℃。
二氧化碳,化学式为CO2,式量44.01,碳氧化物之一,俗名碳酸气,也称碳酸酐或碳酐。
常温下是一种无色无味气体,密度比空气略大,微溶于水,并生成碳酸。
(碳酸饮料基本原理)固态二氧化碳俗称干冰,升华时可吸收大量热,因而用作制冷剂,如人工降雨,也常在舞美中用于制造烟雾。
二氧化碳不参与燃烧,密度比空气略大,所以也被用作灭火剂。
二氧化碳是绿色植物光合作用不可缺少的原料,温室中常用二氧化碳作肥料。
3、甲铵:熔点156℃结构式:NH4COONH24、尿素用途:1做肥料2工业上,用作涂料、胶合剂、油漆3、做牛羊等动物的辅助饲料,使肉和奶增产5、合成机理:2NH3(g)+CO2(g)≒NH4COONH2(l)≒NH2CONH2(l)+H2O(l)6、合成温度:水溶液全循环法T=180-210℃ CO2气提法T=180-190℃①平衡转化率随温度的升高而增加,当达到某一温度时,转化率反而下降。
②最高转化率的温度随氨碳比的增加而降低。
尿素一、简介尿素是第一种以人工合成无机物质而得到的有机化合物,是固体氮肥中含氮量最高的。
尿素是一种高浓度氮肥,属中性速效有机态肥料,也可用于生产多种复合肥料。
二、名称1、化学名称尿素、碳酰二胺、碳酰胺、脲。
2、商品名称三、系统编号四、物质颜色性状1、颜色无色、白色、白色略带微红色。
尿素产品有两种。
结晶尿素呈白色针状或棱柱状晶形,吸湿性强。
粒状尿素为粒径1~2毫米的半透明粒子,外观光洁,吸湿性有明显改善。
20℃时临界吸湿点为相对湿度80%,但30℃时,临界吸湿点降至72.5%,2、性状针状或棒状结晶体或粉末或颗粒。
3、相态固体4、臭味无臭无味。
五、化学结构1、化学组成尿素是由碳、氮、氧和氢组成的有机化合物,含氮量约为46.67%。
2、化学式CON2H4、CO(NH2)2 、CN2H4O,3、分子量60.064、分子结构(结构式)5、分子结构数据6、计算化学数据7、生态化学数据8、毒理学数据六、物化性质1、物理性质1)、溶解性溶于水、醇,不溶于乙醚、氯仿。
尿素易溶于水,在20℃时100毫升水中可溶解105克,水溶液呈中性反应。
2)、酸碱性呈弱碱性。
3)、熔点熔点132.7℃。
4)、密度密度1.335g/cm3。
2、化学性质1)、性质2)、稳定性(化学反应)可与酸作用生成盐。
有水解作用。
在高温下可进行缩合反应,生成缩二脲、缩三脲和三聚氰酸。
加热至160℃分解,产生氨气同时变为氰酸。
尿素在酸、碱、酶作用下(酸、碱需加热)能水解生成氨和二氧化碳。
对热不稳定,加热至150~160℃将脱氨成缩二脲。
若迅速加热将脱氨而三聚成六元环化合物三聚氰酸。
(机理:先脱氨生成异氰酸(HN=C=O),再三聚。
)与乙酰氯或乙酸酐作用可生成乙酰脲与二乙酰脲。
在乙醇钠作用下与丙二酸二乙酯反应生成丙二酰脲(又称巴比妥酸,因其有一定酸性)。
在氨水等碱性催化剂作用下能与甲醛反应,缩聚成脲醛树脂。
与水合肼作用生成氨基脲。
七、制作方法工业上用液氨和二氧化碳为原料,在高温高压条件下直接合成尿素,化学反应如下:2NH3+CO2→NH2COONH4→CO(NH2)2+H2O在造粒中温度过高会产生少量缩二脲,又称双缩脲,八、安全信息与措施1、风险术语2、安全术语3、灭火方法4、紧急处理5、管制信息6、存储方法尿素要避免在盛夏潮湿气候下敞开存放。
尿素安全技术资料第一部分:化学品名称化学品中文名:尿素化学品英文名:carbamide第二部分:成分/组成信息有害成份:脲CAS No:分子式:CH4N2O分子量:60.06第三部分:危害性概述危害性概述:遇明火、高热可燃。
与次氯酸钠、次氯酸钙反应生成有爆炸性的三氯化氮。
受高热分解放出有毒的气体。
本品属微毒类。
对眼睛、皮肤和粘膜有刺激作用。
对环境可能有危害,对水体可造成污染。
慢性毒性:无资料第四部分:急救措施眼睛:提起眼睑,用流动清水或生理盐水冲洗。
就医。
皮肤:脱去污染的衣着,用大量流动清水冲洗。
食入:饮足量温水,催吐。
就医。
吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸停止,立即进行人工呼吸。
就医。
第五部分:消防措施易燃性:可燃烧自燃点:无资料概述:遇明火、高热可燃。
与次氯酸钠、次氯酸钙反应生成有爆炸性的三氯化氮。
受高热分解放出有毒的气体。
灭火方法:消防人员必须穿全身防火防毒服,在上风向灭火。
灭火时尽可能将容器从火场移至空旷处。
然后根据着火原因选择适当灭火剂灭火。
第六部分:泄漏应急处理建议工作人员穿戴适当的防尘面罩及防护服。
将泄漏的物质用惰性物质,如干沙、泥土等,放入适当的废物容器中;避免火源,或使用防火花装备;注意通风,可以采用泡沫灭火器以减少蒸汽的形成;应从上风方向接近泄漏物,并避免闲杂人员接近。
第七部分:操作处置及储存操作注意事项:无资料贮存注意事项:储存于阴凉、通风的库房。
远离火种、热源。
防止阳光直射。
包装密封。
应与氧化剂、酸类、亚硝酸钠、干粉分开存放,切忌混储。
储区应备有合适的材料收容泄漏物。
清洁卫生:使用后及时彻底清洗,避免接触眼睛及皮肤,避免吸入含有该物质的尘土、蒸汽等。
第八部分:接触控制及个人防护职业控制:采取必要的职业控制措施,如操作区域封闭、局部副压通风,或其他控制措施以防止空气中的含量达到危害性的程度。
如果以上条件不能达到,操作人员应穿戴适当的防护装备。
科普小知识:尿素通用名称尿素(Urea)尿素由氨和二氧化碳合成制得,分为工业用和农业用两种。
执行标准产品标准GB/T 2440-2017《尿素》检测标准GB/T 2441.1-2008《尿素的测定方法第1部分:总氮含量》GB/T 2441.2-2010《尿素的测定方法第2部分:缩二脲含量分光光度法》GB/T 2441.3-2010《尿素的测定方法第3部分:水分卡尔·费休法》GB/T 2441.4-2010《尿素的测定方法第4部分:铁含量邻菲啰啉分光光度法》GB/T 2441.5-2010《尿素的测定方法第5部分:碱度容量法》GB/T 2441.6-2010《尿素的测定方法第6部分:水不溶物含量重量法》GB/T 2441.7-2010《尿素的测定方法第7部分:粒度筛分法》GB/T 2441.8-2010《尿素的测定方法第8部分:硫酸盐含量目视比浊法》GB/T 2441.9-2010《尿素的测定方法第9部分:亚甲基二脲含量分光光度法》其它标准GB 18382-2001《肥料标识内容和要求》理化性质尿素的外观通常为无色或白色针状或棒状结晶体,工业或农业品为白色略带微红色固体颗粒,无臭无味。
技术要求根据GB/T 2440-2017《尿素》,农业用(肥料)尿素产品的技术指标应符合表1规定。
使用方法尿素适用于各种作物和土壤,可作基肥、追肥,一般不宜作种肥。
(1)作基肥。
先将尿素撒施于地表,然后进行翻耕。
施用尿素后,不宜马上浇大水,尿素作基肥用量不宜过大,一般占全生育期施氮量的40%左右为宜。
(2)作追肥。
一般采用沟施、穴施。
沟施、穴施时深度应达10cm左右,施用后要覆土,使尿素与土壤紧密结合,避免暴露于地表造成挥发散失。
施用后,不要马上大量浇水,防止随水流失或渗入土壤深层。
尿素施用一般要比其他铵态氮肥提前。
追施总量一般占全生育期施氮量的60%左右,结合不同作物的各生育期对氮肥需求特点进行少量多次的追肥。
尿素的标准化学知识点归纳
尿素的标准化学知识点归纳
尿素的标准
1主题内容与适用范围
本标准规定了尿素的技术要求、试验方法、检验规则以及标志、包装、运输和贮存。
本标准适用于由氨和二氧化碳合成制得的尿素。
其主要用途为农业肥料、塑料、树脂、涂料、医药等工业部门的原料。
分子式:CO(NH2)2
相对分子质量:60.055(根据1987年国际相对原子质量表)
2引用标准
GB/T2441尿素总氮含量的测定蒸馏后滴定法
GB/T2443尿素中缩二脲含量的测定分光光度法
GB/T2444尿素中水分的测定卡尔·费休法
GB/T2445工业用尿素铁含量的测定邻菲
GB/T2446工业用尿素碱度的测定容量法
GB/T2447工业用尿素水不溶物含量的测定重量法
GB/T2448尿素粒度的测定筛分法
GB8569固体化学肥料包装
GB/T13256工业用尿素硫酸盐含量的.测定目视比浊法
3技术要求
3.1外观:颗粒或结晶。
3.2尿素应符合表1的要求:
表1尿素技术指标%
指标名称:工业用农业用
优等品一等品合格品优等品一等品合格品
总氮(N)含量(以干基计)≥46.346.346.346.346.346.0
缩二脲含量≤0.50.91.00.91.01.5
水分(H2O)含量≤0.30.50.70.50.51.0
铁含量(以Fe计)≤0.00050.00050.0010
碱度(以NH3计)≤0.010.020.03
硫酸盐含量(以SO4-2计)≤0.0050.0100.020
水不溶物含量≤0.0050.0100.040
粒度(φ0.85~2.80mm)≥909090909090注:结晶状尿素不控制粒度指标。
4试验方法
4.1总氮含量的测定按照GB/T2441的规定进行。
4.2缩二脲含量的测定按照GB/T2443的规定进行。
4.3水分的测定按照GB/T2444的规定进行。
4.4铁含量的测定按照GB/T2445的规定进行。
4.5碱度的测定按照GB/T2446的规定进行。
4.6硫酸盐含量的测定按照GB/T13256的规定进行。
4.7水不溶物含量的测定按照GB/T2447的规定进行。
4.8粒度的测定按照GB/T2448的规定进行。
5检验规则
5.1尿素应由生产厂的质量检验部门进行检验,生产厂应保证每批出厂的尿素都符合本标准要求,每批出厂的尿素都应附有一定格式的质量证明书,证明书包括下列内容:生产
厂名称、产品名称、商标、产品等级、批号、生产日期、产品净重和本标准编号。
5.2使用单位有权按照本标准规。