铝镁及其化合物的化学方程式和离子方程式
- 格式:doc
- 大小:1.48 MB
- 文档页数:10

铝及其化合物的化学方程式和离子方程式一、铝1、铝在氧气中燃烧:4Al+3O22Al2O32、铝在氯气中燃烧:2Al+3Cl22AlCl33、铝和硫共热:2Al+3S Al2S34、铝与稀硫酸反应:2Al+3H2SO4Al2(SO4)3+3H2↑2Al+6H+2Al3++3H2↑5、铝和氢氧化钠溶液反应:2Al+2NaOH+2H2O2NaAlO2+3H2↑2Al+2OH-+2H2O2AlO2-+3H2↑6、铝和浓硫酸共热:2Al+6H2SO4Al2(SO4)3+3SO2↑+6H2O7、铝和浓硝酸共热:Al+6HNO3Al(NO3)3+3NO2↑+3H2OAl+6H++3NO3-Al3++3NO2↑+3H2O 8、铝和稀硝酸反应:Al+4HNO3Al(NO3)3+NO ↑+2H2OAl+4H++NO3-Al3++NO ↑+2H2O8、铝和硝酸银溶液反应:Al+3AgNO3Al(NO3)3+3AgAl+3Ag+Al3++3Ag9、铝与硫酸铜溶液反应:2Al+3CuSO4Al2(SO4)3+3Cu2Al+3Cu2+2Al3++3Cu10、铝和氧化铁高温下反应:2Al+Fe2O3Al2O3+2Fe11、铝和四氧化三铁高温共热:8Al+3Fe3O44Al2O3+9Fe12、铝和二氧化锰高温共热:4Al+3MnO22Al2O3+3Mn二、氧化铝1、氧化铝与稀硫酸反应:Al 2O 3+3H 2SO 4Al 2(SO 4)3 +3H 2O Al 2O 3+6H +2Al 3++3H 2O2、氧化铝与氢氧化钠溶液反应:Al 2O 3+2NaOH2NaAlO 2+H 2O Al 2O 3+2OH -2AlO 2-+H 2O3、电解氧化铝的熔融液:2Al 2O 34Al +3O 2 ↑ 三、氢氧化铝1、氢氧化铝与稀硫酸反应:2Al(OH)3 +3H 2SO 4Al 2(SO 4)3 +6H 2O Al(OH)3 +3H +Al 3++3H 2O2、氢氧化铝与氢氧化钠溶液反应:Al(OH)3 +NaOH NaAlO 2+2H 2O Al(OH)3 +OH -AlO 2-+2H 2O3、加热氢氧化铝:2Al(OH)3 Al 2O 3+3H 2O四、硫酸铝1、硫酸铝的水溶液呈酸性:Al 2(SO 4)3+6H 2O2Al(OH)3 +3H 2SO 4 Al 3++3H 2OAl(OH)3 +3H +2、硫酸铝溶液中加入少量的氢氧化钠溶液:Al 2(SO 4)3 +6NaOH 3Na 2SO 4+2Al(OH)3 ↓Al 3++3OH -Al(OH)3 ↓3、向硫酸铝溶液中加足量的氢氧化钠溶液: Al 2(SO 4)3 +8NaOH 2NaAlO 2+3Na 2SO 4+4H 2OAl 3++4OH -AlO 2-+2H 2O4、向硫酸铝溶液中加入少量的氢氧化钡溶液:冰晶石电解Al2(SO4)3+3Ba(OH)22Al(OH)3↓+3BaSO4↓2Al3++3SO42-+3Ba2++6OH-2Al(OH)3↓+3BaSO4↓5、向硫酸铝溶液中加入足量的氢氧化钡溶液:Al2(SO4)3+4Ba(OH)2Ba(AlO2)2+3BaSO4↓+4H2O2Al3++3SO42-+3Ba2++8OH-2AlO2-+3BaSO4↓+4H2O 6、向硫酸铝溶液中加入氨水:Al2(SO4)3+6NH3·H2O2Al(OH)3↓+3(NH4)2SO4Al3++3NH3·H2O Al(OH)3↓+3NH4+7、向硫酸铝溶液中加入碳酸钠溶液:Al2(SO4)3+3Na2CO3+3H2O2Al(OH)3↓+3Na2SO4+3CO2↑2Al3++3CO32-+3H2O2Al(OH)3↓+3CO2↑8、向硫酸铝溶液中加入碳酸氢钠溶液(灭火器原理):Al2(SO4)3+6NaHCO32Al(OH)3↓+3Na2SO4+6CO2↑Al3++3HCO3-Al(OH)3↓+3CO2↑9、向硫酸铝溶液中加入偏铝酸钠溶液:Al2(SO4)3+6NaAlO2+12H2O3Na2SO4+8Al(OH)3↓Al3++AlO2-+6H2O4Al(OH)3↓五、偏铝酸钠1、偏铝酸钠溶液呈碱性:NaAlO2+2H2O AI(OH)3+NaOHAlO2-+2H2O Al(OH)3+OH-2、偏铝酸钠溶液滴入少量盐酸:NaAlO2+HCl+H2O Al(OH)3↓+NaClAlO2-+H++H2O Al(OH)3↓3、向偏铝酸钠溶液加入足量盐酸:NaAlO2+4HCl NaCl+AlCl3+2H2OAlO2-+4H+Al3++2H2O4、向偏铝酸钠溶液通入少量二氧化碳气体:2NaAlO2+CO2+3H2O2Al(OH)3↓+Na2CO32AlO2-+CO2+3H2O2Al(OH)3↓+CO32-5、向偏铝酸钠溶液通入足量二氧化碳气体:NaAlO2+CO2+2H2O Al(OH)3+NaHCO3AlO2-+CO2+2H2O Al(OH)3+HCO3-6、向偏铝酸钠溶液中加入硫酸铝溶液:Al2(SO4)3+6NaAlO2+12H2O3Na2SO4+8Al(OH)3↓Al3++AlO2-+6H2O4Al(OH)3↓六、明矾1、明矾净水:Al3++3H2O Al(OH)3(胶体)+3H+2、向明矾溶液中加入少量的氢氧化钡溶液:3Ba(OH)2+2KAl(SO4)22Al(OH)3↓+3BaSO4↓+K2SO4 3Ba2++6OH-+2Al3++3SO42-3BaSO4↓+2Al(OH)3↓3、向明矾溶液中加入足量的氢氧化钡溶液:KAl(SO4)2+2Ba(OH)2KAlO2+2BaSO4↓+2H2OAl3++2SO42-+2Ba2++4OH-AlO2-+2BaSO4↓+2H2O。
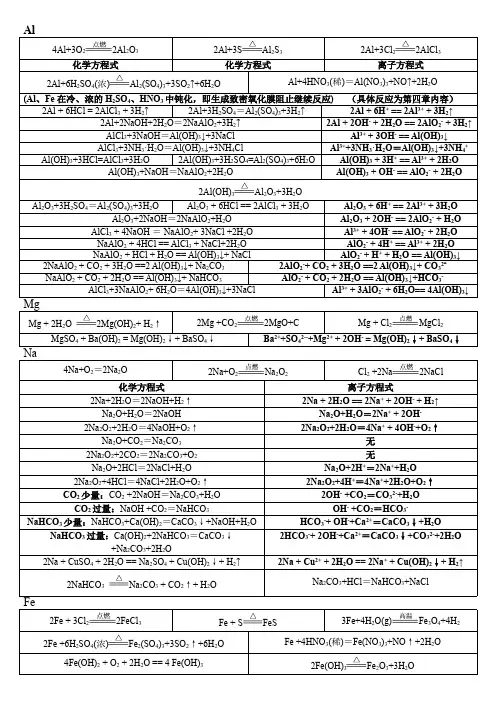

铝及其化合物的化学方程式和离子方程式一、铝1、铝在氧气中燃烧:4Al+3O22Al2O32、铝在氯气中燃烧:2Al+3Cl22AlCl33、铝和硫共热:2Al+3S Al2S34、铝与稀硫酸反应:2Al+3H2SO4Al2(SO4)3+3H2↑2Al+6H+2Al3++3H2↑5、铝和氢氧化钠溶液反应:2Al+2NaOH+2H2O2NaAlO2+3H2↑2Al+2OH-+2H2O2AlO2-+3H2↑6、铝和浓硫酸共热:2Al+6H2SO4Al2(SO4)3+3SO2↑+6H2O7、铝和浓硝酸共热:Al+6HNO3Al(NO3)3+3NO2↑+3H2OAl+6H++3NO3-Al3++3NO2↑+3H2O8、铝和稀硝酸反应:Al+4HNO3Al(NO3)3+NO ↑+2H2OAl+4H++NO3-Al3++NO ↑+2H2O8、铝和硝酸银溶液反应:Al+3AgNO3Al(NO3)3+3AgAl+3Ag+Al3++3Ag9、铝与硫酸铜溶液反应:2Al+3CuSO4Al2(SO4)3+3Cu2Al+3Cu2+2Al3++3Cu10、铝和氧化铁高温下反应:2Al+Fe2O3Al2O3+2Fe11、铝和四氧化三铁高温共热:8Al+3Fe3O44Al2O3+9Fe12、铝和氧化铜高温共热:2Al+3CuO Al2O3+3Cu13、铝和二氧化锰高温共热:4Al+3MnO22Al2O3+3Mn二、氧化铝1、氧化铝与稀硫酸反应:Al 2O 3+3H 2SO4Al 2(SO 4)3 +3H 2O Al 2O 3+6H+2Al 3++3H 2O2、氧化铝与氢氧化钠溶液反应:Al 2O 3+2NaOH2NaAlO 2+H 2O Al 2O 3+2OH-2AlO 2-+H 2O3、电解氧化铝的熔融液:2Al 2O34Al +3O 2↑三、氢氧化铝1、氢氧化铝与稀硫酸反应:2Al(OH)3 +3H 2SO 4Al 2(SO 4)3 +6H 2O Al(OH)3 +3H +Al 3++3H 2O2、氢氧化铝与氢氧化钠溶液反应:Al(OH)3 +NaOH NaAlO 2+2H 2OAl(OH)3 +OH-AlO 2-+2H 2O3、加热氢氧化铝:2Al(OH)3Al 2O 3+3H 2O四、硫酸铝1、硫酸铝溶液与氯化钡溶液混合:Al 2(SO 4)3 +3BaCl 22AlCl 3+3BaSO 4↓SO 42-+Ba 2+BaSO 4↓2、硫酸铝的水溶液呈酸性:Al 2(SO 4)3+6H 2O 2Al(OH)3 +3H 2SO 4 Al 3++3H 2O Al(OH)3 +3H +3、硫酸铝溶液中加入少量的氢氧化钠溶液:Al 2(SO 4)3 +6NaOH 3Na 2SO 4+2Al(OH)3↓Al 3++3OH-Al(OH)3↓4、向硫酸铝溶液中加足量的氢氧化钠溶液: Al 2(SO 4)3 +8NaOH 2NaAlO 2+3Na 2SO 4+4H 2OAl 3++4OH-AlO 2-+2H 2O5、向硫酸铝溶液中加入少量的氢氧化钡溶液: Al 2(SO 4)3 +3Ba(OH)22Al(OH)3↓+3BaSO 4↓2Al 3++3SO 42-+3Ba 2++6OH-2Al(OH)3↓+3BaSO 4↓6、向硫酸铝溶液中加入足量的氢氧化钡溶液:冰晶石电解Al2(SO4)3+4Ba(OH)2Ba(AlO2)2+3BaSO4↓+4H2O2Al3++3SO42-+3Ba2++8OH-2AlO2-+3BaSO4↓+4H2O7、向明矾溶液中加入少量的氢氧化钡溶液:3Ba(OH)2+2KAl(SO4)22Al(OH)3↓+3BaSO4↓+K2SO43Ba2++6OH-+2Al3++3SO42-3BaSO4↓+2Al(OH)3↓8、向明矾溶液中加入足量的氢氧化钡溶液:KAl(SO4)2+2Ba(OH)2KAlO2+2BaSO4↓+2H2OAl3++2SO42-+2Ba2++4OH-AlO2-+2BaSO4↓+2H2O9、向硫酸铝溶液中加入氨水:Al2(SO4)3+6NH3·H2O2Al(OH)3↓+3(NH4)2SO4Al3++3NH3·H2O Al(OH)3↓+3NH4+10、向硫酸铝溶液中加入碳酸钠溶液:Al2(SO4)3+3Na2CO3+3H2O2Al(OH)3↓+3Na2SO4+3CO2↑2Al3++3CO32-+3H2O2Al(OH)3↓+3CO2↑11、向硫酸铝溶液中加入碳酸氢钠溶液:Al2(SO4)3+6NaHCO32Al(OH)3↓+3Na2SO4+6CO2↑Al3++3HCO3-Al(OH)3↓+3CO2↑12、向硫酸铝溶液中加入硫化钠溶液:Al2(SO4)3+3Na2S+6H2O2Al(OH)3↓+3Na2SO4+3H2S ↑2Al3++3S2-+6H2O2Al(OH)3↓+3H2S ↑13、向硫酸铝溶液中加入硫氢化钠溶液:Al2(SO4)3+6NaHS+6H2O2Al(OH)3↓+3Na2SO4+6H2S ↑Al3++3HS-+3H2O Al(OH)3↓+3H2S ↑14、向硫酸铝溶液中加入硅酸钠溶液:Al2(SO4)3+3Na2SiO3+6H2O2Al(OH)3↓+3Na2SO4+3H2SiO3↓2Al3++3SiO32-+6H2O2Al(OH)3↓+3H2SiO3↓15、向硫酸铝溶液中加入偏铝酸钠溶液:Al2(SO4)3+6NaAlO2+12H2O3Na2SO4+8Al(OH)3↓Al3++AlO2-+6H2O4Al(OH)3↓五、偏铝酸钠1、偏铝酸钠溶液呈碱性:NaAlO2+2H2O AI(OH)3+NaOHAlO2-+2H2O Al(OH)3+OH-2、偏铝酸钠溶液滴入少量盐酸:NaAlO2+HCl+H2O Al(OH)3↓+NaClAlO2-+H++H2O Al(OH)3↓3、向偏铝酸钠溶液加入足量盐酸:NaAlO2+4HCl NaCl+AlCl3+2H2OAlO 2-+4H+Al3++2H2O4、向偏铝酸钠溶液通入少量二氧化碳气体:2NaAlO2+CO2+3H2O2Al(OH)3↓+Na2CO32AlO2-+CO2+3H2O2Al(OH)3↓+CO32-5、向偏铝酸钠溶液通入足量二氧化碳气体:NaAlO2+CO2+2H2O Al(OH)3+NaHCO3AlO2-+CO2+2H2O Al(OH)3+HCO3-6、向偏铝酸钠溶液中加入硫酸铝溶液:Al2(SO4)3+6NaAlO2+12H2O3Na2SO4+8Al(OH)3↓Al3++AlO2-+6H2O4Al(OH)3↓7、向偏铝酸钠溶液中加入氯化铵溶液:NaAlO2+NH4Cl+H2O Al(OH)3↓+NaCl+NH3↑AlO2-+NH4++H2O Al(OH)3↓+NH3↑8、向偏铝酸钠溶液中加入氯化铁溶液:3NaAlO2+FeCl3+6H2O3Al(OH)3↓+Fe(OH)3↓+3NaCl3AlO2-+Fe3++6H2O3Al(OH)3↓+Fe(OH)3↓。
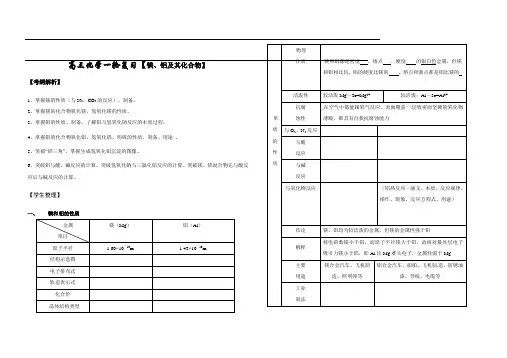
在空气中都能跟氧气反应,表面覆盖一层致密而坚硬的氧化物薄膜,都具有自我抗腐蚀能力铝合金汽车、船舶、飞机制造、防锈油漆、导线、电缆等易错点:(1)常温下,能用铝制容器盛放浓硫酸、浓硝酸的原因是二者能使铝发生“钝化”,而不是铝与浓硫酸、浓硝酸不反应。
(2)铝不但能与酸(H +)反应,还能够与碱溶液反应,表现为特殊性。
2Al +2OH -+2H 2O===2AlO -2+3H 2↑。
其反应机理应为:铝先与强碱溶液中的水反应生成H 2和Al(OH)3,然后Al(OH)3再与NaOH 反应生成H 2O 和NaAlO 2,反应中铝作还原剂,水作氧化剂,NaOH 无电子得失。
(3)铝热反应是在高温干态下进行的置换反应,铝只能与排在金属活动性顺序其后的金属氧化物反应。
铝不能与MgO 反应,铝热反应不能用来冶炼大量的金属铁、铜等(要考虑冶炼成本)。
(4)Mg 在CO 2中能够燃烧,所以活泼金属镁着火不能用干粉灭火器和泡沫灭火器灭火。
同时镁与氮气反应生成Mg 3N 2。
二、铝的重要化合物1.氧化铝(1)物理性质 色态: ;硬度: ;熔点: 。
(2)化学性质①属于两性氧化物,写出有关反应的离子方程式:,②电解 化学方程式为 2Al 2O 3(熔融)=====电解4Al +3O 2↑。
(3)用途熔点很高,是一种较好的耐火材料,天然产刚玉的成分是Al 2O 3,还可制作各种宝石。
2.氢氧化铝 (1)物理性质Al(OH)3是一种难溶于水的白色胶状物质,具有较强的吸附能力。
(2)化学性质 ①两性Al(OH)3的电离方程式为Al(OH)3既能溶于强酸又能溶于强碱,且都生成盐和水。
与强酸反应: , 与强碱溶液反应: 。
②不稳定性Al(OH)3受热分解: 。
(3)制备①向铝盐中加入氨水,离子方程式为 。
②NaAlO 2溶液中通入足量CO 2,离子方程式为 。
③NaAlO 2溶液与AlCl 3溶液混合:离子方程式为 。

化学方程式和离子方程式整理(离子检验、卤素、钠、镁、铝) 1.铵根的鉴定(浓氢氧化钠溶液、加热)__________________________________________2.硫酸根的鉴定(稀盐酸、氯化钡)__________________________________________3.氯气的实验室制备(用浓盐酸、加热、一半HCl被氧化)________________________________________,___________________________________ 4.氯气的工业制备(电解氯化钠溶液)________________________________________,____________________________________ 5.铁在氯气中燃.(棕褐色烟)________________________________________6.铜在氯气中燃烧(棕黄色烟)_________________________________________7.工业制氯化氢(苍白色火焰)________________________________________8.氯气和水的反应(注意可逆)________________________________________,____________________________________ 9.氯气溶于氢氧化钠溶液(尾气吸收)________________________________________,_____________________________________ 10.工业制漂白粉(漂白粉有效成分为次氯酸钙)________________________________________11.漂白粉在空气中易变质(同时也是漂白粉的利用方式之一)_________________________________________12.次氯酸的不稳定性(见光分解)__________________________________________13.氯气通入溴化钾溶液中(工业制溴单质的原理)__________________________________________,____________________________________ 14.氯气通往碘化钾溶液中(工业制碘单质的原理)__________________________________________,___________________________________ 15.溴水滴入碘化钾溶液中__________________________________________,____________________________________ 16.氯、溴、碘离子的鉴定___________________________,__________________________,_______________________ 17.氯化银、溴化银、碘化银见光分解___________________________,__________________________,______________________ 18.钠在空气中缓慢氧化(生成白色固体)_____________________________________19.钠在空气中燃烧(生成淡黄色固体)____________________________________20.钠与水反应(红、嘶、浮、游、熔)______________________________________,______________________________________ 21.钠与硫酸铜溶液反应(先水后盐)______________________________________,_____________________________________ 22.工业制备钠(电解熔融氯化钠)______________________________________23.过氧化钠与水反应_________________________________________24.过氧化钠与二氧化碳反应(可用于呼吸面具)__________________________________________25.碳酸钠溶液与氯化钙溶液反应________________________________________,____________________________________ 26.碳酸钠溶液与氢氧化钙溶液反应(工业制烧碱时,用石灰乳)_______________________________________,_____________________________________ 27.碳酸钠溶液中缓慢滴入少量盐酸并不断搅拌(无二氧化碳产生)_____________________________________,_____________________________________ 28.碳酸钠溶液中加入过量盐酸(有二氧化碳产生)______________________________________,___________________________________ 29.碳酸钠溶液中通入二氧化碳气体(转化为碳酸氢钠)_______________________________________,__________________________________ 30.碳酸氢钠固体受热分解(不稳定)________________________________________31.碳酸氢钠溶液与盐酸反应(比碳酸钠更快产生气体)________________________________________,__________________________________ 32.碳酸氢钠溶液与氢氧化钠溶液反应________________________________________,__________________________________ 33.碳酸氢钠溶液与少量氢氧化钙溶液反应(2:1反应)_______________________________________,____________________________________ 34.碳酸氢钠溶液与过量氢氧化钙溶液反应(1:1反应)______________________________________,_____________________________________ 35.侯氏制碱法原理(第一步生成小苏打,第二步灼烧小苏打得纯碱)_______________________________________,____________________________________ 36.硫酸氢钠溶液与少量氢氧化钡溶液反应(2:1反应)______________________________________,_____________________________________ 37.硫酸氢钠溶液与过量氢氧化钡溶液反应(1:1反应)______________________________________,______________________________________ 38.从海水中提取镁(按书上,分六步)________________________________________,_________________________________________________________________________,_________________________________________________________________________,_________________________________ 39.镁在空气中点燃生成氧化镁(还生成少量的氮化镁)________________________________________40.镁在氮气中燃烧_______________________________________41.镁在二氧化碳气体中燃烧(生成两种固体)________________________________________42.加热分解氢氧化镁或碳酸镁制氧化镁(作耐火材料)________________________________________,_____________________________________ 43.从铝土矿提取铝(涉及四个反应)_______________________________________,_____________________________________,_______________________________________,_____________________________________ 44.氧化铝的两性(可溶于盐酸、氢氧化钠溶液)____________________________________,__________________________________________________________________________,_______________________________________ 45.氢氧化铝的两性(可溶于盐酸、氢氧化钠溶液)____________________________________,__________________________________________________________________________,_______________________________________ 46.氯化铝溶液中加入过量的氨水(实验室制氢氧化铝)_____________________________________,_____________________________________ 47.偏铝酸钠溶液中通入过量的二氧化碳气体(若二氧化碳少量,则生成碳酸钠)_____________________________________,___________________________________________________________________________,______________________________________ 48.氯化铝溶液中逐滴加入氢氧化钠溶液(先有沉淀,后又溶解)_____________________________________,____________________________________________________________________________,______________________________________ 49.氯化铝溶液与过量氢氧化钠溶液反应______________________________________,_______________________________________ 50.氯化铝溶液与偏铝酸钠溶液的反应(铝离子与偏铝酸根不能大量共存)______________________________________,________________________________________ 51.偏铝酸钠溶液中逐滴加入盐酸(先有沉淀,后又溶解)_______________________________________,_______________________________________ _______________________________________,_______________________________________ 52.偏铝酸钠溶液与过量盐酸反应_______________________________________,________________________________________ 53.铝溶于盐酸_______________________________________,_______________________________________ 54.铝溶于氢氧化钠溶液_______________________________________,_____________________________________ 55.铝粉与氧化铁粉在高温下发生铝热反应(用于焊接钢轨,也可冶炼难熔金属)___________________________________________。

点燃 △电解 四.学测考试化学方程式和离子方程式(学测必备材料4)一、钠及其化合物1、钠与氧气(常温): 4Na+O 2=2Na 2O2、钠与氧气(燃烧): 2Na+O 2 Na 2O 23、钠与水反应: 2Na+2H 2O =2NaOH+H 2↑ 2Na + 2H 2O = 2Na + +2OH - + H 2↑4、氧化钠与水反应: Na 2O+H 2O==2NaOH5、碳酸氢钠与氢氧化钠溶液: NaHCO 3 + NaOH== Na 2CO 3+ H 2OHCO 3- + OH - == CO 32- + H 2O6、碳酸氢钠与盐酸: HCl +NaHCO 3=NaCl+H 2O+CO 2↑HCO 3- + H + == CO 2↑ + H 2O7、碳酸氢钠固体加热: 2NaHCO 3 Na 2CO 3 + CO 2↑+ H 2O8、碳酸钠溶液通入二氧化碳: Na 2CO 3+CO 2+H 2O==2NaHCO 3 CO 32- + CO 2+H 2O==2HCO 3-9、大理石与与盐酸反应: CaCO 3+2HCl =CaCl 2+H 2O+CO 2↑CaCO 3 + 2H + == Ca 2+ + CO 2↑+ H 2O二、镁及其化合物 10、镁在氧气中燃烧: 2Mg+O 2 2MgO11、氯化镁溶液与石灰水: MgCl 2 + Ca(OH)2 = CaCl 2+ Mg(OH)2↓ Mg 2+ + 2OH - = Mg(OH)2↓12、氢氧化镁与盐酸反应: Mg(OH)2 + 2HCl = MgCl 2 +2H 2OMg(OH)2 + 2H + = Mg 2+ + 2H 2O 13、电解熔融氯化镁: MgCl 2 Mg + Cl 2↑14、碳酸镁与盐酸: MgCO 3 +2HCl = MgCl 2 + CO 2↑+ H 2OMgCO 3 + 2H + == Mg 2+ + CO 2↑+ H 2O三、铝及其化合物 (Al 2O 3是两性氧化物Al(OH)3是两性氢氧化物15、铝热反应: Fe 2O 3 + 2Al Al 2O 3+2Fe16、铝与盐酸: 2Al + 6HCl = 2AlCl 3 + 3H 2↑2Al + 6H + == 2Al 3+ + 3H 2↑17、铝与氢氧化钠溶液: 2Al+2NaOH+2H 2O =2NaAlO 2+3H 2↑ 2Al + 2OH - + 2H 2O =2AlO 2- + 3H 2↑18、氧化铝与盐酸: Al 2O 3+6HCl=2AlCl 3+3H 2O Al 2O 3 + 6H + = 2Al 3+ + 3H 2O19、氧化铝与氢氧化钠溶液: Al 2O 3+2NaOH =2NaAlO 2+H 2OAl 2O 3 + 2OH - =2AlO 2- + H 2O20、氢氧化铝与盐酸: Al(OH)3+3HCl=AlCl 3+3H 2OAl(OH)3 + 3H + =Al 3+ + 3H 2O21、氢氧化铝与氢氧化钠溶液: Al(OH)3+NaOH =NaAlO 2+2H 2OAl(OH)3 + OH - =AlO 2- + 2H 2O22、加热氢氧化铝: 2Al(OH)3 Al 2O 3+3H 2O 23、电解熔融氧化铝: 2Al 2O 3 4Al+3O 2↑ 点燃 △ 电解24、二氧化碳通入偏铝酸钠溶液中: NaAlO 2+CO 2+2H 2O =Al(OH)3↓+NaHCO 3CO 2 + AlO 2- + 2H 2O == Al(OH)3↓+ HCO 3-25、氯化铝与少量氢氧化钠溶液: AlCl 3+3NaOH =Al(OH)3↓+3NaClAl 3+ + 3OH - == Al(OH)3↓26、氯化铝与过量氢氧化钠溶液反应:AlCl 3 + 4NaOH = NaAlO 2+ 3NaCl + 2H 2OAl 3+ + 4OH - == AlO 2- + 2H 2O27、氯化铝与氨水: AlCl 3+3NH 3·H 2O =Al(OH)3↓+3NH 4Cl Al 3+ + 3NH 3.H 2O == Al(OH)3↓+ 3NH 4+28.明矾净水原理: Al 3++3 H 2O Al(OH)3(胶体) + 3H +四、铁及其化合物29、铁在与氯气中燃烧: 2Fe + 3Cl 2 2FeCl 330、铁在氧气中燃烧: 3Fe + 2O 2 点燃Fe 3O 431、铁与盐酸反应: Fe+2HCl =FeCl 2+H 2↑Fe + 2H + = Fe 2+ + H 2↑32、铁与氯化铁溶液: 2FeCl 3+Fe =3FeCl 2Fe + 2Fe 3+ == 3Fe 2+33、铜与氯化铁溶液: 2FeCl 3+Cu =2FeCl 2+CuCl 2Cu + 2Fe 3+ == 2Fe 2+ + Cu 2+34、氯化铁溶液与氢氧化钠溶液: FeCl 3+3NaOH == Fe(OH)3↓+ 3NaCl Fe 3+ + 3OH - == Fe(OH)3↓35、氯化铁溶液与硫氰化钾溶液: FeCl 3 + 3KSCN == Fe(SCN)3 + 3KClFe 3+ + 3SCN - == Fe(SCN)3(血红色)36、氯水(或氯气)与氯化亚铁溶液: Cl 2 +2FeCl 2 =2FeCl 3Cl 2 + 2Fe 2+ == 2Fe 3+ + 2Cl - 37、氧化铁与一氧化碳: Fe 2O 3 + 3CO △2Fe+3CO 238、氢氧化亚铁与氧气反应: 4Fe(OH)2 + O 2 + 2H 2O == 4 Fe(OH)339、氢氧化铁固体加热: 2F e(OH)3△Fe 2O 3 + 3H 2O (Al 、Fe 在冷、浓的H 2SO 4、HNO 3中钝化)五、铜及其化合物40、铜与氧气反应: 2Cu +O 2△2CuO 41、氢氧化铜固体加热: Cu(OH)2 △ CuO + H 2O42、氢氧化铜与硫酸反应: Cu(OH)2+H 2SO 4=CuSO 4+2H 2OCu(OH)2+ 2H + == Cu 2+ +2 H 2O六、硅及其化合物43、二氧化硅与氢氧化钠溶液: SiO 2+2NaOH =Na 2SiO 3+H 2O SiO 2 + 2OH - = SiO 32-+ H 2O44、二氧化硅与氢氟酸: 4HF+SiO 2=SiF 4↑+2H 2O45、工业上生产普通玻璃的反应: SiO 2+Na 2CO 3 高温Na 2SiO 3+CO 2↑点燃七、硫及其化合物46、硫与氧气:S+O2点燃SO247、二氧化硫被氧气氧化:2SO2+O2△2SO348、二氧化硫与水:SO2+H2O H2SO349、稀硫酸与氢氧化钡溶液:Ba(OH)2+ H2SO4= BaSO4↓ + 2H2OBa2+ + 2OH- + 2H+ + SO42- == BaSO4↓+ 2H2O50、浓硫酸与碳共热:2H2SO4(浓)+C △CO2↑+2SO2↑+2H2O(浓H2SO4只作氧化剂)51、浓硫酸与铜共热:Cu+2H2SO4(浓)△CuSO4+SO2↑+2H2O(H2SO4既表现氧化性又表现酸性)52、工业上接触法制硫酸(1)、以黄铁矿为原料:4FeS2+11O2催化剂△2Fe2O3+8SO22SO2+O2催化剂高温高压2SO3SO3+H2O==H2SO4八、氮气及其化合物53、工业氮气与氢气合成氨气:N2+3H2催化剂高温高压2NH354、氮气与氧气在放电条件下反应:N2+O22NO55、一氧化氮与氧气:2NO+O2=2NO256、二氧化氮与水:3NO2+H2O=2HNO3+NO57、实验室制NH3:2NH4Cl(固)+Ca(OH)2(固)△CaCl2+2NH3↑+2H2O58、氨与氯化氢:NH3+HCl=NH4Cl(白烟)59、氨气与水反应:NH3 + H2O NH3·H2O一水合氨电离NH3·H2O NH4+ + OH-(氨水呈碱性)或:NH3 + H2O NH3·H2O NH4+ + OH60、硝酸的见光、受热分解:4HNO3△4NO2↑+O2↑+2H2O61、稀硝酸与铜:3Cu+ 8HNO3=3Cu (NO3)2+2NO↑+4H2O3Cu +2NO3- + 8H+ == 3Cu2++ 2NO↑+ 4H2O 62、浓硝酸与铜:Cu+4HNO3(浓)==Cu(NO3)2+2NO2↑+2H2OCu +2NO3- + 4H+ == Cu2+ + 2NO2↑+ 2H2O63、浓硝酸与碳共热: 4HNO3(浓)+C △CO2↑+4NO2↑+2H2O64、工业氨的催化氧化制硝酸:(1). 4NH3+5O24NO +6H2O(2)2NO+O2==2NO2(3) 3NO2+H2O=2HNO3+NO九、氯、溴、碘及其化合物65、二氧化锰与浓盐酸共热(实验室制取氯气):4HCl(浓)+MnO 2△MnCl2+Cl2+2H2OMnO2 + 4H++ 2Cl-△Mn2+ + Cl2↑+ 2H2O66、氢气在氯气中燃烧:Cl2 +H22HCl (光照或点燃)67、氯气溶于水:Cl2+H2O HCl +HClOCl2+H2O H++Cl—+HClO68、氯水与碘化钾溶液反应:Cl2 +2KI= 2 KCl+ I2Cl2 + 2I- == 2Cl- + I269、氯气与氢氧化钠溶液反应:Cl2+2NaOH=NaCl+NaClO+H2OCl2 + 2OH- == Cl- + ClO- + H2O70、氯气与石灰乳反应(工业制取漂白粉):2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O71、漂白粉的漂白原理:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO十、原电池和电解池72、由铜、锌、稀硫酸构成的铜锌原电池(写出两极现象)电极反应式:正极:2H+ + 2e- == H2↑(有气泡放出)负极:Zn - 2e- == Zn2+(锌片溶解)电池总反应的化学方程式:Zn +H2SO4=ZnSO4+H2↑离子方程式:Zn + 2H+ == Zn2+ + H 2↑73、钢铁在潮湿的空气中发生电化学腐蚀电极材料:正极:碳,负极:铁正极:O2 + 2H2O + 4e - == 4OH-负极:2Fe - 4e- == 2Fe2+总反应式:2Fe + O2 + 2H2O == 2Fe(OH)2十一、烃74、甲烷与氯气混合光照:(取代反应)CH4 + Cl 2CH3Cl + HCl 等75、乙烯通入溴的四氯化碳溶液中:(加成反应)CH2=CH2 + Br2 CH2BrCH2Br(褪色)76、乙烯与氯化氢在催化剂作用下反应(加成反应):CH2=CH2 +HCl CH3CH2Cl77、乙烯与水在催化剂作用下反应生成乙醇(加成反应):CH2=CH2 + H2O CH3CH2OH78、乙烯在催化剂作用下生成聚乙烯(加聚反应):n CH2=CH279、苯与浓硝酸和浓硫酸的混酸共热(取代反应):+HO-NO2+ H2O十三、食品中的有机化合物80、乙醇的催化氧化(氧化反应):2CH3CH2OH+O2 2CH3COOH+2H2O81、乙醛的催化氧化:2CH3CHO + O 22CH3COOH82、.乙酸与乙醇发生酯化反应:CH3COOH + CH3CH2OH CH3COOCH2CH3 + H2O83、淀粉的水解:(C6H10O5)n (淀粉) + nH2O n C6H12O6(葡萄糖)Cu。



Na 、Mg 、Al 、Fe 及其化合物的化学方程式和离子方程式一、Na 及其化合物的化学方程式和离子方程式 (1)Na 的反应 1、钠和水反应:方程式: 2Na+2H 2O=2NaOH+H 2↑ 离子方程式: 2Na+2H 2O=2Na +2OH -+H 2↑ 2.钠分别和氧气、硫、氯气: 2Na+O 2点燃Na 2O 2 (或加热) 4Na+O 2 = 2Na 2O2Na+S =Na 2S 2Na+Cl 2 点燃2NaCl3.钠分别和盐酸(或硫酸)、醋酸方程式: 2Na+2HCl=2NaCl+H 2↑ 离子方程式: 2Na+2H +=2Na ++H 2↑ 方程式: 2Na+H 2SO 4=Na 2SO 4+H 2↑ 离子方程式: 2Na+2H +=2Na ++H 2↑方程式:2Na+2CH 3COOH=2CH 3COONa+H 2↑ 离子方程式: 2Na+2CH 3COOH=2CH 3COO -+2Na ++H 2↑ 4.钠分别和硫酸铜溶液、氯化铁溶液方程式: 2Na +2H 2O+CuSO 4=Cu(OH)2↓+Na 2SO 4+H 2↑ 离子方程式: 2Na +2H 2O+Cu 2+=Cu(OH)2↓+2Na ++H 2↑ 方程式: 6Na +6H 2O+2FeCl 3=2Fe(OH)3↓+6NaCl+3H 2↑ 离子方程式: 6Na +6H 2O+2Fe 3+=2Fe(OH)3↓+6Na ++3H 2↑(2)Na 的氧化物反应 1.氧化钠分别与水、盐酸方程式: Na 2O+H 2O=2NaOH 离子方程式: Na 2O+H 2O=2Na ++2OH - 方程式: Na 2O+2HCl=2NaCl+H 2O 离子方程式: Na 2O+2H +=2Na ++H 2O 2.过氧化钠分别与盐酸、水方程式: 2Na 2O 2+4HCl=4NaCl+2H 2O+O 2↑ 离子方程式: 2Na 2O 2+4H + =4Na ++2H 2O+O 2↑ 方程式: 2Na 2O 2+2H 2O=4NaOH+O 2↑ 离子方程式: 2Na 2O 2+2H 2O=4Na ++4OH -+O 2↑ 3.过氧化钠分别与二氧化碳:2Na 2O 2+2CO 2=2Na 2CO 3+O 2 (3)Na 2CO 3、NaHCO 3盐的反应1.分别加热碳酸钠和碳酸氢钠固体(鉴别固体Na 2CO 3、NaHCO 3的方法)碳酸钠受热不分解 2NaHCO 3△Na 2CO 3+H 2O+CO 2↑2.碳酸钠和碳酸氢钠溶液分别与少量(或过量)的盐酸反应少量的盐酸时:Na 2CO 3+HCl =NaHCO 3 +NaCl CO 32-+H +=HCO 3-NaHCO 3+HCl =NaCl+CO 2↑+H 2O HCO 3-+H +=CO 2↑+H 2O过量的盐酸时:Na2CO3+2HCl=2NaCl+CO2↑+H2O CO32-+2H+=CO2↑+H2ONaHCO3+HCl=NaCl+CO2↑+H2O HCO3-+H+=CO2↑+H2O3.碳酸钠和碳酸氢钠溶液分别与少量(或过量)的醋酸反应少量的醋酸时:Na2CO3+CH3COOH=NaHCO3+CH3COONaCO32-+ CH3COOH=HCO3-+ CH3COO-NaHCO3+CH3COOH=CH3COONa+CO2↑+H2OHCO3-+ CH3COOH=CO2↑+H2O+ CH3COO-过量的醋酸时:Na2CO3+2CH3COOH=2CH3COONa+ CO2↑+H2OCO32-+ 2CH3COOH=2CH3COO-+CO2↑+H2ONaHCO3+CH3COOH=CH3COONa+CO2↑+H2OHCO3-+ CH3COOH=CO2↑+H2O+ CH3COO-4.二氧化碳通入到碳酸钠溶液中(或通入到饱和的碳酸钠溶液中)CO2+ Na2CO3+H2O=2 NaHCO3CO2+CO32-+H2O=2 HCO3-或 CO2+ Na2CO3+H2O=2 NaHCO3↓ CO2+2Na++CO32-+H2O=2 NaHCO3↓5.碳酸钠溶液与澄清石灰水(或氢氧化钠溶液)混合方程式:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH离子方程式: CO32-+ Ca2+=CaCO3↓碳酸钠溶液与氢氧化钠溶液混合不发生反应6. 碳酸氢钠与少量(或过量)的澄清石灰水混合 (类似:澄清石灰水可以改为氢氧化钡溶液)少量澄清石灰水:2NaHCO3+Ca(OH)2=2H2O+CaCO3↓+ Na2CO32 HCO3-+Ca2++2OH-=2H2O+CaCO3↓+ CO32-过量澄清石灰水:NaHCO3+Ca(OH)2=H2O+CaCO3↓+ NaOHHCO3-+Ca2++OH-=H2O+CaCO3↓7.碳酸氢钠与氢氧化钠溶液混合方程式: NaHCO3+ NaOH=Na2CO3+ H2O 离子方程式: HCO3-+OH-=H2O+CO32-8.电解熔融状态的氯化钠、电解饱和食盐水(注意电极反应式的书写)2NaCl(熔融)=Na+Cl2↑ 2NaCl+2H2O 电解Cl2↑+H2↑+2NaOH 2Cl-+2H2O电解Cl2↑+H2↑+2OH-9.碳酸钠溶液、碳酸氢钠溶液滴2滴酚酞试液都呈色,为什么(用方程式或离子方程式表示) 溶液呈红色CO32-+H2O HCO3-+OH-溶液呈碱性HCO3-+H2O H2CO3+ OH-溶液呈碱性二、Mg 、Al 及其化合物的化学方程式和离子方程式 (1)Mg 的反应1.镁在空气中燃烧2Mg + O 2 2MgO 3Mg +N 2 Mg 3N 2 2Mg + CO 2 2MgO + C 2.镁能溶解在氯化铵溶液中Mg + 2NH 4Cl = MgCl 2 + H 2↑+ NH 3↑ Mg + 2NH 4+= Mg 2++ H 2↑+ NH 3↑ (2) Al 的反应3.铝是活泼金属,为什么可以直接存放在空气中,用简单的文字和方程式说明:4Al+3O 2=2Al 2O 3 在铝的表面形成致密的氧化铝薄膜,将铝和空气隔绝。

化学方程式和离子方程式钠及其化合物一、钠1、钠在氧气中燃烧:2Na+O 2Na2O22、钠在氯气中燃烧:2Na+Cl 22NaCl3、钠常温条件下和氧气反应:4Na+O 22Na2O4、钠和硫共热:2Na+S Na2S5、钠和水反应:2Na+2H2O2NaOH+H2↑2Na+2H2O2Na++2OH-+H2↑6、钠和稀盐酸反应:2Na+2HCl2NaCl+H2↑2Na+2H +2Na++H2↑7、钠投入到硫酸铜溶液中:2Na+CuSO4+2H2O Na2SO4+Cu(OH)2↓+H2↑2Na+Cu2++2H2O2Na++Cu(OH)2↓+H2↑8、向氯化铝溶液中加入少量的钠:6Na+2AlCl3+6H2O6NaCl+2Al(OH)3↓+3H2↑6Na+2Al3++6H2O6Na++Al(OH)3↓+3H2↑9、向氯化铝溶液中加入足量的钠:4Na+AlCl3+2H2O NaAlO2+3NaCl+2H2↑4Na+Al3++2H2O4Na++AlO2-+2H2↑10、钠在高温条件下与四氯化钛反应:4Na+TiCl 44NaCl+Ti二、氧化钠1、氧化钠和水反应:Na2O+H2O=2NaOHNa2O+H2O2Na++2OH-2、氧化钠与二氧化碳反应:Na2O+CO 2Na2CO33、氧化钠与盐酸反应:Na2O+2HCl2NaCl+H2ONa2O+2H +2Na++H2O4、向硫酸铜溶液中加入氧化钠:Na2O+CuSO4+H2O Cu(OH)2↓+Na2SO4Na2O+Cu2++H2O Cu(OH)2↓+2Na+5、向氯化铝溶液中加入少量的氧化钠:3Na2O+2AlCl3+3H2O2Al(OH)3↓+6NaCl3Na2O+2Al3++3H2O===2Al(OH)3↓+6Na+6、向氯化铝溶液中加入足量的氧化钠:2Na2O+AlCl 3NaAlO2+3NaCl2Na2O+Al3+AlO2-+4Na+三、过氧化钠1、过氧化钠与水反应:2Na2O2+2H2O4NaOH+O2↑2Na2O2+2H2O===4Na++4OH-+O2↑2、过氧化钠与二氧化碳反应:2Na2O2+2CO 22Na2CO3+O2↑3、过氧化钠与盐酸反应:2Na2O2+4HCl4NaCl+2H2O+O2↑2Na2O2+4H +4Na++2H2O+O2↑4、向硫酸铜溶液中加入过氧化钠:2Na2O2+2CuSO4+2H2O===2Cu(OH)2↓+2Na2SO4+O2↑2Na2O2+2Cu2++2H2O2Cu(OH)2↓+4Na++O2↑5、向氯化铝溶液中加入少量的过氧化钠:6Na2O2+4AlCl3+6H2O4Al(OH)3↓+12NaCl+3O2↑6Na2O2+4Al3++6H2O4Al(OH)3↓+12Na++3O2↑6、向氯化铝溶液中加入过量的过氧化钠:2Na2O2+AlCl3+2H2O NaAlO2+3NaCl+O2↑2Na2O2+Al3++2H2O AlO2-+4Na++O2↑7、过氧化钠与硫酸亚铁溶液反应:4Na2O2+4FeSO4+6H2O===4Fe(OH)3↓+4Na2SO4+O2↑4Na2O2+4Fe2++6H2O4Fe(OH)3↓+8Na++O2↑四、氢氧化钠1、铝与氢氧化钠溶液反应:2Al+2NaOH+2H2O2NaAlO2+3H2↑2Al+2OH-+2H2O2AlO2-+3H2↑2、氯气通入氢氧化钠溶液中:Cl2+2NaOH NaCl+NaClO+H2OCl2+2OH -Cl-+ClO-+H2O3、氯气通入热的浓氢氧化钠溶液中:3Cl2+6NaOH5NaCl+NaClO3+3H2O3Cl2+6OH -5Cl-+ClO3-+3H2O4、硫和氢氧化钠溶液共热:3S+6NaOH2Na2S+Na2SO3+3H2O3S+6OH -2S2-+SO32-+3H2O5、硅溶于氢氧化钠溶液中:Si+2NaOH+H2O Na2SiO3+2H2↑Si+2OH-+H2O SiO32-+2H2↑6、氧化铝溶于氢氧化钠溶液中:Al2O3+2NaOH2NaAlO2+H2OAl2O3+2OH -2AlO2-+H2O7、向氢氧化钠溶液中通入少量的二氧化碳:2NaOH+CO 2Na2CO3+H2O2OH-+CO 2CO32-+H2O8、向氢氧化钠溶液中通入过量的二氧化碳:NaOH+CO 2NaHCO3 OH-+CO 2HCO3-9、向氢氧化钠溶液中通入少量的二氧化硫:2NaOH+SO 2Na2SO3+H2O2OH-+SO 2SO32-+H2O10、向氢氧化钠溶液中通入过量的二氧化硫:NaOH+SO 2NaHSO3 OH-+SO 2HSO3-11、五氧化二磷与氢氧化钠溶液反应:P2O5+6NaOH2Na3PO4+3H2OP2O5+6OH -2PO43-+3H2O 12、二氧化氮和氢氧化钠溶液反应:2NO2+2NaOH NaNO2+NaNO3+H2O2NO2+2OH -NO2-+NO3-+H2O13、一氧化氮、二氧化氮和氢氧化钠溶液反应:NO+NO2+2NaOH2NaNO2+H2ONO+NO2+2OH -2NO2-+H2O14、将二氧化硅溶于氢氧化钠溶液中:2NaOH+SiO 2Na2SiO3+H2O2OH-+SiO 2SiO32-+H2O15、三氧化硫和氢氧化钠溶液反应:SO3+2NaOH Na2SO4+H2OSO3+2OH -SO42-+H2O16、盐酸和氢氧化钠溶液反应:HCl+NaOH NaCl+H2O H++OH -H2O 17、醋酸和氢氧化钠溶液反应:CH3COOH+NaOH CH3COONa+H2OCH3COOH+OH -CH3COO-+H2O18、向氢氧化钠溶液中通入少量的硫化氢:H2S+2NaOH Na2S+2H2OH2S+2OH -S2-+2H2O19、向氢氧化钠溶液中通入足量的硫化氢:H2S+NaOH NaHS+H2OH2S+OH -HS-+H2O20、硫酸和氢氧化钠溶液反应:H2SO4+2NaOH Na2SO4+2H2OH++OH -H2O21、磷酸溶液氢氧化钠溶液反应:H3PO4+3NaOH Na3PO4+3H2OH3PO4+3OH -PO43-+3H2O22、将氢氧化铝溶于氢氧化钠溶液中:Al(OH)3+NaOH NaAlO2+2H2OAl(OH)3+OH -AlO2-+2H2O23、向硝酸银溶液中加入氢氧化钠溶液:AgNO3+NaOH AgOH ↓+NaNO3Ag++OH -AgOH ↓24、向硫酸铜溶液中加入氢氧化钠溶液:CuSO4+2NaOH Na2SO4+Cu(OH)2↓Cu2++2OH -Cu(OH)2↓25、向氯化铁溶液中加入氢氧化钠溶液:FeCl3+3NaOH Fe(OH)3↓+3NaClFe3++3OH -Fe(OH)3↓26、向氯化铝溶液中加入少量氢氧化钠溶液:AlCl3+3NaOH Al(OH)3↓+3NaClAl3++3OH -Al(OH)3↓27、向氯化铝溶液中加入足量氢氧化钠溶液:AlCl3+4NaOH NaAlO2+3NaCl+2H2OAl3++4OH -AlO2-+2H2O28、向氯化铵溶液加入氢氧化钠溶液,加热:NH4Cl+NaOH NaCl+NH3↑+H2ONH4++OH -NH3↑+H2O29、向碳酸氢铵溶液中加入少量氢氧化钠溶液共热:NH4HCO3+NaOH NaHCO3+NH3↑+H2ONH4++OH -NH3↑+H2O30、向碳酸氢铵溶液中加入足量氢氧化钠溶液共热:NH4HCO3+2NaOH Na2CO3+NH3↑+2H2ONH4++HCO3-+OH -CO32-+NH3↑+2H2O 31、碳酸氢钠溶液与氢氧化钠溶液混合:NaHCO3+NaOH Na2CO3+H2OHCO3-+OH -CO32-+H2O32、向碳酸氢钙溶液中加入少量氢氧化钠溶液:Ca(HCO3)2+NaOH CaCO3↓+NaHCO3+H2OCa2++HCO3-+OH -CaCO3↓+H2O33、向碳酸氢钙溶液中加入过量氢氧化钠溶液:Ca(HCO3)2+2NaOH CaCO3↓+Na2CO3+2H2O Ca2++2HCO3-+2OH -CaCO3+CO32-+2H2O 34、向碳酸氢镁溶液中加入少量的氢氧化钠溶液:Mg(HCO3)2+2NaOH Mg(OH)2↓+2NaHCO3Mg2++OH -Mg(OH)2↓35、向碳酸氢镁溶液中加入过量的氢氧化钠溶液:Mg(HCO3)2+4NaOH Mg(OH)2↓+Na2CO3+2H2O Mg2++2HCO32-+4OH -Mg(OH)2↓+2CO32-+2H2O五、氯化钠1、氯化钠溶液与硝酸银溶液混合:NaCl+AgNO 3AgCl↓+NaNO3Cl-+Ag +AgCl ↓2、氯化钠固体和浓硫酸共热:NaCl+H2SO 4Na2SO4+2HCl↑3、电解饱和的氯化钠溶液:2NaCl+2H2O2NaOH+H2↑+Cl2↑2Cl-+2H2O2OH-+H2↑+Cl2↑4、电解氯化钠的熔融液:2NaCl2Na+Cl2↑六、碳酸钠1、碳酸钠溶液与澄清石灰水反应:Na2CO3+Ca(OH)2CaCO3↓+2NaOHCO32-+Ca2+CaCO3↓2、碳酸钠溶液与氯化钡溶液混合:Na2CO3+BaCl 2BaCO3↓+2NaClCO32-+Ba2+BaCO3↓3、碳酸钠溶液呈碱性:Na2CO3+H2O NaHCO3+NaOHCO32-+H2O HCO3-+OH-4、碳酸钠溶液滴入少量的盐酸:Na2CO3+HCl NaHCO3+NaClCO32-+H +HCO3-5、碳酸钠溶液滴入足量的盐酸:Na2CO3+2HCl2NaCl+CO2↑+H2OCO32-+2H +CO2↑+H2O6、碳酸钠溶液中加入醋酸:Na2CO3+2CH3COOH2CH3COONa+CO2↑+H2O CO32-+2CH3COOH2CH3COO-+CO2↑+H2O7、碳酸钠溶液中通入二氧化碳气体:Na2CO3+CO2+H2O2NaHCO3CO32-+CO2+H2O2HCO3-8、向饱和的碳酸钠溶液中通入二氧化碳气体:Na2CO3+CO2+H2O2NaHCO32Na++CO32-+CO2+H2O2NaHCO3↓9、碳酸钠溶液与氯化铝溶液混合:3Na2CO3+2AlCl3+3H2O===2Al(OH)3↓+6NaCl+3CO2↑3CO32-+2Al3++3H2O2Al(OH)3↓+3CO2↑10、碳酸钠溶液与氯化铁溶液混合:3Na2CO3+2FeCl3+3H2O===2Fe(OH)3↓+6NaCl+3CO2↑3CO32-+2Fe3++3H2O2Fe(OH)3↓+3CO2↑七、碳酸氢钠1、碳酸氢钠溶液呈碱性:NaHCO3+H2O H2CO3+NaOHHCO3-+H2O H2CO3+OH-2、碳酸氢钠溶液滴入盐酸:NaHCO3+HCl NaCl+CO2↑+H2OHCO3-+H +CO2↑+H2O3、碳酸氢钠溶液滴入醋酸:NaHCO3+CH3COOH CH3COONa+CO2↑+H2O HCO3-+CH3COOH CH3COO-+CO2↑+H2O4、碳酸氢钠溶液与氯化铝溶液混合:3NaHCO3+AlCl 3Al(OH)3↓+3NaCl+3CO2↑3HCO3-+Al3+Al(OH)3↓+3CO2↑5、碳酸氢钠溶液与氯化铁溶液混合:3NaHCO3+FeCl 3Fe(OH)3↓+3NaCl+3CO2↑3HCO3-+Fe3+Fe(OH)3↓+3CO2↑6、碳酸氢钠溶液与氢氧化钠溶液混合:NaHCO3+NaOH Na2CO3+H2OHCO3-+OH -CO32-+H2O7、碳酸氢钠溶液中加入过量氢氧化钙溶液:NaHCO3+Ca(OH)2 =CaCO3↓+NaOH+H2OCa2++HCO3-+OH -CaCO3↓+H2O8、碳酸氢钠溶液中加入少量氢氧化钙溶液:2NaHCO3+Ca(OH)2 =CaCO3↓+Na2CO3+2H2OCa2++2HCO3-+2OH -CaCO3↓+CO32-+2H2O 9、碳酸氢钠受热分解:2NaHCO 3Na2CO3+CO2↑+H2O镁及其化合物一、镁1、镁在氧气中燃烧:2Mg+O 22MgO2、镁在氯气中燃烧:Mg+Cl 2MgCl23、镁在氮气中燃烧:3Mg+N 2Mg3N24、镁在二氧化碳中燃烧:2Mg+CO 22MgO+C5、镁与硫共热:Mg+S MgS6、镁与水共热:Mg+2H2O Mg(OH)2+H2↑7、镁和盐酸反应:Mg+2HCl MgCl2+H2↑Mg+2H +Mg2++H2↑8、镁和醋酸反应:Mg+2CH3COOH(CH3COO)2Mg+H2↑Mg+2CH3COOH2CH3COO-+Mg2++H2↑9、镁和氯化铵溶液反应:Mg+2NH4Cl MgCl2+2NH3↑+H2↑Mg+2NH4+Mg2++2NH3↑+H2↑10、将少量的镁投入到氯化铁溶液中:Mg+2FeCl 32FeCl2+MgCl2Mg+2Fe3+Mg2++2Fe2+11、将过量的镁投入到氯化铁溶液中:3Mg+2FeCl 33MgCl2+2Fe3Mg+2Fe3+3Mg2++2Fe12、镁和硫酸铜溶液反应:Mg+CuSO 4MgSO4+CuMg+Cu2+Mg2++Cu 13、镁和浓硫酸反应:Mg+2H2SO 4MgSO4+SO2↑+2H2O14、镁和浓硝酸反应:Mg+4HNO 3Mg(NO3)2+2NO2↑+2H2OMg+4H++2NO3-Mg2++2NO2↑+2H2O15、镁和稀硝酸反应:3Mg+8HNO 33Mg(NO3)2+2NO ↑+4H2O3Mg+8H++2NO3-Mg2++2NO ↑+4H2O二、氧化镁1、氧化镁与盐酸反应:MgO+2HCl MgCl2+H2OMgO+2H +Mg2++H2O2、氧化镁和醋酸反应:MgO+2CH3COOH(CH3COO)2Mg+H2OMgO+2CH3COOH Mg2++2CH3COO-+H2O3、氧化镁溶于氯化铵溶液中:MgO+2NH4Cl MgCl2+2NH3↑+H2OMgO+2NH4+Mg2++2NH3↑+H2O 4、氧化镁投入到氯化铁溶液中:3MgO+2FeCl3+3H2O3MgCl2+2Fe(OH)33MgO+2Fe3++3H2O3Mg2++2Fe(OH)3三、氢氧化镁1、氢氧化镁和盐酸反应:Mg(OH)2+2HCl MgCl2+2H2OMg(OH)2+2H +Mg2++2H2O2、氢氧化镁和醋酸反应:Mg(OH)2+2CH3COOH(CH3COO)2Mg+2H2OMg(OH)2+2CH3COOH2CH3COO-+Mg2++2H2O3、氢氧化镁溶于氯化铵溶液中:Mg(OH)2+2NH4Cl MgCl2+2NH3↑+2H2OMg(OH)2+2NH4+Mg2++2NH3↑+2H2O4、氢氧化镁投入到氯化铁溶液中:3Mg(OH)2+2FeCl 33MgCl2+2Fe(OH)33Mg(OH)2+2Fe3+3Mg2++2Fe(OH)35、氢氧化镁受热分解:Mg(OH)2MgO+H2O四、氯化镁1、氯化镁溶液与硝酸银溶液反应:MgCl2+2AgNO 32AgCl ↓+Mg(NO3)2Cl-+Ag +AgCl ↓2、氯化镁溶液中加入氢氧化钠溶液:MgCl2+2NaOH=Mg(OH)2↓+2NaClMg2++2OH -Mg(OH)2↓3、氯化镁溶液加入氨水:MgCl2+2NH3·H2O Mg(OH)2↓+2NH4ClMg2++2NH3·H2O Mg(OH)2↓+2NH4+4、氯化镁溶液中加入偏铝酸钠溶液:MgCl2+2NaAlO2+4H2O==Mg(OH)2↓+2Al(OH)3↓+2NaCl Mg2++2AlO2-+4H2O Mg(OH)2↓+2Al(OH)3↓5、电解氯化镁的熔融液:MgCl 2Mg+Cl2↑6、电解氯化镁的溶液:MgCl2+2H2O Mg(OH)2↓+H2↑+Cl2↑Mg2++2Cl-+2H2O Mg(OH)2↓+H2↑+Cl2↑五、碳酸镁1、碳酸镁与盐酸反应:MgCO3+2HCl===MgCl2+CO2↑+H2OMgCO3+2H+===Mg2++CO2↑+H2O2、碳酸镁与醋酸溶液反应:MgCO3+2CH3COOH===(CH3COO)2Mg+CO2↑+H2O MgCO3+2CH3COOH===2CH3COO-+Mg2++CO2↑+H2O 3、碳酸镁悬浊液通入二氧化碳气体:MgCO3+CO2+H2O===Mg(HCO3)2MgCO3+CO2+H2O===Mg2++2HCO3-4、碳酸镁加入到氯化铁溶液中:3MgCO3+2FeCl3+3H2O===3MgCl2+2Fe(OH)3↓+3CO2↑3MgCO3+2Fe3++3H2O===3Mg2++2Fe(OH)3↓+3CO2↑5、碳酸镁加入氯化铵溶液中:MgCO3+2NH4Cl===MgCl2+2NH3↑+CO2↑MgCO3+2NH4+===Mg2++2NH3↑+CO2↑6、碳酸镁高温煅烧:MgCO3高温MgO+CO2↑六、碳酸氢镁1、碳酸氢镁与盐酸反应:Mg(HCO3)2+2HCl===MgCl2+2CO2↑+2H2OHCO3-+H+===CO2↑+H2O2、碳酸氢镁与少量的氢氧化钠溶液反应:Mg(HCO3)2+2NaOH===Mg(OH)2↓+2NaHCO3Mg2++2OH-===Mg(OH)2↓3、碳酸氢镁与过量的氢氧化钠溶液反应:Mg(HCO3)2+4NaOH===Mg(OH)2↓+Na2CO3+2H2OMg2++2HCO 3-+4OH-===Mg(OH)2↓+2CO32-+2H2O 4、碳酸氢镁与澄清石灰水反应:Mg(HCO 3)2+2Ca(OH)2===Mg(OH)2↓+2CaCO3↓+2H2O Mg2++2HCO 3-+2Ca2++4OH-===Mg(OH)2↓+2CaCO3↓+2H2O5、碳酸氢镁受热分解:Mg(HCO3)2△MgCO3↓+CO 2↑+H2O 铝及其化合物一、铝1、铝在氧气中燃烧:4Al+3O 22Al2O32、铝在氯气中燃烧:2Al+3Cl 22AlCl33、铝和硫共热:2Al+3S Al2S34、铝与稀硫酸反应:2Al+3H2SO4Al2(SO4)3+3H2↑2Al+6H +2Al3++3H2↑5、铝和氢氧化钠溶液反应:2Al+2NaOH +2H2O2NaAlO2+3H2↑2Al+2OH-+2H2O2AlO2-+3H2↑6、铝和浓硫酸共热:2Al+6H2SO4Al2(SO4)3+3SO2↑+6H2O7、铝和浓硝酸共热:Al+6HNO3Al(NO3)3+3NO2↑+3H2OAl+6H++3NO3-Al3++3NO2↑+3H2O8、铝和稀硝酸反应:Al+4HNO3Al(NO3)3+NO ↑+2H2OAl+4H++NO3-Al3++NO ↑+2H2O8、铝和硝酸银溶液反应:Al+3AgNO3Al(NO3)3+3AgAl+3Ag+Al3++3Ag9、铝与硫酸铜溶液反应:2Al+3CuSO4Al2(SO4)3+3Cu2Al+3Cu2+2Al3++3Cu10、铝和氧化铁高温下反应:2Al+Fe2O3Al2O3+2Fe11、铝和四氧化三铁高温共热:8Al+3Fe3O44Al2O3+9Fe12、铝和氧化铜高温共热:2Al+3CuO Al2O3+3Cu13、铝和二氧化锰高温共热:4Al+3MnO22Al2O3+3Mn二、氧化铝1、氧化铝与稀硫酸反应:Al2O3+3H2SO 4Al2(SO4)3+3H2OAl2O3+6H +2Al3++3H2O2、氧化铝与氢氧化钠溶液反应:Al2O3+2NaOH2NaAlO2+H2OAl2O3+2OH -2AlO2-+H2O3、电解氧化铝的熔融液:2Al2O 34Al+3O2↑三、氢氧化铝1、氢氧化铝与稀硫酸反应:2Al(OH)3+3H2SO4Al2(SO4)3+6H2OAl(OH)3+3H+Al3++3H2O2、氢氧化铝与氢氧化钠溶液反应:Al(OH)3+NaOH NaAlO2+2H2OAl(OH)3+OH-AlO2-+2H2O3、加热氢氧化铝:2Al(OH)3Al2O3+3H2O四、硫酸铝1、硫酸铝溶液与氯化钡溶液混合:Al2(SO4)3+3BaCl22AlCl3+3BaSO4↓SO42-+Ba2+BaSO4↓2、硫酸铝的水溶液呈酸性:Al2(SO4)3+6H2O2Al(OH)3+3H2SO4Al3++3H2O Al(OH)3+3H+3、硫酸铝溶液中加入少量的氢氧化钠溶液:Al2(SO4)3+6NaOH3Na2SO4+2Al(OH)3↓Al3++3OH-Al(OH)3↓4、向硫酸铝溶液中加足量的氢氧化钠溶液:Al2(SO4)3+8NaOH2NaAlO2+3Na2SO4+4H2OAl3++4OH-AlO2-+2H2O5、向硫酸铝溶液中加入少量的氢氧化钡溶液:Al2(SO4)3+3Ba(OH)22Al(OH)3↓+3BaSO4↓2Al3++3SO42-+3Ba2++6OH-2Al(OH)3↓+3BaSO4↓6、向硫酸铝溶液中加入足量的氢氧化钡溶液:Al2(SO4)3+4Ba(OH)2Ba(AlO2)2+3BaSO4↓+4H2O2Al3++3SO42-+3Ba2++8OH-==2AlO2-+3BaSO4↓+4H2O 7、向明矾溶液中加入少量的氢氧化钡溶液:3Ba(OH)2+2KAl(SO4)22Al(OH)3↓+3BaSO4↓+K2SO4 3Ba2++6OH-+2Al3++3SO42-3BaSO4↓+2Al(OH)3↓8、向明矾溶液中加入足量的氢氧化钡溶液:KAl(SO4)2+2Ba(OH)2KAlO2+2BaSO4↓+2H2OAl3++2SO42-+2Ba2++4OH-===AlO2-+2BaSO4↓+2H2O 9、向硫酸铝溶液中加入氨水:Al2(SO4)3+6NH3·H2O2Al(OH)3↓+3(NH4)2SO4Al3++3NH3·H2O Al(OH)3↓+3NH4+10、向硫酸铝溶液中加入碳酸钠溶液:Al2(SO4)3+3Na2CO3+3H2O==2Al(OH)3↓+3Na2SO4+3CO2↑2Al3++3CO32-+3H2O2Al(OH)3↓+3CO2↑11、向硫酸铝溶液中加入碳酸氢钠溶液:Al2(SO4)3+6NaHCO32Al(OH)3↓+3Na2SO4+6CO2↑Al3++3HCO3-Al(OH)3↓+3CO2↑12、向硫酸铝溶液中加入硫化钠溶液:Al2(SO4)3+3Na2S+6H2O==2Al(OH)3↓+3Na2SO4+3H2S↑2Al3++3S2-+6H2O2Al(OH)3↓+3H2S ↑13、向硫酸铝溶液中加入硫氢化钠溶液:Al2(SO4)3+6NaHS+6H2O==2Al(OH)3↓+3Na2SO4+6H2S↑Al3++3HS-+3H2O Al(OH)3↓+3H2S ↑14、向硫酸铝溶液中加入硅酸钠溶液:Al2(SO4)3+3Na2SiO3+6H2O==2Al(OH)3↓+3Na2SO4+3H2SiO3↓2Al3++3SiO32-+6H2O2Al(OH)3↓+3H2SiO3↓15、向硫酸铝溶液中加入偏铝酸钠溶液:Al2(SO4)3+6NaAlO2+12H2O3Na2SO4+8Al(OH)3↓Al3++AlO2-+6H2O4Al(OH)3↓五、偏铝酸钠1、偏铝酸钠溶液呈碱性:NaAlO2+2H2O AI(OH)3+NaOHAlO2-+2H2O Al(OH)3+OH-冰晶石电解2、偏铝酸钠溶液滴入少量盐酸:NaAlO2+HCl+H2O Al(OH)3↓+NaClAlO2-+H++H2O Al(OH)3↓3、向偏铝酸钠溶液加入足量盐酸:NaAlO2+4HCl NaCl+AlCl3+2H2OAlO2-+4H+Al3++2H2O4、向偏铝酸钠溶液通入少量二氧化碳气体:2NaAlO2+CO2+3H2O2Al(OH)3↓+Na2CO32AlO2-+CO2+3H2O2Al(OH)3↓+CO32-5、向偏铝酸钠溶液通入足量二氧化碳气体:NaAlO2+CO2+2H2O Al(OH)3+NaHCO3AlO2-+CO2+2H2O Al(OH)3+HCO3-6、向偏铝酸钠溶液中加入硫酸铝溶液:Al2(SO4)3+6NaAlO2+12H2O3Na2SO4+8Al(OH)3↓Al3++AlO2-+6H2O4Al(OH)3↓7、向偏铝酸钠溶液中加入氯化铵溶液:NaAlO2+NH4Cl+H2O Al(OH)3↓+NaCl+NH3↑AlO2-+NH4++H2O Al(OH)3↓+NH3↑8、向偏铝酸钠溶液中加入氯化铁溶液:3NaAlO2+FeCl3+6H2O===3Al(OH)3↓+Fe(OH)3↓+3NaCl 3AlO2-+Fe3++6H2O3Al(OH)3↓+Fe(OH)3↓。

铝及其化合物的化学方程式和离子方程式文件编码(008-TTIG-UTITD-GKBTT-PUUTI-WYTUI-8256)铝及其化合物的化学方程式和离子方程式一、铝1、铝在氧气中燃烧:4Al+3O2=2Al2O32、铝在氯气中燃烧:2Al+3Cl2=2AlCl33、铝和硫共热:2Al+3S=Al2S34、铝与稀硫酸反应:2Al+3H2SO4=Al2(SO4)3+3H2↑2Al+6H+=2Al3++3H2↑5、铝和氢氧化钠溶液反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑6、铝和浓硫酸共热:2Al+6H2SO4=Al2(SO4)3+3SO2↑+6H2O7、铝和浓硝酸共热:Al+6HNO3=Al(NO3)3+3NO2↑+3H2O8、铝和稀硝酸反应:Al+4HNO3=Al(NO3)3+NO↑+2H2O9、铝和硝酸银溶液反应:Al+3AgNO3=Al(NO3)3+3AgAl+3Ag10、铝与硫酸铜溶液反应:2Al+3CuSO4=Al2(SO4)3+3Cu2Al+3Cu211、铝和氧化铁高温下反应:2Al+Fe2O3=Al2O3+2Fe12、铝和四氧化三铁高温共热:8Al+3Fe3O4=4Al2O3+9Fe13、铝和氧化铜高温共热:2Al+3CuO=Al2O3+3Cu14、铝和二氧化锰高温共热:4Al+3MnO2=2Al2O3+3Mn二、氧化铝1、氧化铝与稀硫酸反应:Al2O3+3H2SO4=Al2(SO4)3+3H2OAl2O3+6H2、氧化铝与氢氧化钠溶液反应:Al2O3+2NaOH=2NaAlO2+H2OAl2O3+2OH3、电解氧化铝的熔融液:2Al2O3=4Al+3O2↑三、氢氧化铝1、氢氧化铝与稀硫酸反应:2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O2、氢氧化铝与氢氧化钠溶液反应:Al(OH)3+NaOH=NaAlO2+2H2O3、加热氢氧化铝:2Al(OH)3=Al2O3+3H2O四、硫酸铝1、硫酸铝溶液与氯化钡溶液混合:Al2(SO4)3+3BaCl2=2AlCl3+3BaSO4↓2、硫酸铝的水溶液呈酸性:Al2(SO4)3+6H2O=2Al(OH)3+3H2SO43、硫酸铝溶液中加入少量的氢氧化钠溶液:Al2(SO4)3+6NaOH=3Na2SO4+2Al(OH)3↓4、向硫酸铝溶液中加足量的氢氧化钠溶液Al2(SO4)3+8NaOH=2NaAlO2+3Na2SO4+4H2O5、向硫酸铝溶液中加入少量的氢氧化钡溶液:Al2(SO4)3+3Ba(OH)2=2Al(OH)3↓+3BaSO4↓6、向硫酸铝溶液中加入足量的氢氧化钡溶液:冰晶石电解Al2(SO4)3+4Ba(OH)2=Ba(AlO2)2+3BaSO4↓+4H2O7、向明矾溶液中加入少量的氢氧化钡溶液:3Ba(OH)2+2KAl(SO4)2=2Al(OH)3↓+3BaSO4↓+K2SO48、向明矾溶液中加入足量的氢氧化钡溶液:KAl(SO4)2+2Ba(OH)2=KAlO2+2BaSO4↓+2H2O9、向硫酸铝溶液中加入氨水:Al2(SO4)3+6NH3·H2O=2Al(OH)3↓+3(NH4)2SO410、向硫酸铝溶液中加入碳酸钠溶液:Al2(SO4)3+3Na2CO3+3H2O=2Al(OH)3↓+3Na2SO4+3CO2↑Al2(SO4)3+6NaHCO3=2Al(OH)3↓+3Na2SO4+6CO2↑12、向硫酸铝溶液中加入硫化钠溶液:Al2(SO4)3+3Na2S+6H2O=2Al(OH)3↓+3Na2SO4+3H2S↑13、向硫酸铝溶液中加入硫氢化钠溶液:Al2(SO4)3+6NaHS+6H2O=2Al(OH)3↓+3Na2SO4+6H2S↑14、向硫酸铝溶液中加入硅酸钠溶液:Al2(SO4)3+3Na2SiO3+6H2O=2Al(OH)3↓+3Na2SO4+3H2SiO3↓15、向硫酸铝溶液中加入偏铝酸钠溶液:Al2(SO4)3+6NaAlO2+12H2O=3Na2SO4+8Al(OH)3↓五、偏铝酸钠1、偏铝酸钠溶液呈碱性:NaAlO2+2H2O=AI(OH)3+NaOH2、偏铝酸钠溶液滴入少量盐酸:NaAlO2+HCl+H2O=Al(OH)3↓+NaCl3、向偏铝酸钠溶液加入足量盐酸:NaAlO2+4HCl=NaCl+AlCl3+2H2O4、向偏铝酸钠溶液通入少量二氧化碳气体:2NaAlO2+CO2+3H2O=2Al(OH)3↓+Na2CO35、向偏铝酸钠溶液通入足量二氧化碳气体:NaAlO2+CO2+2H2O=Al(OH)3+NaHCO36、向偏铝酸钠溶液中加入硫酸铝溶液:Al2(SO4)3+6NaAlO2+12H2O=3Na2SO4+8Al(OH)3↓7、向偏铝酸钠溶液中加入氯化铵溶液:NaAlO2+NH4Cl+H2O=Al(OH)3↓+NaCl+NH3↑3NaAlO2+FeCl3+6H2O=3Al(OH)3↓+Fe(OH)3↓+3NaCl。
欢迎阅读镁及其化合物的化学方程式和离子方程式一、镁1、镁在氧气中燃烧:2Mg+O22MgO 2、镁在氯气中燃烧:Mg+Cl 2MgCl23、镁在氮气中燃烧:3Mg+N2Mg3N24、镁在二氧化碳中燃烧:2Mg+CO22MgO+C5S67MgClMg8COOH(CHCOOH2CH9Cl MgCl+Mg102FeClMg 1133Mg+2Fe3+3Mg2++2Fe12、镁和硫酸铜溶液反应:Mg+CuSO4MgSO4+CuMg+Cu2+Mg2++Cu13、镁和浓硫酸反应:Mg+2H2SO4MgSO4+SO2↑+2H2O14、镁和浓硝酸反应:Mg+4HNO3Mg(NO3)2+2NO2↑+2H2OMg+4H++2NO3-Mg2++2NO2↑+2H2O15、镁和稀硝酸反应:3Mg+8HNO33Mg(NO3)2+2NO ↑+4H2O3Mg+8H++2NO3-Mg2++2NO ↑+4H2O二、氧化镁1、氧化镁与盐酸反应:MgO+2HCl MgCl2+H2OMgO+2H+Mg2++H2O2、氧化镁和醋酸反应:MgO+2CH3COOH(CH3COO)2Mg+H2O2+-3Cl MgClMg4O3MgClO3Mg12HCl MgCl+Mg22CH3MgClMg4、氢氧化镁投入到氯化铁溶液中:3Mg(OH)2+2FeCl33MgCl2+2Fe(OH)33Mg(OH)2+2Fe3+3Mg2++2Fe(OH)35、氢氧化镁受热分解:Mg(OH)2MgO+H2O四、氯化镁1、氯化镁溶液与硝酸银溶液反应:MgCl2+2AgNO32AgCl ↓+Mg(NO3)2Cl-+Ag+AgCl ↓2、氯化镁溶液中加入氢氧化钠溶液:MgCl2+2NaOH=Mg(OH)2↓+2NaClMg2++2OH-Mg(OH)2↓3、氯化镁溶液加入氨水:MgCl2+2NH3·H2O Mg(OH)2↓+2NH4ClMg2++2NH3·H2O Mg(OH)2↓+2NH4+4、氯化镁溶液中加入偏铝酸钠溶液:MgCl2+2NaAlO2+4H2O Mg(OH)2↓+2Al(OH)3↓+2NaClMg2++2AlO2-+4H2O Mg(OH)2↓+2Al(OH)3↓56Mg(OH)12345、碳酸镁加入氯化铵溶液中:MgCO3+2NH4Cl===MgCl2+2NH3↑+CO2↑MgCO3+2NH4+===Mg2++2NH3↑+CO2↑6、碳酸镁高温煅烧:MgCO3高温MgO+CO2↑六、碳酸氢镁1、碳酸氢镁与盐酸反应:Mg(HCO3)2+2HCl===MgCl2+2CO2↑+2H2OHCO3-+H+===CO2↑+H2O2、碳酸氢镁与少量的氢氧化钠溶液反应:Mg(HCO3)2+2NaOH===Mg(OH)2↓+2NaHCO3Mg2++2OH-===Mg(OH)2↓3、碳酸氢镁与过量的氢氧化钠溶液反应:Mg(HCO3)2+4NaOH===Mg(OH)2↓+Na2CO3+2H2OMg2++2HCO3-+4OH-===Mg(OH)2↓+2CO32-+2H2O4、碳酸氢镁与澄清石灰水反应:Mg(HCO3)2+2Ca(OH)2===Mg(OH)2↓+2CaCO3↓+2H2OMg2++2HCO3-+2Ca2++4OH-===Mg(OH)2↓+2CaCO3↓+2H2O5。
铝及其化合物的化学方程式和离子方程式一、铝1、铝在氧气中燃烧:4Al+3O22Al2O32、铝在氯气中燃烧:2Al+3Cl22AlCl33、铝和硫共热:2Al+3S Al2S34、铝与稀硫酸反应:2Al+3H2SO4Al2(SO4)3+3H2↑2Al+6H+2Al3++3H2↑5、铝和氢氧化钠溶液反应:2Al+2NaOH+2H2O2NaAlO2+3H2↑2Al+2OH-+2H2O2AlO2-+3H2↑6、铝和浓硫酸共热:2Al+6H2SO4Al2(SO4)3+3SO2↑+6H2O7、铝和浓硝酸共热:Al+6HNO3Al(NO3)3+3NO2↑+3H2OAl+6H++3NO3-Al3++3NO2↑+3H2O8、铝和稀硝酸反应:Al+4HNO3Al(NO3)3+NO ↑+2H2OAl+4H++NO3-Al3++NO ↑+2H2O8、铝和硝酸银溶液反应:Al+3AgNO3Al(NO3)3+3AgAl+3Ag+Al3++3Ag9、铝与硫酸铜溶液反应:2Al+3CuSO4Al2(SO4)3+3Cu2Al+3Cu2+2Al3++3Cu10、铝和氧化铁高温下反应:2Al+Fe2O3Al2O3+2Fe11、铝和四氧化三铁高温共热:8Al+3Fe3O44Al2O3+9Fe12、铝和氧化铜高温共热:2Al+3CuO Al2O3+3Cu13、铝和二氧化锰高温共热:4Al+3MnO22Al2O3+3Mn二、氧化铝1、氧化铝与稀硫酸反应:Al 2O 3+3H 2SO4Al 2(SO 4)3 +3H 2O Al 2O 3+6H+2Al 3++3H 2O2、氧化铝与氢氧化钠溶液反应:Al 2O 3+2NaOH2NaAlO 2+H 2O Al 2O 3+2OH-2AlO 2-+H 2O3、电解氧化铝的熔融液:2Al 2O34Al +3O 2 ↑三、氢氧化铝1、氢氧化铝与稀硫酸反应:2Al(OH)3 +3H 2SO 4Al 2(SO 4)3 +6H 2O Al(OH)3 +3H +Al 3++3H 2O2、氢氧化铝与氢氧化钠溶液反应:Al(OH)3 +NaOH NaAlO 2+2H 2O Al(OH)3 +OH -AlO 2-+2H 2O3、加热氢氧化铝:2Al(OH)3 Al 2O 3+3H 2O四、硫酸铝1、硫酸铝溶液与氯化钡溶液混合:Al 2(SO 4)3 +3BaCl 22AlCl 3+3BaSO 4 ↓SO 42-+Ba 2+BaSO 4 ↓2、硫酸铝的水溶液呈酸性:Al 2(SO 4)3+6H 2O 2Al(OH)3 +3H 2SO 4 Al 3++3H 2O Al(OH)3 +3H +3、硫酸铝溶液中加入少量的氢氧化钠溶液:Al 2(SO 4)3 +6NaOH3Na 2SO 4+2Al(OH)3 ↓Al 3++3OH-Al(OH)3 ↓4、向硫酸铝溶液中加足量的氢氧化钠溶液: Al 2(SO 4)3 +8NaOH 2NaAlO 2+3Na 2SO 4+4H 2OAl 3++4OH-AlO 2-+2H 2O5、向硫酸铝溶液中加入少量的氢氧化钡溶液: Al 2(SO 4)3 +3Ba(OH)22Al(OH)3 ↓+3BaSO 4 ↓2Al 3++3SO 42-+3Ba 2++6OH-2Al(OH)3 ↓+3BaSO 4 ↓6、向硫酸铝溶液中加入足量的氢氧化钡溶液:冰晶石电解Al2(SO4)3+4Ba(OH)2Ba(AlO2)2+3BaSO4↓+4H2O2Al3++3SO42-+3Ba2++8OH-2AlO2-+3BaSO4↓+4H2O7、向明矾溶液中加入少量的氢氧化钡溶液:3Ba(OH)2+2KAl(SO4)22Al(OH)3↓+3BaSO4↓+K2SO43Ba2++6OH-+2Al3++3SO42-3BaSO4↓+2Al(OH)3↓8、向明矾溶液中加入足量的氢氧化钡溶液:KAl(SO4)2+2Ba(OH)2KAlO2+2BaSO4↓+2H2OAl3++2SO42-+2Ba2++4OH-AlO2-+2BaSO4↓+2H2O9、向硫酸铝溶液中加入氨水:Al2(SO4)3+6NH3·H2O2Al(OH)3↓+3(NH4)2SO4Al3++3NH3·H2O Al(OH)3↓+3NH4+10、向硫酸铝溶液中加入碳酸钠溶液:Al2(SO4)3+3Na2CO3+3H2O2Al(OH)3↓+3Na2SO4+3CO2↑2Al3++3CO32-+3H2O2Al(OH)3↓+3CO2↑11、向硫酸铝溶液中加入碳酸氢钠溶液:Al2(SO4)3+6NaHCO32Al(OH)3↓+3Na2SO4+6CO2↑Al3++3HCO3-Al(OH)3↓+3CO2↑12、向硫酸铝溶液中加入硫化钠溶液:Al2(SO4)3+3Na2S+6H2O2Al(OH)3↓+3Na2SO4+3H2S ↑2Al3++3S2-+6H2O2Al(OH)3↓+3H2S ↑13、向硫酸铝溶液中加入硫氢化钠溶液:Al2(SO4)3+6NaHS+6H2O2Al(OH)3↓+3Na2SO4+6H2S ↑Al3++3HS-+3H2O Al(OH)3↓+3H2S ↑14、向硫酸铝溶液中加入硅酸钠溶液:Al2(SO4)3+3Na2SiO3+6H2O2Al(OH)3↓+3Na2SO4+3H2SiO3↓2Al3++3SiO32-+6H2O2Al(OH)3↓+3H2SiO3↓15、向硫酸铝溶液中加入偏铝酸钠溶液:Al2(SO4)3+6NaAlO2+12H2O3Na2SO4+8Al(OH)3↓Al3++AlO2-+6H2O4Al(OH)3↓五、偏铝酸钠1、偏铝酸钠溶液呈碱性:NaAlO2+2H2O AI(OH)3+NaOHAlO2-+2H2O Al(OH)3+OH-2、偏铝酸钠溶液滴入少量盐酸:NaAlO2+HCl+H2O Al(OH)3↓+NaClAlO2-+H++H2O Al(OH)3↓3、向偏铝酸钠溶液加入足量盐酸:NaAlO2+4HCl NaCl+AlCl3+2H2OAlO2-+4H+Al3++2H2O4、向偏铝酸钠溶液通入少量二氧化碳气体:2NaAlO2+CO2+3H2O2Al(OH)3↓+Na2CO32AlO2-+CO2+3H2O2Al(OH)3↓+CO32-5、向偏铝酸钠溶液通入足量二氧化碳气体:NaAlO2+CO2+2H2O Al(OH)3+NaHCO3AlO2-+CO2+2H2O Al(OH)3+HCO3-6、向偏铝酸钠溶液中加入硫酸铝溶液:Al2(SO4)3+6NaAlO2+12H2O3Na2SO4+8Al(OH)3↓Al3++AlO2-+6H2O4Al(OH)3↓7、向偏铝酸钠溶液中加入氯化铵溶液:NaAlO2+NH4Cl+H2O Al(OH)3↓+NaCl+NH3↑AlO2-+NH4++H2O Al(OH)3↓+NH3↑8、向偏铝酸钠溶液中加入氯化铁溶液:3NaAlO2+FeCl3+6H2O3Al(OH)3↓+Fe(OH)3↓+3NaCl3AlO2-+Fe3++6H2O3Al(OH)3↓+Fe(OH)3↓。
第二讲 铝、镁及其重要化合物[2020备考·最新考纲]1.掌握铝的主要性质及其应用。
2.掌握铝的重要化合物的主要性质及其应用。
镁的性质Mg 是较活泼的金属,常温下能被空气中的O 2氧化,表面生成一层致密的氧化膜。
镁在纯氧中剧烈燃烧,发出耀眼的白光。
镁不易和冷水反应,但能与沸水迅速反应。
铝的物理性质注意:铝是地壳中元素含量最高的金属元素。
掌握铝的化学性质与用途(1)铝的化学性质图中标号反应的化学方程式或离子方程式:②2Al +3Cl 2=====△2AlCl 3④2Al +2OH -+2H 2O===2AlO -2+3H 2↑⑤2Al +Fe 2O 3=====高温2Fe +Al 2O 3(铝热反应)(2)铝的制备及用途氧化铝氢氧化铝(1)物理性质白色胶状固体,不溶于水,有较强的吸附性。
(2)化学性质①Al(OH)3的电离②两性氢氧化物注意:Al(OH)3不溶于弱酸(如H 2CO 3),也不溶于弱碱(如氨水)。
③受热分解:2Al(OH)3=====△Al 2O 3+3H 2O 。
(3)制备Al(OH)3的三种方法方法一:可溶性铝盐溶液与过量氨水反应离子方程式:Al 3++3NH 3·H 2O===Al(OH)3↓+3NH +4。
方法二:向可溶性偏铝酸盐溶液中通入过量CO 2离子方程式:AlO -2+2H 2O +CO 2===Al(OH)3↓+HCO -3。
方法三:相互促进水解法常见的铝盐(1)硫酸铝钾是由两种不同的金属离子和一种酸根离子组成的复盐。
(2)明矾的化学式为KAl(SO 4)2·12H 2O ,它是无色晶体,可溶于水,水溶液pH <7(填“<”“>”或“=”)。
明矾可以净水,其净水的原理是:Al 3++3H 2OAl(OH)3(胶体)+3H +,Al(OH)3胶体吸附水中杂质形成沉淀而净水。
(3)明矾溶液与Ba(OH)2溶液反应的离子方程式①Al3+恰好完全沉淀:2Al3++3SO2-4+3Ba2++6OH-===2Al(OH)3↓+3BaSO4↓。
高中必修化学方程式无机化学部分一、钠及其化合物1.钠与氧气:常温:4Na +O 2=2Na 2O 点燃:2Na +O 2Na 2O 22.钠与水反应:2Na +2H 2O =2NaOH +H 2↑离子方程式:2Na +2H 2O =2Na ++2OH -+H 2↑ 3.钠与硫酸反应:2Na +H 2SO 4=Na 2SO 4+H 2↑2Na +2HCl =2NaCl +H 2↑4.氧化钠与水反应:Na 2O +H 2O =2NaOH5.过氧化钠与二氧化碳反应:2Na 2O 2+2CO 2=2Na 2CO 3+O 2Na 2O +2HCl =2NaCl +H 2O2Na 2O 2+4HCl =4NaCl +2H 2O +O 2↑6.过氧化钠与水反应:2Na 2O 2+2H 2O =4NaOH +O 2↑离子方程式:2Na 2O 2+2H 2O =4Na ++4OH -+O 2↑7.NaOH -2-NaOH 8.NaOH Na 39.制取O 1.3O 22Al 3S22.33.4.铝和5.6.4]-7.332328.氢氧化铝和NaOH 溶液:Al(OH)3+NaOH=Na[Al(OH)4]离子方程式:Al(OH)3+OH -=[Al(OH)4]-9.氢氧化铝受热分解:2Al(OH)3Al 2O 3+3H 2O10.硫酸铝与氨水反应(实验室制取氢氧化铝):Al 2(SO 4)3+6NH 3·H 2O =2Al(OH)3↓+3(NH 4)2SO 4离子方程式:Al 3++3NH 3·H 2O =Al(OH)3↓+3NH 4+11.AlCl 3溶液中加入碱溶液:Al 3++3OH -(少)=Al(OH)3↓Al 3++4OH -(过)=[Al(OH)4]-12.往四羟基合铝酸*溶液中通入CO 2:2[Al(OH)4]-+CO 2(少)=2Al(OH)3↓+CO 32-+H 2O[Al(OH)4]-+CO 2(过)=Al(OH)3↓+HCO 3-13.四羟基合铝酸*与酸反应:[Al(OH)4]-+H +(少)=Al(OH)3↓+H 2O[Al(OH)4]-+4H +(过)=Al 3++4H 2O14.电解氧化铝(工业制铝):2Al 2O 34Al +3O 2↑同时有CO 2和H 2O 时先和CO 2反应通电冰晶石15.铝的双水解反应:3[Al(OH)4]-+Al3+三、铁及其化合物1.铁与氧气反应:3Fe+2O2Fe3O4铁与硫反应:Fe+S FeS(黑)2.铁与盐酸反应:Fe+2HCl=FeCl2+H2↑离子方程式:Fe+2H+=Fe2++H2↑3.铁与CuSO4溶液:Fe+CuSO4=FeSO4+Cu离子方程式:Fe+Cu2+=Fe2++Cu4.铁和水蒸气:3Fe+4H2O(g)高温Fe3O4+4H2↑5.氧化亚铁与盐酸反应:FeO+2HCl=FeCl2+H2O离子方程式:FeO+2H+=Fe2++H2O氧化铁(铁红)与盐酸反应:Fe2O3+6HCl=2FeCl3+3H2O离子方程式:Fe2O3+6H+=2Fe3++3H2O四氧化三铁与酸反应:Fe3O4+8H+=2Fe2++2Fe3++4H2O3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O(与氧化性酸)6.CO7.8.9.311.除去12.FeCl13.FeCl14.15.2Fe316.O17.铁红18.21.O2SiO2.3.4.5.6.7.二氧化硅与氢氧化钠溶液反应:SiO2+2NaOH=Na2SiO3+H2O8.二氧化硅与碳反应(制粗硅):SiO2(石英砂)+2C(焦炭)高温Si(粗硅)+2CO↑制取高纯硅:Si(粗)+2Cl2高温SiCl4SiCl4+2H2高温Si(纯)+4HCl9.硅酸钠与盐酸反应:Na2SiO3+2HCl=H2SiO3↓+2NaCl离子方程式:SiO32-+2H+=H2SiO3↓10.往硅酸钠溶液中通入二氧化碳:Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3(生成透明的硅酸凝胶)11.二氧化硅与纯碱反应:SiO2+Na2CO3高温Na2SiO3+CO2↑12.二氧化硅与石灰石反应:SiO2+CaCO3高温CaSiO3(不溶)+CO2↑13.加热硅酸:H2SiO3SiO2+H2O五、氯及其化合物1.实验室制氯气:MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O离子方程式:MnO2+4H++2Cl -Mn2++Cl2↑+2H2O高锰酸钾制氯气:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O高氯酸钾制氯气:6HCl+KClO3=3Cl2↑+KCl+3H2O2.钠在氯气中燃烧:2Na+Cl 22NaCl铁在氯气中燃烧:2Fe+3Cl 22FeCl3铜在氯气中燃烧:Cu+Cl 2CuCl2氢气在氯气中燃烧:H2+Cl 22HCl3.4.O)2Na5.2HClO6.-7.8.9.NaClO+10.2H2O11.12.【1.6H++I-3.2Fe+3Br22FeBr I2FeI5.H2+Br22HBr6.H7.X2+H2O1.铜与非金属单质:2Cu+O22CuO2Cu+S Cu2S2.4CuO 高温2Cu2O+O2↑3.氢氧化铜:Cu(OH)2CuO+H2OCu(OH)2+4NH3·H2O=Cu(NH3)4(OH)2(氢氧化四氨合铜)+4H2O4.CuSO4·5H2O CuSO4+5H2O↑5.碱式碳酸铜:Cu2(OH)2CO3+2H2SO4=2CuSO4+CO2↑+3H2O2Cu+O2+H2O+CO2=Cu2(OH)2CO3Cu2(OH)2CO32CuO+CO2↑+H2O↑6.检验还原性糖:CH3CHO+2Cu(OH)2+NaOH→CH3COONa+Cu2O+3H2O七、硫及其化合物1.硫在空气中燃烧:S+O 2SO2硫与氢气加热:S+H 2H2S硫与铜加热:S+2Cu Cu2S硫与钠加热:S+2Na Na2S硫与汞加热:S+Hg HgS硫与铝加热:3S+2Al Al2S3硫与氢氧化钠加热:3S+6NaOH2Na2S+Na2SO3+3H2O2.硫与生石灰:2CaO+2S+3O2高温2CaSO43.二氧化硫的反应:SO2+H2O H2SO3SO2+H2O+2NH3=(NH4)2SO3SO2+Na2O少量SO过量SO4.SO25.6.SO27.8.9.10.SO2SO2(11.SO22HI12.SO213.FeS+14.3SO3215.16.17.铜(浓)2H硫与浓硫酸反应:S+2H2SO4(浓)3SO2↑+2H2O硫化氢与浓硫酸反应:H2S+2H2SO4(浓)=S↓+SO2+2H2O18.黑火药爆炸:S+2KNO3+3C K2S+3CO2↑+N2↑S+6HNO3(浓)H2SO4+6NO2↑+2H2OC+4HNO3(浓)CO2↑+4NO2↑+2H2O19.硫与碱反应:3S+6KOH2K2S+K2SO3+3H2O3S+6NaOH2Na2S+Na2SO3+3H2O20.Na2SO3与H2SO4反应:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O八、氮及其化合物1.氮气和氧气反应:N 2+O 22NO 氮气和镁:N 2+3MgMg 3N 22.工业合成氨:N 2+3H 23.一氧化氮与氧气反应:224.NO 2溶于水:3NO 2+H 2O =2HNO 3+NO5.氨气溶于水:NH 3+H 2O NH 3·H 2O 氨水显弱碱性(电离方程式):NH 3·H 2ONH 4++OH -6.浓氨水受热分解NH 3·H 2O△NH 3↑+H 2O7.氨气和氯化氢:HCl +NH 3=NH 4Cl Cl33NaOH -NH 2)Fe(NO )Fe(NO -NH 2NO2CO 2+N 2 九、镁及其化合物 1.2Mg +O 22MgO3Mg +N 2Mg 3N 22.2Mg +CO 2C +2MgO3.Mg +2H 2O Mg(OH)2+H 2↑(沸水)4.MgO +H 2O =Mg(OH)2(缓慢)5.Mg 3N 2+6H 2O =2NH 3↑+3Mg(OH)26.MgCl 2(熔融)Mg +Cl 2↑有机化学部分一、烷烃1.甲烷和氯气取代:CH 4+Cl 2CH 3Cl +HCl放电 催化剂光照光照CH 3Cl +Cl 2CH 2Cl 2+HClCH 2Cl +Cl 2CHCl 3(氯仿)+HCl CHCl 3+Cl 2CCl 4+HCl2.甲烷的裂解:CH 4C +2H 23.十六烷裂化:C 16H 34C 8H 18+C 8H 16二、烯烃1.CH 2=CH 2+Br 2CH 2Br —CH 2Br2.CH 2=CH 2+H 2OCH 3CH 2OH11.OH )2Ag(NH CHO OH(CHOH)CH 2342+O H 3NH 2Ag COONH OH(CHOH)CH Δ23442++↓+−→−12.CH 3CHO +2Cu(OH)2CH 3COOH +Cu 2O ↓+2H 2O13.2CH 3COOH +2Na2CH 3COONa +H 2↑14.酯化反应:CH 3COOH +CH 3CH 2OHCH 3+H 2O五、油脂、糖类1.酯的水解:CH 3COOCH 2CH 3+NaOHCH 3COONa +CH 3CH 2OH2.C 6H 12O 6(s)+6O 2(g)6CO 2(g)+6H 2O(l)3.葡萄糖发酵制取酒精:C 6H 12O 62CH 3CH 2OH +2CO 2↑4.C 12H 22O 11+H 2OC 6H 12O 6+C 6H 12O 6光照 光照高温催化剂 加热、加压催化剂△催化剂催化剂蔗糖葡萄糖果糖5.C 12H 22O 11+H 2O2C 6H 12O 6麦芽糖葡萄糖6.(C 6H 10O 5)n +nH 2OnC 6H 12O 6 淀粉/纤维素葡萄糖7.油脂的硬化(氧化):C 17H 33COO-CH 2C 17H 35COO-CH 2C 17H33COO-CH +3H 2C 17H 35COO-CH C 17H 33COO-CH 2C 17H 35COO-CH 28.皂化反应:C 17H 35COO-CH 2CH 2-OH C 17H 35COO-CH +3NaOH3C 17H 35COONa +CH-OH C 17H 35COO-CH 2CH 2-OH9.10.11.OOO =CC =O CH 3CH 3催化剂催化剂 催化剂 加压、加热。
系列二 主族金属专题8 镁铝及其化合物一、镁单质(1)镁在自然界没有单质存在,存在于各类硅酸盐和碳酸盐矿物里,如菱镁矿(MgCO 3)、白云石(CaCO 3·MgCO 3)、光卤石(KCl·MgCl 2·6H 2O)等。
海水中的镁是提取镁的主要来源,海水中的镁即使提取100万年也不会减少0.01%。
镁也是叶绿素的主要成分,在人体内镁以磷酸盐、碳酸盐的形式分布于骨头和肌肉中,缺乏会引起肌肉的颤动、脉象的混乱。
(2)强还原性:不论在固态或水溶液中都表现出强还原性,常用作还原剂。
高温下,镁夺取氧的能力特别强,甚至能在二氧化碳里燃烧,如2Mg+CO 2=====点燃2MgO+C ;也能够还原二氧化硅,2Mg+SiO 2=====点燃2MgO+Si ;常温下,由于镁表面的氧化膜导致镁不与水反应,但是加热下可以反应,Mg+2H 2O ====△Mg(OH)2+H 2↑。
(3)镁可以与大多数非金属和几乎所有的酸反应。
如2Mg+O 2=====点燃2MgO ,Mg+Cl 2=====点燃MgCl 2,Mg+S =====点燃MgS ,3Mg+N 2=====点燃Mg 3N 2(Mg 3N 2的特殊性质:Mg 3N 2+6H 2O =====3Mg (OH )2↓+2NH 3↑,导致其只能干态制取)。
镁不能和氢氟酸反应,因为MgF 2难溶会阻碍继续反应。
(4)格氏试剂:在醚的溶液中,镁能与卤代烃作用生成在有机化学中应用广泛的格氏试剂:Mg + RX =====醚RMgX(5)制取单质镁:一般是先从海水中得到氯化镁,然后电解熔融的氯化镁,MgCl 2(熔融) =====电解Mg+Cl 2↑。
二、镁的化合物(1)MgO 俗称菱苦土,是一种白色粉末。
MgO 对水呈一定惰性,特别是高温火烧后的MgO 难溶于水。
煆烧温度在923K 左右制成轻质MgO ,煆烧温度在1923K 以上制成重质MgO 。
铝及其化合物的化学方程式和离子方程式一、铝1、铝在氧气中燃烧:2、铝在氯气中燃烧:3、铝和硫共热:4、铝与稀硫酸反应:5、铝和氢氧化钠溶液反应:6、铝和浓硫酸共热:7、铝和浓硝酸共热:8、铝和稀硝酸反应:8、铝和硝酸银溶液反应:9、铝与硫酸铜溶液反应:10、铝和氧化铁高温下反应:11、铝和四氧化三铁高温共热:12、铝和氧化铜高温共热:13、铝和二氧化锰高温共热:二、氧化铝1、氧化铝与稀硫酸反应:2、氧化铝与氢氧化钠溶液反应:3、电解氧化铝的熔融液:三、氢氧化铝1、氢氧化铝与稀硫酸反应:2、氢氧化铝与氢氧化钠溶液反应:3、加热氢氧化铝:四、硫酸铝1、硫酸铝溶液与氯化钡溶液混合:2、硫酸铝的水溶液呈酸性:3、硫酸铝溶液中加入少量的氢氧化钠溶液:4、向硫酸铝溶液中加足量的氢氧化钠溶液:5、向硫酸铝溶液中加入少量的氢氧化钡溶液:6、向硫酸铝溶液中加入足量的氢氧化钡溶液:7、向明矾溶液中加入少量的氢氧化钡溶液:8、向明矾溶液中加入足量的氢氧化钡溶液:9、向硫酸铝溶液中加入氨水:10、向硫酸铝溶液中加入碳酸钠溶液:11、向硫酸铝溶液中加入碳酸氢钠溶液:12、向硫酸铝溶液中加入硫化钠溶液:13、向硫酸铝溶液中加入硫氢化钠溶液:14、向硫酸铝溶液中加入硅酸钠溶液:15、向硫酸铝溶液中加入偏铝酸钠溶液:五、偏铝酸钠1、偏铝酸钠溶液呈碱性:2、偏铝酸钠溶液滴入少量盐酸:3、向偏铝酸钠溶液加入足量盐酸:4、向偏铝酸钠溶液通入少量二氧化碳气体:5、向偏铝酸钠溶液通入足量二氧化碳气体:6、向偏铝酸钠溶液中加入硫酸铝溶液:7、向偏铝酸钠溶液中加入氯化铵溶液:8、向偏铝酸钠溶液中加入氯化铁溶液:铝及其化合物的化学方程式和离子方程式一、铝1、铝在氧气中燃烧:4Al+3O22Al2O32、铝在氯气中燃烧:2Al+3Cl22AlCl33、铝和硫共热:2Al+3S Al2S34、铝与稀硫酸反应:2Al+3H2SO4Al2(SO4)3+3H2↑2Al+6H+2Al3++3H2↑5、铝和氢氧化钠溶液反应:2Al+2NaOH+2H2O2NaAlO2+3H2↑2Al+2OH-+2H2O2AlO2-+3H2↑6、铝和浓硫酸共热:2Al+6H2SO4Al2(SO4)3+3SO2↑+6H2O7、铝和浓硝酸共热:Al+6HNO3Al(NO3)3+3NO2↑+3H2OAl+6H++3NO3-Al3++3NO2↑+3H2O8、铝和稀硝酸反应:Al+4HNO3Al(NO3)3+NO ↑+2H2OAl+4H++NO3-Al3++NO ↑+2H2O8、铝和硝酸银溶液反应:Al+3AgNO3Al(NO3)3+3AgAl+3Ag+Al3++3Ag9、铝与硫酸铜溶液反应:2Al+3CuSO4Al2(SO4)3+3Cu2Al+3Cu2+2Al3++3Cu10、铝和氧化铁高温下反应:2Al+Fe2O3Al2O3+2Fe11、铝和四氧化三铁高温共热:8Al+3Fe3O44Al2O3+9Fe12、铝和氧化铜高温共热:2Al+3CuO Al2O3+3Cu13、铝和二氧化锰高温共热:4Al+3MnO22Al2O3+3Mn二、氧化铝1、氧化铝与稀硫酸反应:Al 2O 3+3H 2SO4Al 2(SO 4)3 +3H 2O Al 2O 3+6H+2Al 3++3H 2O2、氧化铝与氢氧化钠溶液反应:Al 2O 3+2NaOH2NaAlO 2+H 2O Al 2O 3+2OH-2AlO 2-+H 2O3、电解氧化铝的熔融液:2Al 2O3+3O 2 ↑三、氢氧化铝1、氢氧化铝与稀硫酸反应:2Al(OH)3 +3H 2SO 4Al 2(SO 4)3 +6H 2OAl(OH)3 +3H +Al 3++3H 2O2、氢氧化铝与氢氧化钠溶液反应:Al(OH)3 +NaOH NaAlO 2+2H 2O Al(OH)3 +OH -AlO 2-+2H 2O3、加热氢氧化铝:2Al(OH)3 Al 2O 3+3H 2O四、硫酸铝1、硫酸铝溶液与氯化钡溶液混合:Al 2(SO 4)3 +3BaCl 22AlCl 3+3BaSO 4 ↓SO 42-+Ba 2+BaSO 4 ↓2、硫酸铝的水溶液呈酸性:Al 2(SO 4)3+6H 2O2Al(OH)3 +3H 2SO 4Al 3++3H 2OAl(OH)3 +3H +3、硫酸铝溶液中加入少量的氢氧化钠溶液:Al 2(SO 4)3 +6NaOH3Na 2SO 4+2Al(OH)3 ↓Al 3++3OH -Al(OH)3 ↓4、向硫酸铝溶液中加足量的氢氧化钠溶液: Al 2(SO 4)3 +8NaOH 2NaAlO 2+3Na 2SO 4+4H 2OAl 3++4OH -AlO 2-+2H 2O5、向硫酸铝溶液中加入少量的氢氧化钡溶液: Al 2(SO 4)3 +3Ba(OH)22Al(OH)3 ↓+3BaSO 4 ↓2Al 3++3SO 42-+3Ba 2++6OH -2Al(OH)3 ↓+3BaSO 4 ↓6、向硫酸铝溶液中加入足量的氢氧化钡溶液:冰晶石电解Al2(SO4)3+4Ba(OH)2Ba(AlO2)2+3BaSO4↓+4H2O2Al3++3SO42-+3Ba2++8OH-2AlO2-+3BaSO4↓+4H2O7、向明矾溶液中加入少量的氢氧化钡溶液:3Ba(OH)2+2KAl(SO4)22Al(OH)3↓+3BaSO4↓+K2SO43Ba2++6OH-+2Al3++3SO42-3BaSO4↓+2Al(OH)3↓8、向明矾溶液中加入足量的氢氧化钡溶液:KAl(SO4)2+2Ba(OH)2KAlO2+2BaSO4↓+2H2OAl3++2SO42-+2Ba2++4OH-AlO2-+2BaSO4↓+2H2O9、向硫酸铝溶液中加入氨水:Al2(SO4)3+6NH3·H2O2Al(OH)3↓+3(NH4)2SO4Al3++3NH3·H2O Al(OH)3↓+3NH4+10、向硫酸铝溶液中加入碳酸钠溶液:Al2(SO4)3+3Na2CO3+3H2O2Al(OH)3↓+3Na2SO4+3CO2↑2Al3++3CO32-+3H2O2Al(OH)3↓+3CO2↑11、向硫酸铝溶液中加入碳酸氢钠溶液:Al2(SO4)3+6NaHCO32Al(OH)3↓+3Na2SO4+6CO2↑Al3++3HCO3-Al(OH)3↓+3CO2↑12、向硫酸铝溶液中加入硫化钠溶液:Al2(SO4)3+3Na2S+6H2O2Al(OH)3↓+3Na2SO4+3H2S ↑2Al3++3S2-+6H2O2Al(OH)3↓+3H2S ↑13、向硫酸铝溶液中加入硫氢化钠溶液:Al2(SO4)3+6NaHS+6H2O2Al(OH)3↓+3Na2SO4+6H2S ↑Al3++3HS-+3H2O Al(OH)3↓+3H2S ↑14、向硫酸铝溶液中加入硅酸钠溶液:Al2(SO4)3+3Na2SiO3+6H2O2Al(OH)3↓+3Na2SO4+3H2SiO3↓2Al3++3SiO32-+6H2O2Al(OH)3↓+3H2SiO3↓15、向硫酸铝溶液中加入偏铝酸钠溶液:Al2(SO4)3+6NaAlO2+12H2O3Na2SO4+8Al(OH)3↓Al3++AlO2-+6H2O4Al(OH)3↓五、偏铝酸钠1、偏铝酸钠溶液呈碱性:NaAlO2+2H2O AI(OH)3+NaOHAlO2-+2H2O Al(OH)3+OH-2、偏铝酸钠溶液滴入少量盐酸:NaAlO2+HCl+H2O Al(OH)3↓+NaClAlO2-+H++H2O Al(OH)3↓3、向偏铝酸钠溶液加入足量盐酸:NaAlO2+4HCl NaCl+AlCl3+2H2OAlO2-+4H+Al3++2H2O4、向偏铝酸钠溶液通入少量二氧化碳气体:2NaAlO2+CO2+3H2O2Al(OH)3↓+Na2CO32AlO2-+CO2+3H2O2Al(OH)3↓+CO32-5、向偏铝酸钠溶液通入足量二氧化碳气体:NaAlO2+CO2+2H2O Al(OH)3+NaHCO3AlO2-+CO2+2H2O Al(OH)3+HCO3-6、向偏铝酸钠溶液中加入硫酸铝溶液:Al2(SO4)3+6NaAlO2+12H2O3Na2SO4+8Al(OH)3↓Al3++AlO2-+6H2O4Al(OH)3↓7、向偏铝酸钠溶液中加入氯化铵溶液:NaAlO2+NH4Cl+H2O Al(OH)3↓+NaCl+NH3↑AlO2-+NH4++H2O Al(OH)3↓+NH3↑8、向偏铝酸钠溶液中加入氯化铁溶液:3NaAlO2+FeCl3+6H2O3Al(OH)3↓+Fe(OH)3↓+3NaCl3AlO2-+Fe3++6H2O3Al(OH)3↓+Fe(OH)3↓。
铝及其化合物的化学方程式和离子方程式
一、铝
1、铝在氧气中燃烧:
2、铝在氯气中燃烧:
3、铝和硫共热:
4、铝与稀硫酸反应:
5、铝和氢氧化钠溶液反应:
6、铝和浓硫酸共热:
7、铝和浓硝酸共热:
8、铝和稀硝酸反应:
8、铝和硝酸银溶液反应:
9、铝与硫酸铜溶液反应:
10、铝和氧化铁高温下反应:
11、铝和四氧化三铁高温共热:
12、铝和氧化铜高温共热:
13、铝和二氧化锰高温共热:
二、氧化铝
1、氧化铝与稀硫酸反应:
2、氧化铝与氢氧化钠溶液反应:
3、电解氧化铝的熔融液:
三、氢氧化铝
1、氢氧化铝与稀硫酸反应:
2、氢氧化铝与氢氧化钠溶液反应:
3、加热氢氧化铝:
四、硫酸铝
1、硫酸铝溶液与氯化钡溶液混合:
2、硫酸铝的水溶液呈酸性:
3、硫酸铝溶液中加入少量的氢氧化钠溶液:
4、向硫酸铝溶液中加足量的氢氧化钠溶液:
5、向硫酸铝溶液中加入少量的氢氧化钡溶液:
6、向硫酸铝溶液中加入足量的氢氧化钡溶液:
7、向明矾溶液中加入少量的氢氧化钡溶液:
8、向明矾溶液中加入足量的氢氧化钡溶液:
9、向硫酸铝溶液中加入氨水:
10、向硫酸铝溶液中加入碳酸钠溶液:
11、向硫酸铝溶液中加入碳酸氢钠溶液:
12、向硫酸铝溶液中加入硫化钠溶液:
13、向硫酸铝溶液中加入硫氢化钠溶液:
14、向硫酸铝溶液中加入硅酸钠溶液:
15、向硫酸铝溶液中加入偏铝酸钠溶液:
五、偏铝酸钠
1、偏铝酸钠溶液呈碱性:
2、偏铝酸钠溶液滴入少量盐酸:
3、向偏铝酸钠溶液加入足量盐酸:
4、向偏铝酸钠溶液通入少量二氧化碳气体:
5、向偏铝酸钠溶液通入足量二氧化碳气体:
6、向偏铝酸钠溶液中加入硫酸铝溶液:
7、向偏铝酸钠溶液中加入氯化铵溶液:
8、向偏铝酸钠溶液中加入氯化铁溶液:
铝及其化合物的化学方程式和离子方程式
一、铝
1、铝在氧气中燃烧:4Al+3O22Al2O3
2、铝在氯气中燃烧:2Al+3Cl22AlCl3
3、铝和硫共热:2Al+3S Al2S3
4、铝与稀硫酸反应:2Al+3H2SO4Al2(SO4)3+3H2↑
2Al+6H+2Al3++3H2↑
5、铝和氢氧化钠溶液反应:2Al+2NaOH+2H2O2NaAlO2+3H2↑
2Al+2OH-+2H2O2AlO2-+3H2↑
6、铝和浓硫酸共热:2Al+6H2SO4Al2(SO4)3+3SO2↑+6H2O
7、铝和浓硝酸共热:Al+6HNO3Al(NO3)3+3NO2↑+3H2O
Al+6H++3NO3-Al3++3NO2↑+3H2O
8、铝和稀硝酸反应:Al+4HNO3Al(NO3)3+NO ↑+2H2O
Al+4H++NO3-Al3++NO ↑+2H2O
8、铝和硝酸银溶液反应:Al+3AgNO3Al(NO3)3+3Ag
Al+3Ag+Al3++3Ag
9、铝与硫酸铜溶液反应:2Al+3CuSO4Al2(SO4)3+3Cu
2Al+3Cu2+2Al3++3Cu
10、铝和氧化铁高温下反应:2Al+Fe2O3Al2O3+2Fe
11、铝和四氧化三铁高温共热:8Al+3Fe3O44Al2O3+9Fe
12、铝和氧化铜高温共热:2Al+3CuO Al2O3+3Cu
13、铝和二氧化锰高温共热:4Al+3MnO22Al2O3+3Mn
二、氧化铝
1、氧化铝与稀硫酸反应:Al2O3+3H2SO4Al2(SO4)3+3H2O Al2O3+6H+2Al3++3H2O
2、氧化铝与氢氧化钠溶液反应:Al O+2NaOH2NaAlO+H O
3、电解氧化铝的熔融液:2Al 2O
34Al +3O 2 ↑
三、氢氧化铝
1、氢氧化铝与稀硫酸反应:2Al(OH)3 +3H 2SO 4
Al 2(SO 4)3 +6H 2O Al(OH)3 +3H +
Al 3++3H 2O
2、氢氧化铝与氢氧化钠溶液反应:Al(OH)3 +NaOH NaAlO 2+2H 2O Al(OH)3 +OH -
AlO 2-
+2H 2O
3、加热氢氧化铝:2Al(OH)3 Al 2O 3+3H 2O
四、硫酸铝
1、硫酸铝溶液与氯化钡溶液混合:Al 2(SO 4)3 +3BaCl 2
2AlCl 3+3BaSO 4 ↓
SO 42-
+Ba 2
+BaSO 4 ↓
2、硫酸铝的水溶液呈酸性:Al 2(SO 4)3+6H 2O 2Al(OH)3 +3H 2SO 4 Al 3++3H 2O Al(OH)3 +3H +
3、硫酸铝溶液中加入少量的氢氧化钠溶液:Al 2(SO 4)3 +6NaOH
3Na 2SO 4+2Al(OH)3 ↓
Al 3+
+3OH
-
Al(OH)3 ↓
4、向硫酸铝溶液中加足量的氢氧化钠溶液: Al 2(SO 4)3 +8NaOH 2NaAlO 2+3Na 2SO 4+4H 2O
Al 3+
+4OH
-
AlO 2-
+2H 2O
5、向硫酸铝溶液中加入少量的氢氧化钡溶液: Al 2(SO 4)3 +3Ba(OH)2
2Al(OH)3 ↓+3BaSO 4 ↓
2Al 3+
+3SO 42-
+3Ba 2+
+6OH
-
2Al(OH)3 ↓+3BaSO 4 ↓
6、向硫酸铝溶液中加入足量的氢氧化钡溶液: Al 2(SO 4)3 +4Ba(OH)2
Ba(AlO 2)2 +3BaSO 4 ↓+4H 2O
2Al 3+
+3SO 42-
+3Ba 2+
+8OH
-
2AlO 2-
+3BaSO 4 ↓+4H 2O
7、向明矾溶液中加入少量的氢氧化钡溶液:
3Ba(OH)2 +2KAl(SO 4)2
2Al(OH)3 ↓+3BaSO 4 ↓+K 2SO 4
3Ba 2+
+6OH -
+2Al 3+
+3SO 42
-
3BaSO 4 ↓+2Al(OH)3 ↓
8、向明矾溶液中加入足量的氢氧化钡溶液: KAl(SO ) +2Ba(OH)
KAlO +2BaSO ↓+2H O
冰晶石
电解
9、向硫酸铝溶液中加入氨水:Al2(SO4)3+6NH3·H2O2Al(OH)3↓+3(NH4)2SO4
Al3++3NH3·H2O Al(OH)3↓+3NH4+
10、向硫酸铝溶液中加入碳酸钠溶液:
Al2(SO4)3+3Na2CO3+3H2O2Al(OH)3↓+3Na2SO4+3CO2↑
2Al3++3CO32-+3H2O2Al(OH)3↓+3CO2↑
11、向硫酸铝溶液中加入碳酸氢钠溶液:
Al2(SO4)3+6NaHCO32Al(OH)3↓+3Na2SO4+6CO2↑
Al3++3HCO3-Al(OH)3↓+3CO2↑
12、向硫酸铝溶液中加入硫化钠溶液:
Al2(SO4)3+3Na2S+6H2O2Al(OH)3↓+3Na2SO4+3H2S ↑
2Al3++3S2-+6H2O2Al(OH)3↓+3H2S ↑
13、向硫酸铝溶液中加入硫氢化钠溶液:
Al2(SO4)3+6NaHS+6H2O2Al(OH)3↓+3Na2SO4+6H2S ↑
Al3++3HS-+3H2O Al(OH)3↓+3H2S ↑
14、向硫酸铝溶液中加入硅酸钠溶液:
Al2(SO4)3+3Na2SiO3+6H2O2Al(OH)3↓+3Na2SO4+3H2SiO3↓
2Al3++3SiO32-+6H2O2Al(OH)3↓+3H2SiO3↓
15、向硫酸铝溶液中加入偏铝酸钠溶液:
Al2(SO4)3+6NaAlO2+12H2O3Na2SO4+8Al(OH)3↓
Al3++AlO2-+6H2O4Al(OH)3↓
五、偏铝酸钠
1、偏铝酸钠溶液呈碱性:NaAlO2+2H2O AI(OH)3+NaOH
AlO2-+2H2O Al(OH)3+OH-
2、偏铝酸钠溶液滴入少量盐酸:NaAlO2+HCl+H2O Al(OH)3↓+NaCl
AlO2-+H++H2O Al(OH)3↓
3、向偏铝酸钠溶液加入足量盐酸:NaAlO2+4HCl NaCl+AlCl3+2H2O
AlO2-+4H+Al3++2H2O
4、向偏铝酸钠溶液通入少量二氧化碳气体:2NaAlO+CO+3H O2Al(OH)↓+Na CO
5、向偏铝酸钠溶液通入足量二氧化碳气体:NaAlO2+CO2+2H2O Al(OH)3+NaHCO3
AlO2-+CO2+2H2O Al(OH)3+HCO3-
6、向偏铝酸钠溶液中加入硫酸铝溶液:
Al2(SO4)3+6NaAlO2+12H2O3Na2SO4+8Al(OH)3↓
Al3++AlO2-+6H2O4Al(OH)3↓
7、向偏铝酸钠溶液中加入氯化铵溶液:NaAlO2+NH4Cl+H2O Al(OH)3↓+NaCl+NH3↑
AlO2-+NH4++H2O Al(OH)3↓+NH3↑
8、向偏铝酸钠溶液中加入氯化铁溶液:
3NaAlO2+FeCl3+6H2O3Al(OH)3↓+Fe(OH)3↓+3NaCl
3AlO2-+Fe3++6H2O3Al(OH)3↓+Fe(OH)3↓。