人教版高中物理选修3-3第八章习题课
- 格式:docx
- 大小:54.95 KB
- 文档页数:8

3理想气体的状态方程记一记理想气体的状态方程知识体系一个模型——理想气体一个方程——理想气体的状态方程三个特例——p1V1T1=p2V2T2⎩⎪⎨⎪⎧T1=T2时,p1V1=p2V2V1=V2时,p1T1=p2T2p1=p2时,V1T1=V2T2辨一辨1.理想气体也不能严格地遵守气体实验定律.(×)2.实际气体在温度不太低、压强不太大的情况下,可看成理想气体.(√)3.一定质量的理想气体,当压强不变而温度由100 ℃上升到200 ℃时,其体积增大为原来的2倍.(×)4.气体由状态1变到状态2时,一定满足方程p1V1T1=p2V2T2.(×)5.一定质量的理想气体体积增大到原来的4倍,可能是因为压强减半且热力学温度加倍.(√)想一想什么样的气体才是理想气体?理想气体的特点是什么?提示:在任何温度、任何压强下都严格遵从实验定律的气体;特点:①严格遵守气体实验定律及理想气体状态方程,是一种理想化模型.②理想气体分子本身的大小与分子间的距离相比可忽略不计,分子不占空间,可视为质点.③理想气体分子除碰撞外,无相互作用的引力和斥力.④理想气体分子无分子势能的变化,内能等于所有分子热运动的动能之和,只和温度有关.思考感悟:练一练=1.有一定质量的理想气体,如果要使它的密度减小,可能的办法是( )A .保持气体体积一定,升高温度B .保持气体的压强和温度一定,增大体积C .保持气体的温度一定,增大压强D .保持气体的压强一定,升高温度解析:由ρ=m /V 可知,ρ减小,V 增大,又由pV T =C 可知A 、B 、C 三项错,D 项对.答案:D2.对于一定质量的理想气体,下列状态变化中可能的实现是( )A .使气体体积增加而同时温度降低B .使气体温度升高,体积不变、压强减小C .使气体温度不变,而压强、体积同时增大D .使气体温度升高,压强减小、体积减小解析:由理想气体状态方程pV T =恒量得A 项中只要压强减小就有可能,故A 项正确;而B 项中体积不变,温度与压强应同时变大或同时变小,故B 项错;C 项中温度不变,压强与体积成反比,故不能同时增大,故C 项错;D 项中温度升高,压强减小,体积减小,导致pV T 减小,故D 项错误.答案:A3.一定质量的理想气体,经历一膨胀过程,这一过程可以用图上的直线ABC 来表示,在A 、B 、C 三个状态上,气体的温度T A 、T B 、T C 相比较,大小关系为( )A .TB =T A =T CB .T A >T B >T CC .T B >T A =T CD .T B <T A =T C解析:由图中各状态的压强和体积的值可知:p A · V A =p C ·V C <p B ·V B ,因为pV T =恒量,可知T A =T C <T B .答案:C4.如图所示,1、2、3为p -V 图中一定量理想气体的三种状态,该理想气体由状态1经过程1→3→2到达状态2.试利用气体实验定律证明:p 1V 1T 1=p 2V 2T 2. 证明:由题图可知1→3是气体等压过程,据盖—吕萨克定律有:V 1T 1=V 2T3→2是等容过程,据查理定律有:p 1T =p 2T 2联立解得p 1V 1T 1=p 2V 2T 2.要点一对理想气体的理解1.(多选)关于理想气体,下列说法中正确的是()A.严格遵守玻意耳定律、盖—吕萨克定律和查理定律的气体称为理想气体B.理想气体客观上是不存在的,它只是实际气体在一定程度上的近似C.和质点的概念一样,理想气体是一种理想化的模型D.一定质量的理想气体,内能增大,其温度可能不变解析:理想气体是一种理想化模型,是对实际气体的科学抽象;温度不太低、压强不太大的情况下可以把实际气体近似视为理想气体;理想气体在任何温度、任何压强下都遵从气体实验定律,A、B、C三项正确;理想气体的内能只与温度有关,温度升高,内能增大,温度降低,内能减小,D项错误.答案:ABC2.(多选)关于理想气体,下列说法正确的是()A.温度极低的气体也是理想气体B.压强极大的气体也遵从气体实验定律C.理想气体是对实际气体的抽象化模型D.理想气体实际并不存在解析:气体实验定律是在压强不太大、温度不太低的情况下得出的,温度极低、压强极大的气体在微观上分子间距离变小,趋向于液体,故答案为C、D两项.答案:CD要点二对理想气体状态方程的理解和应用3.(多选)一定质量的理想气体,初始状态为p、V、T,经过一系列状态变化后,压强仍为p,则下列过程中可以实现的是() A.先等温膨胀,再等容降温B.先等温压缩,再等容降温C.先等容升温,再等温压缩D.先等容降温,再等温压缩解析:根据理想气体状态方程pVT=C,若经过等温膨胀,则T不变,V增加,p减小,再等容降温,则V不变,T降低,p减小,最后压强p肯定不是原来值,A项错,同理可以确定C项也错,正确为B、D两项.答案:BD4.一定质量的气体,从初态(p0、V0、T0)先经等压变化使温度上升到32T0,再经等容变化使压强减小到12p0,则气体最后状态为()A.12p0、V0、32T0 B.12p0、32V0、34T0C.12p0、V0、34T0 D.12p0、32V0、T0解析:在等压过程中,V∝T,有V0T0=V33T02,V3=32V0,再经过一个等容过程,有:p032T0=p02T3,T3=34T0,所以B项正确.答案:B5.如图所示,一定质量的空气被水银封闭在静置于竖直平面的U形玻璃管内,右管上端开口且足够长,右管内水银面比左管内水银面高h,能使h变小的原因是()A.环境温度升高B.大气压强升高C.沿管壁向右管内加水银D.U形玻璃管自由下落解析:对于左端封闭气体,温度升高,由理想气体状态方程可知:气体发生膨胀,h增大,故A项错.大气压升高,气体压强将增大,体积减小,h减小,故B项对.向右管加水银,气体压强增大,内、外压强差增大,h将增大,所以C项错.当管自由下落时,水银不再产生压强,气体压强减小,h变大,故D项错.答案:B6.一水银气压计中混进了空气,因而在27 ℃、外界大气压为758 mmHg时,这个水银气压计的读数为738 mmHg,此时管中水银面距管顶80 mm.当温度降至-3 ℃时,这个气压计的读数为743 mmHg,求此时的实际大气压值为多少?解析:画出该题初、末状态的示意图分别写出被封闭气体的初、末状态的状态参量p1=758 mmHg-738 mmHg=20 mmHgV1=(80 mm)·S(S是管的横截面积)T1=(273+27) K=300 Kp2=p-743 mmHgV2=(738+80) mm·S-743(mm)·S=75(mm)·ST2=(273-3)K=270 K将数据代入理想气体状态方程p1V1 T1=p2V2 T2解得p=762.2 mmHg.答案:762.2 mmHg要点三理想气体变化的图象7.在下图中,不能反映理想气体经历了等温变化→等容变化→等压变化,又回到原来状态的图是()解析:根据p -V ,p -T 、V -T 图象的意义可以判断,其中D 项显示的理想气体经历了等温变化→等压变化→等容变化,与题意不符.答案:D8.图中A 、B 两点代表一定质量理想气体的两个不同的状态,状态A 的温度为T A ,状态B 的温度为T B ;由图可知( )A. T B =2T AB. T B =4T AC. T B =6T AD. T B =8T A 解析:对于A 、B 两个状态应用理想气体状态方程p A V A T A =p B V B T B可得:T B T A =p B V B p A V A =3×42×1=6,即T B =6T A ,C 项正确. 答案:C基础达标1.关于一定质量的理想气体发生状态变化时,其状态参量p 、V 、T 的变化情况不可能的是( )A .p 、V 、T 都减小B .V 减小,p 和T 增大C.p和V增大,T减小D.p增大,V和T减小解析:由理想气体状态方程pVT=C可知,p和V增大,则pV增大,T应增大.C项不可能.答案:C2.(多选)理想气体的状态方程可以写成pVT=C,对于常量C,下列说法正确的是()A.对质量相同的任何气体都相同B.对质量相同的同种气体都相同C.对质量不同的不同气体可能相同D.对质量不同的不同气体一定不同解析:理想气体的状态方程的适用条件就是一定质量的理想气体,说明常量C仅与气体的种类和质量有关,实际上也就是只与气体的物质的量有关.对质量相同的同种气体当然常量是相同的,而对质量不同的不同气体,只要物质的量是相同的,那么常量C也是可以相同的.答案:BC3.(多选)对一定质量的理想气体,下列说法正确的是() A.体积不变,压强增大时,气体分子的平均动能一定增大B.温度不变,压强减小时,气体的密度一定减小C.压强不变,温度降低时,气体的密度一定减小D.温度升高,压强和体积可能都不变解析:由pVT=C(常量)可知,V不变、p增大时T增大,故A项正确;T增大时,p与V至少有一个要发生变化,故D错误;把V=mρ代入pVT=C得pmρT=C,由此式可知,T不变时,ρ随p的减小而减小,故B项正确;p不变时,ρ随T的减小而增大,故C 项错误.答案:AB4.(多选)关于理想气体的状态变化,下列说法中正确的是()A.一定质量的理想气体,当压强不变而温度由100 ℃上升到200 ℃时,其体积增大为原来的2倍B .一定质量的理想气体由状态1变到状态2时,一定满足方程p 1V 1T 1=p 2V 2T 2C .一定质量的理想气体体积增大到原来的4倍,可能是压强减半,热力学温度加倍D .一定质量的理想气体压强增大到原来的4倍,可能是体积加倍,热力学温度减半解析:理想气体状态方程p 1V 1T 1=p 2V 2T 2中的温度是热力学温度,不是摄氏温度,A 项错误,B 项正确;由理想气体状态方程及各量的比例关系即可判断C 项正确,D 项错误.答案:BC5.光滑绝热的轻质活塞把密封的圆筒容器分成A 、B 两部分,这两部分充有温度相同的气体,平衡时V A :V B =1:2,现将A 中气体温度加热到127 ℃,B 中气体温度降低到27 ℃,待重新平衡后,这两部分气体体积的比V A ′:V B ′为( )A .1:1B .2:3C .3:4D .2:1解析:对A 部分气体有:p A V A T A =p A ′V ′A T A ′① 对B 部分气体有:p B V B T B =p B ′V B ′T B ′② 因为p A =p B ,p A ′=p B ′,T A =T B ,所以由①②得V A V B =V A ′T B ′V B ′T A ′,所以V A ′V B ′=V A T A ′V B T B ′=1×4002×300=23答案:B6.如图所示,内壁光滑的汽缸和活塞都是绝热的,缸内被封闭的理想气体原来体积为V ,压强为p ,若用力将活塞向右压,使封闭的气体体积变为V 2,缸内被封闭气体的( )A .压强等于2pB .压强大于2pC .压强小于2pD .分子势能增大了解析:汽缸绝热,压缩气体,其温度必然升高,由理想气体状态方程pV T =C (恒量)可知,T 增大,体积变为V 2,则压强大于2p ,故B 项正确,A 、C 两项错,理想气体分子无势能的变化,D 项错.答案:B7.(多选)如图所示,一定质量的理想气体,从图示A 状态开始,经历了B 、C 状态,最后到D 状态,下列判断正确的是( )A .A →B 温度升高,压强不变B .B →C 体积不变,压强变大C .B →C 体积不变,压强不变D .C →D 体积变小,压强变大解析:由图象可知,在A →B 的过程中,气体温度升高、体积变大,且体积与温度成正比,由pV T =C ,气体压强不变,是等压过程,故A 项正确;由图象可知,在B →C 是等容过程,体积不变,而热力学温度降低,由pV T =C 可知,压强p 减小,故B 、C 两项错误;由图象可知,在C →D 是等温过程,体积减小,由pV T =C可知,压强p 增大,故D 项正确.答案:AD8.一气泡从30 m 深的海底升到海面,设水底温度是4 ℃,水面温度是15 ℃,那么气泡在海面的体积约是水底时的( )A .3倍B .4倍C .5倍D .12倍解析:根据理想气体状态方程:p 1V 1T 1=p 2V 2T 2,知V 2V 1=p 1T 2p 2T 1,其中T 1=(273+4) K =277 K ,T 2=(273+15) K =288 K ,故T 2T 1≈1,而p 2=p 0≈10ρ水 g ,p 1=p 0+p ≈40 ρ水 g ,即p 1p 2≈4,故V 2V 1≈4.故选B 项.答案:B9.(多选)如图所示,用活塞把一定质量的理想气体封闭在导热汽缸中,用水平外力F 作用于活塞杆,使活塞缓慢向右移动,由状态①变化到状态②.如果环境保持恒温,分别用p 、V 、T 表示该理想气体的压强、体积、温度.气体从状态①变化到状态②,此过程可用下图中哪几个图象表示( )解析:由题意知,由状态①到状态②过程中,温度不变,体积增大,根据pV T =C 可知压强将减小.对A 项图象进行分析,p -V图象是双曲线即等温线,且由状态①到状态②体积增大,压强减小,故A 项正确;对B 项图象进行分析,p -V 图象是直线,温度会发生变化,故B 项错误;对C 项图象进行分析,可知温度不变,但体积增大,故C 项错误;对D 项图象进行分析,可知温度不变,压强减小,D 项正确.答案:AD10.如图所示为伽利略设计的一种测温装置示意图,玻璃管的上端与导热良好的玻璃泡连通,下端插入水中,玻璃泡中封闭有一定量的空气.若玻璃管中水柱上升,则外界大气的变化可能是( )A .温度降低,压强增大B .温度升高,压强不变C .温度升高,压强减小D .温度不变,压强减小解析:由题意可知,封闭空气温度与大气温度相同,封闭空气体积随水柱的上升而减小,将封闭空气近似看作理想气体,根据理想气体状态方程pV T =常量,若温度降低,体积减小,则压强可能增大、不变或减小,A 项正确;若温度升高,体积减小,则压强一定增大,B 、C 两项错误;若温度不变,体积减小,则压强一定增大,D 项错误.答案:A11.某不封闭的房间容积为20 m 3,在温度为7 ℃、大气压强为9.8×104 Pa 时,室内空气质量为25 kg.当温度升高到27 ℃、大气压强为1.0×105 Pa 时,室内空气的质量是多少?(T =273 K +t )解析:假设气体质量不变,末态体积为V 2,由理想气体状态方程有:p 1V 1T 1=p 2V 2T 2, 解得V 2=p 1V 1T 2p 2T 1=9.8×104×20×3001.0×105×280=21.0 m 3. 因为V 2>V 1,即有部分气体从房间内流出,设剩余气体质量为m 2,由比例关系有:V 1V 2=m 2m 1,m 2=m 1V 1V 2=23.8 kg.答案:23.8 kg12.图甲为1 mol 氢气的状态变化过程的V -T 图象,已知状态A 的参量为p A =1 atm ,T A =273 K ,V A =22.4×10-3 m 3,取1 atm=105 Pa ,在图乙中画出与甲图对应的状态变化过程的p -V 图,写出计算过程并标明A 、B 、C 的位置.解析:据题意,从状态A 变化到状态C 的过程中,由理想气体状态方程可得:p A V A T A =p C V C T C ,p C =1 atm ,从A 变化到B 的过程中有:p A V A T A=p B V B T B,p B =2 atm. A 、B 、C 的位置如图所示.答案:见解析13.[2019·潍坊高二检测]内燃机汽缸里的混合气体,在吸气冲程结束瞬间,温度为50 ℃,压强为1.0×105 Pa ,体积为0.93 L .在压缩冲程中,把气体的体积压缩为0.155 L 时,气体的压强增大到1.2×106 Pa.这时混合气体的温度升高到多少摄氏度?解析:气体初状态的状态参量为p 1=1.0×105 Pa ,V 1=0.93 L ,T 1=(50+273) K =323 K.气体末状态的状态参量为p 2=1.2×106 Pa ,V 2=0.155 L ,T 2为未知量.由p 1V 1T 1=p 2V 2T 2可求得T 2=p 2V 2p 1V 1T 1, 将已知量代入上式,得T 2=1.2×106×0.1551.0×105×0.93×323 K =646 K , 所以混合气体的温度t =(646-273) ℃=373 ℃.答案:373 ℃能力达标14.[2019·长春市质检]如图所示,绝热气缸开口向上放置在水平地面上,一质量m =10 kg,横截面积S=50 cm2的活塞可沿气缸无摩擦滑动;被封闭的理想气体温度t=27 ℃时,气柱长L=22.4 cm.已知大气压强为标准大气压p0=1.0×105Pa,标准状况下(压强为一个标准大气压,温度为0 ℃)理想气体的摩尔体积为22.4 L,阿伏加德罗常数N A=6.0×1023mol-1,g=10 m/s2.求:(计算结果保留两位有效数字)(1)被封闭理想气体的压强;(2)被封闭气体内所含分子的数目.解析:(1)被封闭理想气体的压强为p=p0+mg Sp=1.2×105 Pa(2)由p0V0T0=pVT得标准状况下的体积为V0=pVT0 p0T被封闭气体内所含分子的数目为N=N A V0 V m解得N=3.3×1022个答案:(1)1.2×105 Pa(2)3.3×1022。

§气体之单元测试(一)制作:_____________审核:______________班级: .组名: . 姓名: .时间:年月日【学习指导】:1兴趣、好奇心、不断尝试、自主性、积极性2动脑思考,头脑清晰3狠抓落实,而且要有具体的落实措施4听懂是骗人的,看懂是骗人的,做出来才是自己的5独立、限时、满分作答6不仅要去学习,而且要学出效果,还要提高效率。
7保证效果就要每个点都要达标。
达标的标准是能够“独立做(说、写)出来”,不达标你的努力就体现不出来8该记的记,该理解的理解,该练习的练习,该总结的总结,勿懈怠!9费曼学习法:确定一个学习的知识点;假设你在教授别人该知识点;遇到卡壳时回顾相关知识点;简化你的语言,达到通俗易懂的程度。
该法尤其适合概念、定义、定理、定律等的理解和记忆。
10明确在学习什么东西,对其中的概念、定律等要追根溯源,弄清来龙去脉才能理解透彻、应用灵活11总结:11.1每题总结:每做完一道题都要总结该题涉及的知识点和方法11.2题型总结:先会后熟,一种题型先模仿、思考,弄懂后,总结出这类题型的出现特征、解题方法,然后再多做几道同类型的,直到遇到这种题型就条件反射得知道怎么做11.3小节总结:总结该小节的知识结构、常见题型及做法11.4章节总结:总结该章节的知识结构、常见题型及做法12多做多思,孰能生巧,熟到条件反射,这样一是能见到更多的出题方式,二是能提高做题速度13根据遗忘曲线,进行循环复习14步骤规范,书写整洁,条理清晰15步骤一步一步的写,最好不要把几个公式合成一个式子来写,因为有步骤分16错题本的建立:在每次发的试卷资料的右上角写上日期,同一科目的试卷按日期顺序放好。
在做错的题号上画叉号,在不会做的题号上画问号,以后就是一本很好的错题集。
其他资料亦如此处理。
这种方式简单实用。
同时,当你积攒到一定程度,看到自己做过的厚厚的资料,难道不会由衷的产生一种成就感么?!【一分钟德育】(将下面的内容对照自身,理论要落地)“六先六后”学习法为什么有些同学天天埋头苦读,考试成绩却不理想?为什么有些同学要玩得尽兴兴,学习成绩却很拔尖?一个很重要的原因就是学习方法的正确与否。

高中物理选修3-3第八章经典习题1.如图,由U形管和细管连接的玻璃泡A、B和C浸泡在温度均为0°C的水槽中,B的容积是A的3倍。
阀门S将A和B两部分隔开。
A内为真空,B和C内都充有气体。
U形管内左边水银柱比右边的低60mm。
打开阀门S,整个系统稳定后,U形管内左右水银柱高度相等。
假设U形管和细管中的气体体积远小于玻璃泡的容积。
(1)求玻璃泡C中气体的压强(以mmHg为单位);(2)将右侧水槽的水从0°C加热到一定温度时,U形管内左右水银柱高度差又为60mm,求加热后右侧水槽的水温。
2.内径均匀的L形直角细玻璃管,一端封闭,一端开口竖直向上,用水银柱将一定质量空气封存在封闭端内,空气柱长4 cm,水银柱高58 cm,进入封闭端长2 cm,如图所示,温度是87 ℃,大气压强为75 cmHg,求:(1)在图示位置空气柱的压强p1是多少?(2)在图示位置,要使空气柱的长度变为3 cm,温度必须降低到多少度?3.如图中,圆筒形容器内的弹簧下端挂一个不计重力的活塞,活塞与筒壁间的摩擦不计,活塞上面为真空,当弹簧自然长度时,活塞刚好能触及容器底部,如果在活塞下面充入t1=27 ℃的一定质量某种气体,则活塞下面气体的长度h=30cm,问温度升高到t2=90 ℃时气柱的长度为多少?4.如图所示,重G1的活塞a和重G2的活塞b,将长为L的气室分成体积比为1﹕2的A、B 两部分,温度是127℃,系统处于平衡状态,当温度缓慢地降到27℃时系统达到新的平衡,求活塞a、b移动的距离。
5.一个质量可不计的活塞将一定质量的理想气体封闭在上端开口的直立筒形气缸内,活塞上堆放着铁砂,如图所示,最初活塞搁置在气缸内壁的卡环上,气体柱的高度为H0,压强等于大气压强P0,现对气体缓慢加热,当气体温度升高了△T=60K时,活塞(及铁砂)开始离开卡环而上升,继续加热直到气柱高度为H1=1.5H0.此后在维持温度不变的条件下逐渐取走铁砂,直到铁砂全部取走时,气柱高度变为H2=1.8H0.求此时气体的温度.(不计活塞与气缸之间的摩擦)6.一气缸竖直放置,内截面积S=50cm2,质量m=10kg的活塞将一定质量的气体封闭在缸内,气体柱长h0=15cm,活塞用销子销住,缸内气体的压强P=2.4×105Pa,温度177℃。

第4节气体热现象的微观意义1.气体分子的运动特点:(1)分子间的距离较大,除碰撞外不受力的作用而做匀速直线运动;(2)分子间的碰撞十分频繁,分子运动杂乱无章,无规则。
2.气体分子的速率都呈“中间多,两头少”的分布。
3.温度越高,气体分子热运动越激烈。
4.从微观角度来看:气体压强是大量气体分子对容器的碰撞而产生的,其大小跟两个因素有关:一个是气体分子的平均动能,二是分子的密集程度。
一、随机性与统计规律、气体分子运动的特点1.随机性与统计规律(1)必然事件:在一定条件下必然出现的事件。
(2)不可能事件:在一定条件下不可能出现的事件。
(3)随机事件:在一定条件下可能出现,也可能不出现的事件。
(4)统计规律:大量随机事件整体表现出来的规律。
2.气体分子运动的特点气体分子间距离比较大,分子间的作用力很弱,除相互碰撞或跟器壁碰撞外,可理想性以认为分子不受力而做匀速直线运动,因而气体能充满它能达到的整个空间分子之间频繁地发生碰撞,使每个分子的速度大小和方向频繁地改变,分子的运现实性动杂乱无章(1)分子的运动杂乱无章,在某一时刻,向着任何一个方向运动的分子都有,而且规律性向着各个方向运动的气体分子数目都相等(2)气体分子的速率各不相同,但遵守速率分布规律,即出现“中间多、两头少”的分布规律二、气体温度和气体压强的微观意义1.气体温度的微观意义(1)温度越高,分子的热运动越剧烈。
(2)理想气体的热力学温度T与分子的平均动能E k成正比,即:T=a E k(式中a是比例常数),因此可以说,温度是分子平均动能的标志。
2.气体压强的微观意义(1)气体的压强是大量气体分子频繁地碰撞容器而产生的。
(2)影响气体压强的两个微观因素:一个是气体分子的平均动能,一个是分子的密集程度。
三、对气体实验定律的微观解释玻意耳定律一定质量的气体,温度保持不变时,分子的平均动能是一定的。
在这种情况下,体积减小时,分子的密集程度增大,气体的压强就增大,反之,压强减小查理定律一定质量的气体,体积保持不变时,分子的密集程度保持不变。
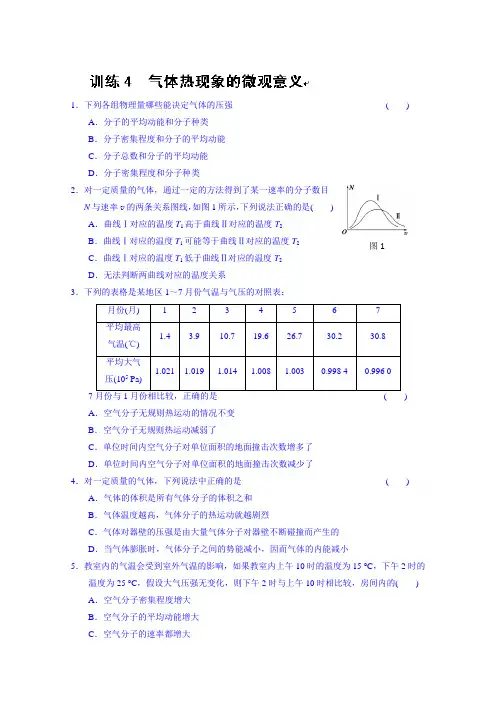
1.下列各组物理量哪些能决定气体的压强() A.分子的平均动能和分子种类B.分子密集程度和分子的平均动能C.分子总数和分子的平均动能D.分子密集程度和分子种类N与速率v的两条关系图线,如图1所示,下列说法正确的是()A.曲线Ⅰ对应的温度T1高于曲线Ⅱ对应的温度T2B.曲线Ⅰ对应的温度T1可能等于曲线Ⅱ对应的温度T2图1 C.曲线Ⅰ对应的温度T1低于曲线Ⅱ对应的温度T2D.无法判断两曲线对应的温度关系3.下列的表格是某地区1~7月份气温与气压的对照表:7)A.空气分子无规则热运动的情况不变B.空气分子无规则热运动减弱了C.单位时间内空气分子对单位面积的地面撞击次数增多了D.单位时间内空气分子对单位面积的地面撞击次数减少了4.对一定质量的气体,下列说法中正确的是()A.气体的体积是所有气体分子的体积之和B.气体温度越高,气体分子的热运动就越剧烈C.气体对器壁的压强是由大量气体分子对器壁不断碰撞而产生的D.当气体膨胀时,气体分子之间的势能减小,因而气体的内能减小5.教室内的气温会受到室外气温的影响,如果教室内上午10时的温度为15 °C,下午2时的温度为25 °C,假设大气压强无变化,则下午2时与上午10时相比较,房间内的()A.空气分子密集程度增大B.空气分子的平均动能增大C.空气分子的速率都增大D.空气质量增大6.一定质量的气体,下列叙述正确的是() A.如果体积减小,气体分子在单位时间内对单位面积器壁的碰撞次数一定增多B.如果压强增大,气体分子在单位时间内对单位面积器壁的碰撞次数一定增多C.如果温度升高,气体分子在单位时间内对单位面积器壁的碰撞次数一定增多D.如果分子密度增大,气体分子在单位时间内对单位面积器壁的碰撞次数一定增多7.如图2所示,一定质量的理想气体由状态A沿平行于纵轴的直线变化到状态B,则它的状态变化过程是()A.气体的温度不变B.气体的内能增加C.气体分子的平均速率减少D.气体分子在单位时间内与器壁在单位面积上碰撞的次数不变8.一定质量的理想气体,在压强不变的条件下,温度升高,体积增大,从分子动理论的观点来分析,正确的是()A.此过程中分子的平均速率不变,所以压强保持不变B.此过程中每个气体分子碰撞器壁的平均冲击力不变,所以压强保持不变C.此过程中单位时间内气体分子对单位面积器壁的碰撞次数不变,所以压强保持不变D.以上说法都不对9.一定质量的某种理想气体,当体积减小为原来的一半时,其热力学温度变为原来的2倍时,它的压强变为原来的多少?试从压强和温度的微观意义进行解释.10.一定质量的理想气体由状态A经状态B变成状态C,其中A→B过程为等压变化,B→C 过程为等容变化.已知V A=0.3 m3,T A=T C=300 K,T B=400 K.(1)求气体在状态B时的体积.(2)说明B→C过程压强变化的微观原因.答案1.B2.C3.D4.BC5.B6.B7.B8.D9.4倍解释见解析解析由理想气体状态方程pVT=恒量得,压强变为原来的4倍,从微观角度看,气体压强的大小跟两个因素有关:一个是气体分子的平均动能,一个是气体分子的密集程度,当体积减小为原来的一半时,气体分子的密集程度变为原来的两倍,这时气体的压强相应地变为原来的两倍,这时还要从另外一个因素考虑,即增加气体分子的平均动能,而图2气体分子的平均动能是由温度来决定的,气体的热力学温度变为原来的2倍,这时压强便在这两个因素(体积减小——分子密度程度增大,温度升高——分子的平均动能增大)的共同作用下变为原来的4倍.10.(1)0.4 m3(2)见解析解析(2)B→C气体体积不变,分子数密度不变,温度降低,分子平均动能减小,压强减小.。

一、基础练1.为了控制温室效应,各国科学家都提出了不少方法和设想.有人根据液态CO2密度大于海水密度的事实,设想将CO2液化后,送入深海海底,以减小大气中CO2的浓度.为使CO2液化,最有效的措施是( )A.减压、升温 B.增压、升温C.减压、降温 D.增压、降温2.如图1所示甲、乙为一定质量的某种气体的等容或等压变化图象,关于这两个图象的正确说法是( )图1A.甲是等压线,乙是等容线B.乙图中p-t线与t轴交点对应的温度是-273.15℃,而甲图中V -t线与t轴的交点不一定是-273.15℃.C.由乙图可知,一定质量的气体,在任何情况下都是p与t成直线关系D.乙图表明随温度每升高1℃,压强增加相同,但甲图随温度的升高压强不变3.向固定容器内充气,当气体压强为p ,温度为27℃时,气体的密度为ρ,当温度为327℃,气体压强为1.5p 时,气体的密度为( ) A .0.25ρ B .0.5ρ C .0.75ρ D .ρ 4.关于理想气体的状态变化,下列说法中正确的是( )A .一定质量的理想气体,当压强不变而温度由100℃上升到200℃时,其体积增大为原来的2倍B .气体由状态1变到状态2时,一定满足方程p 1V 1T 1=p 2V 2T 2C .一定质量的理想气体体积增大到原来的4倍,可能是压强减半,热力学温度加倍D .一定质量的理想气体压强增大到原来的4倍,可能是体积加倍,热力学温度减半 二、提升练5.一定质量的理想气体,处在某一状态,经下列哪个过程后会回到原来的温度( )A .先保持压强不变而使它的体积膨胀,接着保持体积不变而减小压强B .先保持压强不变而使它的体积减小,接着保持体积不变而减小压强C .先保持体积不变而增大压强,接着保持压强不变而使它的体积膨胀D .先保持体积不变而减小压强,接着保持压强不变而使它的体积膨胀 6.图2将一根质量可忽略的一端封闭的塑料管子插入液体中,在力F的作用下保持平衡,如图2所示的H值大小与下列哪个量无关( )A.管子的半径B.大气压强C.液体的密度D.力F7.一绝热隔板将一绝热长方形容器隔成两部分,两边分别充满气体,隔板可无摩擦移动.开始时,左边的温度为0℃,右边的温度为20℃,当左边的气体加热到20℃,右边的气体加热到40℃时,则达到平衡状态时隔板的最终位置( )A.保持不动 B.在初始位置右侧C.在初始位置左侧 D.决定于加热过程8.图3如图3所示,一端封闭的粗细均匀的玻璃管,开口向上竖直放置,管中有两段水银柱封闭了两段空气柱,开始时V1=2V2,现将玻璃管缓慢地均匀加热,则下述说法中正确的是( )A.加热过程中,始终保持V1′=2V2′B.加热后V1′>2V2′C.加热后V1′<2V2′D.条件不足,无法确定题号12345678答案。

高中物理学习材料(灿若寒星**整理制作)1.查理定律(等容变化):一定质量的某种气体,在体积不变的情况下,________与________成正比.表达式p =________或p 1T 1=________或p 1p 2=________,此定律的适用条件为:气体的________不变,气体的________不变,请用p —T 图和p —t 图表达等容变化:___________. 2.盖—吕萨克定律(等压变化):一定质量的某种气体,在压强不变的情况下,其________与________________成正比.表达式V =________或V 1T 1=____________或V 1V 2=__________,此定律的适用条件为:气体________不变,气体________不变.请用V —T 图和V —t 图表达等压变化: ____________________________.3.对于一定质量的气体,在体积不变时,压强增大到原来的两倍,则气体温度的变化情况是( )A .气体的摄氏温度升高到原来的两倍B .气体的热力学温度升高到原来的两倍C .气体的摄氏温度降为原来的一半D .气体的热力学温度降为原来的一半4.一定质量的气体,压强保持不变,下列过程可以实现的是( ) A .温度升高,体积增大 B .温度不变,体积增大 C .温度升高,体积减小 D .温度不变,体积减小 5.图1如图1所示,直线a 和b 分别表示同一气体在不同体积V 1和V 2下的等容变化图线,试比较V 1和V 2的关系.6.图2如图2所示,直线a和b分别表示同一气体在压强p1和p2下做等压变化的图象.试比较p1和p2的大小.【概念规律练】知识点一等容变化规律1.电灯泡内充有氮、氩混合气体,如果要使电灯泡内的混合气体在500℃时的压强不超过一个大气压,则在20℃的室温下充气,电灯泡内气体的压强至多能充到多少?2.一定质量的气体,在体积不变的条件下,温度由0℃升高到10℃时,其压强的增量为Δp1,当它由100℃升高到110℃时,所增压强为Δp2,则Δp1与Δp2之比是()A.10∶1 B.373∶273C.1∶1 D.383∶283知识点二等压变化规律3.图3如图3所示,一端开口的钢制圆筒,在开口端上面放一活塞.活塞与筒壁间的摩擦及活塞的重力不计,现将其开口端向下,竖直缓慢地放入7℃的水中,在筒底与水面相平时,恰好静止在水中,这时筒内气柱长为14 cm,当水温升高到27℃时,钢筒露出水面的高度为多少?(筒的厚度不计)4.一定质量的理想气体,在压强不变的情况下,温度由5℃升高到10℃,体积的增量为ΔV1;温度由10℃升高到15℃,体积的增量为ΔV2,则()A.ΔV1=ΔV2B.ΔV1>ΔV2C.ΔV1<ΔV2D.无法确定知识点三图象问题5.图4如图4所示是一定质量的理想气体的三种升温过程,那么,以下四种解释中,正确的是() A.a→d的过程气体体积增加B.b→d的过程气体体积不变C.c→d的过程气体体积增加D.a→d的过程气体体积减小6.图5一定质量的某种气体自状态A经状态C变化到状态B,这一过程在V-T图上表示如图5所示,则()A.在过程AC中,气体的压强不断变大B.在过程CB中,气体的压强不断变小C.在状态A中,气体的压强最大D.在状态B中,气体的压强最大【方法技巧练】用控制变量法分析液柱移动问题7.图6两端封闭的内径均匀的直玻璃管,水平放置,如图6所示,V左<V右,温度均为20℃,现将右端空气柱降为0℃,左端空气柱降为10℃,则管中水银柱将()A.不动B.向左移动C.向右移动D.无法确定是否移动8.图7如图7所示,两端封闭、粗细均匀、竖直放置的玻璃管内有一段长为h的水银柱,将管内气体分为两部分.已知l2=2l1,若使两部分气体同时升高相同的温度,管内水银柱将如何移动?(设原来温度相同)1.对于一定质量的气体,以下说法正确的是()A.气体做等容变化时,气体的压强和温度成正比B.气体做等容变化时,温度升高1℃,增加的压强是原来压强的1/273C.气体做等容变化时,气体压强的变化量与温度的变化量成正比D.由查理定律可知,等容变化中,气体温度从t1升高到t2时,气体压强由p1增加到p2,且p2=p1[1+(t2-t1)/273]2.一定质量的气体,在体积不变时,温度由50℃加热到100℃,气体的压强变化情况是() A.气体压强是原来的2倍B.气体压强比原来增加了50273 C.气体压强是原来的3倍D.气体压强比原来增加了50 3233.图8如图8所示是一定质量的理想气体的p-t图象,在气体由状态A变化到B的过程中,其体积()A.一定不变B.一定减小C.一定增大D.不能判定怎样变化4.图9一定质量的气体做等压变化时,其V-t图象如图9所示,若保持气体质量不变,而改变气体的压强,再让气体做等压变化,则其等压线与原来相比,下列可能正确的是() A.等压线与V轴之间夹角变小B.等压线与V轴之间夹角变大C.等压线与t轴交点的位置不变D.等压线与t轴交点的位置一定改变5.如图10所示是一定质量的气体从状态A经B到状态C再到状态A的p-T图象,由图可知()图10A.V A=V B B.V B>V CC.V B=V C D.V A>V C6.图11如图11所示是一定质量的理想气体的两种升温过程,对两种升温过程的正确解释是() A.a、b所在的图线都表示等容变化B.V a∶V b=3∶1C.p a∶p b=3∶1D.两种过程中均升高相同温度,气体压强的增量Δp a∶Δp b=3∶17.图12如图12所示,某同学用封有气体的玻璃管来测绝对零度,当容器水温是30刻度线时,空气柱长度为30 cm;当水温是90刻度线时,空气柱的长度是36 cm,则该同学测得的绝对零度相当于刻度线()A.-273 B.-270C.-268 D.-2718.图13如图13所示,两根粗细相同、两端开口的直玻璃管A和B,竖直插入同一水银槽中,各用一段水银柱封闭着一定质量同温度的空气,空气柱长度H1>H2,水银柱长度h1>h2,今使封闭气柱降低相同的温度(大气压保持不变),则两管中气柱上方水银柱的移动情况是() A.均向下移动,A管移动较多B.均向上移动,A管移动较多C.A管向上移动,B管向下移动D.无法判断9.图14如图14所示,A、B两容器容积相等,用粗细均匀的细玻璃管连接,两容器内装有不同气体,细管中央有一段水银柱,在两边气体作用下保持平衡时,A中气体的温度为0℃,B中气体温度为20℃,如果将它们的温度都降低10℃,则水银柱将()A.向A移动B.向B移动C.不动D.不能确定题号123456789答案10.图15如图15所示,圆柱形汽缸倒置在水平粗糙的地面上,汽缸内被活塞封闭着一定质量的空气.汽缸质量为M=10 kg,缸壁厚度不计,活塞质量m=5.0 kg,其圆面积S=50 cm2,与缸壁摩擦不计.在缸内气体温度为27℃时,活塞刚好与地面接触并对地面恰好无压力.现设法使缸内气体温度升高,问当缸内气体温度升高到多少摄氏度时,汽缸对地面恰好无压力?(大气压强p0=105 Pa,g取10 m/s2)11.一定质量的空气,27℃时的体积为1.0×10-2 m3,在压强不变的情况下,温度升高100℃时体积是多大?12.图16如图16所示为0.3 mol的某种气体的压强和温度关系的p-t图线.p0表示1个标准大气压,则在状态B时气体的体积为多少?13.图17如图17所示,一定质量的某种气体从状态A 经B 、C 、D 再回到A ,问AB 、BC 、CD 、DA 各是什么过程?已知气体在状态A 时体积为1 L ,求其在状态B 、C 、D 时的体积各为多少,并把此图改画为p -V 图.第2节 气体的等容变化和等压变化课前预习练1.压强p 热力学温度T CTp 2T 2 T 1T 2质量 体积 . 2.体积V 热力学温度T CT V 2T 2 T 1T 2质量 压强3.B [一定质量的气体体积不变时,压强与热力学温度成正比,即p 1T 1=p 2T 2,得T 2=p 2T 1p 1=2T 1,B 正确.]4.A [一定质量的气体,压强保持不变时,其热力学温度和体积成正比,则温度升高,体积增大;温度降低,体积减小;温度不变,体积也不发生变化,故A 正确.] 5.V 2<V 1解析 如题图所示,让气体从体积为V 1的某一状态开始做一等温变化,末状态体积为V 2.p 1<p 2,根据玻意耳定律可知V 1>V 2.直线斜率越大,表示体积越小.则在p —T 图中斜率大的V 小,故V 2<V 1. 6.p 1>p 2解析 让气体从压强为p 1的某一状态开始做一等容变化,末状态的压强为p 2.由图象可知T 1>T 2.根据查理定律p 1T 1=p 2T 2可得 p 1>p 2.所以直线斜率越大,表示变化过程的压强越小. 课堂探究练 1.0.38 atm解析 忽略灯泡容积的变化,气体为等容变化,找出气体的初、末状态,运用查理定律即可求解.灯泡内气体初、末状态的参量分别为气体在500 ℃,p 1=1 atm ,T 1=(273+500)K =773 K. 气体在20℃时,热力学温度为T 2=(273+20)K =293 K.由查理定律p 1T 1=p 2T 2得p 2=T 2T 1p 1=293773×1 atm ≈0.38 atm方法总结 一定质量的某种气体在体积不变的情况下,压强p 与热力学温度T 成正比,即pT=C (常数)或p 1T 1=p 2T 2.2.C [由查理定律得Δp =p T ΔT .一定质量的气体在体积不变的条件下ΔpΔT=恒量,温度由0℃升高到10℃和由100℃升高到110℃,ΔT =10 K 相同,故压强的增量Δp 1=Δp 2,C 项正确.] 方法总结 查理定律的重要推论:一定质量的气体,从初状态(p 、T )开始,发生一个等容变化过程,其压强的变化量Δp 与温度的变化量ΔT 间的关系为:Δp ΔT =p T 或Δp 1ΔT 1=Δp 2ΔT 2.3.1 cm解析 当水温升高时,筒内的气体发生的一个等压变化过程.设筒底露出水面的高度为h .当t 1=7℃即T 1=280 K 时,V 1=14 cm 长气柱;当T 2=300 K 时,V 2=(14 cm +h )长气柱.由等压过程的关系有V 2T 2=V 1T 1,即14+h 300=14280,解得h =1 cm ,也就是钢筒露出水面的高度为1 cm.方法总结 一定质量的某种气体,在压强不变的情况下,其体积V 与热力学温度T 成正比,即V T =C (常数)或V 1T 1=V 2T 2. 4.A [由盖—吕萨克定律V 1T 1=V 2T 2可得V 1T 1=ΔV ΔT ,即ΔV =ΔT T 1·V 1,所以ΔV 1=5278×V 1,ΔV 2=5283×V 2(V 1、V 2分别是气体在5℃和10℃时的体积),而V 1278=V 2283,所以ΔV 1=ΔV 2,A 正确.]方法总结 盖—吕萨克定律的重要推论:一定质量的气体从初状态(V 、T )开始发生等压变化,其体积的改变量ΔV 与温度的变化量ΔT 之间的关系是:ΔV ΔT =V T 或ΔV 1ΔT 1=ΔV 2ΔT 25.AB [p —T 图的等容线是延长线过原点的直线,且体积越大,直线的斜率越小.由此可见,a 状态对应体积最小,c 状态对应体积最大,所以选项A 、B 是正确的.]方法总结 一定质量的气体,等容过程中p —T 图线是过原点的倾斜直线,其斜率越大,体积越小.6.AD [气体在AC 变化过程中是等温变化,由pV =C 可知,体积减小,压强增大,故A 正确;在CB 变化过程中,气体的体积不发生变化,即为等容变化,由p /T =C 可知,温度升高,压强增大,故B 错误;综上所述,在ACB 过程中气体的压强始终增大,所以气体在状态B 时的压强最大,故C 错误,D 正确.]方法总结 在V -T 图象中,比较两个状态的压强大小,还可以用这两个状态到原点连线的斜率大小来判断,斜率越大,压强越小;斜率越小,压强越大.7.C [设降温后水银柱不动,则两段空气柱均为等容变化,初始状态左右压强相等,即p 左=p 右=p对左端Δp 左ΔT 左=p 左T 左,则Δp 左=ΔT 左T 左p 左=10293p同理右端Δp 右=20293p所以Δp 右>Δp 左即右侧压强降低得比左侧多,故液柱向右移动,选项C 正确.] 8.水银柱将向上移动解析 假设上、下两部分气体的体积不变,由查理定律得到Δp =ΔT 上Tp ,则对上端Δp 上=ΔTT 上p 上对下端Δp 下=ΔT 下T 下p 下其中ΔT 上=ΔT 下,T 上=T 下,p 上<p 下所以Δp 上<Δp 下,即下端压强升高得比上端多,故液柱向上移动.方法总结 此类问题研究三个状态参量(p 、V 、T )之间的相互关系,我们可以先保持其中一个物理量不变,从而确定其它两个量之间的相互关系,进而研究各量之间的关系.在液柱移动问题中,我们可以先假设两边气体体积不变,由ΔpΔT=C 分别研究两边压强与温度的关系,得到两边压强变化量Δp 的大小关系,从而确定液柱移动情况. 课后巩固练1.C [一定质量的气体做等容变化,气体的压强是跟热力学温度成正比,跟摄氏温度不是正比关系,A 错;根据Δp =ΔTTp 知,只有0℃时,B 选项才成交,故B 错误;气体压强的变化量,总是跟变化的温度成正比,无论是摄氏温度,还是热力学温度,C 正确;p 2p 1=t 2+273t 1+273,解得p 2=p 1(1+t 2-t 1273+t 1),由此可判断D 错误.]2.D [根据查理定律p 1T 1=p 2T 2得p 2=T 2T 1p 1=373323p 1,即压强变为原来的373323倍.p 2-p 1=(373323-1)p 1=50323p 1,气体压强比原来增加了50323,所以正确答案为D.]3.D [图中横坐标表示的是摄氏温度t .若BA 的延长线与t 轴相交在-273.15℃,则表示A 到B 过程中体积是不变的.但是,由图中无法做出这样的判定.所以,应选D. ]4.ABC [对于定质量的等压线,其V -t 图象的延长线一定过-273.15℃的点,故C 正确;由于题目中没有给定压强p 的变化情况,因此A 、B 都有可能,故选A 、B 、C.] 5.A6.ACD [在p -T 图象中,过原点的直线表示等容变化.图线斜率k =p T ∝1V;在T 相同的条件下,p ∝k =tan α,即p a ∶p b =tan 60°∶tan 30°=3∶1,V a ∶V b =1∶3,故选A 、C 、D.] 7.B [此情景为等压过程,有两个状态.t 1=30刻线,V 1=30S 和t 2=90刻线,V 2=36S设T =t 刻线+x ,则由盖—吕萨克定律得V 1t 1+x =V 2t 2+x 即30S 30刻线+x =36S90刻线+x解得x =270刻线,所以绝对零度相当于-270刻线,选B.]8.A [因为在温度降低过程中,被封闭气柱的压强恒等于大气压强与水银柱因自重而产生的压强之和,故封闭气柱均做等压变化.并由此推知,封闭气柱下端的水银面高度不变.根据盖—吕萨克定律的分比形式ΔV =ΔTT·V ,因A 、B 管中的封闭气柱,初温T 相同,温度降低量ΔT 也相同,且ΔT <0,所以ΔV <0,即A 、B 管中气柱的体积都减小;又因为H 1>H 2,A 管中气柱的体积较大,|ΔV 1|>|ΔV 2|,A 管中气柱减小得较多,故A 、B 两管气柱上方的水银柱均向下移动,且A 管中的水银柱下移得较多.本题的正确答案是选项A.]9.A [由Δp =ΔT T p ,可知Δp ∝1T,而T A =273.15 K ,T B =293.15 K ,所以A 部分气体压强减小的多,水银柱将向A 移动.]10.127℃解析 因为当温度T 1=(273+27) K =300 K 时,活塞对地面恰好无压力,列平衡方程:p 1S +mg =p 0S ,解得p 1=p 0-mg S =105 Pa -5×1050×10-4 Pa =0.9×105 Pa 若温度升高,气体压强增大,汽缸恰对地面无压力时,列平衡方程:p 2S =p 0S +Mg ,解得p 2=p 0+Mg S =105 Pa +10×1050×10-4 Pa =1.2×105 Pa 根据查理定律:p 1T 1=p 2T 2,即0.9×105300=1.2×105273+t解得t =127℃. 11.1.33×10-2 m 3解析 一定质量的空气,在等压变化过程中,可以运用盖—吕萨克定律进行求解,空气的初、末状态参量分别为初状态:T 1=(273+27) K =300 K ,V 1=1.0×10-2 m 3末状态:T 2=(273+27+100) K =400 K由盖—吕萨克定律V 1T 1=V 2T 2得,气体温度升高100℃时的体积为 V 2=T 2T 1V 1=400300×1.0×10-2 m 3=1.33×10-2 m 3 12.8.4 L解析 此气体在0℃时,压强为1个标准大气压,所以它的体积为22.4 L ×0.3=6.72 L ,根据图线所示,从p 0到A 状态,气体是等容变化,A 状态的体积为6.72 L ,温度为(127+273) K =400 K ,从A 状态到B 状态为等压变化,B 状态的温度为(227+273) K =500 K ,根据盖—吕萨克定律V A T A =V B T B ,V B =V A T B T A =6.72×500400L =8.4 L. 13.见解析解析 AB 过程是等容升温升压,BC 过程是等压升温增容即等压膨胀,CD 过程是等温减压增容即等温膨胀,DA 过程是等压降温减容即等压压缩.已知V A =1 L ,V B =1 L(等容过程)由V C T C =V B T B (等压过程)得V C =V B T B T C =1450×900 L =2 L 由p D V D =p C V C (等温过程)得V D =p C V C p D =3×21L =6 L 改画的p -V 图如下图所示.。

3 理想气体的状态方程第二课时理想气体状态方程的综合应用A级抓基础1.空气压缩机的储气罐中储有1.0 atm的空气6.0 L,现再充入1.0 atm的空气9.0 L.设充气过程为等温过程,空气可看作理想气体,则充气后储气罐中气体压强为( )A.2.5 atm B.2.0 atmC.1.5 atm D.1.0 atm解析:取全部气体为研究对象,由p1V1+p2V2=pV1得p=2.5 atm,故A正确.答案:A2.用打气筒将压强为1 atm的空气打进自行车胎内,如果打气筒容积ΔV=500 cm3,轮胎容积V=3 L,原来压强p=1.5 atm.现要使轮胎内压强变为p′=4 atm,问用这个打气筒要打气(设打气过程中空气的温度不变( )A.5次B.10次C.15次D.20次解析:因为温度不变,可应用玻意耳定律的分态气态方程求解.pV+np1ΔV=p′V,代入数据得1.5 atm×3 L+n×1 atm×0.5 L=4 atm×3 L,解得n=15.5.(多选)装有两种不同气体的容积相同的两个容器A、B,用均匀的长直玻璃管水平连接,管内有一段水银柱,将两部分气体隔开,当A的温度低于B的温度17 ℃时,水银恰好平衡,位于管中央,如图所示.为使水银柱保持在中央,则两容器的温度变化是()A.升高相同温度B.使A、B升高到相同温度C.使两容器升温后的热力学温度之比等于它们的初状态的热力学温度之比D.使两容器温度变化量之比等于它们的初状态的热力学温度之比解析:假设水银柱不动,对A:=,ΔpA=pA′-pA=TA′-pA=pA,同理对B得:ΔpB=pB,初始时,TA=TB-17,pA=pB,整理得:=或=.由此判断C、D正确.答案:CD6.(多选)如图所示,在光滑的水平面上,有一个内外壁都光滑的气缸,气缸的质量为M,气缸内有一质量为m(m<M)的活塞,密封一部分理想气体,气缸处于静止状态.现用水平恒力F向左推活塞.当活塞与气缸的加速度均为a时,封闭气体的压强为p1,体积为V1;若用同样大小的水平恒力F向右推气缸,当活塞与气缸的加速度均为a时,封闭气体的压强为p2,体积为V2,设封闭气体的质量和温度均不变,则()A.p1>p2B.p1<p2C.V1>V2D.V1<V2解析:向左推时,对于气缸p1S-p0S=Ma,解得p1=p0+;向右推时,对于活塞p2S-p0S=ma,解得p2=p0+,可见p1>p2,由玻意耳定律得V1<V2.故选项A、D正确.答案:AD7.如图,A,B是体积相同的气缸,B内有一导热的、可在气缸内无摩擦滑动的、体积不计的活塞C,D为不导热的阀门.起初,阀门关闭,A内装有压强p1=2.0×105 Pa,温度T1=300 K的氮气.B内装有压强p2=1.0×105 Pa,温度T2=600 K的氧气.打开阀门D,活塞C向右移动,最后达到平衡,以V1和V2分别表示平衡后氮气和氧气的体积,则V1∶V2=(假定氧气和氮气均为理想气体,并与外界无热交换,连接气缸的管道体积可忽略).解析:对于A容器中的氮气,其气体状态为初状态:p1=2.0×105 Pa,V1=V,T1=300 K,末状态:p1′=p,V1′=V1(题目所设),T1′=T.由气体状态方程可知:=.①对于B容器中的氧气,其气体状态为初状态:p2=1.0×105 Pa,V2=V,T2=600 K,末状态:p2′=p,V2′=V2(题目所设),T2′=T,由气态方程可知:=.②联立①②消去T、V,可得:V1===.V2答案:4∶18.一端开口的U形管内由水银柱封有一段空气柱,大气压强为76 cmHg,当气体温度为27 ℃时空气柱长为8 cm,开口端水银面比封闭端水银面低2 cm,如图所示.(1)当气体温度上升到多少摄氏度时,空气柱长为10 cm?(2)若保持温度为27 ℃不变,在开口端加入多长的水银柱能使空气柱长为6 cm?解析:(1)p1=p0-ph=74 cmHg,V1=8·S,T1=300 K,p2=p0+ph=78 cmHg,。

高中物理选修3-3课后习题和答案以及解释.txt54就让昨日成流水,就让往事随风飞,今日的杯中别再盛着昨日的残痕;唯有珍惜现在,才能收获明天。
课后练习一10(大纲版)高二物理同步复习课程第7讲分子热运动能量守恒(一)主讲人:孟卫东1.已知金刚石的密度为ρ=3.5×103 kg/m3,现有一块体积为4.0×10-8m3的一小块金刚石,它含有多少个碳原子?假如金刚石中的碳原子是紧密地挨在一起,试估算碳原子的直径?(保留两位有效数字)答案:2.2×10-10 m详解:先求出此金刚石质量,然后除以一个碳原子的质量,就是碳原子个数。
碳原子紧密排在一起的模型,就是一个一个的小球紧密相连,整个金刚石看成一个正方体,于是一条边上碳原子个数就是碳原子总个数的三次方根。
金刚石一条边的长度就是体积的三次方根。
然后边长除以一条边上碳原子个数就是碳原子直径。
2.关于布朗运动,下列说法中正确的是 ( )A.布朗运动就是分子的运动B.布朗运动是组成固体微粒的分子无规则的反映C.布朗运动是液体分子无规则运动的反映D.观察时间越长,布朗运动越显著答案:C详解:布朗运动是液体无规则运动的反映,它本身不是分子运动。
布朗运动的显著程度和观察时间无关,和液体温度,运动微粒的质量等有关。
3.关于分子间相互作用力,以下说法正确的是( )A.分子间的相互作用力是由组成分子的原子内部的带电粒子间的相互作用而引起的B.温度越高,分子间的相互作用力就越大C.分子力实质上就是分子间的万有引力D.分子引力不等于分子斥力时,违背了牛顿第三定律答案:A详解:A是正确的理论知识。
分子间作用力大小与分子距离有关,和温度无关。
另外,分子引力和分子斥力明显不是作用力和反作用力,不能乱套用牛顿第三定律。
4.关于分子间的相互作用力的以下说法中,正确的是( )A.当分子间的距离r=r0时,分子力为零,说明此时分子间不存在作用力B.当r>r0时,随着分子间距离的增大分子间引力和斥力都增大,但引力比斥力增加得快,故分子力表现为引力C. r<r0时,随着分子间距离的增大分子间引力和斥力都增大,但斥力比引力增加得快,故分子力表现为斥力D.当分子间的距离r>10-9m时,分子间的作用力可以忽略不计答案:D详解:r=r0时分子引力和斥力数值相等,分子间作用力合力是0,但不能说分子间没作用力,A错。

第八章气体〔情景切入〕空气是地球上的动植物生存的必要条件。
动物呼吸、植物光合作用都离不开空气;大气层可以使地球上的温度保持相对稳定,如果没有大气层,白天温度会很高,而夜间温度会很低;风、云、雨、雪的形成都离不开大气。
假设没有空气,我们的地球上将是一片荒芜的沙漠,没有一丝生机。
为更好地认识我们赖以生存的空气就需要掌握气体的性质和变化规律。
〔知识导航〕本章知识是热学部分的重要内容,研究的是气体实验三定律、理想气体状态方程以及对气体热现象的微观解释。
本章可分为两个单元:第一单元为前三节,介绍理想气体的三个实验定律和在此基础上推导出的理想气体状态方程。
第二单元为第四节,学习用分子动理论和统计观点对气体实验定律进行具体和比较详细的解释。
本章重点:理想气体状态方程。
本章难点:气体热现象的微观意义。
〔学法指导〕本章的学习内容,是分子动理论和统计观点的一次具体应用。
学习本章知识,要注重两个方面:一是通过实验,发现气体的宏观规律,并能灵活应用这些规律解决气体的状态变化问题;二是能用分子动理论和统计观点解释这些规律。
同时,对理想气体这种理想化模型也要能从宏观、微观两个角度加深理解。
第一节气体的等温变化【素养目标定位】※※掌握玻意耳定律的内容、表达式及适用条件※了解p-V图象的物理意义课前预习反馈知识点1等温变化1.气体的状态参量研究气体的性质时常用气体的__温度__、__压强__和体积,这三个参量来描述气体的状态。
2.等温变化一定质量的气体,在__温度不变__的条件下其压强与__体积__变化时的关系。
知识点2实验:探究等温变化的规律1.实验器材如图所示,有铁架台,带压力表的注射器、铁夹等。
2.研究对象注射器内__被封闭的一段空气柱__。
3.数据收集空气柱的压强p由上方的__压力表__读出,体积V用刻度尺上读出的空气柱的__长度l__乘以气柱的__横截面积S__计算。
用手把柱塞向下或向上拉,读出体积与压强的几组值。
4.数据处理以__压强p__为纵坐标,以__体积的倒数1V__为横坐标作出p-1V图象。

1.个别事物的出现具有____________,但大量事物出现的机会却遵从一定的____________.2.由于气体分子间的距离比较大,分子间的作用力很弱,通常认为,气体分子除了相互碰撞或者跟器壁碰撞外,不受力而做________________,因而气体会充满它所能达到的整个空间.分子之间频繁地发生碰撞,使每个分子的速度大小和方向频繁地改变,造成气体分子做____________________.3.分子的运动杂乱无章,在某一时刻,向着任何一个方向运动的分子都有,而且向着各个方向运动的气体分子数目都________;气体分子的速率各不相同,但遵守速率分布规律,即呈现“________________”的分布规律.而且____________,分子的热运动越激烈.4.气体的压强是大量气体分子频繁的____________而产生的.气体的压强在数值上等于大量气体分子作用在器壁____________的平均作用力.单位体积内的气体分子数越多,分子在单位时间内对单位面积器壁碰撞的次数就越多,压强就越____;温度越高,气体分子运动的平均动能越大,每个分子对器壁碰撞的作用力就会越____,气体的压强也就越____.由此可知:气体的压强由气体分子的____________和____________决定.5.(1)一定质量的某种理想气体,温度保持不变时,分子的平均动能是________的.在这种情况下,体积减小时,分子的________________,气体的压强就________.这就是对玻意耳定律的微观解释.(2)一定质量的某种理想气体,体积保持不变时,分子的密集程度____________.在这种情况下,温度升高时,分子的平均动能________,气体的压强就________.这就是对查理定律的微观解释.(3)一定质量的某种理想气体,温度升高时,分子的平均动能________;只有气体的体积同时________,使分子的密集程度________,才能保持压强不变.这就是盖—吕萨克定律的微观解释.6.关于气体分子,下列说法中正确的是()A.由于气体分子间的距离很大,气体分子在任何情况下都可以视为质点B.气体分子除了碰撞以外,可以自由地运动C.气体分子之间存在相互斥力,所以气体对容器壁有压强D.在常温常压下,气体分子间的相互作用力可以忽略7.对于气体分子的运动,下列说法正确的是()A.一定温度下某理想气体的分子碰撞十分频繁,但同一时刻,每个分子的速率都相等B.一定温度下某理想气体的分子速率一般不等,但速率很大和速率很小的分子数目相对较少C.一定温度下某理想气体的分子做杂乱无章的运动可能会出现某一时刻所有分子都朝同一方向运动的情况D.一定温度下的某理想气体,当温度升高时,其中某10个分子的动能可能减少【概念规律练】知识点一气体分子运动的特点1.为什么气体既没有一定的体积,也没有一定的形状?知识点二气体温度的微观意义2.如图1所示为一定质量的氧气分子在0℃和100℃两种不同情况下的速率分布情况,由图可以判断以下说法中正确的是()图1A.温度升高,所有分子的运动速率均变大B.温度越高,分子的平均速率越小C.0℃和100℃氧气分子的速率都呈现“中间多,两头少”的分布特点D.100℃的氧气与0℃的氧气相比,速率大的分子所占比例较大知识点三气体压强的微观意义3.在一定温度下,当一定量气体的体积增大时,气体的压强减小,这是由于()A.单位体积内的分子数变少,单位时间内对单位面积器壁碰撞的次数减少B.气体分子的密集程度变小,分子对器壁的吸引力变小C.每个分子对器壁的平均撞击力都变小D.气体分子的密集程度变小,单位体积内分子的重量变小4.图2如图2所示,两个完全相同的圆柱形密闭容器,甲中装有与容器容积相等的水,乙中充满空气,试问:(1)两容器各侧壁压强的大小关系及压强的大小决定于哪些因素?(容器容积恒定)(2)若让两容器同时做自由落体运动,容器侧壁上所受压强将怎样变化?知识点四对气体实验定律的微观解释5.一定质量的理想气体,在压强不变的条件下,体积增大,则()A.气体分子的平均动能增大B.气体分子的平均动能减小C.气体分子的平均动能不变D.条件不足,无法判定气体分子平均动能的变化情况6.封闭的汽缸内有一定质量的气体,如果保持气体体积不变,当温度升高时,以下说法正确的是()A.气体的密度增大B.气体的压强增大C.气体分子的平均动能减小D.每秒撞击单位面积器壁的气体分子数增多【方法技巧练】影响气体压强因素的判定方法7.对于一定质量的理想气体,下列说法中正确的是()A.当分子热运动变得剧烈时,压强必变大B.当分子热运动变得剧烈时,压强可以不变C.当分子间的平均距离变大时,压强必变小D.当分子间的平均距离变大时,压强必变大8.一定质量的某种理想气体,当体积减小为原来的一半时,其热力学温度变为原来的2倍时,它的压强变为原来的多少?试从压强和温度的微观意义进行解释.1.下列关于气体分子运动的特点,正确的说法是()A.气体分子运动的平均速率与温度有关B.当温度升高时,气体分子的速率分布不再是“中间多,两头少”C.气体分子的运动速率可由牛顿运动定律求得D.气体分子的平均速度随温度升高而增大2.气体分子运动的特点是()A.分子除相互碰撞或跟容器壁碰撞外,可在空间里自由移动B.分子的频繁碰撞致使它做杂乱无章的热运动C.分子沿各个方向运动的机会均等D .分子的速率分布毫无规律3.在一定温度下,某种理想气体分子的速率分布应该是( ) A .每个分子速率都相等B .每个分子速率一般都不相等,速率很大和速率很小的分子数目都很少C .每个分子速率一般都不相等,但在不同速率范围内,分子数的分布是均匀的D .每个分子速率一般都不相等,速率很大和速率很小的分子数目都很多 4.气体的压强是由于气体分子的下列哪种原因造成的( ) A .气体分子间的作用力 B .对器壁的碰撞力 C .对器壁的排斥力 D .对器壁的万有引力5.密闭容器中气体的压强是( ) A .由于重力产生的B .由于分子间的相互作用力产生的C .大量气体分子频繁碰撞器壁产生的D .在失重的情况下,密闭容器内的气体对器壁没有压强6.密封在圆柱形容器内的气体上半部分密度为ρ,压强为p ,则下半部分气体的压强和密度分别为( )A .p ,ρ B.p 2,ρ2C .2p,2ρ D.p2,ρ7.一定质量的气体,下列叙述中正确的是( )A .如果体积减小,气体分子在单位时间内对单位面积器壁的碰撞次数一定增大B .如果压强增大,气体分子在单位时间内对单位面积器壁的碰撞次数一定增大C .如果温度升高,气体分子在单位时间内对单位面积器壁的碰撞次数一定增大D .如果分子密度增大,气体分子在单位时间内对单位面积器壁的碰撞次数一定增大8.注射器中封闭着一定质量的气体,现在缓慢压下活塞,下列物理量发生变化的是( ) A .气体的压强 B .气体分子的平均速率 C .单位体积内的分子数 D .气体的密度9.一定质量的理想气体处于平衡状态Ⅰ.现设法使其温度降低而压强升高,达到平衡状态Ⅱ,则( )A .状态Ⅰ时气体的密度比状态Ⅱ时的大B .状态Ⅰ时分子的平均动能比状态Ⅱ时的大C .状态Ⅰ时分子间的平均距离比状态Ⅱ时的大D .状态Ⅰ时每个分子的动能都比状态Ⅱ时的分子平均动能大10.x 、y 两容器中装有相同质量的氦气,已知x 容器中氦气的温度高于y 容器中氦气的温度,但压强却低于y 容器中氦气的压强.由此可知( )A .x 中氦气分子的平均动能一定大于y 中氦气分子的平均动能B .x 中每个氦分子的动能一定都大于y 中每个氦分子的动能C .x 中动能大的氦气分子数一定多于y 中动能大的氦气分子数D .x 中氦分子的热运动一定比y 中氦分子的热运动剧烈 11.如图3所示,图3一定质量的理想气体由状态A 沿平行于纵轴的直线变化到状态B ,则它的状态变化过程是( )A.气体的温度不变B.气体的内能增加C.气体分子的平均速率减少12.理想气体的热力学温度T与分子的平均动能E k成正比,即:T=a E k(式中a是比例常数),因此可以说,________是分子平均动能的标志.13.从宏观上看,一定质量的气体体积不变仅温度升高或温度不变仅体积减小都会使压强增大,从微观上看,这两种情况有没有什么区别?14.一定质量的理想气体由状态A经状态B变为状态C,其中A→B过程为等压变化,B→C 过程为等容变化.已知V A=0.3 m3,T A=T C=300 K、T B=400 K.(1)求气体在状态B时的体积.(2)说明B→C过程压强变化的微观原因.第4节气体热现象的微观意义课前预习练1.偶然因素统计规律2.匀速直线运动无规则的热运动3.相等中间多,两头少温度越高4.碰撞器壁单位面积上大大大密集程度平均动能5.(1)一定密集程度增大增大(2)保持不变增大增大(3)增大增大减小6.BD7.BD课堂探究练1.因为气体分子间的距离较大,大约是分子直径的10倍,所以能够把分子看做是没有大小的质点,并可以认为分子间的相互作用力为零,气体分子除了相互碰撞或者跟器壁碰撞之外,不受到力的作用,可在空间内自由移动,因而能充满它所能达到的空间,所以气体既没有一定的体积,也没有一定的形状.方法总结 气体分子间距较大,可以在空间内自由移动,因而能充满它所能达到的整个空间,注意气体分子的这个特点. 2.CD方法总结 气体分子速率分布表现出“中间多、两头少”的分布规律.当温度升高,速率大的分子数增多,速率小的分子数减少,分子的平均速率增大.温度越高,分子的热运动越剧烈. 3.A方法总结 温度一定时,单位体积内分子数越多,单位时间内与器壁单位面积碰撞的分子数就越多,因而压强越大;若温度升高,则分子的平均动能增大,分子运动越剧烈,一方面使单位时间内碰到器壁单位面积上的分子数增多,另一方面也使一个分子与器壁碰撞一次时对器壁的平均冲击力增大,使压强增大.所以气体压强大小宏观上看跟温度和气体分子的密度有关,微观上看跟单位体积内的分子数和分子的平均速率有关. 4.见解析解析 (1)对甲容器,顶壁的压强为零,底面的压强最大,其数值为p =ρgh (h 为上下底面间的距离).左右两侧壁的压强自上而下,由小变大,其数值大小与侧壁上各点距水面的竖直距离x 的关系是p =ρgx .对乙容器,各处器壁上的压强大小都相等,其大小决定于气体的密度和温度.(2)甲容器做自由落体运动时器壁各处的压强均为零.乙容器做自由落体运动时,器壁各处的压强不发生变化.方法总结 (1)掌握好气体分子压强的微观解释.(2)千万不要混淆液体和气体压强,而要从它们产生的原因上加以区别. 5.A方法总结 本题也可以从微观角度来分析,体积增大气体分子密度减小,要想压强不变,分子平均动能必须增大,即撞击器壁的作用力变大. 6.BD方法总结 要从微观上理解查理定律.即:体积不变,则分子密度不变,温度升高,分子平均动能增大,分子撞击器壁的作用力变大,所以气体的压强增大. 7.B8.4倍 解释见解析解析 由理想气体状态方程pVT=恒量得,压强变为原来的4倍,从微观角度看,气体压强的大小跟两个因素有关:一个是气体分子的平均动能,一个是气体分子的密集程度,当体积减小为原来的一半时,气体分子的密集程度变为原来的两倍,这时气体的压强相应地变为原来的两倍,这时还要从另外一个因素考虑,即增加气体分子的平均动能,而气体分子的平均动能是由温度来决定的,气体的热力学温度变为原来的2倍,这时压强便在这两个因素(体积减小——分子密度程度增大,温度升高——分子的平均动能增大)的共同作用下变为原来的4倍. 方法总结 微观上影响气体压强的是分子的平均动能和分子的密集程度.因为温度是分子平均动能的标志,一定质量的气体、分子的密集程度决定于气体的体积,所以宏观上影响气体压强的因素是气体的温度和体积.所以,在遇到影响压强的因素判断时,可从微观角度,也可由理想气体状态方程pVT=C 从宏观角度得出结论.课后巩固练 1.A 2.ABC 3.B 4.B 5.C 6.A 7.B 8.ACD 9.BC10.ACD 11.B 12.温度 13.见解析解析 因为一定质量的气体的压强是由单位体积内的分子数和气体的温度决定的,气体温度升高,气体分子运动加剧,分子的平均速率增大,分子撞击器壁的作用力增大,故压强增大.气体体积减小时,虽然分子的平均速率不变,分子对容器的撞击力不变,但单位体积内的分子数增多,单位时间内撞击器壁的分子数增多,故压强增大,所以这两种情况下在微观上是有区别的.14.(1)0.4 m 3 (2)见解析解析 (1)A →B 由盖—吕萨克定律,得V A T A =V B T B ,故V B =T B T A V A =400300×0.3 m 3=0.4 m 3(2)B →C 过程气体的体积不变,分子密度不变,温度降低,分子平均动能减小,压强减小.小课堂:如何培养中学生的自主学习能力?自主学习是与传统的接受学习相对应的一种现代化学习方式。
第3节理想气体的状态方程1.理想气体:在任何温度、任何压强下都遵从气体实验定律的气体,实际气体在压强不太大、温度不太低时可看作理想气体。
2.理想气体状态方程:p 1V 1T 1=p 2V 2T 2或pV T=C 。
3.适用条件:一定质量的理想气体。
一、理想气体 1.定义在任何温度、任何压强下都严格遵从气体实验定律的气体。
2.理想气体与实际气体在温度不低于零下几十摄氏度、压强不超过大气压的几倍时,可以把实际气体当成理想气体来处理。
如图8-3-1所示。
图8-3-1二、理想气体的状态方程 1.内容一定质量的某种理想气体,在从一个状态变化到另一个状态时,压强跟体积的乘积与热力学温度的比值保持不变。
2.公式p 1V 1T 1=p 2V 2T 2或pVT=C (恒量)。
3.适用条件一定质量的理想气体。
1.自主思考——判一判(1)实际气体在常温常压下可看作理想气体。
(√)(2)一定质量的理想气体从状态1变化到状态2,经历的过程不同,状态参量的变化不同。
(×)(3)pVT=C 中的C 是一个与气体p 、V 、T 有关的常量。
(×) (4)一定质量的气体,体积、压强不变,只有温度升高。
(×) (5)一定质量的气体,温度不变时,体积、压强都增大。
(×) (6)一定质量的气体,体积、压强、温度都可以变化。
(√) 2.合作探究——议一议(1)在实际生活中理想气体是否真的存在?有何意义?提示:不存在。
是一种理想化模型,不会真的存在,是对实际气体的科学抽象。
(2)对于一定质量的理想气体,当其状态发生变化时,会不会只有一个状态参量变化,其余两个状态参量不变呢,为什么?提示:不会。
根据理想气体状态方程,对于一定质量的理想气体,其状态可用三个状态参量p 、V 、T 来描述,且pVT=C (定值)。
只要三个状态参量p 、V 、T 中的一个发生变化,另外两个参量中至少有一个会发生变化。
高中物理人教版选修3-3 课后习题整理第七章分子动理论1. 把一片很薄的均匀薄膜放在盐水中,把盐水密度调理为 1.2 ×10 3 kg/m 3时薄膜能在盐水中悬浮。
用天平测出尺寸为10 cm ×20 cm 的这类薄膜的质量是36 g ,请计算这类薄膜的厚度。
2. 在做“用油膜法估测分子的大小”实验时,每10 4 mL 油酸酒精溶液中有纯油酸6 mL 。
用注射器测得75 滴这样的溶液为 1 mL 。
把 1 滴这样的溶液滴入盛水的浅盘里,把玻璃板盖在浅盘上并描绘出油酸膜轮廓,如图7.1-4 所示。
图中正方形小方格的边长为 1 cm 。
(1)1 滴油酸酒精溶液中含有纯油酸的体积是多少?(2)油酸膜的面积是多少?(3)按以上数据,估量油酸分子的大小。
3.把铜分子当作球形,试估量铜分子的直径。
已知铜的密度为 8.9 ×10 3 kg/m 3,铜的摩尔质量为 6.4 ×10 - 2 kg/mol。
4.在标准状态下,氧气分子之间的均匀距离是多少?已知氧气的摩尔质量为 3.2 ×10 - 2 kg/mol ,1 mol 气体处于标准状态时的体积是 2.24 ×10 - 2 m 3。
2.以下对于布朗运动的说法能否正确?说明道理。
(1)布朗运动就是分子的无规则运动。
(2)布朗运动证明,构成固体小颗粒的分子在做无规则运动。
(3)一锅水中撒一点胡椒粉,加热时发现水中的胡椒粉在翻腾。
这说明温度越高布1 / 5朗运动越强烈。
(4)在显微镜下能够察看到煤油中小粒尘埃的布朗运动,这说明煤油分子在做无规则运动。
1. 请描绘:当两个分子间的距离由小于r 0 渐渐增大,直至远大于r 0时,分子间的引力如何变化?分子间的斥力如何变化?分子间引力与斥力的协力又如何变化?2.当两个分子间的距离由图 7.3-2 中的 r 0 渐渐增大时,分子间互相作使劲的协力会出现一个极大值。
你可否用实质生活中的例子说明分子间互相作用的协力确实存在着这样的极大值?3.为何物体能够被压缩,但压缩得越小,进一步压缩就越困难?第八章气体1. 一个足球的容积是2.5 L。
第八章气体综合练习一、知识梳理(课前完成)1.玻意耳定律描述了气体的_______变化规律:一定质量的某种气体,在温度不变的情况下,压强p与体积V成________。
公式:____________,或 __________一定质量的某种气体,等温变化的p-V图象是_______线,称为等温线。
一定质量的气体,不同温度下的等温线不同。
2.查理定律描述了气体的________变化规律:一定质量的某种气体,在体积不变的情况下,压强p与热力学温度T成________。
公式:________________,或 ___________一定质量的某种气体,等容变化的p-T图象是___________,称为等容线。
一定质量的气体,不同体积下的等容线不同。
3.盖-吕萨克定律描述了气体的_________变化规律:一定质量的某种气体,在压强不变的情况下,体积V与热力学温度T成________比。
公式:___________,或 ___________一定质量的某种气体,等压变化的V-T图象是______________,称为等压线。
一定质量的气体,不同压强下的等压线不同。
4.理想气体的状态方程:一定质量的某种理想气体在从一个状态1变化到另一个状态2时,尽管其p、T、V都可能改变,但是压强跟体积的乘积与热力学温度的比值___________。
公式:_____________。
或___________5.气体分子运动的特点:大量分子做无规则运动,速率有大有小,但分子的速率却按一定的规律分布,温度越高,分子的热运动越激烈。
6.气体热现象的的微观意义:从微观的角度看,气体的压强是大量气体分子__________而产生的。
气体分子的平均动能决定于________,分子的密集程度决定于________。
所以:气体压强与________和________有关。
一定质量的气体,温度保持不变时,分子的平均动能是一定的;体积保持不变时,分子的密集程度保持不变;温度升高时,分子的__________增大。
最新⼈教版⾼中物理选修3-3第⼋章同步测试题及答案最新⼈教版⾼中物理选修3-3第⼋章同步测试题及答案第⼋章⽓体1 ⽓体的等温变化A 级抓基础1.⼀定质量的⽓体,压强为3 atm ,保持温度不变,当压强减⼩了2 atm ,体积变化了4 L ,则该⽓体原来的体积为( )A.43 L B .2 L C.83L D .3 L 解析:设原来的体积为V ,则3V =(3-2)(V +4),得V =2 L.答案:B2.⼀个⽓泡由湖⾯下20 m 深处缓慢上升到湖⾯下10 m 深处,它的体积约变为原来体积的( )A .3倍B .2倍C .1.5倍D .0.7倍解析:⽓泡缓慢上升过程中,温度不变,⽓体等温变化,湖⾯下20 m 处,⽔的压强约为2个标准⼤⽓压(1个标准⼤⽓压相当于10 m⽔产⽣的压强),故p 1=3 atm ,p 2=2 atm ,由p 1V 1=p 2V 2,得:V 2V 1=p 1p 2=3 atm 2 atm=1.5,故C 项正确.答案:C3.(多选)⼀位质量为60 kg 的同学为了表演“轻功”,他⽤打⽓筒给4只相同的⽓球充以相等质量的空⽓(可视为理想⽓体),然后将这4只⽓球以相同的⽅式放在⽔平⽊板上,在⽓球的上⽅放置⼀轻质塑料板,如图所⽰.在这位同学慢慢站上轻质塑料板正中间位置的过程中,球内⽓体温度可视为不变.下列说法正确的是( )A .球内⽓体压强变⼤B .球内⽓体压强变⼩C .球内⽓体体积变⼤D .球内⽓体体积变⼩解析:⽓球被压后,⽓压变⼤,根据玻意⽿定律公式pV =C ,故体积缩⼩,即A 、D 正确,B 、C 错误.答案:AD4.如图所⽰,活塞的质量为m,缸套的质量为M,通过弹簧吊在天花板上,汽缸内封住⼀定质量的⽓体,缸套和活塞间⽆摩擦,活塞⾯积为S,⼤⽓压强为p0,则封闭⽓体的压强为()A.p=p0+MgS B.p=p0+(M+m)gSC.p=p0-MgS D.p=mgS解析:以缸套为研究对象,有pS+Mg=p0S,所以封闭⽓体的压强p=p0-MgS,故应选C.对于活塞封闭⽓体类问题压强的求法,灵活选取研究对象会使问题简化.答案:C5.如图所⽰,竖直放置的U形管,左端开⼝,右端封闭,管内有a、b两段⽔银柱,将A、B两段空⽓柱封闭在管内.已知⽔银柱a 长h1为10 cm,⽔银柱b两个液⾯间的⾼度差h2为5 cm,⼤⽓压强为75 cmHg,则空⽓柱A、B的压强分别是多少?解析:设管的横截⾯积为S,选a的下端为参考液⾯,它受向下的压⼒为(p A+p h1)S,受向上的⼤⽓压⼒为p0S,由于系统处于静⽌状态,则(p A+p h1)S=p0S,所以p A=p0-p h1=(75-10)cmHg=65 cmHg,再选b的左下端为参考液⾯,由连通器原理知:液柱h2的上表⾯处的压强等于p B,则(p B+p h2)S=p A S,所以p B=p A-p h2=(65-5)cmHg=60 cmHg.答案:65 cmHg60 cmHgB级提能⼒6.各种卡通形状的氢⽓球,受到孩⼦们的喜欢,特别是年幼的⼩孩,⼩孩⼀不⼩⼼松⼿,氢⽓球会飞向天空,上升到⼀定⾼度会胀破,是因为()A.球内氢⽓温度升⾼B.球内氢⽓压强增⼤C.球外空⽓压强减⼩D.以上说法均不正确解析:⽓球上升时,由于⾼空处空⽓稀薄,球外⽓体的压强减⼩,球内⽓体要膨胀,到⼀定程度时,⽓球就会胀破.答案:C7.已知两端开⼝的“”型管,且⽔平部分⾜够长,⼀开始如图所⽰,若将玻璃管稍微上提⼀点,或稍微下降⼀点时,被封闭的空⽓柱的长度分别会()A.变⼤;变⼩B.变⼤;不变C.不变;不变D.不变;变⼤解析:上提时空⽓柱压强不变,空⽓柱的长度不变;下降时空⽓柱压强变⼩,空⽓柱长度变⼤,所以D选项正确.答案:D8.(多选)在室内,将装有5 atm的6 L⽓体的容器的阀门打开后,从容器中逸出的⽓体相当于(设室内⼤⽓压强p0=1 atm)() A.5 atm,3 L B.1 atm,24 LC.5 atm,4.8 L D.1 atm,30 L解析:当⽓体从阀门跑出时,温度不变,所以p1V1=p2V2,当p2=1 atm时,得V2=30 L,逸出⽓体30 L-6 L=24 L,B正确.据p2(V2-V1)=p1V1′得V1′=4.8 L,所以逸出的⽓体相当于5 atm下的4.8 L⽓体,C正确.故应选B、C.答案:BC9.如图所⽰,⼀试管开⼝朝下插⼊盛⽔的⼴⼝瓶中,在某⼀深度静⽌时,管内有⼀定的空⽓.若向⼴⼝瓶中缓慢倒⼊⼀些⽔,则试管将()A.加速上浮B.加速下沉C.保持静⽌D.以原静⽌位置为平衡位置上下振动解析:题图中试管在⽔下某深度处于静⽌状态,浮⼒(等于排开⽔的重⼒)与试管重⼒相平衡.当试管中空⽓压强稍⼤些,即试管稍下移或向⼴⼝瓶中加⽔时,试管内的空⽓被压缩,浮⼒将减⼩,试管将下沉,在下沉的过程中,空⽓所受压强越来越⼤,浮⼒越来越⼩,试管将加速下沉.答案:B10.如图所⽰,两端开⼝的U形玻璃管两边粗细不同,粗管横截⾯积是细管的2倍.管中装⼊⽔银,两管中⽔银⾯与管⼝距离均为12 cm,⼤⽓压强为p0=75 cmHg.现将粗管管⼝封闭,然后将细管管⼝⽤⼀活塞封闭并将活塞缓慢推⼊管中,直⾄两管中⽔银⾯⾼度差达6 cm为⽌,求活塞下移的距离(假设环境温度不变).解析:设粗管中⽓体为⽓体1.细管中⽓体为⽓体2.对粗管中⽓体1:有p0L1=p1L1′右侧液⾯上升h1,左侧液⾯下降h2,有S1h1=S2h2,h1+h2=6 cm,得h1=2 cm,h2=4 cmL1′=L1-h1解得:p1=90 cmHg对细管中⽓体2:有p0L1=p2L2′p2=p1+Δh解得:L2′=9.375 cm因为h=L1+h2-L2′解得:h=6.625 cm答案:6.625 cm11.(2016·海南卷)如图,密闭⽓缸两侧与⼀U形管的两端相连,⽓缸壁导热;U形管内盛有密度为ρ=7.5×102kg/m3的液体.⼀活塞将⽓缸分成左、右两个⽓室,开始时,左⽓室的体积是右⽓室的体积的⼀半,⽓体的压强均为p0=4.5×103Pa.外界温度保持不变.缓慢向右拉活塞使U形管两侧液⾯的⾼度差h=40 cm,求此时左、右两⽓室的体积之⽐.取重⼒加速度⼤⼩g=10 m/s2,U形管中⽓体的体积和活塞拉杆的体积忽略不计.解析:设初始状态时⽓缸左⽓室的体积为V01,右⽓室的体积为V02;当活塞⾄⽓缸中某位置时,左、右⽓室的压强分别为p1、p2,体积分别为V1、V2,由玻意⽿定律,得p0V01=p1V1①p0V02=p2V2②依题意有V01+V02=V1+V2③由⼒的平衡条件,有p2-p1=ρgh,④联⽴①②③④式,并代⼊题给数据,得2V21+3V01V1-9V201=0,⑤由此解得V1=32V01(另⼀解不合题意,舍去)⑥由③⑥式和题给条件,得V1∶V2=1∶1.答案:1∶1第⼋章⽓体2 ⽓体的等容变化和等压变化A 级抓基础1.⼀定质量的⽓体,压强保持不变,下列过程可以实现的是()A.温度升⾼,体积增⼤B.温度升⾼,体积减⼩C.温度不变,体积增⼤D.温度不变,体积减⼩解析:⼀定质量的⽓体,压强保持不变时,其体积和热⼒学温度成正⽐,则温度升⾼,体积增⼤;温度降低,体积减⼩;温度不变,体积也不发⽣变化,故A 正确.答案:A2.对于⼀定质量的⽓体,在体积不变时,压强增⼤到原来的⼆倍,则⽓体温度的变化情况是()A.⽓体的摄⽒温度升⾼到原来的⼆倍B.⽓体的热⼒学温度升⾼到原来的⼆倍C.⽓体的摄⽒温度降为原来的⼀半D.⽓体的热⼒学温度降为原来的⼀半解析:⼀定质量的⽓体体积不变时,压强与热⼒学温度成正⽐,即p 1T 1=p 2T 2,得T 2=p 2T 1p 1=2T 1,B 正确. 答案:B3.贮⽓罐内的某种⽓体,在密封的条件下,温度从13 ℃上升到52 ℃,则⽓体的压强()A.升⾼为原来的4倍B.降低为原来的14C.降低为原来的2225D.升⾼为原来的2522解析:⽓体体积不变,由查理定律p 1p 2=T 1T 2得p 2p 1=T 2T 1=273+52273+13=2522答案:D4.(多选)⼀定质量的理想⽓体在等压变化中体积增⼤了12,若⽓体原来温度是27 ℃,则温度的变化是()A.升⾼到450 KB.升⾼了150 ℃C.升⾼到40.5 ℃D.升⾼到450 ℃解析:⽓体做等压变化,由盖-吕萨克定律V 1V 2=T 1T 2得V 1V 1+12V 1=273+27T 2,T 2=450 K ,ΔT =(450-300)K =150 K =150 ℃,故A 、B 对.答案:AB5.如图为0.3 mol 的某种⽓体的压强和温度关系的pt 图线,p 0表⽰1个标准⼤⽓压,则在状态B 时⽓体的体积为()A.5.6 LB.3.2 LC.1.2 LD.8.4 L解析:此⽓体在0 ℃时,压强为标准⼤⽓压,所以它的体积应为22.4×0.3 L =6.72 L.根据图线所⽰,从p 0到A 状态,⽓体是等容变化,A 状态的体积为6.72 L ,温度为(127+273)K =400 K.从A 状态到B 状态为等压变化,B 状态的温度为(227+273)K =500 K ,根据盖-吕萨克定律V A T A =V B T B,得V B =V A T B T A =6.72×500400L =8.4 L. 答案:D6.⽤易拉罐盛装碳酸饮料⾮常卫⽣和⽅便,但如果剧烈碰撞或严重受热会导致爆炸.我们通常⽤的可乐易拉罐容积V =355 mL.假设在室温(17 ℃)罐内装有0.9V 的饮料,剩余空间充满CO 2⽓体,⽓体压强为1 atm.若易拉罐承受的压强为1.2 atm ,则保存温度不能超过多少?解析:取CO 2⽓体为研究对象,则:初态:p 1=1 atm ,T 1=(273+17) K =290 K.末态:p 2=1.2 atm ,T 2=未知量.⽓体发⽣等容变化,由查理定律p 2p 1=T 2T 1得:T 2=p 2p 1T 1=1.2×2901K =348 K , t =(348-273)℃=75 ℃.答案:75 ℃7.⼀个密封的钢管内装有空⽓,在温度为20 ℃时,压强为1 atm ,若温度上升到80 ℃,管内空⽓的压强约为()A.4 atmB.14atm C.1.2 atm D.56atm 解析:由p 1p 2=T 1T 2得:1p 2=273+20273+80, p 2≈1.2 atm.答案:C8.⼀定质量的⽓体,在体积不变的条件下,温度由0 ℃升⾼到10 ℃时,其压强的增量为Δp 1,当它由100 ℃升⾼到110 ℃时,所增压强Δp 2,则Δp 1与Δp 2之⽐是()A.10∶1B.373∶273C.1∶1D.383∶283解析:由查理定律得Δp =p TΔT ,⼀定质量的⽓体在体积不变的条件下,Δp ΔT=恒量,温度由0 ℃升⾼到10 ℃和由100 ℃升⾼到110 ℃,ΔT =10 K 相同,故压强的增量Δp 1=Δp 2,C 项正确.答案:C9.如图所⽰,某同学⽤封有⽓体的玻璃管来测绝对零度,当容器⽔温是30刻度线时,空⽓柱长度为30 cm ;当⽔温是90刻度线时,空⽓柱的长度是36 cm ,则该同学测得的绝对零度相当于刻度线()A.-273B.-270C.-268D.-271解析:当⽔温为30刻度线时,V 1=30S ;当⽔温为90刻度线时,V 2=36S ,设T =t 刻线+x ,由盖-吕萨克定律得V 1t 1+x =V 2t 2+x,即30S 30刻线+x =36S 90刻线+x,解得x =270刻线,故绝对零度相当于-270刻度,故选B.答案:B10.(多选)如图所⽰,⼀定质量的空⽓被⽔银封闭在静置于竖直平⾯的U 形玻璃管内,右管上端开⼝且⾜够长,右管内⽔银⾯⽐左管内⽔银⾯⾼h ,能使h 变⼤的原因是()A.环境温度升⾼B.⼤⽓压强升⾼C.沿管壁向右管内加⽔银D.U 形玻璃管⾃由下落解析:对左管被封⽓体:p =p 0+p h ,由pV T=k ,可知当温度T 升⾼,⼤⽓压p 0不变时,h 增加,故A 正确;⼤⽓压升⾼,h 减⼩,B 错;向右管加⽔银时,由温度T 不变,p 0不变,V 变⼩,p 增⼤,即h 变⼤,C 正确;U 形管⾃由下落,⽔银完全失重,⽓体体积增加,h 变⼤,D 正确.答案:ACD11.如图所⽰,上端开⼝的圆柱形⽓缸竖直放置,截⾯积为5× 10-3 m 2,⼀定质量的⽓体被质量为2.0 kg 的光滑活塞封闭在⽓缸内,其压强为 Pa (⼤⽓压强取1.01×105 Pa ,g 取10 m/s 2).若从初温27 ℃开始加热⽓体,使活塞离⽓缸底部的⾼度由0.50 m 缓慢地变为0.51 m ,则此时⽓体的温度为℃.解析:p 1=F S =mg S =2×105×10-3Pa =0.04×105 Pa ,所以p =p 1+p 0=0.04×105 Pa +1.01×105 Pa =1.05×105 Pa ,由盖-吕萨克定律得V 1T 1=V 2T 2,即0.5S 273+27=0.51S 273+t,所以t =33 ℃. 答案:1.05×105 3312.容积为2 L 的烧瓶,在压强为1.0×105 Pa 时,⽤塞⼦塞住,此时温度为27 ℃,当把它加热到127 ℃时,塞⼦被打开了,稍过⼀会⼉,重新把盖⼦塞好,停⽌加热并使它逐渐降温到27 ℃,求:(1)塞⼦打开前的最⼤压强;(2)27 ℃时剩余空⽓的压强.解析:塞⼦打开前,瓶内⽓体的状态变化为等容变化.塞⼦打开后,瓶内有部分⽓体会逸出,此后应选择瓶中剩余⽓体为研究对象,再利⽤查理定律求解.(1)塞⼦打开前,选瓶中⽓体为研究对象初态:p 1=1.0×105 Pa ,T 1=(273+27)K =300 K.末态:p 2=?,T 2=(273+127)K =400 K.由查理定律,可得p 2=T 2×p 1T 1=400×1.0×105300Pa ≈1.33×105Pa.(2)塞⼦塞紧后,选瓶中剩余⽓体为研究对象.初态:p ′1=1.0×105Pa ,T ′1=400 K.末态:p ′2=?T ′2=300 K.由查理定律,可得p ′2=T ′2×p ′1T ′1=300×1.0×105400 Pa =0.75×105Pa.答案:(1)1.33×105Pa (2)0.75×105Pa第⼋章⽓体3 理想⽓体的状态⽅程第⼀课时理想⽓体的状态⽅程A 级抓基础1.(多选)对⼀定质量的理想⽓体( )A .若保持⽓体的温度不变,则当⽓体的压强减⼩时,⽓体的体积⼀定会增⼤B .若保持⽓体的压强不变,则当⽓体的温度减⼩时,⽓体的体积⼀定会增⼤C .若保持⽓体的体积不变,则当⽓体的温度减⼩时,⽓体的压强⼀定会增⼤D .若保持⽓体的温度和压强都不变,则⽓体的体积⼀定不变解析:⽓体的三个状态参量变化时,⾄少有两个同时参与变化,故D 对;T 不变时,由pV =恒量知,A 对;p 不变时,由V T=恒量知,B 错;V 不变时,由p T=恒量知,C 错.答案:AD2.关于理想⽓体的状态变化,下列说法中正确的是()A.⼀定质量的理想⽓体,当压强不变⽽温度由100 ℃上升到200 ℃时,其体积增⼤为原来的2倍B.⽓体由状态1变化到状态2时,⼀定满⾜⽅程p 1V 1T 1=p 2V 2T 2C.⼀定质量的理想⽓体体积增⼤到原来的4倍,可能是压强减半,热⼒学温度加倍D.⼀定质量的理想⽓体压强增⼤到原来的4倍,可能是体积加倍,热⼒学温度减半解析:⼀定质量的理想⽓体压强不变,体积与热⼒学温度成正⽐,温度由100 ℃上升到200 ℃时,体积增⼤为原来的1.27倍,故A 错误;理想⽓体状态⽅程成⽴的条件为质量不变,B 项缺条件,故错误;由理想⽓体状态⽅程pV T=恒量可知,C 正确,D 错误. 答案:C3.⼀定质量的⽓体,从初态(p 0、V 0、T 0)先经等压变化使温度上升到32T 0,再经等容变化使压强减⼩到12p 0,则⽓体最后状态为() A.12p 0、V 0、32T 0 B.12p 0、32V 0、34T 0 C.12p 0、V 0、34T 0 D.12p 0、32V 0、T 0 解析:在等压过程中,V ∝T ,有V 0T 0=V 33T 02,V 3=32V 0,再经过⼀个等容过程,有p 032T 0=p 02T 3,T 3=34T 0,所以B 正确. 答案:B4.(多选)⼀定质量的理想⽓体,初始状态为p 、V 、T ,经过⼀系列状态变化后,压强仍为p ,则下列过程中可以实现的是()A.先等温膨胀,再等容降温B.先等温压缩,再等容降温C.先等容升温,再等温压缩D.先等容降温,再等温压缩解析:根据理想⽓体的状态⽅程pV T=C ,若经过等温膨胀,则T 不变,V 增加,p 减⼩,再等容降温,则V 不变,T 降低,p 减⼩,最后压强p 肯定不是原来值,A 错;同理可以确定C 也错,正确选项为B 、D.答案:BD5.氧⽓瓶的容积是40 L ,其中氧⽓的压强是130 atm ,规定瓶内氧⽓压强降到10 atm 时就要重新充氧,有⼀个车间,每天需要⽤1 atm 的氧⽓400 L ,这瓶氧⽓能⽤⼏天?(假定温度不变)解析:⽤如图所⽰的⽅框图表⽰思路.由V1→V2:p1V1=p2V2,V2=p1V1p2=130×4010L=520 L,由p2(V2-V1)=p3V3,V3=p2(V2-V1)p3=10×4801L=4 800 L,则V3400 L=12天.答案:12天B级提能⼒6.如图所⽰是⼀定质量的某种⽓体状态变化的pV图象,⽓体由状态A变化到状态B的过程中,⽓体分⼦平均速率的变化情况是()A.⼀直保持不变B.⼀直增⼤C.先减⼩后增⼤D.先增⼤后减⼩解析:由题图象可知,p A V A=p B V B,T A=T B,则A、B在同⼀等温线上.由于离原点越远的等温线温度越⾼,所以A状态到B状态温度应先升后降,故分⼦平均速率先增⼤后减⼩.答案:D7.下图表⽰⼀定质量的理想⽓体,从状态1出发经过状态2和3,最终⼜回到状态1.那么,在如下pT图象中,反映了上述循环过程的是()解析:由图知:1到2压强不变,2到3体积不变,3到1温度不变.由四个选项中知B正确.答案:B8.(多选)⼀定质量的理想⽓体经历如图所⽰的⼀系列过程,ab、bc、cd和da这四段过程在p-T图上都是直线段,ab和cd的延长线通过坐标原点O,bc垂直于ab,由图可以判断()A.ab过程中⽓体体积不断减⼩B.bc过程中⽓体体积不断减⼩C.cd过程中⽓体体积不断增⼤D.da过程中⽓体体积不断增⼤解析:由p-T图线的特点可知a、b在同⼀条等容线上,过程中体积不变,故A错;c、d在同⼀条等容线上,过程中体积不变,故C错;在p-T图线中,图线的斜率越⼤与之对应的体积越⼩,因此b→c 的过程体积减⼩,同理d→a的过程体积增⼤,故B、D 均正确.答案:BD9.密封的体积为2 L的理想⽓体,压强为2 atm,温度为27 ℃.加热后,压强和体积各增加20%,则它的最后温度是W.解析:根据理想⽓体状态⽅程,有p1V1 T1=p2V2 T2,即2×2300=2×2(1+20%)2T2,得T2=432 K.答案:432 K10.(汽缸类问题)如图所⽰,汽缸长为L=1 m,固定在⽔平⾯上,汽缸中有横截⾯积为S=100 cm2的光滑活塞,活塞封闭了⼀定质量的理想⽓体,当温度为t=27 ℃,⼤⽓压强为p0=1×105 Pa时,⽓柱长度为l=90 cm,汽缸和活塞的厚度均可忽略不计.(1)如果温度保持不变,将活塞缓慢拉⾄汽缸右端⼝,此时⽔平拉⼒F的⼤⼩是多少?(2)如果汽缸内⽓体温度缓慢升⾼,使活塞移⾄汽缸右端⼝时,⽓体温度为多少摄⽒度?解析:(1)设活塞到达缸⼝时,被封闭⽓体压强为p1,则p1S=p0S-F由玻意⽿定律得:p0lS=p1LS解得:F=100 N(2)温度缓慢升⾼时,⽓体做等压变化,由盖—吕萨克定律得:lS 300 K=LS 273 K+t′解得:t′≈60.3 ℃.答案:(1)100 N(2)60.3 ℃第⼋章⽓体3 理想⽓体的状态⽅程第⼆课时理想⽓体状态⽅程的综合应⽤A级抓基础1.空⽓压缩机的储⽓罐中储有1.0 atm的空⽓6.0 L,现再充⼊1.0 atm的空⽓9.0 L.设充⽓过程为等温过程,空⽓可看作理想⽓体,则充⽓后储⽓罐中⽓体压强为()A.2.5 atm B.2.0 atmC.1.5 atm D.1.0 atm解析:取全部⽓体为研究对象,由p1V1+p2V2=pV1得p=2.5 atm,。
第八章 第3节1.(江苏省徐州市2017-2018学年高二下学期期中)下图为伽利略设计的一种测温装置示意图,玻璃管的上端与导热良好的玻璃泡连通,下端插入水中,玻璃泡中封闭有一定量的空气。
若玻璃管内水柱上升,则外界大气的变化可能是( A )A .温度降低,压强增大B .温度升高,压强不变C .温度升高,压强减小D .温度不变,压强减小解析:对于一定质量的理想气体pV =CT ,得出V =C T p。
当温度降低,压强增大时,体积减小,故A 正确。
当温度升高,压强不变时,体积增大,故B 错。
当温度升高,压强减小时,体积增大,故C 错。
当温度不变,压强减小时,体积增大,故D 错。
2.(多选)(福建省龙海二中2017年高二下学期期末)一定质量理想气体的状态经历了如图所示的ab 、bc 、cd 、da 四个过程,其中bc 的延长线通过原点,cd 垂直于ab 且与水平轴平行,da 与bc 平行,则气体体积在( AB )A .ab 过程中不断增加B .bc 过程中保持不变C .cd 过程中不断增加D .da 过程中保持不变解析:首先,因为bc 的延长线通过原点,所以bc 是等容线,即气体体积在bc 过程中保持不变,B 正确;ab 是等温线,压强减小则体积增大,A 正确;cd 是等压线,温度降低则体积减小,C 错误;连接aO 交cd 于e ,则ae 是等容线,即V a =V e ,因为V d <V e ,所以V d <V a ,所以da 过程中体积不是保持不变,D 错误。
3.(湖北省孝感一中、应城一中等五校2018届高三上学期期末)如图所示,在两端封闭的均匀半圆(圆心为O )管道内封闭一定质量的理想气体,管内有不计质量、可自由移动的活塞P ,将管内气体分成两部分,OP 与管道的水平直径的夹角θ=45°。
其中两部分气体的温度均为T 0=300K ,压强均为p 0=1×105Pa ,现对活塞左侧气体缓慢加热,而保持活塞右侧气体温度不变,当可动活塞缓慢移到管道最低点时(不计摩擦),求:(1)活塞右侧气体的压强;(2)活塞左侧气体的温度。
高中物理学习材料
(马鸣风萧萧**整理制作)
习题课理想气体状态方程的应用
一、基础练
1.为了控制温室效应,各国科学家都提出了不少方法和设想.有人根据液态CO2密度大于海水密度的事实,设想将CO2液化后,送入深海海底,以减小大气中CO2的浓度.为使CO2液化,最有效的措施是()
A.减压、升温B.增压、升温
C.减压、降温D.增压、降温
2.如图1所示甲、乙为一定质量的某种气体的等容或等压变化图象,关于这两个图象的正确说法是()
图1
A.甲是等压线,乙是等容线
B.乙图中p-t线与t轴交点对应的温度是-273.15℃,而甲图中V-t线与t轴的交点不一定是-273.15℃.
C.由乙图可知,一定质量的气体,在任何情况下都是p与t成直线关系
D.乙图表明随温度每升高1℃,压强增加相同,但甲图随温度的升高压强不变
3.向固定容器内充气,当气体压强为p,温度为27℃时,气体的密度为ρ,当温度为327℃,气体压强为1.5p时,气体的密度为()
A.0.25ρB.0.5ρC.0.75ρD.ρ
4.关于理想气体的状态变化,下列说法中正确的是()
A.一定质量的理想气体,当压强不变而温度由100℃上升到200℃时,其体积增大为原来
的2倍
B .气体由状态1变到状态2时,一定满足方程p 1V 1T 1=p 2V 2
T 2
C .一定质量的理想气体体积增大到原来的4倍,可能是压强减半,热力学温度加倍
D .一定质量的理想气体压强增大到原来的4倍,可能是体积加倍,热力学温度减半 二、提升练
5.一定质量的理想气体,处在某一状态,经下列哪个过程后会回到原来的温度( ) A .先保持压强不变而使它的体积膨胀,接着保持体积不变而减小压强 B .先保持压强不变而使它的体积减小,接着保持体积不变而减小压强 C .先保持体积不变而增大压强,接着保持压强不变而使它的体积膨胀 D .先保持体积不变而减小压强,接着保持压强不变而使它的体积膨胀 6.
图2
将一根质量可忽略的一端封闭的塑料管子插入液体中,在力F 的作用下保持平衡,如图2所示的H 值大小与下列哪个量无关( ) A .管子的半径 B .大气压强 C .液体的密度 D .力F 7.一绝热隔板将一绝热长方形容器隔成两部分,两边分别充满气体,隔板可无摩擦移动.开始时,左边的温度为0℃,右边的温度为20℃,当左边的气体加热到20℃,右边的气体加热到40℃时,则达到平衡状态时隔板的最终位置( ) A .保持不动 B .在初始位置右侧 C .在初始位置左侧 D .决定于加热过程 8.
图3
如图3所示,一端封闭的粗细均匀的玻璃管,开口向上竖直放置,管中有两段水银柱封闭了两段空气柱,开始时V 1=2V 2,现将玻璃管缓慢地均匀加热,则下述说法中正确的是( ) A .加热过程中,始终保持V 1′=2V 2′ B .加热后V 1′>2V 2′ C .加热后V 1′<2V 2′
图4
如图4所示,一个密闭的汽缸,被活塞分成体积相等的左、右两室,汽缸壁与活塞是不导热的;它们之间没有摩擦,两室中气体的温度相等.现利用右室中的电热丝对右室加热一段时
间.达到平衡后,左室的体积变为原来体积的3
4
,气体的温度T 1=300 K .求右室气体的温
度.
10.
图5
粗细均匀的U形管,右端封闭有一段空气柱,两管内水银面高度差为19 cm,封闭端空气柱长度为40 cm,如图5所示,问向左管内再注入多少水银可使两管水银面等高?已知外界大气压强p0=76 cmHg,注入水银过程中温度保持不变.
11.如图6所示为一太阳能空气集热器,底面及侧面为隔热材料,顶面为透明玻璃板,集热器容积为V0,开始时内部封闭气体的压强为p0,经过太阳曝晒,气体温度由T0=300 K升至T1=350 K.
图6
(1)求此时气体的压强.
(2)保持T 1=350 K 不变,缓慢抽出部分气体,使气体压强再变回到p 0.求集热器内剩余气体的质量与原来总质量的比值.
12.一活塞将一定质量的理想气体封闭在水平固定汽缸内,开始时气体体积为V 0,温度为
27℃,在活塞上施加压力,将气体体积压缩到2
3
V 0,温度升高到57℃.设大气压强p 0=1.0×105
Pa ,活塞与汽缸壁摩擦不计. (1)求此时气体的压强.
(2)保持温度不变,缓慢减小施加在活塞上的压力使气体体积恢复到V 0,求此时气体的压强.
习题课 理想气体状态方程的应用
1.D
2.AD [由查理定律p =CT =C (t +273.15)及盖—吕萨克定律V =CT =C (t +273.15)可知,甲
图是等压线,乙图是等容线,故A 正确;由“外推法”可知两种图线的反向延长线与t 轴的交点温度为-273.15℃,即热力学温度的0 K ,故B 错;查理定律及盖—吕萨克定律是气体的实验定律,都是在温度不太低、压强不太大的条件下得出的,当压强很大,温度很低时,这些定律就不成立了,故C 错;由于图线是直线,故D 正确.]
3.C [由理想气体状态方程得pV 300=1.5pV ′
600
,
所以V ′=43V ,所以ρ′=3
4
ρ=0.75ρ,应选C.]
4.C [一定质量的理想气体压强不变,体积与热力学温标成正比,温度由100℃上升到200℃时,体积增大为原来的1.27倍,故A 错误;理想气体状态方程成立的条件为质量不变,B
项缺条件故错误;由理想气体状态方程pV
T
=C 得C 项正确,D 错误.]
5.AD [
由于此题要经过一系列状态变化后回到初始温度,所以先在p -V 坐标中画出等温变化图线,然后在图线上任选一点代表初始状态,根据各个选项中的过程画出图线,如图所示,从图线的发展趋势来看,有可能与原来的等温线相交说明经过变化后可能回到原来的温度,选项A 、D 正确.] 6.B [
分析管子的受力如右图所示,由受力平衡有
p 0S +F =pS ,又p =p 0+ρgH ,故H =p -p 0ρg =F ρgS =F
ρg πr 2
,与大气压强无关,故选B.]
7.B [设温度变化过程中气体的体积不变,据查理定律得: p 2T 2=p 1T 1⇒p 2-p 1p 1=T 2-T 1T 1⇒Δp =p 1T 1
ΔT . 对左边气体,Δp 左=p 左273×20;对右边气体Δp 右=p 右
293
×20.因初始p 左=p 右,故Δp 左>Δp 右.即
隔板将向右侧移动.本题的正确答案为B.]
8.A [在整个加热过程中,上段气柱的压强始终保持为p 0+h 1不变,下段气柱的压强始终为p 0+h 1+h 2不变,所以整个过程为等压变化.根据盖—吕萨克定律得
V 1T =V 1′
T ′,即V 1′=T ′T V 1
, V 2T =V 2′
T ′,即V 2′=T ′T V 2
. 所以V 1′V 2′=V 1V 2=21,即V 1′=2V 2′.]
9.500 K
解析 根据题意对汽缸中左、右两室中气体的状态进行分析:
左室的气体:加热前p 0、V 0、T 0,加热后p 1、3
4V 0、T 1;
右室的气体:加热前p 0、V 0、T 0,加热后p 1、5
4
V 0、T 2;
根据理想气体状态方程有
左室气体p 0V 0
T 0=p 134V 0T 1
,
右室气体p 0V 0
T 0=p 154V 0T 2,
所以p 134V 0300 K =p 154V 0T 2
,
所以T 2=500 K. 10.39 cm
解析 以右管中被封闭气体为研究对象,气体在初状态下其p 1=p 0-p h =(76-19) cmHg =57 cmHg ,V 1=L 1S =40S ;末状态p 2=p 0=76 cmHg ,V 2=L 2S .则由玻意耳定律得:57×40 S =76×L 2S ,L 2=30 cm.需注入的水银柱长度应为h +2(L 1-L 2)=39 cm.
11.(1)76p 0 (2)6
7
解析 (1)设升温后气体的压强为p 1,
由查理定律得p 0T 0=p 1
T 1
①
代入数据得p 1=7
6
p 0②
(2)抽气过程可视为等温膨胀过程,设膨胀后的总体积为V ,由玻意耳定律得p 1V 0=p 0V ③
联立②③式解得V =7
6
V 0④
设剩余气体的质量与原来气体的总质量之比为K ,由题意得K =V 0
V
⑤
联立④⑤式解得K =6
7
⑥
12.(1)1.65×105 Pa (2)1.1×105 Pa
解析 (1)由理想气体状态方程得p 0V 0T 0=p 1V 1
T 1
,所以此时气体的压强为
p 1=p 0V 0T 0·T 1V 1=1.0×105×V 0300×3302
3V 0
Pa =1.65×105 Pa.
(2)由玻意耳定律p 1V 1=p 2V 2,知
p 2=p 1V 1
V 2=1.65×105×2
3V 0
V 0
Pa =1.1×105 Pa。