
离子液体双水相技术萃取头孢呋辛酯及其机理探究
谷
华*
1,2
谭树华
*1
李悦1
何佳
1
1
(中国药科大学,分析化学教研室,南京210009)
2
(中国药科大学,药物质量与安全预警教育部重点实验室,南京210009)
摘 要 通过研究离子液体3-甲基咪唑四氟硼酸盐([Bmim]BF 4)-Na 2CO 3双水相体系对头孢呋辛酯的萃取性能,建立了萃取环境水样中头孢呋辛酯的双水相法三考察了双水相体系组成及相关条件对萃取率的影
三结果表明,Na 2CO 3用量为0.8~2.0g ,[Bmim]BF 4用量为1~,萃取率有所增加三与[Bmim]Cl/Na 2CO 3双水相体系相比,[Bmim]BF 4/Na 2CO 3双三热力学参数ΔG ?T <0,ΔH ?T >0,ΔS ?T >0,说明萃取过程的主要推动力为三在最佳萃取条件下,用此方法萃取环境水样中的头孢呋辛酯,二次萃取率大于93%,重现性三整个萃取过程快速二高效且无乳化现象三关键词 离子液体双水相;萃取;头孢呋辛酯
2011-09-21收稿;2011-12-22接受本文系 重大新药创制 科技重大专项(No.2009ZX09301-006)和 重大新药创制 科技重大专项(No.2009ZX09103-653)资助*E -
mail:dochehua@https://www.doczj.com/doc/fb16736533.html,;tanshuhua126@https://www.doczj.com/doc/fb16736533.html, 1 引 言
头孢呋辛酯(Cefuroxime axetil)为头孢呋辛的酯化物,因在体内水解后释放出头孢呋辛而发挥其抗
菌活性,在临床方面有广泛应用三目前其萃取方法主要为有机溶剂萃取法,采用乙酸乙酯[1]等作为萃取剂,但这种传统方法萃取液易乳化,挥发性大,易造成环境污染,存在潜在的危险三
双水相体系是指两种高聚物之间或高聚物与无机盐之间在水中以适当的浓度溶解后形成的互不相
溶的两相体系[2]三与传统的萃取体系相比,具有操作条件温和二易于放大和可连续操作等优点三离子液体是一种低蒸汽压二低熔点和酸性可调的绿色介质三2003年,Rogers 课题组最先报道出一种新型的双水相体系 离子液体/盐双水相(ILATPS)[3],这种体系由离子液体和无机盐形成三该体系结合了离子液体和双水相萃取的优点,如蒸汽压低二不易乳化二分离效率高二可连续操作二环境友好等,因此这种高效而温和的新型绿色分离体系受到了广泛的关注[4~10]三-1-丁基-3-甲基咪唑和碳酸钠组成的双水相体系([Bmim]BF 4/Na 2CO 3)萃取头孢呋辛酯,的影响,建立了萃取环境水样中头孢呋辛酯的方法三相对于传统萃取方法,此方法整个过程快速二高效且无乳化现象,为离子液体代替传统挥发性萃取溶剂提供了可能性三
2 实验部分
2.1 仪器与试剂
BS124S 型电子天平(赛多利斯科学仪器(北京)有限公司);UV1800紫外分光光度计(日本岛津公司);HWS -10A 恒温水浴锅(北京东方精瑞科技发展有限公司);头孢呋辛酯(含量99%,鲁南药业提供);四氟硼酸-1-丁基-3-甲基咪唑([Bmim]BF 4)和氯化-1-丁基-3-甲基咪唑([Bmim]Cl),含量均为99.9%,由中国科学院兰州物理化学研究所绿色化学与催化中心提供;Na 2CO 3(上海凌峰公司);其它试剂均为分析纯;水为二次蒸馏水,无干扰测定的紫外杂质三
2.2 实验方法
2.2.1 绘制相图 在298K 下,在烧杯中加入5mL 离子液体,加水溶解,缓慢加入Na 2CO 3固体,直至体系浑浊,记录加入的Na 2CO 3量三加入适量水使溶液澄清,向体系中继续加入Na 2CO 3,直至体系再次
浑浊,如此往复,以离子液体在体系中的质量分数为横坐标,Na 2CO 3的质量分数为纵坐标绘制相图三2.2.2 双水相对药物的萃取 在10mL 离心管中加入适量离子液体[Bmim]BF 4或[Bmim]Cl ,5mL 去离子水和适量Na 2CO 3固体,置于37?水浴,待盐完全溶解后,冷却至室温三加入1mL 头孢呋辛酯溶液(5
?10-4
mol/L )
,适量去离子水,振荡5min ,以2000r/min 离心10min ,使两相明显分开,静置2min ,准确量取两相的体积三以空白双水相溶液为对照,在278nm 处,298K 条件下测定两相中头孢呋辛酯的吸光
度三利用公式(1),测定萃取效率E 三
E =C t
V t C t V t +C b
V b (1)
其中,C t 和C b 分别为上相和下相中的药物浓度,
V t 和V b 分别为上相和下相的体积三3 结果与讨论
3.1 相图
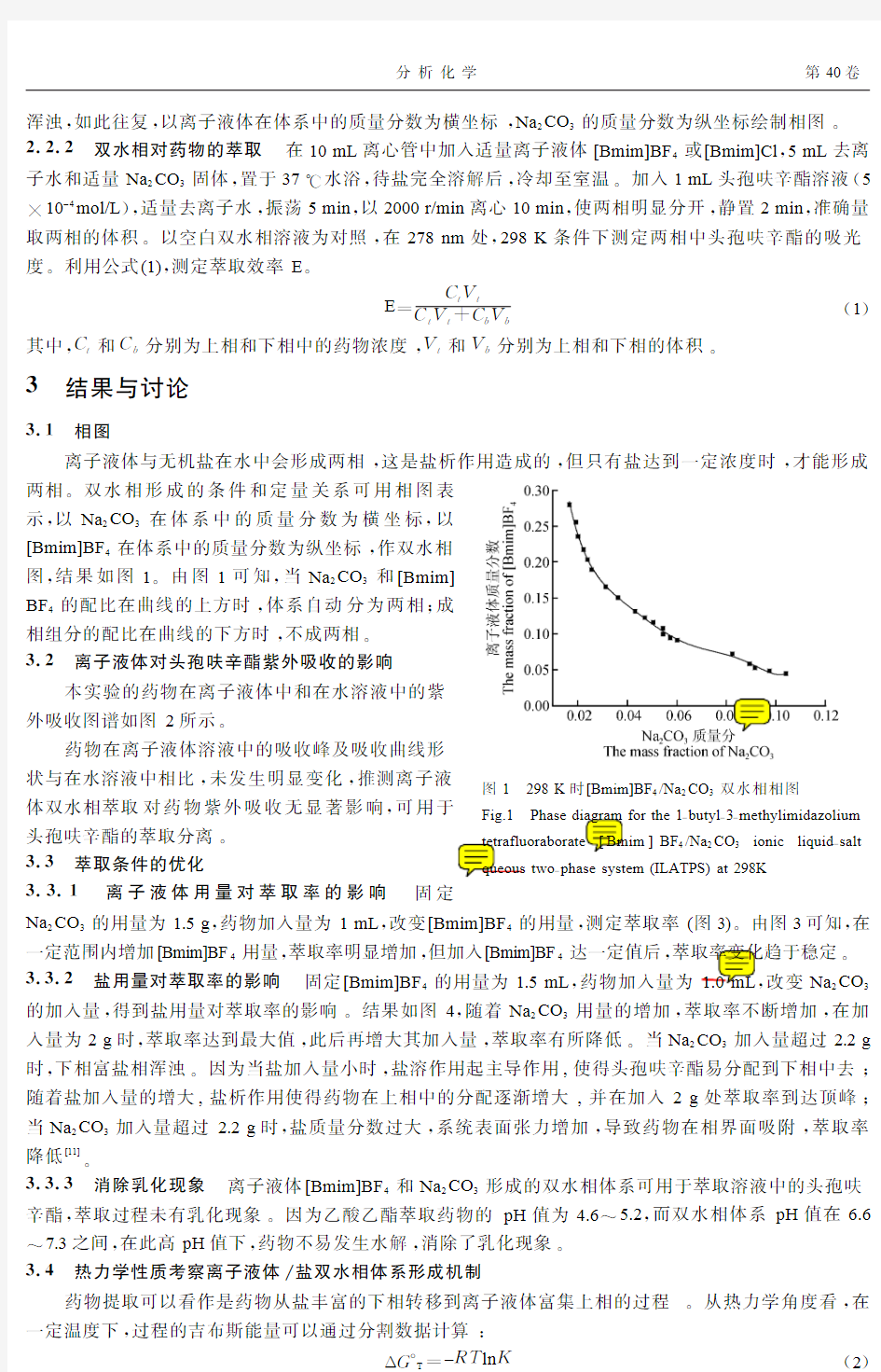
离子液体与无机盐在水中会形成两相,这是盐析作用造成的,但只有盐达到一定浓度时,才能形成 图1 298K 时[Bmim]BF 4/Na 2CO 3双水相相图Fig.1 Phase
for the 1-butyl -
3-methylimidazolium ]BF 4/Na 2CO 3ionic liquid -salt two -
phase system (ILATPS)at 298K 两相三双水相形成的条件和定量关系可用相图表示,以Na 2CO 3在体系中的质量分数为横坐标,以[Bmim]BF 4在体系中的质量分数为纵坐标,作双水相图,结果如图1三由图1可知,当Na 2CO 3和[Bmim]BF 4的配比在曲线的上方时,体系自动分为两相;成相组分的配比在曲线的下方时,不成两相三
3.2 离子液体对头孢呋辛酯紫外吸收的影响
本实验的药物在离子液体中和在水溶液中的紫外吸收图谱如图2所示三
药物在离子液体溶液中的吸收峰及吸收曲线形状与在水溶液中相比,未发生明显变化,推测离子液体双水相萃取对药物紫外吸收无显著影响,可用于头孢呋辛酯的萃取分离三
3.3 萃取条件的优化3.3.1 离子液体用量对萃取率的影响 固定
Na 2CO 3的用量为1.5g ,药物加入量为1mL ,改变[Bmim]BF 4的用量,测定萃取率(图3)三由图3可知,在一定范围内增加[Bmim]BF 4用量,萃取率明显增加,但加入[Bmim]BF 4达一定值后,三
3.3.2 盐用量对萃取率的影响 固定[Bmim]BF 4的用量为1.5mL ,药物加入量为改变Na 2CO 3的加入量,得到盐用量对萃取率的影响三结果如图4,随着Na 2CO 3用量的增加,萃取率不断增加,在加入量为2g 时,萃取率达到最大值,此后再增大其加入量,萃取率有所降低三当Na 2CO 3加入量超过2.2g 时,下相富盐相浑浊三因为当盐加入量小时,盐溶作用起主导作用,使得头孢呋辛酯易分配到下相中去;随着盐加入量的增大,盐析作用使得药物在上相中的分配逐渐增大,并在加入2g 处萃取率到达顶峰;当Na 2CO 3加入量超过2.2g 时,盐质量分数过大,系统表面张力增加,导致药物在相界面吸附,萃取率降低[11]三
3.3.3 消除乳化现象 离子液体[Bmim]BF 4和Na 2CO 3形成的双水相体系可用于萃取溶液中的头孢呋辛酯,萃取过程未有乳化现象三因为乙酸乙酯萃取药物的pH 值为
4.6~
5.2,而双水相体系pH 值在
6.6
~7.3之间,
在此高pH 值下,药物不易发生水解,消除了乳化现象三3.4 热力学性质考察离子液体/盐双水相体系形成机制
药物提取可以看作是药物从盐丰富的下相转移到离子液体富集上相的过程三从热力学角度看,在一定温度下,过程的吉布斯能量可以通过分割数据计算:
ΔG ?T =-R T ln K
(2)
分析化学第40卷
图2 不同溶液中的头孢呋辛酯紫外吸收图谱Fig.2 UV -
vis spectra of Cefuroxime axetil in different media
C 头孢呋辛酯=5?10-4mol /L ,[Bmim]BF 4?水
V )
C Cefuroxime axetil =5?10-4mol/L,[Bmim]BF 4?H 2O =1?10(V /V )
图3 298K 时[Bmim]BF 4用量对头孢萃取效率的影响Fig.3 Effect of amount of [Bmim]BF 4used on extraction at
298K
图4 298K 时Na 2CO 3用量对头孢呋辛酯萃取效率的影响
Fig.4 Effect of amount of Na 2CO 3at 298K
其中,K 是分割系数,T 是温度,R 是气体常数三
ΔH ?变化和ΔS ?熵变可以从ln K 对1/T 的线性方程的斜率和截距分别计算[7]:
ln K =-ΔH ?T /R T +ΔS ?T
/R (3)
表1 头孢呋辛酯在[Bmim]BF 4/Na 2CO 3双水相中分配的热力
学参数
Table 1Transfer thermodynamic properties for cefuroxime axetil 28835.87-8572.075315.8148.2129838.47-9043.145315.8148.2130841.26-9525.855315.8148.2131844.27
10020.20
5315.81
48.21
计算结果如表1所示,ΔG ?T <0,ΔH ?T >0,ΔS ?T >0,
表明头孢呋辛酯的分配是被熵变控制的,这是疏水性相互作用的特点[12]三因此,热力学研究结果表明疏水性相互作用是[Bmim]BF 4/Na 2CO 3双水相体系萃取头孢呋辛酯的主要推动力三
从热力学数据可以看出,离子液体/盐双水相的形成是一种离子液体和无机盐竞争水分子的过程三
在这种竞争关系中,无机盐因对水分子更有亲和力而占优势[13,14]三换言之,水分子有从离子液体周围迁移到无机盐周围的趋势三将药物加入水中,水分子将其溶解并包围在药物分子周围,此时,向体系中加入适量[Bmim]BF 4和Na 2CO 3,盐颗粒逐渐溶解,不断与[Bmim]BF 4竞争水分子三在这种竞争中,盐更具优势,所以水分子逐渐从药物周围迁移到盐周围,使得[Bmim]BF 4溶解药物的能力增加三体系最终分成两相,药物被萃取到上层的[Bmim]BF 4相中三萃取示意图见图5三
3.5 不同阴离子离子液体对药物萃取的影响
固定盐种类,改变离子液体为[Bmim]BF 4或[Bmim]Cl ,测定萃取率三不同阴离子离子液体加入对萃取率的影响见图6三
向体系中加入1.5mL [Bmim]BF 4后,逐渐加入Na 2CO 3三Na 2CO 3加入量少于0.8g 时不成相;Na 2CO 3加入量在0.8~2.2g 时体系分成两相,上相为[Bmim]BF 4富集相,下相为盐相;Na 2CO 3加入量大于2.2g 时,出现盐不溶现象三向体系中加入1.5mL [Bmim]Cl 后,逐渐加入Na 2CO 3,当Na 2CO 3加入量少于2.2g 时不成相;Na 2CO 3加入量在2.2~2.4g 时体系分成两相,上相为[Bmim]Cl 富集相,下相为盐相;Na 2CO 3加入量大于
第期谷雨等:离子液体双水相技术萃取头孢呋辛酯及其机理探究
图5 离子液体双水相萃取头孢呋辛酯过程示意图
Fig.5 Schematic diagram of separating cefuroxime axetil in ILATPS.
图6 不同阴离子的离子液体双水相对头孢呋辛酯萃
取率的影响Fig.6 Different anions of ILATPS
of Cefu -
roxime axetil
2.4g 时,出现盐不溶现象三
[Bmim]BF 4和[Bmim]Cl 均可以萃取头孢呋辛酯,但考虑到[Bmim]Cl 在室温下呈现固态,需加热到70?才可溶解,且其成相范围窄,故[Bmim]BF 4用于双水相萃取头孢呋辛酯有明显优势三
3.6 应用3.6.1 分析方法验证 为了考察头孢呋辛酯测定方法的可靠性;对测定头孢呋辛酯含量的方法进行了专属性,线性,精密度的方法验证三
实验结果表明,空白双水相及空白水样在278nm 处对头孢呋辛酯的吸收无影响,在1.52?10-5~4.55?10-5mol/L 范围内,头孢呋辛酯的浓度和在278nm 的吸光度呈线性趋势,线性方程为A =18540C +
0.0005(R =0.9999),5次重复测定RSD 为0.084%,精密度良好三
3.6.2 萃取环境水样的头孢呋辛酯 为了检测离子液体双水相的实际效用,将其应用于实际水样中的药物萃取三,秦淮河水和自来水进行分析,将水样用布氏漏斗抽滤,用0.45m m 表2 [Bmim]BF 4/Na 2CO 3双水相在水样中萃取头孢呋辛脂结果
Table 2 Results of [Bmim]BF 4/Na 2CO 3ILATPS extraction of cefu -roxime axetil in real water sample
水样Sample 加入量Added (mmol/L)
萃取率Extraction (%)
相对标准偏差
RSD (%,n =5)
秦淮河水Qin Huai River
0.593.3 3.1193.2 4.51.593.5 3.6玄武湖水Xuan WuLake
0.5
92.5 5.4193.1 5.21.593.8 4.6自来水
Running Water
0.593.1 3.3193.3 4.31.5
94.0
5.2
微孔滤膜过滤,按辛酯含量三结果表明,各空白水样及溶剂在278nm 处并无吸收干扰,头孢呋辛酯残留三在最佳[4/
Na 2CO 3双水相组成条件下,采用标准加入法分别在3个水平萃取药物,一次萃取后,分离两相,下相中继续加入[Bmim]BF 4,进行二次萃取,合并两次萃取的上相,计算头孢呋辛酯萃取率和平行操作5次的RSD%三结果如表2所示,用[Bmim]BF 4/Na 2CO 3双水相系统萃取环境水样的头孢呋辛酯,萃取率大于93%,重现性好三
本研究建立了[Bmim]BF 4/Na 2CO 3双水相体系萃取头孢呋辛酯的新方法三考察了Na 2CO 3浓度,离子液体用量,离子液体种类对萃取率的影响,对萃取机理进行了初步探究,并将[Bmim]BF 4/Na 2CO 3双水相体系用于环境水样中的头孢呋辛酯萃取三结果表明,在一定范围内增加Na 2CO 3浓度和[Bmim]BF 4用量,可以提高萃取率;相对于[Bmim]Cl/Na 2CO 3体系,[Bmim]BF 4/Na 2CO 3双水相体系更适合萃取头孢
分析化学第40卷
呋辛酯;萃取的推动力主要是疏水性相互作用;环境水样萃取头孢呋辛酯的二次萃取率可以达到93%,重现性好,不易乳化三R e f e r e n c e s
1 L o n g n i D ,A l p e g
i a n iM ,C a b r iW ,F e l i s i C .P C T .W O ,03/024977A ,20032 M a d e i r aPP ,T e i x e i r aJA ,M a c e d oEA ,M i k h e e v aL M ,Z a s l a v s k y YB .J .C h r o m a t o g
r .A ,2008,1185(1):85~923 K e i t hEG ,G r a n tAB ,H e a t h e rD W ,J o n a t h a nG H ,R i c h a r dPS ,J o h nD H ,R o b i nDR.J .A m .C h e m .S o c .,2003,125(22):6632~6633
4 C H E N M i n g -L i ,F U H a i -K u o ,M E N G H a o ,WA N GJ i a n -H u a .C h i n e s e J .A n a l .C h e m .,2010,38(9):1299~1304陈明丽,付海阔,孟皓,王建华.分析化学,2010,38(9):1299~1304
5 L uY M ,L u WJ ,W a n g W ,G u oQ W ,Y a n g YZ .T a l a n t a ,2011,85(3):1621~1626
6 J i a n g Y Y ,X i aH S ,Y u J ,G u oC ,L i uH Z .C h e m .E n g .J .,2009,147(1):22~26
7 P e iYC ,W a n g J J ,W uK ,X u a nXP ,L uXJ .S e p a r .P u r i f .M
e t h o d ,2009,64(3):288~2958 S u s a n n eD ,P a u l i n aS ,U d oK.B i o c h e m .E n g .
J .,2009,46(2):176~1859 WA N GL i a n g ,Z HU H o n g ,S U N Y a n -T a o ,X U N Y i n g -J i e ,WA N G Q i n g -W e i ,Y A N Y o n g -S h e n g .C h i n e s e J .A n a l .C h e m .,2011,39(5):709~712
王良,朱红,孙艳涛,徐英杰,王庆伟,闫永胜.分析化学,2011,39(5):709~71210 H a n J ,W a n g Y ,Y uCL ,L i CX ,Y a nYS ,L i uY ,W a n g L .A n a l .C h i m .A c t a .,2011,685(2):138~14511 T r i n d a d e IP ,D i o g o M M ,P r a z e r e sD M F ,M a r c o s JC .J .C h r o m a t o g r .A ,2005,1082(2):176~18412 B i a n c oP H ,G r y cS .L a n g
m u i r .,2004,20(1):169~17413 B r i d g e sNJ ,G u t o w s k iK E ,R o g
e r sRD.G r e e nC h e m .,2007,9(2):177~18314 T r i n d a d e JR ,V i s a kZP ,B l e s i cM ,M a r r u c h o IM ,C o u t i n h o JAP ,L o p e s JNC ,R e b e l oLPN.J .P h y
s .C h e m .B ,2007,111(18):4737~4741
t r
a c t i o
na n dM e c
h a n i s mI
n v e s t i g
a t i o no fT r a c eC e f u r o x i m eA x e t i l W a t e r S a m p l e sU s i n g I o n i cL i q u i d -S a l tA q u e o u sT w o -p h a s e S y
s t e m G U Y u 1,H E H u a *1,
2,T A NS h u -H u a *1,L IY u e 1,H EJ i a 1
1
(D e p a r t m e n t o f A n a l y t i c a lC h e m i s t r y ,C h i n aP h a r m a c e u t i c a lU n i v e r s i t y ,N a n j i n g 210009,C h i n a )2(K e y L a b o r a t o r y o f D r u g Q u a l i t y C o n t r o l a n dP h a r m a c o v i g i l a n c e ,C h i n aP h a r m a c e u t i c a lU n i v e r s i t y ,
M i n i s t r y o f E d u c a t i o n ,C h i n aP h a r m a c e u t i c a lU n i v e r s i t y ,N a n j i n g 2
10009,C h i n a )A b s t r a c t A s a n e f f e c t i v e e x t r a c t i o nm e t h o d ,i o n i c l u e o u s t w o -p h a s e s y s t e m s (I L A T P S )b a s e d o n 1-b u t y l -
3-m e t h y l i m i d a z o l i u mt e t r a f l u o r a b o r a t e (F 4)a n dN a 2C O 3h a sb e e nu s e d t oe x t r a c t c e f u r o x i m e a x e t i l .E f f e c t s o f t h e i o n i c l i q u i d s c o n c e n t r a t i o n ,N a 2C O 3d
o s a g e a n ds o n i c l i q u i d s o n t h e e x t r a c t i o nh a v eb e e ni n v e s t i g a t e d .T h et h e r m o d y n a m i c p a r a m e t e r s (ΔG ?T ,n dΔS ?T )w e r e d e t e r m i n e d .T h o d w a sa p p
l i e dt ot h ed e t e r m i n a t i o no fc m ea x e t i l i nr e a lw a t e r s a m h e r e s u l t s t h a t e x t r a c t i o n e y o f c e f u r o x i m e a x f o u n d t o ew i t h i n c r N a 2C O 3a n ]B e r a n g 2C O 30.8-2.0g a n ]B F 41-2p a r e d w i t ]C l /N a 2C O 3P S ]B F 4O 3I L A T P Sh a sm o r ea d v a n t a g e s .T h e t h e r m o -d y n a m i c p a r a m e t e r sΔ,ΔH ?T >0,ΔS ?T >0i
l l u s t r a t et h a th y d r o p h o b i c i n t e r a c t i o n sw e r et h e m a i nd r i v i n g f o r c e i n t m ]B F 4/N a 2C O 3I
L A T P So f c e f u r o x i m e a x e t i l e x t r a c t i o n ,t h e e x t r a c t i o n p r o c e s s d i dn o to c c u re m u l s i f i c a t i o n .U n d e rt h eo p t i m u m c o n d i t i o n s ,m o r et h a n93%o f t h ec e f u -
r o x i m e a x e t i l i n r e a lw a t e r c o u l db e e x t r a c t e d i n t o t h e i o n i c l i q u i d -r i c h p h a s e i n a t w o -s t e p e x t r a c t i o n .K e y w o r d s I o n i c l i q u i d a q u e o u s t w o -p h a s e s y s t e m s ;E x t r a c t i o n ;C e f u r o x i m e a x e t i l (R e c e i v e d 21S e p t e m b e r 2011;a c c e p
t e d 22D e c e m b e r 2011)第期谷雨等:离子液体双水相技术萃取头孢呋辛酯及其机理探究
双水相萃取法的应用及研究进展 摘要:双水相萃取技术作为一项新的分离技术日益受到重视,它与传统的萃取及其它分离技 术相比具有操作条件温和、处理、量大、易于连续操作等优点,从而使其能广泛应用于生物分离工程中。本文介绍了双水相的形成、双水相萃取技术的基本原理以及影响物质分配系数的因素。同时对双水相萃取技术的研究进展及其应用进行了综述。 关键词:双水相萃取分离纯化进展 一:方法 随着基因工程、蛋白质工程、细胞培养工程、代谢工程等高新技术研究工作的广泛开展,各种高附加值的生化新产品不断涌现,对生化分离技术也提出了越来越高的要求。包括精馏、吸收、萃取、蒸发、结晶在内传统的分离技术有三大特点:分离过程伴随有相的变化;筛分过程不能实现分子级别的分离;精制过程成本极高,这些特征对于节约能源、生物分离、环境 保护、资源开发、替代能源、高纯材料等当代化学工程与科学技术发展不相适应。围绕以上几个问题的讨论就构成了分离技术研究与发展的主流,即新型分离技术产生的背景。双水相萃取技术始于20世纪60年代,从1956年瑞典伦德大学Albertsson发现双水相体系[2]到1979年德国GBF的Kula等人将双水相萃取分离技术应用于生物产品分离,虽然只有20多年的历史,但由于其条件温和,容易放大,可连续操作,目前,已成功的应用于蛋白质、核酸和病毒等生物产品的分离和纯化,双水相体系也已被成功的应用到生物转化及生物分析中。 双水相现象是当两种聚合物或一种聚合物与一种盐溶于同一溶剂时,由于聚合物之间或聚合物与盐之间的不相溶性,使得聚合物或无机盐浓度达到一定值时,就会分成不相溶的两相,因使用的溶剂是水,因此称为双水相原则上,无论是天然的还是合成的亲水聚合物,绝大多数在与另一种聚合物水溶液混合时都可分成两相,构成双水相体系。 双水相萃取与水一有机相萃取的原理相似,都是依据物质在两相间的选择性分配,但萃取体系的性质不同。当物质进入双水相体系后,由于表面性质、电荷作用和各种力(如憎水键、氢键和离子键等)的存在和环境的影响,使其在上、下相中的浓度不同。对于某一 物质,只要选择合适的双水相体系,控制一定的条件,就可以得到合适的分配系数,从而达到分离纯化之目的。 二:讨论 双水相萃取是一项可以利用不复杂的设备,并在温和条件下进行简单的操作就可获得较高收率和有效成分的新型分离技术。因此,广泛应用于生物化学、细胞生物学和生物化工等领域。然而有关双水相分配的基础研究还不够,工业化的一些关键问题还没有解决。为此,有必要加强这方面的基础研究,解决大规模萃取生物活性物质的工艺条件和设备方面的问题,促进双水相萃取技术的不断发展。 影响双水相萃取的因素比较复杂,主要包括静电作用、疏水作用和界面张力等。通过对各个因素的调节,可以极大地提高蛋白质的选择性,达到向一相富集的目的。A 1}'帅的组分性质千差万别,从晶体到无定形聚合物、从非极性到极性、从电解质到非电解质、从无扫L 小分子到有扫L高分子甚至生物大分子,这些都不可避免地造成理论计算的复杂性,以至 于现在还没有一套比较完善的理论来衡量各个影响因素之问的关系和解释生物大分子在体 系中的分配扫L理.有关A丁PS分配模型的研究中,较为成功的有的渗透维里模型,以及晶格模型。前者在预测聚合物的成相行为和蛋白质的分配上有较高的准确度;后者在粒子的能
综述与专论 离子液体在催化反应和萃取分离中的 研究和应用进展 顾彦龙 石 峰 邓友全 (中国科学院兰州化学物理研究所生态与绿色化学中心,甘肃兰州730000) 摘 要 离子液体研究已从/绿色0化学化工快速扩展到功能材料、能源、资源环境以及生命科学等领域,典型地体现了科学技术发展中的多学科交叉与综合.本文就离子液体在催化反应和萃取分离中的研究进展进行初步的总结与评述,以期为以后的研究工作提供参考.关键词 离子液体 催化 分离分析 绿色化学中图分类号 T Q 03117 文献标识码 A 文章编号 0438-1157(2004)12-1957-07 RESEARCH AN D A PPL ICA T ION OF ION IC LIQ U IDS IN CAT ALY SIS A ND SEPARAT ION GU Yanlong,SH I Feng and DENG Youquan (Centr e f or Gr een Chemistry and Catalysis,L anz hou I nstitute of Chemical Phy sics , Chinese A cademy of Sciences ,L anz hou 730000,Gansu ,China) Abstract The study of room temperature ionic liquids has been rapidly expanded into functional materials,energy,env ironmental protection and life sciences from green chemistry and chemical engineering,w hich typically demonstrates the interaction and integ ration of multiple disciplines in the development of science and technology.In this paper,the recent research and application of the room temperature ionic liquid in catalysis and separation are summarized and discussed to provide reference for future w ork.Keywords ionic liquid,catalysis,separation and analysis,green chemistry 2004-09-08收到初稿,2004-11-01收到修改稿. 联系人:邓友全.第一作者:顾彦龙,男,27岁,博士研究生. 基金项目:国家自然科学基金资助项目(No 120225309). 引 言 近年来,人们从生存和发展的经验教训中进一步认识到环境保护和可持续发展的重要性,实施从源头控制污染和清洁生产战略已形成了世界性的共识.在日趋激烈的化工市场中,对环境保护方面的严格要求促使化学化工与催化研究的重点也转向开发绿色和清洁技术以及环境友好催化体系等方向上来.而综合考察某一生产过程是否绿色化和清洁化 的标准包括反应物料的选择、催化体系的设计、废弃物的排放、能源利用的合理性以及产品绿色度等多个方面.严格的绿色化标准迫使人们去打破传统,寻找一种更理想的生产途径.在这方面,离子液体应运而生,正发挥着独特的作用. Received date:2004-09-08. Corresponding author:Prof.DE NG Youquan.E -mail:ydeng @ns 1lzb 1ac 1cn Foundation item:supported by the National Natural Sci ence Foun -dation of China (No 120225309). 离子液体是完全由特定阳离子和阴离子构成的在室温或近于室温下呈液态的物质.与固态物质相比较,它是液态的;与传统的液态物质相比较,它是离子的.因而,与其他固体或液体材料相比,离 第55卷 第12期 化 工 学 报 Vo l 155 l 12 2004年12月 Journal of Chemical Industr y and Engineer ing (China) December 2004
双水相萃取技术 早在1896年,Beijerinck发现,当明胶与琼脂或明胶与可溶性淀粉溶液相混时,得到一个混浊不透明的溶液,随之分为两相,上相富含明胶,下相富含琼脂(或淀粉,这种现象被称为聚合物的不相溶性(incompatibility,从而产生了双水相体系(Aqueous two phase system,ATPS。 传统的双水相体系是指双高聚物双水相体系,其成相机理是由于高聚物分子的空间阻碍作用,相互无法渗透,不能形成均一相,从而具有分离倾向,在一定条件下即可分为二相。一般认为只要两聚合物水溶液的憎水程度有所差异,混合时就可发生相分离,且憎水程度相差越大,相分离的倾向也就越大。可形成双水相体系的聚合物有很多,典型的聚合物双水相体系有聚乙二醇(polyethylene glycol,略作PEG/葡聚糖(dextran,聚丙二醇(polypropylene glycol/聚乙二醇和甲基纤维素(methylcellulose/葡聚糖等。另一类双水相体系是由聚合物/盐构成的。此类双水相体系一般采用聚乙二醇(polyethylene glycol作为其中一相成相物质,而盐相则多采用硫酸盐或者磷酸盐。 萃取原理 双水相萃取与水-有机相萃取的原理相似,都是依据物质在两相间的选择性分配。当萃取体系的性质不同时,物质进入双水相体系后,由于表面性质、电荷作用和各种力(如憎水键、氢键和离子键等的存在和环境因素的影响,使其在上、下相中的浓度不同。物质在双水相体系中分配系数K可用下式表示: K= C上/ C下 其中K为分配系数,C上和C下分别为被分离物质在上、下相的浓度。 分配系数K等于物质在两相的浓度比,由于各种物质的K值不同,可利用双水相萃取体系对物质进行分离。其分配情况服从分配定律,即,“在一定温度一定压强下,如果一个物质溶解在两个同时存在的互不相溶的液体里,达到平衡后,该物质在两相中浓度比等于常数”,分离效果由分配系数来表征。
高等分离工程课程论文双水相萃取技术的发展与应用 随着基因工程、蛋白质工程、细胞培养工程、代谢工程等高新生物技术研究工作的广泛展开,各种生化新产品不断涌现,对生化分离技术也提出了越来越高的要求。但由于大部分的生物产品原液是具有低浓度和生物活性的,对分离条件以及环境要求及其苛刻,使得传统的液液萃取已不能适应分离要求,因此一种新型的液液分离技术-双水相萃取技术应运而生,双水相萃取技术是利用组分在两水相间分配的差异而进行组分的分离提纯的技术。由于双水相萃取分离过程条件温和、可调节因素多、易于放大和操作,并可借助传统溶剂萃取的相关理论和经验,不存在有机溶剂残留问题,特别适用于生物物质的分离和提纯。目前,双水相萃取技术已被广泛地应用于医药化学、细胞生物学、生物化工和食品工业等领域,被认为是生物工程中一种具有广阔应用前景的分离技术,在电化学生物传感器中生物活性分子的制备中至关重要。 1 双水相萃取的基本要点 1.1 双水相萃取的原理 双水相萃取是依据物质在两相间的选择性分配,但萃取体系的性质不同。当 物质进入双水相体系后,由于表面性质、电荷作用和各种力(如憎水键、氢键和 离子键等)的存在和环境的影响,使其在上、下相中的浓度不同。对于某一物质,
只要选择合适的双水相体系,控制一定的条件,就可以得到合适的分配系数,从而达到分离纯化之目的。 将两种不同的水溶性聚合物的水溶液混合时,当聚合物浓度达到一定值,体系会自然的分成互不相溶的两相,这就是双水相体系。双水相体系的形成主要是由于高聚物之间的不相溶性,即高聚物分子的空间阻碍作用,相互无法渗透,不能形成均一相,从而具有分离倾向,在一定条件下即可分为二相。一般认为只要两聚合物水溶液的憎水程度有所差异,混合时就可发生相分离,且憎水程度相差越大,相分离的倾向也就越大。 1.2 双水相的种类 双水相萃取中使用的双水相是由两种互不相溶的高分子溶液或者互不相溶的盐溶液和高分子溶液组成。最常见的就是聚乙二醇(PEG)/葡聚糖(Dextran)和PEG/无机盐(硫酸盐、磷酸盐等)体系,其次是聚合物/低分子量组分、离子液体体系和高分子电解质/高分子表面活性剂体系。此外,还有被称为智能聚合物的双水相体系,智能聚合物又称刺激-响应型聚合物(Stimulus-responsive polymers)或环境敏感聚合物(Environmentally-sensitive polymers)。智能聚合物是一种功能高分子材料,当外界环境(如温度、pH值、离子强度、外加试剂、光、电场或磁场等)发生微小变化时,聚合物分子的微观结构会发生快速、可逆的转变,使其从亲水性变为疏水性。智能聚合物的双水相体系有:温度敏感型双水相体系、酸度敏感型双水相体系、光响应型双水相体系、亲和功能双水相体系。 1.3 双水相萃取体系的特点 双水相萃取技术设备简单、在温和条件下进行简单操作就可获得较高的收率和纯度。与一些传统的分离方法相比,双水相萃取技术具有以下特点: (1) 整个体系的含水量高 (70% ~90% ) ,萃取是在接近生物物质生理环境的条件下进行,故而不会引起生物活性物质失活或变性; (2) 单级分离提纯效率高。通过选择适当的双水相体系,一般可获得较大的分配系数,也可调节被分离组分在两相中的分配系数,使目标产物有较高的收率;(3) 传质速率快,分相时间短。双水相体系中两相的含水量一般都在 80%左右,界面张力远低于水-有机溶剂两相体系,故传质过程和平衡过程快速;
一种基于分散液液位萃取发展的使用离子液体对水样中多环芳烃进行分析的方法 马修女佩纳,马卡门卡赛斯,马卡门梅胡托,拉斐尔切拉 分析化学系,营养与食品科学,食品研究和分析,圣地亚哥德孔波, 15782圣地亚哥德孔波斯特拉,西班牙大学。 文章信息: 文章历史: 收稿日期 2009年 4月 15日 修订日期 2009年 7月 9日 接受于 09年 7月 17日 网上提供 XXX 关键词: 多环芳烃、离子液体、分散液液萃取、水质分析、液相色谱 摘要: 一种简单,快速,有效的基于离子液体 -分散液液微萃取(IL-DLLME 技术第一次测定了水样中 18种多环芳烃 (PAHs的含量。离子液体(1-辛基 -3-甲基咪唑六氟磷酸盐与可以从多环芳烃样本基质中提取的分析物之间的化学亲和力使他们能够富集起来。因此,这种技术结合了提取、浓缩分析物为一体,避免了使用有毒的氯化溶剂。影响萃取效率的因素, 比如离子液体的类型和体积, 分散剂的类型和体积,萃取时间,分散步骤,离心时间和离子强度等都得到了优化。萃取物的分析采用高效液相色谱法(HPLC 与荧光检测器(Flu 。该优化方法呈现良好的精确度,只有 1.2%到 5.7%的标准偏差值。对所有这些考虑的化合物, 其检测限(在 0.1 到7 ng L- 1之间
都低于欧盟建议的限制。分散液液微萃取对不同化合物的萃取率介于 90.3%至103.8%之间。此外也实现了较高的富集因子(301-346。该优化方法的萃取率与液液萃取作比较。最后,该方法已成功应用于实际水样的多环芳烃分析 (自来水、瓶装水、喷泉、井水、河水、雨水、废水处理及原废水 2009, Elsevier B.V.版权所有。 1. 导言 有必要在环境管制法例中列出一些多环芳烃的毒性性质 [1,2]。许多环保机构为了保护环境和人类健康,将饮用水和天然水中多环芳烃限制在非常低的水平。 在饮用水方面,美国环境保护署(EPA 和世界卫生组织(WHO 建议例行监测苯并[a]芘(B[a]P . 美国环保局规定,其最高浓度不得超过200 ng L- 1 [3], 而世界卫生组织规定的苯并 [a]芘的最高容许浓度为700 ng L - 1[4]。除了到 B [a]芘,欧盟的指令 98/83/EC [5]的规定苯并 [b]荧蒽 (B[b]F,苯并 [k]荧 (B[k]F, 苯并 [g,h,i]苝 (B[g,h,i]P 和 . 茚并 [1,2,3 - C 类, D]芘 (I[1,2,3-c,d]P。最高污染物水平值分别定为 , 对剧毒 B[a]P为10ngL - 1,对剩余的多环芳烃的总量为100ngL - 1。 欧盟也对浅水域的不同类型下的这类化合物制定了非常严格的限制。对 B[a]P 的限制是年平均值为50ngL - 1、最高容许浓度为100 ngL - 1。对 B[b]F– B[k]F 和 B[g,h,i]P– I[1,2,3-c,d]P的年平均值和最高容许浓度分别限制在30 ngL- 1和2ngL - 1,作为。萘(Naph, 1200 ngL - 1,荧蒽(Flt, 100 ngL - 1和蒽(Anth, 100 ngL - 1也包括在这个指令中。 美国环保局和欧盟制定了水中低浓度多环芳烃的常规量化, 这需要高效合理的分析方法的发展。这些化合物通常用液液萃取 (LLE [8,9]和固相萃取 (SPE [10]两种方法从水样中提取。然而, 现在分析化学的趋势是简化样品的制备。因此, 在过去几年里, 微技术在辨别多环芳烃方面正发挥着重要的作用。固相微萃取 (SPME [11],搅拌吸附萃取 (SBSE[12]和液相微萃取 (LPME [13,14]已经替代了传统的 LLE 和 SPE 技术。
离子液体在分离提纯中的应用 发表时间:2017-06-15T10:56:08.377Z 来源:《基层建设》2017年6期作者:张艳平[导读] 本文主要介绍了离子液体在分离分析上的应用及近几年离子液体研究应用的进展。 安徽太平矿业有限公司安徽省宿州 234000 摘要:室温离子液体是熔点在室温附近的一类熔融盐,以熔点低、蒸汽压小、电化学窗口宽、酸性能调节及良好的溶解性等诸多特点在电化学、有机合成、催化、分离、提纯等领域应用广泛。本文主要介绍了离子液体在分离分析上的应用及近几年离子液体研究应用的进展。现在所要解决的核心问题就是离子液体在萃取分离提纯过程中的应用,并展望了离子液体在分离方面的应用前景和发展方向。 关键词:离子液体;分离;合成;提纯;应用 1、导言 室温离子液体,简称离子液体, 是一类室温或相近温度下完全由离子组成的有机液体化合物。它一般由有机阳离子和无机阴离子相互结合而成的一种室温或低温下呈液态的盐类化合物。与一般有机溶剂不同,离子液体很难挥发,所以实验室使用它无毒性且无污染。并且,我们很轻松地从离子液体中萃取出产物进一步回收催化剂,可以实现多次循环使用这些液体进而实现了绿色化的合成,因此它被称为”绿色溶剂”。离子液体因其诸多特点在电化学、有机合成、催化、分离等多方面领域得到广泛的应用。 2、离子液体的合成和性质 2.1离子液体的合成 离子液体的种类很多,改变阳离子、阴离子可以有不同的组合,可以设计合成出多种不同的离子液体。具有代表性的离子液体合成是由甲基咪唑与卤代烷烃直接合成中间产物,然后再与含有目标负离子的无机盐离子或有机盐离子反应生成相应的离子液体。 2.2 离子液体的性质 2.2.1熔点熔点是无机盐、有机盐等化合物的一个重要的物理特征,也是判别其是否构成离子液体的重要标志。目前对于某些盐类熔点低的原因不是很清楚,大多数认为可能有以下几个原因:组成盐类化合物的阳离子对称性较低;分子间的相互作用弱(如氢键等);电荷平均分布在阳离子上,以及晶体的低效堆积]等。 2.2.2粘度离子液体的粘度主要取决于离子液体间范德华作用力大小以及形成氢键的能力。离子液体的粘度和范德华作用力的关系可由1-甲基-3-丁基咪唑离子液体的粘度随阴离子变化的结果中得出,当阴离子CF3COO-变为C3F7COO-时,离子液体的粘度明显增加。这是因为C3F7COO-阴离子具有更强的范德华力作用。 2.2.3密度现在研究大多认为:离子液体的密度主要取决于组成离子液体的阴离子和阳离子。选择合适的阴离子确定离子液体的密度范围,而选择合适的阳离子则可以更精细的调节离子的密度。 2.2.4电导率和电化学窗口RTILs在纯度较高时有极好的的导电性,较高的离子迁移率,稳定而又较宽的电化学窗口。氯铝酸离子液体的电导率和电化学窗口都与氯化铝和季铵盐的摩尔比有关系。 2.2.5蒸汽压及溶解性离子液体与水分子及其他溶剂相比,其内部存在非常大的库仑作用力,一价的异号离子间的相互作用能最大可达100千焦每摩,这是水的十倍。因此RTILs在较高的温度和真空度下也会保持相当低的蒸汽压力。由于RTILs具有很强的极性,对多种有机化合物、无机化合物以及多种聚合材料具有特殊的溶解能力,是唯一能够溶解各种氢化物(如NaH和CaH2)、碳化物、氮化物、以及各种氧化物和硫化物等相当多化合物的理想溶剂。 3、离子液体在分离提纯中的应用 3.1离子液体在萃取、分离中的应用 分离提纯回收产物始终以来一直是化学合成中的难题。用水做溶剂进行萃取分离有机物一般只适用于亲水性物质,而且蒸馏技术也不能用于蒸发性较差的物质,过多的使用有机溶剂又会引起物质之间的交叉污染。离子液体在液-液萃取分离上,离子液体溶剂能溶解多种有机化合物、无机化合物、有机金属化合物、无机金属化合物,同时离子液体与大多数有机溶剂不发生混溶,这就是说离子液体更加适合作为液-液萃取的新介质。 3.2离子液体在毛细管电泳中的应用 由于RTILs具有超高的电导率,可作为电解质添加剂用于毛细管电泳分离。Yanes等认为,离子液体在毛细管表层形成了一层带电荷的薄层(见图1),离子液体的咪唑阳离子与样品相互作用促进了样品在毛细管中的迁移进而导致色谱分离。他们分离了一系列酚类化合物,并且考察了不同烷基取代的离子液体对萃取分离中的影响。得到了较好的分离效率和色谱重复性。Jiang等采用类似的方法分离了溶菌酶、细胞图1 色素、胰蛋白酶原和胰凝乳蛋白酶原等碱性蛋白,同样得到了比较好的分离效率和色谱重复性。 3.3离子液体在气相色谱上的应用 离子液体作为气相固定相表现出两种不同与其他物质的特性。当分离的样品是中性或非极性样品时,样品在色谱柱上的保留与样品在其他非极性色谱柱上的保留是一致的,结果还表明,阴离子为氯离子的离子液体与含有强给电子和推电子基团的样品具有强的作用。 3.4离子液体在液相色谱中的应用
双水相萃取技术 D09生物张燊睿092203112 内容提要:本文主要叙述双水相萃取技术的概念,原理,操作,未来发展方向以及在生物、食品工业中的应用。 Abstract:This paper mainly describes the two aqueous phase extraction technology concept, principle, operation, the future development direction as well as in the biological, food industry application 关键词:萃取、分离、双水相体系、提取、生物分离、未来发展、亲和作用。 引言:随着基因工程、蛋白质工程、细胞培养工程、、代谢工程等高新技术研究工作的广泛的开展,各种高附加值得食品生化新产品不断涌现,对食品、生化等分离技术提出了越来越高的要求。包括精馏、吸取、萃取、蒸发、结晶在内传统的分离技术的三大特点:分离过程伴随有相的变化;筛分过程不能实现分子级别的分离;精制过程成本极高,这些特征对于节约能源、生物分离、环境保护、资源开发、替代能源、高纯材料等当代化学工程与科学技术不相适应。围绕以上几个问题的讨论就构成了分离技术研究与发展的主流,即新型分离技术产生的背景。 双水相系统:基因工程产品如蛋白质和酶往往是胞内产品,需经细胞破碎后才能提取、纯化,细胞颗粒尺寸的变化给固-液分离带来了困难,同时这类产品的活性和功能对pH值、温度和离子强度等环境因素特别敏感。由于它们在有机溶剂中的溶解度低并且会变性,因此传统的溶剂萃取法并不适合。采用在有机相中添加表面活性剂产生反胶束的办法可克服这些问题,但同样存在相的分离问题。当两种聚合物、一种聚合物与一种亲液盐或是两种盐(一种是离散盐且另一种是亲液盐)在适当的浓度或是在一个特定的温度下相混合在一起时就形成的。 例如用聚乙二醇(PEG Mr为6000)/磷酸钾系统从大肠杆菌匀浆中提取β-半乳糖苷酶。这是一个很有前途的新的分离方法,特别适用于生物工程得出的产品的分离。 一.双水相萃取原理: 双水相萃取技术又称水溶液两相分配技术(partition of two aqueoue phase system)近年来发现的、引人注目的、极有前途的新型分离技术。早在1896年,荷兰微生物学家Beijerinck[1]发现,把明胶与琼脂或明胶与可溶性淀粉溶液混合时得到一种不透明的混合溶液,静止后风味两相,上相含大部分水,下相含大部分琼脂,而两相的主要成分都是水,人们把这种现象称为聚合物的不相溶性,由此产生了双水相萃取。1955年,瑞典伦德大学的Albertsson[2]首次利用双水相技术从单细胞藻类中分离淀粉核,从此开创了双水相分配技术。1979年德国GBF 的Kula和Kroner等[3]水相体系用于提取酶和蛋白质,使胞内酶提取过程大为改善。几十年来,国内外的研究者们已经就双水相分配技术的各个方面展开了系统的研究,包括新型双水相体统的开发,成相机理研究、系统物性的测定、热力学性质的研究生物大分子及小分子活性物质的分配、萃取工艺流程的设计、工业化大生产中的应用以及聚合物的回收等等,并取得很大进展。 双水相萃取的聚合物不相容性:根据热力学第二定律,混合是熵增过程可以自发进行,但分子间存在相互作用力,这种分子间作用力随相对分子质量增大而增大。当两种高分子聚合物之间存在相互排斥作用时,由于相对分子质量较大
[收稿日期] 2007-05-29;修回日期 2007-09-29 [基金项目] 云南省中青年学术技术带头人后备人才培养计划(2006PY 01-50);云南省应用基础研究计划项目(2006E 0032M ) [作者简介] 刘利梅(1978-),女,内蒙古商都县人,云南师范大学化学化工学院硕士研究生,主要研究方向为离子液体合成与应用;苏永庆 (1964-),男,云南昆明市人,云南师范大学化学化工学院教授,博士,E 唱mail :su -yongqing @yahoo .com 离子液体在金属离子萃取中的研究进展 刘利梅,苏永庆,李 琮,贺 飞,何永福,钟 云 (云南师范大学化学化工学院,昆明 650092) [摘要] 介绍了离子液体的定义,发展历史,性质等,重点阐述用于金属离子萃取的离子液体的性质、合成方法和发展方向。 [关键词] 离子液体;萃取;金属离子;绿色溶剂 [中图分类号] TQ 028畅3+ 2 [文献标识码] A [文章编号] 1009-1742(2007)11-0187-04 随着人们环境保护意识的提高,传统的易挥发性有机溶剂给环境所造成的污染受到越来越多的关注。寻找无公害、对环境友好的绿色溶剂来代替传统有机溶剂已势在必行。近年来一种新型的物质———离子液体,受到化学家们的广泛关注。离子液体是离子态的有机物质,蒸气压极小,不易挥发,不易燃,对热稳定,是近年来绿色化学的热点研究领域之一;又因其独特的性质,在有机合成、物质分离[1] 、 电化学 [2] 等领域的应用中显示了广阔的应用前景。 液液萃取分离过程作为一种有效的分离方法,应用的范围极为广泛,在传统的萃取操作过程中,萃取剂的选择通常是以萃取效果为衡量标准,对环境的影响考虑较少,致使大量使用挥发性强、易燃、易挥发、有一定毒性的有机溶剂,给环境带来了严重污染。按照绿色化学的思想,将来液液萃取分离过程必须使用绿色溶剂,从源头上消除传统有机萃取剂对环境的污染,把整个工艺过程变成绿色环保工艺 [3] 。 离子液体不可燃、不挥发且可溶解许多有机、无 机化合物,是新型萃取溶剂的发展方向。许多文献 [4~6] 报道了利用离子液体萃取水中的有机物、金 属离子的研究,结果表明离子液体作为萃取溶剂在液-液萃取中有极大的应用价值。文章即介绍室温离子液体对金属离子萃取分离方面的研究进展 情况。 1 离子液体简述 1.1 离子液体定义 离子液体是指呈液态的离子化合物,如熔融状态的氯化钠。离子化合物通常为无机金属化合物,在室温时都是固体,所以在以往的印象中离子液体必然是与高温相联系的,但高温状态下,物质活性大、易分解,很少作为反应或分离溶剂使用。另外,离子液体也不等同于电解质溶液,在这种液体中没有电中性的分子,完全由阴离子和阳离子组成。目前在学术界最为关注的所谓离子液体,是指在室温或者室温附近很大的温度范围内均为液态的离子化合物 [7] ,又称室温离子液体或室温熔融盐,即在室温 及相近温度下完全由离子组成的有机液体化合物。1.2 离子液体的发展历史简介 离子液体的历史[8] 并不是很长,第一个有文献 记载的离子液体是在1914年发现的[EtNH 3][NO 3] (硝酸乙基胺) [9] ,熔点为12℃,干燥时易爆炸。也 有一些学者认为第一个离子液体或者室温熔盐可以追溯到19世纪中期,是在傅克反应中观察到的“红油”,当时这个发现并没有受到重视。1948年美国专利 [10~12] 报道了主要用于电镀领域的AlCl 3型离子 液体,他们把卤化乙基吡啶和无水AlCl 3混合时,制 7 812007年第9卷第11期
双水相萃取和超临界萃取的方法与特点 专业生物工程092 课程酶工程 老师王明力 学生吴志洪 学号 0908110342 2012年12月25日
双水相萃取和超临界萃取的方法与特点 摘要:双水相萃取技术是一种高效温和的新分离技术,它与传统的萃取及其它分离技术相比具有操作条件温和、处理量大、易于连续操作等优点,从而使其能广泛应用于生物分离工程中。同时文章简要介绍了超临界流体萃取的基本原理和特点及其应用,其中超临界CO2萃取是最常用的.随着研究的深入和认识的加强,超临界流体技术作为一项可持续的绿色工艺,将具有广泛的应用前景。 关键词:双水相萃取超临界流体萃取 Abstract: Phasepartitioning technology is a kind of high efficient mild new separation technique ,and the traditional extraction and other separation technology compared with mild conditions, large quantity of operation, easy for operation, which makes its advantages such as extensively applied in biological separation engineering.And his article introduces the basic principle of supercritical fluid extraction and it,s application ,The supercritical CO2extraction is the most commonly used.With the deepening of research and understanding of the strengthen, supercritical fluid technology as a sustainable green technology, has a broad prospect of application.
摘要利用离子液体1甲基3丁基咪唑六氟磷酸盐(C4)和1甲基3己基咪唑六氟磷酸盐(C6)以及传统有机溶剂二氯甲烷作萃取溶剂,研究了它们在不同条件下萃取水环境中的环境内分泌干扰物壬基酚和辛基酚的萃取性能,结果表明,二氯甲烷达萃取平衡的时间(20 min)比离子液体(60 min)短;当水相的pH值发生变化时,离子液体和二氯甲烷的萃取率均随pH值的增大而降低;盐析效应显示离子液体受盐效应影响很小,而二氯甲烷受盐效应的影响大;壬基酚和辛基酚浓度增大导致萃取率降低; 离子液体和二氯甲烷的萃取率均随温度的升高而升高,适当的提高温度有利于萃取率的提高。用离子液体萃取水溶液中有机物质,表现出和传统萃取溶剂相类似的一些性质,如酸度、温度、分析物的浓度均对其萃取率有一定影响。 关键词离子液体,二氯甲烷,萃取性能,壬基酚,辛基酚 1 引言 本实验选择了最常用的、在空气和水中都稳定的离子液体1甲基3丁基咪唑六氟磷酸盐(以下简称C4)和1甲基3己基咪唑六氟磷酸盐(以下简称C6)以及传统有机溶剂二氯甲烷作萃取溶剂,比较了它们萃取水环境中的环境内分泌干扰物壬基酚和辛基酚的萃取性能。结果表明:离子液体与传统有机溶剂相比,在液液萃取中既有相似之处,也有其独特的地方。离子液体取代传统有机溶剂应用于溶剂萃取具有潜在的发展前景。 2 实验部分 2.1 仪器与试剂 THZC型恒温振荡器l为分析纯,NaOH和HCl为优级纯,壬基酚和辛基酚为标准品。离子液体C4(由1甲基3丁基咪唑阳离子和六氟磷酸阴离子组成);离子液体C6([HMIM][PF6],由1甲基3己基咪唑阳离子和六氟磷酸阴离子组成),离子液体C4、C6按照文献[2]合成,其结构经核磁共振和红外谱图确证, 2.2 实验方法 色谱柱:C18柱(5 μm,200 mm×4.6 mm i.d.,Kromasil);检测器:荧光检测器;激发波长223 nm,发射波长302 nm;流动相:乙腈∶水=4∶1(V/V),流速:1 mL/min;柱温:35℃;进样量:20 μL。 萃取过程:将萃取溶剂0.4 mL加入20 mL具塞离心管中,再加入水样(含壬基酚和辛基酚均为50 μg/L)20 mL,放入恒温摇床中振荡,控制一定的温度,转速为120 r/min,萃取一定时间后,静止分层,用滴管小心将上层水相移出,下层离子液体加乙腈至1 mL,直接进液相色谱测定壬基酚和辛基酚的含量,二氯甲烷用N2气吹干,加乙腈至1mL,直接进液相色谱测定,水相中的壬基酚和辛基酚的含量采用物料衡算法求得,经实验验证,用反萃取法测得的含量与物料衡算法求得的含量相对偏差小于10%。 3 结果与讨论 3.1 萃取平衡时间比较 以离子液体C4和C6及传统有机溶剂二氯甲烷为萃取溶剂萃取水样中的壬基酚和辛基酚,分别萃取5、10、20、30、60、90和120 min,测得相应的萃取率,探求达萃取平衡的时间,随着时间的推移,离子液体C4和C6对壬基酚和辛基酚的萃取率呈上升趋势,在60 min 达到最大萃取率,60 min以后萃取率基本保持不变,可以推断在60 min时壬基酚和辛基酚在两相间的分配达到了平衡,以下用离子液体作萃取溶剂时,时间均设定为60 min。由图2b 可见,随着时间的推移二氯甲烷对壬基酚和辛基酚的萃取率到20 min时达到最大值。20~30 min萃取率保持不变,所以在20 min时达到萃取平衡。30 min后,萃取率下降,这主要是
简述离子液体及其在萃取分离中的研究应用 摘要:离子液体作为一种环境友好的新型绿色溶剂,具有独特的性质,目前已在萃取分离领域得到很好的研究和应用.本文重点介绍了离子液体在萃取分离有机物、金属离子、气体分子和生物分子方面的应用研究。关键词:离子液体;萃取;分离; 1.引言 目前广泛应用的萃取分离技术有液相萃取、固相萃取、微波萃取、液膜萃取等.随着近几年绿色化学的兴起,离子液体作为继超临界流体CO2以来的又一新型溶剂,在样品前处理中分离、富集的应用也得到进一步发展,给传统的萃取分离注入了新的内容. 离子液体是一类新型的绿色介质,具有不易挥发、导电性强、粘度大、蒸气压小、性质稳定、可设计性、对许多无机盐和有机物有良好的溶解性等优点,因而其应用领域非常广泛,目前离子液体已在萃取分离、电化学、化学、环境、生物技术、材料等诸多领域都得到开发和应用。基于离子液体萃取效率高、可循环利用等优点,其在传统的萃取中的应用研究很多,并且具有广泛的应用前景。 2.离子液体简介 2.1 离子液体的结构和分类 离子液体,又称室温离子液体,或室温熔融盐,是指在室温或接近室温时呈液态,并由有机阳离子和无机阴离子组成的熔融盐体系.按照阴阳离子排列组合方式的不同,离子液体的种类有很多.目前通常根据有机阳离子母体的不同,将离子液体分为4类,分别是咪唑盐类(I)、季铵盐类(II)、吡啶盐类(Ⅲ)、季膦盐类(IV)[1].离子液体的种类并不仅限于此,其他代表性的离子液体还有锍盐离子液体、手性离子液体,两性离子液体等。 2.2离子液体的特点 与传统有机溶剂和电解质相比,离子液体的主要特点是:①蒸汽压低,不易挥发;②具有较大的稳定温度范围和较高的化学稳定性;③具有较大的结构可调性,适合用作分离溶剂;④具有介质和催化双重功能,对于许多无机和有机物质溶解性好;⑤离子液体作为电解质具有较大的电化学窗口、导电性、热稳定性和抗氧化性等[2]。总之离子液体兼有液体与固体的功能特性,因此被称为“液体”分子筛. 3.离子液体在萃取分离中的应用
(19)中华人民共和国国家知识产权局 (12)发明专利申请 (10)申请公布号 (43)申请公布日 (21)申请号 201910140429.3 (22)申请日 2019.02.26 (71)申请人 中国科学院城市环境研究所 地址 361021 福建省厦门市集美区集美大 道1799号 申请人 中国科学院大学 (72)发明人 付明来 徐垒 (51)Int.Cl. C22B 7/00(2006.01) C22B 26/12(2006.01) C22B 47/00(2006.01) C22B 23/00(2006.01) (54)发明名称 一种利用离子液体萃取锂离子电池浸出液 金属离子的方法 (57)摘要 本发明属于废旧锂离子电池正极材料回收 再利用技术领域。本发明提供一种基于离子液体 的绿色萃取分离方法,实现废旧镍钴锰酸锂电池 正极片浸出液金属离子的萃取分离。本发明涉及 的一种利用离子液体萃取锂离子电池浸出液金 属离子的方法,包括萃取、分离、反萃取等步骤, 实现废旧锂电池浸出液金属离子的萃取分离,无 需添加有机溶剂稀释剂,萃取剂稳定性好,能够 多次循环利用, 萃取容量高。权利要求书1页 说明书3页 附图1页CN 109694957 A 2019.04.30 C N 109694957 A
权 利 要 求 书1/1页CN 109694957 A 1.一种利用离子液体萃取锂离子电池浸出液金属离子的方法,其特征在于,包括以下步骤: (1)萃取过程: 离子液体中加入一定体积的水以降低粘度,取萃取剂与锂电池正极片金属离子浸出液以一定体积比混合,在30-80摄氏度条件下,振荡混合一定时间; (2)分离过程: 5000转每分钟的条件下,离心2分钟,萃取相与萃余相分层,分离两相; (3)反萃过程: 萃取相中加入一定体积的反萃取剂混合,在30-80摄氏度条件下,振荡混合一定时间,分层后分离两相,得到再生的离子液体。 2.根据权利要求1所述的一种利用离子液体萃取锂离子电池浸出液中金属离子的方法,其特征在于,所用的离子液体为三己基十四烷基氯化膦、三己基十四烷基溴化膦或三正丁基十四烷基氯化膦中的任意一种。 3.根据权利要求1所述的一种利用离子液体萃取锂离子电池浸出液中金属离子的方法,其特征在于,锂离子电池浸出液为钴酸锂电池浸出液、镍钴锰酸锂电池浸出液、锰酸锂电池浸出液、磷酸铁锂电池浸出液中的任意一种。 4.根据权利要求1所述的一种利用离子液体萃取锂离子电池浸出液中金属离子的方法,其特征在于,离子液体中为降低粘度,加入水的体积为离子液体体积的1%-30%。 5.根据权利要求1所述的一种利用离子液体萃取锂离子电池浸出液中金属离子的方法,其特征在于,萃取剂与锂电池正极片金属离子浸出液的体积比为2:1、1:1、1:2、1:3中的任意一种。 6.根据权利要求1所述的一种利用离子液体萃取锂离子电池浸出液中金属离子的方法,其特征在于,萃取/反萃取温度条件为30-80摄氏度。 7.根据权利要求1所述的一种利用离子液体萃取锂离子电池浸出液中金属离子的方法,其特征在于,萃取/反萃取振荡时间为5-60分钟。 2
一、双水相系统的相图绘制 1.实验目的 了解制作双水相系统的相图的方法,加深对相图的认识。 2.实验原理 相图是研究两水相萃取的基础,双水相形成条件和定量关系常用相图来表示。图1是典型的高聚物-高聚物-水双水相体系的直角坐标相图,两种聚合物A、B以适当比例溶于水就会分别形成有不同组成、度的两相,上相组成用T点表示,下相组成用B点表示,由图1可知上下相所含高聚物有所偏重,上相主要含B,下相主要含A。曲线TCB称为结线,直线TMB称为系线。结线上方是两相区,下方为单相区,若配比取在曲线上,则混合后,溶液恰好从澄清变为混浊。组成在系线上的点,分为两相后,其上下相组成分别为T和B,T、B量的多少服从相图的杠杆定律。即T和B相质量之比等于系线上MB与MT的线段长度之比。又由于两相密度相差很小,故上下相体积之比也近似等于系线上MB与MT线段长度之比。 图1 A-B-水双水相体系相图 O aqueous two-phase system Figure 1 The phase diagram of the A-B-H 2 3.实验器材和试剂 (1)器材:电子台秤,漩涡混合器,大试管,滴定管,密度计,温度计。(2)试剂:聚乙二醇,硫酸铵,硫酸镁。 4.操作方法 (1)溶液的配制 配制40%的盐(硫酸铵或硫酸镁)溶液 配制40%的聚乙二醇溶液,液体聚乙二醇可用纯溶液。 (2)相图的制作
精确称取一定质量(0.7000g 左右)PEG 溶液于大试管中,按表1所列第1列数据,加入0.5mL 去离子水,用滴定管缓慢滴加已配好的40%的盐溶液,并不断在漩涡混合器上混合,观察溶液的澄清程度,直至试管内液体出现浑浊为止。记录盐溶液的加量(g)。然后,按表格所列第2列数据加入水,溶液澄清,继续向试管中滴加盐溶液并不断混匀,直至再次达到浑浊,如此反复操作。计算每次达到浑浊时,PEG 和盐在系统总量中的质量分数,将实验数据填入表中,以PEG 的质量分数为纵坐标,某种盐的质量分数为横坐标作图,即得到一条双节线的相图。 表1相图制作表 编 号 水 /g (NH 4)2SO 4溶液加量/g 纯(NH 4)2SO 4累计量/g 溶液累计总量/g (NH 4)2SO 4质量分 数/% PEG 质量分数/% 1 0.5 3.1315 0.895 4.3786 20.4 4.79 2 0.3 2.1792 1.5186 5.9511 21.85 3.02 3 0.3 2.0456 2.1 9.2867 22.65 2.26 4 0.3 3.1372 3.0 12.6738 23.68 1.65 5 0.5 6.0769 4.7 19.3276 24.52 1.08 6 0.5 6.1909 6.5 26.0138 25.02 0.8 7 0.5 6.8585 8.5 33.4596 25.32 0.62 根据以上数据以(NH 4)2SO 4质量分数为横坐标,以PEG 质量分数为纵坐标即可做出相图。 二、双水相系统比例的选择 根据相图,选择五个成相比例。 三、蛋白酶酶活标准曲线的绘制—— Folin 酚法或紫外分光光度法 PEG4000与MgSO4双水相图 y = 0.0995x 2 - 5.3887x + 73.334 2012345 6 20 21 22 2324 25 26 MgSO4% P E G 4000%