
染色体变异
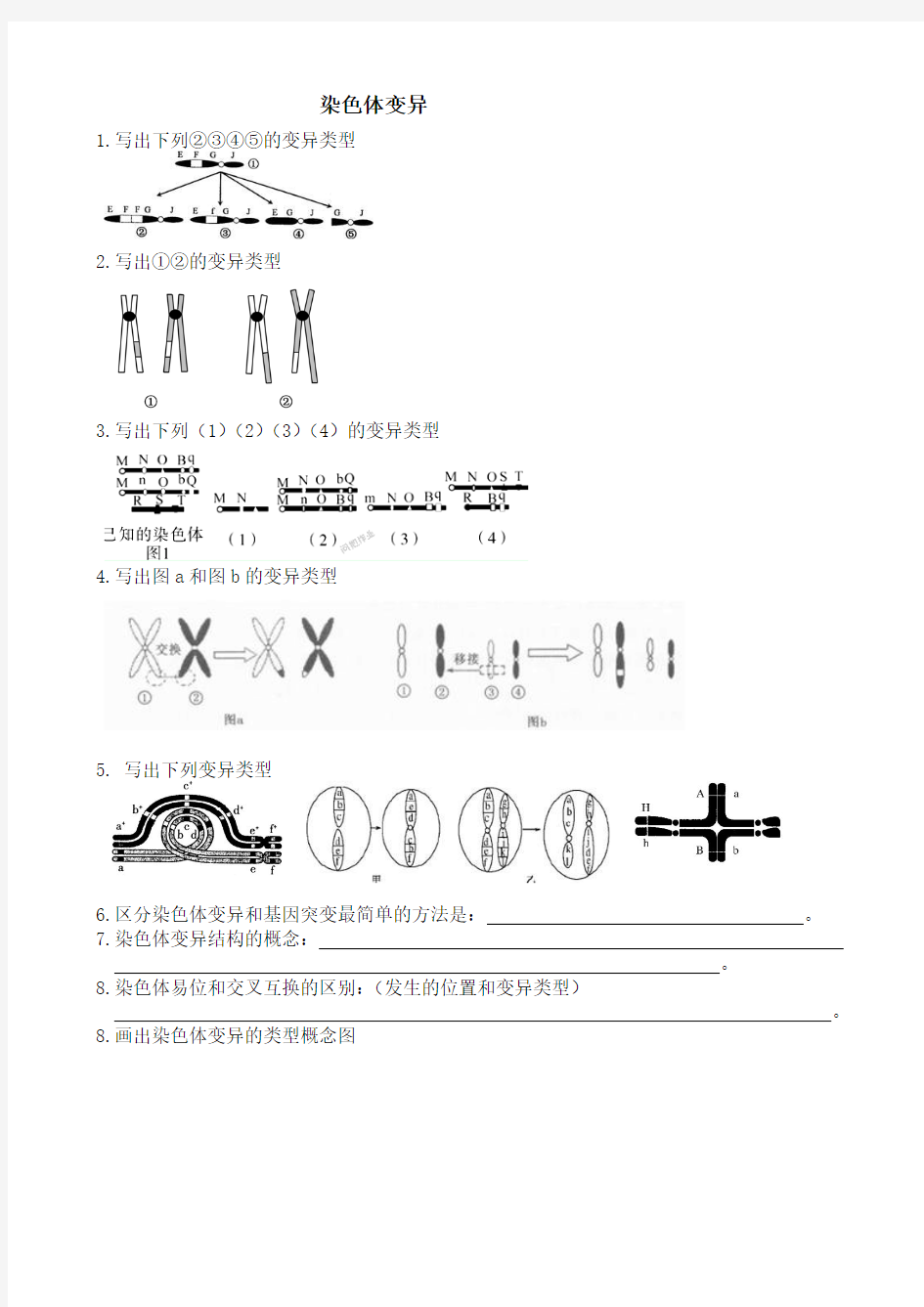
1.写出下列②③④⑤的变异类型
2.写出①②的变异类型
3.写出下列(1)(2)(3)(4)的变异类型
4.写出图a和图b的变异类型
5. 写出下列变异类型
6.区分染色体变异和基因突变最简单的方法是:。
7.染色体变异结构的概念:
。
8.染色体易位和交叉互换的区别:(发生的位置和变异类型)
。
8.画出染色体变异的类型概念图
9.染色体组的概念:。
10.写出下列细胞中染色体组数和每个染色体组的染色体组成
(1)
(2)
(3)
(4)
(5)
11.染色体组的判断方法
(1)若根据染色体判断:
(2)若根据基因组成:
12.判断个体倍性的方法(两步走):
①
②
13.培养多倍体的方法有,多倍体形成的原理:
。多倍体植株有哪些特征:
。诱导多倍体时用成熟的叶片还是幼嫩的呢?
14.单倍体的概念,单倍体植株的特点
。单倍体育种的优点:,原因是。
练习类:
课时练习1
1.由于种种原因,某生物体内某条染色体上多了几个或少了几个基因,这种遗传物质的变化属于
A.基因内部结构的改变 B.染色体结构变异
C.染色体数目变异 D.染色单体的交叉互换
2.基因突变和染色体变异的重要区别是
A.基因突变在光学显微镜下看不见
B.染色体变异是定向的,基因突变是不定向的
C.基因突变是可遗传的
D.染色体变异是不能遗传的
3.果蝇的棒眼现象是
A.基因突变造成 B.常染色体部分缺失造成
C.基因重组造成 D.染色体部分重复造成
4.下列不会引起染色体变异的是
A.染色体断裂的片段移到非同源染色体上
B.减数第一次分裂四分体时同源染色体的交叉互换
C.同一条染色体上某一段颠倒180度
D .一条染色体的断裂片段连到同源染色体的相应部位
5.是正常的两条同源染色体,则下图所示是指染色体结构的 A .倒位 B .缺失 C .易位
D .重复 6.基因重组、基因突变和染色体变异三者的共同点是 A.都能产生可遗传的变异 B.都能产生新的基因 C.产生的变异均对生物不利 D.产生的变异均对生物有利 7.已知某物种的一条染色体上依次排列着 M 、N 、O 、p 、q 五个基因,如图列出 的若干种变化中,不属于染色体结构
12.某生物的正常体细胞的染色体数目为12条,是三倍体,下图中表示其正常体细胞的是
13.右图中①和②表示发生在常染色体上的变异。①和②所表示的变异类型分别属于
A. 易位和易位
B. 易位和重组
C. 重组和易位
D. 重组和重组 14.填表: A M N O P Q
M N O
B
15.右图所示的细胞为三倍体的是
16.在三倍体无籽西瓜的培养过程中,将二倍体普通西瓜幼苗用秋水仙素处理,待植株成熟接受普通二倍体西瓜的正常花粉后,发育成的果实,其果皮、种皮、胚芽、胚乳细胞的染色体组数依次为
A.4、2、2、4 B.4、4、3、5
C.3、3、3、4 D.4、4、3、6
,用秋水仙素处理幼苗后得到的植17.基因型为AABBCC的豌豆与aabbcc的豌豆杂交产生的F
1
株是
A.二倍体 B.三倍体 C.四倍体 D.六倍体
18.农业生产上,常用人工诱导多倍体的育种方法来提高作物产量。在下列四组多倍体植物中,最有经济价值的一组是
A.玉米和高粱B.甘蔗和甜菜
C.水稻和棉花D.油菜和大豆
19.香蕉是天然三倍体,所以它:
A.无果实,无种子,进行无性生殖 B.有果实,有种子,进行种子繁殖
C.无果实,有种子,进行种子繁殖 D.有果实,无种子,进行无性生殖
20. 右图是果蝇体细胞染色体组成图解,请据图回答:
(1)写出与性别有关的染色体的名称:____。
(2)此果蝇是____倍体,一个染色体组的染色体数是____条,同一个
染色体组里的每条染色体上的DNA分子所携带的遗传信息______。
(3)图中含有_____对同源染色体。
(4)图中含有_________条常染色体。
(5)图中含有______条性染色体。
(6)此种果蝇的一精原细胞进行染色体复制后能产生___个初级精母细胞,产生___个次级精母细胞,产生个生殖细胞。
三、智能拓展训练:
21.将一粒花药培育成幼苗,对它的茎尖用秋水仙素处理,长大后该植株能正常开花结果。该植株下列细胞中哪一细胞与其他三种细胞染色体数目不相同()
A.根细胞 B.种皮细胞C.子房壁细胞 D.果实细胞
22.在减数分裂过程中,由于偶然因素,果蝇的一对性染色体没有分开,由此产生的不正常的卵细胞中的染色体数目为()
A.3+XY B.3+X或3+Y
C.3或3+XY D.3或3+XX
23.下列有关三倍体西瓜育种及原理的流程图
(1)用秋水仙处理时,可诱导多倍体的产生。因为这个部位的细胞具有的特征。秋水仙素的作用在此为。
(2)三倍体植株需要授以二倍体的成熟花粉,这一操作的目的在于。
(3)四倍体母本上结出的果实,其果肉细胞含个染色体组,种子中的胚含个染色体组。三倍体植株不能进行减数分裂的原因是,由此而获得三倍体无籽西瓜。
(4)三倍体西瓜高产,优质,无籽。这些事实说明染色体组增倍的意义在于。上述过程需要的时间周期为。
(5)用适当浓度的生长素溶液处理未授粉的番茄花蕾,子房发育成无籽果实;用四倍体西瓜和二倍体西瓜杂交,获得三倍体西瓜植株,给其雌蕊授以二倍体西瓜的花粉,子房发育成无籽西瓜。试问:
番茄的无籽性状是否能遗传?;
若取此番茄植株的枝条扦插,长成的植株所结果实中是否有种子?。
三倍体西瓜无性繁殖后,无籽性状是否能遗传?;
若取其枝条扦插,长成的植株子房壁细胞有个染色体组。
(6)已知普通西瓜红色瓤(R)对黄色瓤(r)为显性。如果用普通红色瓤纯合的西瓜苗用秋水仙素处理后开花,授以普通黄瓤西瓜的花粉,则结出的瓜瓤 __ 色;所结种子的胚的基因型为 ____ 。
课时练习2
1.关于单倍体的叙述正确的是
5.下图是甲、乙两种生物的体细胞内染色体情况示意图,则染色体数与图示相同的甲、乙两种生物体细胞的基因型可依次表示为 A .甲:AaBb 乙:AAaBbb B .甲:AaaaBBbb 乙:AaBB C .甲:AAaaBbbb 乙:AaaBBb
D .甲:AaaBbb 乙:AAaaBbbb
6.用基因型为AaBb 的玉米花药培养出来的单倍体幼苗,经过染色体加倍后,培养成多倍体纯合子的过程如图示:
(1)进行①的生理过程是________,②可能的基因型是________。 (2)③过程叫做________,这个过程依据的原理是________。
(3)进行④过程用的化学药剂是____________,这个过程叫做________________, 其原理是_________________
7.下表中,有的示意图是细胞中染色体的组成,有的给出的是细胞核中的基因型,据此判断出①~⑦中分别有多少个染色体组?
。
8.下图均为某生物的细胞分裂过程模式图,请分析回答:
(1)在这些细胞中没有同源染色体的是图 ,图A 、C 含有的染色体组数分别为 、 。
(2)若该个体有两对等位基因(A 和a ,B 和b )分别位于两对同源染色体上,图D 的基因组成可能是_______ ___。
(3)将该生物的某部位经低温处理一段时间后,发现其中某些细胞的染色体数目加倍,原因是 。用什么化学药品处理也可得到类似的结果?
二、能力提升自测:
9.用基因型为DdTt 植株所产生的花粉粒,经分别离体培养成幼苗,再用秋水仙素处理,使其成为二倍体,这些幼苗长成后的自交后代: A .全部为纯合体 B .全部为杂合体 C .1/16为纯合体 D .4/16为纯合体
10.从理论上讲,下列各组杂交产生的结果中错误的是
A.二倍体×四倍体→三倍体
B.二倍体×二倍体→二倍体
C.二倍体×六倍体→四倍体
D.三倍体×三倍体→三倍体
11.用一定浓度的秋水仙素处理二倍体番茄的幼苗茎尖,植株成熟后,所获得果实的果皮细
胞中和根尖细胞中分别含有的染色体组数是
A .4和2
B .2和4
C
.2和2
D .4和4
12.双子叶植物大麻(2N=20)为雌雄异株,性别决定方式为XY 型。若将其花药离体培养,将幼苗用秋水仙素处理,所得植株的染色体组成应是
A B C D E
A.18+XY B.18+XX C.18+XX或YY D.18+XX或XY
13.下列有关水稻的叙述,错误的是
A.二倍体水稻含有两个染色体组
B.二倍体水稻经秋水仙素处理,可得到四倍体水稻,稻穗、米粒变大
C.二倍体水稻与四倍体水稻杂交,可得到三倍体水稻,含三个染色体组
D.二倍体水稻的花粉经离体培养,可得到单倍体水稻,稻穗、米粒变小
14.萝卜和甘蓝杂交,能得到的种子一般都是不育的,但偶尔有个别种子种下去后可产生能育的后代,产生这种现象的原因是
A.基因自由组合
B.基因突变
C.染色体数目加倍
D.染色体结构变异
15.用花药离体培养法得到马铃薯单倍体植株,当它进行减数分裂时,能观察到染色体两两配对,共有12对。据此可推知马铃薯是
A.二倍体
B.三倍体
C.四倍体
D.六倍体
16.单倍体经秋水仙素处理,得到的
①一定是二倍体②一定是多倍体③是二倍体或多倍体
④一定是杂合体⑤一定是纯合子⑥是纯合子或杂合子
A.①⑥ B.③⑤ C.③⑥D.②④
17.已知小麦的基因型为AaBbCc,三对基因分别位于三对同源染色体上,利用其花药进行离体培养,获得n株小麦,其中基因型为aabbcc的个体占()
A.n/4 B.n/8 C.n/16 D.0
18.某植物的体细胞含有三个染色体组。则该植株()A.是多倍体B.不能繁殖
C.不能进行正常减数分裂D.每个染色体组含有三条染色体
(三)智能拓展训练:
19. 基因型为Aa的西瓜经秋水仙素加倍后,形成的四倍体在减数分裂时,形成配子的基因型
比例是
A. 3:1
B. 1:2:1
C. 1:4:1
D. 1:6:1
2017—2018学年度下学期高一物理组 主备教师:夏春青 第五章曲线运动 一、教学目标 使学生在理解曲线运动的基础上,进一步学习曲线运动中的两种特殊运动,抛体运动以及圆周运动,进而学习向心加速度并在牛顿第二定律的基础上推导出向心力,结合生活中的实际问题对曲线运动进一步加深理解。 二、教学内容 1.曲线运动及速度的方向; 2.合运动、分运动的概念; 3.知道合运动和分运动是同时发生的,并且互不影响; 4.运动的合成和分解; 5.理解运动的合成和分解遵循平行四边形定则; 6.知道平抛运动的特点,理解平抛运动是匀变速运动,会用平抛运动的规律解答有关问题; 7.知道什么是匀速圆周运动; 8.理解什么是线速度、角速度和周期; 9.理解各参量之间的关系;10.能够用匀速圆周运动的有关公式分析和解决有关问题;11.知道匀速圆周运动是变速运动,存在加速度。12.理解匀速圆周运动的加速度指向圆心,所以叫做向心加速度;13.知道向心加速度和线速度、角速度的关系;14.能够运用向心加速度公式求解有关问题;15.理解向心力的概念,知道向心力大小与哪些因素有关.理解公式的确切含义,并能用来计算;会根据向心力和牛顿第二定律的知识分析和讨论与圆周运动相关的物理现象; 16.培养学生的分析能力、综合能力和推理能力,明确解决实际问题的思路和方法。 三、知识要点 §5-1 曲线运动 & 运动的合成与分解 一、曲线运动 1.定义:物体运动轨迹是曲线的运动。
涉及的公式: 船 v d t = m in , θsin d x = 2.条件:运动物体所受合力的方向跟它的速度方向不在同一直线上。 3.特点:①方向:某点瞬时速度方向就是通过这一点的曲线的切线方向。 ②运动类型:变速运动(速度方向不断变化)。 ③F 合≠0,一定有加速度a 。 ④F 合方向一定指向曲线凹侧。 ⑤F 合可以分解成水平和竖直的两个力。 4.运动描述——蜡块运动 二、运动的合成与分解 1.合运动 与分运动的关系:等时性、 独立性、等效性、矢量性。 2.互成角度的两个分运动的合运动的判断: ①两个匀速直线运动的合运动仍然是匀速直线运动。 ②速度方向不在同一直线上的两个分运动,一个是匀速直线运动,一个是匀变速直线运动,其合运动是匀变速曲线运动,a 合为分运动的加速度。 ③两初速度为0的匀加速直线运动的合运动仍然是匀加速直线运动。 ④两个初速度不为0的匀加速直线运动的合运动可能是直线运动也可能是曲线运动。当两个分运动的初速度的和速度方向与这两个分运动的和加速度在同一直线上时,合运动是匀变速直线运动,否则即为曲线运动。 三、有关“曲线运动”的两大题型(一)小船过河问题 模型一:过河时间t 最短:模型二:直接位移x 最短:模型三:间接位移x 最短: § 一、抛体运动 当v 水
高中化学必修2知识点总结归纳 高中化学必修2知识点总结归纳 ★熟背前20号元素,熟悉1~20号元素原子核外电子的排布: H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca 2.原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里;②各电子层最多容纳的电子数是2n2;③最外层电子数不超过8个(K层为最外层不超过2个),次外层不超过18个,倒数第三层电子数不超过32个。 电子层:一(能量最低)二三四五六七 对应表示符号: K L M N O P Q 3.元素、核素、同位素 元素:具有相同核电荷数的同一类原子的总称。 核素:具有一定数目的质子和一定数目的中子的一种原子。 同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素。(对于原子来说) 二、元素周期表 1.编排原则: ①按原子序数递增的顺序从左到右排列 ②将电子层数相同的各元素从左到右排成一横行。(周期序数=原子的电子层数) ③把最外层电子数相同的元素按电子层数递增的顺序从上到下
排成一纵行。 主族序数=原子最外层电子数 第ⅠA族碱金属元素:Li Na K Rb Cs Fr (Fr是金属性最强的元素,位于周期表左下方) 第ⅦA族卤族元素:F Cl Br I At (F是非金属性最强的元素,位于周期表右上方) ★判断元素金属性和非金属性强弱的方法: (1)金属性强(弱)——①单质与水或酸反应生成氢气容易(难); ②氢氧化物碱性强(弱);③相互置换反应(强制弱)Fe+CuSO4=FeSO4+Cu。 (2)非金属性强(弱)——①单质与氢气易(难)反应;②生成的氢化物稳定(不稳定);③最高价氧化物的水化物(含氧酸)酸性强(弱);④相互置换反应(强制弱)2NaBr+Cl2=2NaCl+Br2。 相互连接的电极插入电解质溶液构成闭合回路。 (4)电极名称及发生的反应: 负极:较活泼的金属作负极,负极发生氧化反应, 电极反应式:较活泼金属-ne-=金属阳离子 负极现象:负极溶解,负极质量减少。 正极:较不活泼的金属或石墨作正极,正极发生还原反应, 电极反应式:溶液中阳离子+ne-=单质 正极的现象:一般有气体放出或正极质量增加。 (5)原电池正负极的判断方法:
高一化学必修二知识点总结归纳总复习提纲 第一章 物质结构 元素周期律 一、原子结构 质子(Z 个) 原子核 注意: 中子(N 个) 质量数(A)=质子数(Z)+中子数(N) 1.原子) 原子序数=核电荷数=质子数=原子的核外电子数 核外电子(Z 个) ★熟背前20号元素,熟悉1~20号元素原子核外电子的排布: H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca 2.原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里;②各电子 层最多容纳的电子数是2n 2 ;③最外层电子数不超过8个(K 层为最外层不超过2个),次外层不超过18个,倒数第三层电子数不超过32个。 电子层(n): 一(能量最低) 二 三 四 五 六 七 对应表示符号: K L M N O P Q 3.元素、核素、同位素 元素:具有相同核电荷数的同一类原子的总称。 核素:具有一定数目的质子和一定数目的中子的一种原子。 同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素。(对于原子来说) 二、元素周期表 1.编排原则: ①按原子序数递增的顺序从左到右排列 ②将电子层数相同......的各元素从左到右排成一横行..。(周期序数=原子的电子层数) ③把最外层电子数相同........的元素按电子层数递增的顺序从上到下排成一纵行.. 。 主族序数=原子最外层电子数 核外电子层数 元素种类 第一周期 1 2种元素 短周期 第二周期 2 8种元素 周期 第三周期 3 8种元素 元 (7个横行) 第四周期 4 18种元素 素 (7个周期) 第五周期 5 18种元素 周 长周期 第六周期 6 32种元素 期 第七周期 7 未填满(已有26种元素) 表 主族:ⅠA ~ⅦA 共7个主族
第一章立体几何初步 1、柱、锥、台、球的结构特征 (1)棱柱:定义:两个面互相平行,其余各面都是四边形,且每相邻两个四边形的公共边都互相平行的几何体。 分类:以底面多边形的边数作为分类的标准分为三棱柱、四棱柱、五棱柱等。 表示:用各顶点字母,如五棱柱' ' ' ' 'E D C B A ABCDE-或用对角线的端点字母,如五棱柱' AD。 几何特征:两底面是对应边平行的全等多边形;侧面、对角面都是平行四边形;侧棱平行且相等;平行于底面的截面是与底面全等的多边形。 (2)棱锥:定义:有一个面是多边形,其余各面都是有一个公共顶点的三角形,由这些面所围成的几何体。 分类:以底面多边形的边数作为分类的标准分为三棱锥、四棱锥、五棱锥等 表示:用各顶点字母,如五棱锥' ' ' ' 'E D C B A P- 几何特征:侧面、对角面是三角形;平行于底面的截面与底面相似,其相似比等于顶点到截面距离与高的比。(3)棱台:定义:用一个平行于棱锥底面的平面去截棱锥,截面和底面之间的部分 分类:以底面多边形的边数作为分类的标准分为三棱态、四棱台、五棱台等 表示:用各顶点字母,如五棱台' ' ' ' 'E D C B A P- 几何特征:①上下底面是相似平行多边形②侧面是梯形③侧棱交于原棱锥的顶点。 (4)圆柱:定义:以矩形一边所在直线为轴旋转,其余三边旋转所成的曲面所围成的几何体。 几何特征:①底面是全等的圆;②母线与轴平行;③轴与底面圆的半径垂直;④侧面展开图是一个矩形。(5)圆锥:定义:以直角三角形一条直角边为旋转轴,旋转一周所成的曲面所围成的几何体。 几何特征:①底面是一个圆;②母线交于圆锥的顶点;③侧面展开图是一个扇形。 (6)圆台:定义:用一个平行于圆锥底面的平面去截圆锥,截面和底面之间的部分 几何特征:①上下底面是两个圆;②侧面母线交于原圆锥顶点;③侧面展开图是一弓形。 (7)球体:定义:以半圆的直径所在直线为旋转轴,半圆面旋转一周形成的几何体 几何特征:①球的截面是圆;②球面上任意一点到球心的距离等于半径。 2、空间几何体的三视图 定义三视图:正视图(光线从几何体的前面向后面正投影);侧视图(从左向右)、俯视图(从上向下) 注:正视图反映了物体上下、左右的位置关系,即反映了物体的高度和长度; 俯视图反映了物体左右、前后的位置关系,即反映了物体的长度和宽度; 侧视图反映了物体上下、前后的位置关系,即反映了物体的高度和宽度。 3、空间几何体的直观图——斜二测画法 斜二测画法特点:①原来与x轴平行的线段与'x轴平行且长度不变; ②原来与y轴平行的线段与'y轴平行,长度减为原来的一半。 4、柱体、锥体、台体的表面积与体积 (1)几何体的表面积为几何体各个面的面积的和。 (2)特殊几何体表面积公式(c为底面周长,h为高,'h为斜高,l为母线) ch S= 直棱柱侧面积 rh Sπ 2 = 圆柱侧 ' 2 1 ch S= 正棱锥侧面积 rl Sπ = 圆锥侧面积 ') ( 2 1 2 1 h c c S+ = 正棱台侧面积 l R r Sπ) (+ = 圆台侧面积 ()l r r S+ =π2 圆柱表 ()l r r S+ =π 圆锥表 ()2 2R Rl rl r S+ + + =π 圆台表 (3)柱体、锥体、台体的体积公式
高一化学必修二期中考试知识点总结归纳 第一章物质结构元素周期律 一、原子结构 原子序数=核电荷数=质子数=原子的核外电子数 ★熟背前20号元素,熟悉1~20号元素原子核外电子的排布: H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca 2.原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里;②各电子层最多容纳的电子数是2n2;③最外层电子数不超过8个(K层为最外层不超过2个),次外层不超过18个,倒数第三层电子数不超过32个。 电子层:一(能量最低)二三四五六七 对应表示符号:K L M N O P Q 3.元素、核素、同位素 元素:具有相同核电荷数的同一类原子的总称。 核素:具有一定数目的质子和一定数目的中子的一种原子。 同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素。(对于原子来说) 二、元素周期表 1.编排原则: ①按原子序数递增的顺序从左到右排列 ②将电子层数相同 ......的各元素从左到右排成一横行 ..。(周期序数=原子的电子层数) ③把最外层电子数相同 ..。 ........的元素按电子层数递增的顺序从上到下排成一纵行主族序数=原子最外层电子数 2.结构特点:
三、元素周期律 1.元素周期律:元素的性质(核外电子排布、原子半径、主要化合价、金属性、非 金属性)随着核电荷数的递增而呈周期性变化的规律。元素性质的周期性变化实质是 ... 元素原子核外电子排布的周期性变化 ................的必然结果。 2.同周期元素性质递变规律 第ⅠA族碱金属元素:Li Na K Rb Cs Fr (Fr是金属性最强的元素,位于周期表左下方) 第ⅦA族卤族元素:F Cl Br I At (F是非金属性最强的元素,位于周期表右上方) ★判断元素金属性和非金属性强弱的方法: (1)金属性强(弱)——①单质与水或酸反应生成氢气容易(难);②氢氧化物
抛体运动知识要点 一、匀变速直线运动的特征和规律: 匀变速直线运动:加速度是一个恒量、且与速度在同一直线上。 基本公式:、、 (只适用于匀变速直线运动)。 当v0=0、a=g(自由落体运动),有 v t=gt 、、、。 当V0竖直向上、a= -g(竖直上抛运动)。 注意:(1)上升过程是匀减速直线运动,下落过程是匀加速直线运动。 (2)全过程加速度大小是g,方向竖直向下,全过程是匀变速直线运动 (3)从抛出到落回抛出点的时间:t总= 2V0/g=2t上=2 t下 (4)上升的最大高度(相对抛出点):H=v02/2g (5)*上升、下落经过同一位置时的加速度相同,而速度等值反向 (6)*上升、下落经过同一段位移的时间相等。 (7)*用全程法分析求解时:取竖直向上方向为正方向,S>0表示此时刻质 点的位置在抛出点的上方;S<0表示质点位置在抛出点的下方。v t >0表示方向向上;v t <0表示方向向下。在最高点a=-gv=0。 二、运动的合成和分解: 1.两个匀速直线运动的物体的合运动是___________________运动。一般来说,两个直线运动的合运动并不一定是____________运动,也可能是_____________运动。合运动和分运动进行的时间是__________的。 2.由于位移、速度和加速度都是______量,它们的合成和分解都按照_________法则。 三、曲线运动: 曲线运动中质点的速度沿____________方向,曲线运动中,物体的速度方向随时间而变化,所以曲线运动是一种__________运动,所受的合力一定.必具有_________。物体做曲线运动的条件是________________ 。 四、平抛运动(设初速度为v0): 1.特征:初速度方向____________,加速度____________。是一种。。。 2.性质和规律: 水平方向:做______________运动,v X=v0、x=v0t。 竖直方向:做______________运动,v y=gt=、y=gt2/2=。 合速度:V=,合位移S=。 3.平抛运动的飞行时间由决定,与无关。
第一章 立体几何初步 1.柱、锥、台、球的结构特征 (1)棱柱:有两个面互相平行,其余各面都是四边形,且每相邻两个四边形的公共边都互相平行,由这些面所围成的几何体。 (2)棱锥:有一个面是多边形,其余各面都是有一个公共顶点的三角形,由这些面所围成的几何体 (3)棱台:用一个平行于棱锥底面的平面去截棱锥,截面和底面之间的部分 (4)圆柱:以矩形的一边所在的直线为轴旋转,其余三边旋转所成的曲面所围成的几何体 (5)圆锥:以直角三角形的一条直角边为旋转轴,旋转一周所成的曲面所围成的几何体 (6)圆台:用一个平行于圆锥底面的平面去截圆锥,截面和底面之间的部分 (7)球体:以半圆的直径所在直线为旋转轴,半圆面旋转一周形成的几何体 2. 空间几何体的表面积和体积: (1)侧面积公式: ① 直棱柱S ch =(c 为底面周长,h 为高) ② 正棱锥' 12S ch = (c 为底面周长,'h 为斜高) ③ 正棱台'121 ()2 S c c h =+(12c c 、分别为上下底面的周长,'h 为斜高) ④ 圆柱2S rh π=(r 为底面半径,h 为高) ⑤ 圆锥S rl π=(r 为底面半径,l 为母线长) ⑥ 圆台12()S r r l π=+(12r r 、分别为上下底面半径,l 为母线长) (2)体积公式: ① 棱柱V Sh =(S 为底面积,h 为高)
② 棱锥1 3 V Sh =(S 为底面积,h 为高) ③ 棱台121 ()3V S S h =+(12S S 、分别为上下底面积,h 为高) ④ 圆柱2V Sh r h π==(S 为底面积,r 为底面半径,h 为高) ⑤ 圆锥211 33V Sh r h π==(S 为底面积,r 为底面半径,h 为高) ⑥ 圆台121 ()3V S S h =+(12S S 、分别为上下底面积,h 为高) (3)球: 24S R π= ②球的体积公式:34 3 V R π= (R 表示球的半径) ③球的任意截面的圆心与球心的连线垂直截面,若设球的半径为R ,截面圆的半径是r ,截面圆的圆心与球心的连线长为d ,则:222d R r =-。 3.空间几何体的三视图 ①正视图(从前向后); ②侧视图(从左向右); ③俯视图(从上向下). 4.空间几何体的直观图——斜二测画法 斜二测画法特点:① '''045x o y ∠= ; ②原来与x 轴平行的线段仍然与x 平行且长度不变; ③原来与y 轴平行的线段仍然与y 平行,长度为原来的一半。 第二章 直线与平面的位置关系
地理必修二 第一章人口的变化 第一节人口的数量变化 第一节人口数量变化 一. 人口的自然增长 1. 决定性影响因素:人口自然增长率:人口自然增长率=出生率-死亡率
(出生率:一年内出生的婴儿数占总人数的比率。死亡率:一年内死亡的人数占总人数的比率。) 2. 其他影响因素:人口基数。 3. 时间特征:近百多年来增长迅速。 4. 空间特征:存在地区差异。 5. 两类国家人口增长情况比较: 两类国家人口增长情况比较 自然增长 特点增长快慢的原因今后变化趋 势 经济发达人口数量比 发达国 家增长缓慢社会福利保障完 善较稳定,一教育文化水平高些国家还会生育观念淡薄逐渐减少。 政治上独立 采取控制人 口 发展中 国家增长较快民族经济的发展的措施,人口 增 医疗卫生事业的 进步长将趋于缓 慢。
二. 人口增长模式及其转变 1. 构成指标和类型: ①构成指标:出生率、死亡率、人口自然增长率。 ②类型:原始型:出生率高,死亡率高,自然增长率低,增长缓慢。 传统型:出生率高,死亡率低,自然增长率高,增长迅速。 现代型:出生率低,死亡率低,自然增长率低,增长缓慢。 2. 转变的根本原因:生产力的发展。 3. 空间差异: ①发达国家已步入现代型。 ②我国基本实现从传统型向现代型转变(源于计划生育政策的实施)。 ③世界仍处于传统型像现代型过渡。 注:人口增长图,人口增长模式及其转变示意图 第二节人口的空间变化 一.人口的迁移 1.人口迁移就是一段时间内人的居住地在国际或本国范围内发生改
变。 2.判断依据:居住地的变更,时间的持续性(约一年以上),超越一 定行政界限。 3.分类:国际人口迁移,国内人口迁移。 4.国际人口迁移特点: ①二战前,伴随地理大发现,集团性、大批移民为主。 ②二战后,流向发达国家,定居移民减少,短期流动的人口增多。 5.新中国成立之后国内人口迁移特点: 新中国成立之后国内人口迁移特点 影响因素迁移特 点流向地区 新中国成立到 20计划经济,有计划无 世纪80年代中 期严格的户籍管 理有组织 20世纪80年改革开放自发,从农村向城 市 代中期以来数量大从内地向沿 海 二.影响人口迁移的因素
高中化学必修2知识点归纳总结大全 第一章物质结构元素周期律 一、原子结构 1. 原子(A z X )原子核质子(Z 个) 中子( N 个) 核外电子( Z 个) 注意:质量数 (A) =质子数 (Z) +中子数 (N) 原子序数 = 核电荷数 = 质子数 = 原子的核外电子数 ★熟背前 20 号元素,熟悉 1 ~ 20 号元素原子核外电子的排布: H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca 2. 原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里; ②各电子层最多容纳的电子数是 2n2 ;③最外层电子数不超过 8 个( K 层为最外层不超过 2 个),次外层不超过 18 个,倒数第三层电子数不超过 32 个。 电子层:一(能量最低)二三四五六七 对应表示符号: K L M N O P Q 3. 元素、核素、同位素 元素:具有相同核电荷数的同一类原子的总称。 核素:具有一定数目的质子和一定数目的中子的一种原子。 同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素。 ( 对于原子来说 ) 二、元素周期表 1. 编排原则:①按原子序数递增的顺序从左到右排列 ②将电子层数相同的各元素从左到右排成一横行。(周期序数=原子的电子层数) ③把最外层电子数相同的元素按电子层数递增的顺序从上到下排成一纵行。 主族序数=原子最外层电子数 2. 结构特点: 核外电子层数元素种类 第一周期 1 2 种元素 短周期第二周期 2 8 种元素 周期第三周期 3 8 种元素 元( 7 个横行、第四周期 4 18 种元素
思想政治必修二知识点总结 第一单元公民的政治生活 第一课生活在人民当家作主的国家 第一框题:人民民主专政:本质是人民当家作主 一、广泛真实的民主 2、国家的根本属性:阶级性。 3、国家的性质,是由占统治阶级地位的阶级的性质决定。 我国国家性质:中华人民共和国是工人阶级领导的、以工农联盟为基础的人民民主专政的社会主义国家。 4、我国人民民主专政的最大特点:对占全国人口绝大多数的人民实行民主,对极少数敌视和破坏社会主义事业的敌对分子实行专政。 5、人民民主专政的本质是人民当家作主。 6、人民民主具有广泛性和真实性: (1)广泛性:民主主体广泛;民主权利广泛。 (2)真实性:人民当家作主的权利有制度、法律和物质保障;广大人民利益得到充分实现。 7、人民民主专政的职能:对少数敌人实行专政。 (3)民主是专政的基础,专政是民主的保障。统治阶级的民主是被统治阶级的专政。 二、坚持人民民主专政是正义的事情 1、为什么要坚持人民民主专政? (1)四项基本原则是我国立国之本。人民民主专政作为四项基本原则之一,已被写入宪法。 (2)是社会主义现代化建设的政治保证。 2、人民民主专政新的时代内容: (1)突出为社会主义经济建设服务的国家职能; (2)为改革开放和社会主义现代化建设创造良好的国内条件和国际环境了; (3)重视法制建设,依照宪法和法律治理国家; (4)发展人民民主,加强民主制度建设。 第二框题:政治权利和义务:参与政治生活的准则 一、政治权利与自由 1、政治生活的全部内容,是以依法行使政治权利、履行政治义务为基础。 2、权利和自由的含义:公民依法参与国家政治生活、管理国家事务和社会事务、表达意愿的权利和自由就是公民的政治权利和自由。 3、政治权利和自由: (1)选举权和被选举权——基本民主权利,行使这个权利是公民参与国家管理的基础和标志。 (2)政治自由——言论、出版、集会、结社、游行、示威 (3)监督权——批评、建议、申诉、控告、检举 二、政治义务 1、维护国家统一和民族团结——国家统一、民族团结是我国顺利进行社会主义现代化建设的根本保证,也是实现公民的政治权利和其它权利的重要保证。 2、遵守宪法和法律——宪法和法律是党的主张和人民意志相统一的体现,公民根本的行为准则。 3、维护国家安全、荣誉和利益——实现国家富强民族振兴的重要保证,是爱国主义的体现,是公民义不容辞的职责。 4、服兵役和参加民兵组织。 三、公民参与政治生活基本原则 1、坚持公民在法律面前一律平等的原则。
高中数学 必修2知识点 第一章 空间几何体 1.1柱、锥、台、球的结构特征 1.2空间几何体的三视图和直观图 1 三视图: 正视图:从前往后 侧视图:从左往右 俯视图:从上往下 2 画三视图的原则: 长对齐、高对齐、宽相等 3直观图:斜二测画法 4斜二测画法的步骤: (1).平行于坐标轴的线依然平行于坐标轴; (2).平行于y 轴的线长度变半,平行于x ,z 轴的线长度不变; (3).画法要写好。 5 用斜二测画法画出长方体的步骤:(1)画轴(2)画底面(3)画侧棱(4)成图 1.3 空间几何体的表面积与体积 (一 )空间几何体的表面积 1棱柱、棱锥的表面积: 各个面面积之和 2 圆柱的表面积 3 圆锥的表面积2 r rl S ππ+= 4 圆台的表面积2 2 R Rl r rl S ππππ+++= 5 球的表面积2 4R S π= (二)空间几何体的体积 1柱体的体积 h S V ?=底 2锥体的体积 h S V ?=底31 3台体的体积 h S S S S V ?++ =)3 1 下下 上上( 4球体的体积 33 4 R V π= 第二章 直线与平面的位置关系 2.1空间点、直线、平面之间的位置关系 2.1.1 1 平面含义:平面是无限延展的 2 平面的画法及表示 (1)平面的画法:水平放置的平面通常画成一个平行四边形,锐角画成450 ,且横边画成邻边的2倍长(如图) (2)平面通常用希腊字母α、β、γ等表示,如平面α、平面β等,也可以用表示平面的平行四边形的四个顶点或者相对的两个顶点的大写字母来表示,如平面AC 、平面ABCD 等。 3 三个公理: (1)公理1:如果一条直线上的两点在一个平面内,那么这条直线在此平面内 符号表示为 A ∈L B ∈L => L α A ∈α B ∈α 公理1作用:判断直线是否在平面内 D C B A α L A · α 222r rl S ππ+=
地理必修二知识点总结 第一章人口的变化 第一节人口的数量变化 一、人口的自然增长 1、10年来人口增长 历史时期人类的生产劳动人口数量和增长情况人口变化的原因 农业革命之前主要从事采集和狩猎人口数量化少,增长缓慢人们获取食物的能力低,抵御疾病和灾难水平差,死亡率高 农业革命至工业革命期间利用简单的工具从事农业活动人口数量增多,增长速度加快耕作和灌溉技术发展,食物供应变得稳定而可靠,死亡率下降 工业革命以后工业生产活动迅速扩大和发展人口数量继续增加,增长速度更加迅猛用科学技术武装起来的人类不断壮大着改造自然的能力,人们能获得充足的食物和完善的医疗服务,死亡率降低 2、人口自然增长最根本因素:生产力水平的高低 决定因素:自然增长率、出生率、死亡率 3、发达国家与发展中国家人口增长差异 自然增长率水平人口增长特点及成因今后变化趋势 发达国家保持较低水平受生育观念、生活质量、社会经济发展水平影响,增长缓慢今后几十年,人口数量将比较稳定,一些国家还会逐渐减少 发展中国家水平较高由于政治独立,民族经济发展,医疗卫生事业进步,死亡率下降,人口增长很快采取了控制人口的措施,人口增长速度将趋缓,但人口数量还将增加 中国水平较低增长缓慢人口基数大 4、人口的发展一定要与经济社会发展相协调,与环境的承载力相适应。 二、人口增长模式及其转变 5、人口增长模式与相应人口问题 人口增长人口问题 历原始低增长阶段——“高高低”模式——原始型人口增长过快 史加速增长阶段———“高低高”模式——传统型——————儿童比重过大 轨增长减缓阶段——人口增长缓慢 迹低速增长阶段——“低低低”模式——现代型———————人口老龄化 6、影响人口模式转变的因素:生产力水平、国家政策、自然环境、社会福利、文化观念 7、为什么大多数发展中国家的人口增长模式尚未进入现代型?生产力水平低、城市化水平低、社会制度。 第二节人口的空间变化 一、人口的迁移
高中化学必修2知识点归纳总结 第一单元原子核外电子排布与元素周期律 一、原子结构 质子(Z个) 原子核注意: 中子(N个)质量数(A)=质子数(Z)+中子数(N) 1.X 原子序数=核电荷数=质子数=原子的核外电子 核外电子(Z个) ★熟背前20号元素,熟悉1~20号元素原子核外电子的排布: H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca 2.原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里;②各电子层最多容纳的电子数是2n2;③最外层电子数不超过8个(K层为最外层不超过2个),次外层不超过18个,倒数第三层电子数不超过32个。 电子层:一(能量最低)二三四五六七对应表示符号: K L M N O P Q 3.元素、核素、同位素 元素:具有相同核电荷数的同一类原子的总称。 核素:具有一定数目的质子和一定数目的中子的一种原子。 同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素。(对于原子来说) 二、元素周期表 1.编排原则: ①按原子序数递增的顺序从左到右排列 ②将电子层数相同 ..。(周期序数=原子的电子层数)......的各元素从左到右排成一横行 ③把最外层电子数相同 ..。 ........的元素按电子层数递增的顺序从上到下排成一纵行 主族序数=原子最外层电子数 2.结构特点: 核外电子层数元素种类 第一周期 1 2种元素 短周期第二周期 2 8种元素 周期第三周期 3 8种元素 元(7个横行)第四周期 4 18种元素 素(7个周期)第五周期 5 18种元素 周长周期第六周期 6 32种元素 期第七周期 7 未填满(已有26种元素)表主族:ⅠA~ⅦA共7个主族 族副族:ⅢB~ⅦB、ⅠB~ⅡB,共7个副族 (18个纵行)第Ⅷ族:三个纵行,位于ⅦB和ⅠB之间 (16个族)零族:稀有气体 三、元素周期律 1.元素周期律:元素的性质(核外电子排布、原子半径、主要化合价、金属性、非金属性) 随着核电荷数的递增而呈周期性变化的规律。元素性质的周期性变化实质是元素原子核外电 .......... 子排布的周期性变化 .........的必然结果。 2.同周期元素性质递变规律
第1章 空间几何体1 1 .1柱、锥、台、球的结构特征 1. 2空间几何体的三视图和直观图 11 三视图: 正视图:从前往后 侧视图:从左往右 俯视图:从上往下 22 画三视图的原则: 长对齐、高对齐、宽相等 33直观图:斜二测画法 44斜二测画法的步骤: (1).平行于坐标轴的线依然平行于坐标轴; (2).平行于y 轴的线长度变半,平行于x ,z 轴的线长度不变; (3).画法要写好。 5 用斜二测画法画出长方体的步骤:(1)画轴(2)画底面(3)画侧棱(4)成图 1.3 空间几何体的表面积与体积 (一 )空间几何体的表面积 1棱柱、棱锥的表面积: 各个面面积之和 2 圆柱的表面积 3 圆锥的表面积2 r rl S ππ+= 4 圆台的表面积22R Rl r rl S ππππ+++= 5 球的表面积2 4R S π= (二)空间几何体的体积 1柱体的体积 h S V ?=底 2锥体的体积 h S V ?=底31 3台体的体积 h S S S S V ?++=)31 下下上上( 4球体的体积 33 4 R V π= 第二章 直线与平面的位置关系 2.1空间点、直线、平面之间的位置关系 222r rl S ππ+=
2.1.1 1 平面含义:平面是无限延展的 2 平面的画法及表示 (1)平面的画法:水平放置的平面通常画成一个平行四边形, 锐角画成450,且横边画成邻边的2倍长(如图) (2)平面通常用希腊字母α、β、γ等表示,如平面α、平面β等,也可以用表示平面的平行四边形的四个顶点或者相对的两个顶点的大写字母来表示,如平面AC 、平面ABCD 等。 3 三个公理: (1)公理1:如果一条直线上的两点在一个平面内,那么这条直线在此平面内 符号表示为 A ∈L B ∈L => L α A ∈α B ∈α 公理1作用:判断直线是否在平面内 (2)公理2:过不在一条直线上的三点,有且只有一个平面。 符号表示为:A 、B 、C 三点不共线 => 有且只有一个平面α, 使A ∈α、B ∈α、C ∈α。 公理2 作用:确定一个平面的依据。 (3)公理3:如果两个不重合的平面有一个公共点,那么它们有且只有一条过该点的公共直线。 符号表示为:P ∈α∩β =>α∩β=L ,且P ∈L 公理3作用:判定两个平面是否相交的依据 2.1.2 空间中直线与直线之间的位置关系 1 空间的两条直线有如下三种关系: 相交直线:同一平面内,有且只有一个公共点; 平行直线:同一平面内,没有公共点; 异面直线: 不同在任何一个平面内,没有公共点。 2 公理4:平行于同一条直线的两条直线互相平行。 符号表示为:设a 、b 、c 是三条直线 a ∥ b c ∥b 强调:公理4实质上是说平行具有传递性,在平面、空间这个性质都适用。 公理4作用:判断空间两条直线平行的依据。 3 等角定理:空间中如果两个角的两边分别对应平行,那么这两个角相等或互补 4 注意点: ① a'与b'所成的角的大小只由a 、b 的相互位置来确定,与O 的选择无关,为了简便,点O 一般取在两直线中的一条上; ② 两条异面直线所成的角θ∈(0, ); ③ 当两条异面直线所成的角是直角时,我们就说这两条异面直线互相垂直,记作a ⊥b ; ④ 两条直线互相垂直,有共面垂直与异面垂直两种情形; ⑤ 计算中,通常把两条异面直线所成的角转化为两条相交直线所成的角。 2.1.3 — 2.1.4 空间中直线与平面、平面与平面之间的位置关系 1、直线与平面有三种位置关系: D C B A α L A · α C · B · A · α P · α L β 共面直线 =>a ∥c 2
高一化学必修二知识点归纳 1、最简单的有机化合物甲烷 氧化反应CH4(g)+2O2(g)→CO2(g)+2H2O(l) 取代反应CH4+Cl2(g)→CH3Cl+HCl 烷烃的通式:CnH2n+2n≤4为气体、所有1-4个碳内的烃为气体,都难溶于水,比水轻 碳原子数在十以下的,依次用甲、乙、丙、丁、戊、己、庚、辛、壬、癸 同系物:结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物 同分异构体:具有同分异构现象的化合物互称为同分异构 同素异形体:同种元素形成不同的单质 同位素:相同的质子数不同的中子数的同一类元素的原子 2、来自石油和煤的两种重要化工原料 乙烯C2H4(含不饱和的C=C双键,能使KMnO4溶液和溴的溶液褪色) 氧化反应2C2H4+3O2→2CO2+2H2O 加成反应CH2=CH2+Br2→CH2Br-CH2Br(先断后接,变内接为外接) 加聚反应nCH2=CH2→[CH2-CH2]n(高分子化合物,难降解,白色 污染) 乙烯的产量是衡量国家石油化工发展水平的标志
苯是一种无色、有特殊气味的液体,有毒,不溶于水,良好的有 机溶剂 苯的结构特点:苯分子中的碳碳键是介于单键和双键之间的一种独特的键 氧化反应2C6H6+15O2→12CO2+6H2O 取代反应溴代反应+Br2→-Br+HBr 硝化反应+HNO3→-NO2+H2O 加成反应+3H2→ 3、生活中两种常见的有机物 乙醇 良好的有机溶剂,溶解多种有机物和无机物,与水以任意比互溶,醇官能团为羟基-OH 与金属钠的反应2CH3CH2OH+Na→2CH3CHONa+H2 氧化反应 完全氧化CH3CH2OH+3O2→2CO2+3H2O 不完全氧化2CH3CH2OH+O2→2CH3CHO+2H2O(Cu作催化剂) 乙酸CH3COOH官能团:羧基-COOH无水乙酸又称冰乙酸或冰醋酸。 弱酸性,比碳酸强 CH3COOH+NaOH→CH3COONa+H2O2CH3COOH+CaCO3→Ca(CH3COO)2+H2O+C O2↑ 酯化反应醇与酸作用生成酯和水的反应称为酯化反应。 原理酸脱羟基醇脱氢。 CH3COOH+C2H5OH→CH3COOC2H5+H2O
<政治生活>2 必修思想政治 第一课:生活在人民当家作主的国家 ★★(一)我国的国家性质——人民民主专政的社会主义国家 ★1.人民民主专政的特点:对占全国人口绝大多数的人民实行民主,对极少数敌视和破坏社会主义事业的敌人实行专政。 ★2.人民民主专政的本质:人民当家作主。 ★3.人民民主的特点: (1)人民民主的广泛性:人民享有广泛的民主权利;民主主体的广泛性。 (2)人民民主的真实性:人民当家作主的权利有制度、法律和物质的保障;随着经济的发展和社会的进步,广大人民的利益得到日益充分的实现。 4.为什么要坚持人民民主专政 (1)四项基本原则是立国之本,是我国国家生存发展的政治基石。坚持人民民主专政作为四项基本原则之一,已被写入我国宪法。 ★(2)坚持人民民主专政是社会主义现代化建设的政治保证。 ①只有充分发扬社会主义民主,确保人民当家作主的地位,保证人民依法享有广泛的权利和自由,尊重和保障人权,才能调动亿万人民群众投身于社会主义现代化建设的积极性。 ②只有坚持国家的专政职能,打击一切破坏社会主义建设的敌对势力和敌对分子,才能保障人民民主,维护国家长治久安。 5.怎样坚持人民民主专政?(略 P7) 6.我国政府关于人权问题的观点:(1)生存权、发展权是根本和重要的人权。(2)保护和促进人权,必须从保障人民的生存权、发展权这个环节入手;(3)实现人权的根本途径是促进经济发展和社会进步;(4)国家主权是一国人民充分享受人权的前提和保障。 ★★(二)公民的政治权利与义务 1.我国公民的政治权利和自由:选举权和被选举权;政治自由;监督权。 2.我国公民必须履行的政治性义务:维护国家统一和民族团结。遵守宪法和法律。维护国家安全、荣誉和利益。服兵役和参加民兵组织。 ★★3.我国公民参与政治生活的基本原则:1)坚持公民在法律面前一律平等原则;2)坚持权利与义务统一的原则;3)坚持个人利益与国家利益相结合的原则。 4.坚持公民在法律面前一律平等原则。 公民平等的享受权利,平等的履行义务,平等的适用法律。 ①任何公民都平等的享有宪法、法律规定的权利,同时必须平等的履行宪法、法律规定的义务。 ②任何公民的合法权利都受到保护。 ③任何公民的违法犯罪行为都要受到法律的制裁。 ★5.坚持权利与义务统一的原则。 (1)是什么? 在我国公民的权利和义务是统一的,二者不可分离。 权力和义务在法律关系上是相对应而存在的,权利和义务都是实现人民利益的手段和途径公民在法律上既是权利的主体,又是义务的主体,权力的实现需要义务的履行;义务的履行确保权利的实现。
高中数学必修二 ·空间几何体 1.1空间几何体的结构 棱柱 定义:有两个面互相平行,其余各面都是四边形,且每相邻两个四边 形的公共边都互相平行,由这些面所围成的几何体。 分类:以底面多边形的边数作为分类的标准分为三棱柱、四棱柱、 五棱柱等。 表示:用各顶点字母,如五棱柱或用对角线的端点字母,如 五棱柱 ' ''''E D C B A ABCDE - 几何特征:两底面是对应边平行的全等多边形;侧面、对角面都是平行四边形;侧棱平行 且相等;平行于底面的截面是与底面全等的多边形。 棱锥 定义:有一个面是多边形,其余各面都是有一个公共顶点的三角形, 由这些面所围成的几何体 分类:以底面多边形的边数作为分类的标准分为三棱锥、四棱锥、 五棱锥等 表示:用各顶点字母,如五棱锥' ''''E D C B A P - 几何特征:侧面、对角面都是三角形;平行于底面的截面与底面相似,其相似比等于顶点到截面距离与高的比的平方。 棱台 定义:用一个平行于棱锥底面的平面去截棱锥,截面和底面之间 的部分 分类:以底面多边形的边数作为分类的标准分为三棱态、四棱台、 五棱台等 表示:用各顶点字母,如四棱台ABCD —A'B'C'D' 几何特征:①上下底面是相似的平行多边形 ②侧面是梯形 ③侧棱交于原棱锥的顶点 圆柱 定义:以矩形的一边所在的直线为轴旋转,其余三边旋转所成的 曲面所围成的几何体 几何特征:①底面是全等的圆;②母线与轴平行;③轴与底面 圆的半径垂直;④侧面展开图是一个矩形。
圆锥 定义:以直角三角形的一条直角边为旋转轴,旋转一周所成的 曲面所围成的几何体 几何特征:①底面是一个圆;②母线交于圆锥的顶点;③侧面 展开图是一个扇形。 圆台 定义:用一个平行于圆锥底面的平面去截圆锥,截面和底面之 间的部分 几何特征:①上下底面是两个圆;②侧面母线交于原圆锥的顶点; ③侧面展开图是一个弓形。 球体 定义:以半圆的直径所在直线为旋转轴,半圆面旋转一周形成的几何体 几何特征:①球的截面是圆;②球面上任意一点到球心的距离等于半径。 1.2空间几何体的三视图和直观图 1.中心投影与平行投影 中心投影:把光由一点向外散射形成的投影叫做中心投影。 平行投影:在一束平行光照射下形成的投影叫做平行投影。 2.三视图 正视图:从前往后 侧视图:从左往右 俯视图:从上往下 画三视图的原则:长对齐、高对齐、宽相等 3.直观图:斜二测画法 斜二测画法的步骤: (1).平行于坐标轴的线依然平行于坐标轴; (2).平行于y轴的线长度变半,平行于x,z轴的线长度不变;(3).画法要写好。
高一化学必修二知识点总结归纳总复习提纲 第一章 物质结构 元素周期律 一、原子结构 质子(Z 个) 原子核 注意: 中子(N 个) 质量数(A)=质子数(Z)+中子数(N) 1.) 原子序数=核电荷数=质子数=原子的核外电子(Z 个) 》 2.原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里;②各电子层最多容纳的电子数是2n 2;③最外层电子数不超过8个(K 层为最外层不超过2个),次外层不超过18个,倒数第三层电子数不超过32个。 电子层: 一(能量最低) 二 三 四 五 六 七 对应表示符号: K L M N O P Q 3.元素、核素、同位素 元素:具有相同核电荷数的同一类原子的总称。 核素:具有一定数目的质子和一定数目的中子的一种原子。 同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素。(对于原子来说) 二、元素周期表 1.编排原则: ①按原子序数递增的顺序从左到右排列 、 ②将电子层数相同......的各元素从左到右排成一横行..。(周期序数=原子的电子层数) ③把最外层电子数相同........的元素按电子层数递增的顺序从上到下排成一纵行..。 主族序数=原子最外层电子数 2.结构特点: 7周期 主族:ⅠA ~ⅦA 共7个主族 族 副族:ⅢB ~ⅦB 、ⅠB ~ⅡB ,共7个副族 (18个纵行) 第Ⅷ族:三个纵行,位于ⅦB 和ⅠB 之间 (16个族) 零族:稀有气体 三、元素周期律 1.元素周期律:元素的性质(核外电子排布、原子半径、主要化合价、金属性、非金属
性)随着核电荷数的递增而呈周期性变化的规律。元素性质的周期性变化实.质是元素原 ..... 子核外电子排布的周期性变化 .............的必然结果。 、 第ⅠA族碱金属元素:Li Na K Rb Cs Fr(Fr是金属性最强的元素,位于周期表左下方) 第ⅦA族卤族元素:F Cl Br I At (F是非金属性最强的元素,位于周期表右上方) ★判断元素金属性和非金属性强弱的方法: